油包油型辣椒素乳剂的制备与体外透皮研究
2022-04-12杨棣华麦蕴华
钟 仲 杨棣华 麦蕴华
1.广东省佛山市禅城区人民医院药械科,广东佛山 528000;2.广州中医药大学第一附属医院药学部,广东广州 510006
慢性瘙痒是许多皮肤病伴随的症状,且往往难以治疗。 辣椒素(C18H27NO3),又名辣椒碱、辣椒辣素,是从辣椒中提取的一种具有挥发性和刺激性的香草酰胺类生物碱,是辣椒总碱中含量最高的一种,具有抗炎、抗菌、抗肿瘤、抗氧化、抗肥胖、缓解疼痛和慢性瘙痒等多种药理活性[1-7]。 辣椒素作为一种治疗慢性疼痛和瘙痒的传统药物, 其作用机制是竞争性抑制辣椒素受体(transient receptor potential vanilloid type 1,TRPV1),使节前纤维对各种物理刺激、内源性、外源性化学刺激和炎症因子刺激无应答[8]。 辣椒素与TRPV1 的结合,最初会引起疼痛和灼烧,持续使用后,神经元的去功能化导致其持久缓解疼痛和瘙痒。 陈丹等[9]研究发现,梅花针刺联合辣椒素和积雪苜软膏能明显抑制烧伤患者的瘙痒。 有文献报道显示,8%的辣椒碱贴剂用于治疗短期和中期的神经性疼痛均有较好的效果[10]。 目前市售辣椒碱主要以0.025%~0.1%含量的乳剂为主,剂量较低,且乳剂在皮肤上停留时间短,需每日多次给药,限制了其应用[11]。
油包油型乳剂是将亲脂性药物溶解在一种油中并分散在另外一种不相溶的油中形成的一种新型制剂[12-15]。 这种包裹住载药油的乳剂在皮肤上形成一层水不溶性薄膜,API 通过扩散传递到皮肤, 具有含药量高、释放缓慢、渗透率恒定等特点。高压均质法是制备乳剂的一种常规方法,具有操作简单和效率高的特点[16]。 本研究采用二甲基硅油和蓖麻油作为两种油相,以聚乙二醇辛基苯基醚(Triton X100)作为表面活性剂[13],利用高压均质机制备油包油型辣椒素乳剂,采用正交试验, 制备释放性能较好的辣椒素乳剂,并以右旋糖酐致小鼠瘙痒模型研究其药效,拟开发一种新型缓解瘙痒症的外用制剂。
1 实验材料
1.1 仪器
AH00D 纳米高压均质机(ATS);U3000 型高效液相色谱仪(美国Thermo Scientific 公司);改良Franz透皮扩散池(7 ml,3.14 cm2)。
1.2 试药与试剂
辣椒素(武汉远城药业,批号:201904);辣椒素对照品(成都普思生物科技股份有限公司,纯度>99.0%,批号:PS011155);辣椒素软膏(规格:2.5 mg/10 g,长春普华制药股份有限公司,批号:201127);蓖麻油(分析纯,天津市大茂化学试剂厂,批号:20190815);二甲基硅油(医用级,美国道康宁,型号:QP1-9140,黏度:20、100、500 mPa·s);Triton X100(美国Sigma 公司);乙腈(色谱纯);其他试剂均为分析纯。
1.3 动物
SD 大鼠20 只、昆明小鼠24 只[雌雄各半,SPF级,来源:珠海百试通生物科技有限公司,动物许可证号:SCXK(粤)2020-0051]。 本研究经佛山市禅城区人民医院实验动物伦理委员会审查,符合实验动物伦理规范和要求。
1.4 统计学方法
采用SPSS 23.0 统计学软件进行数据分析,经正态性检验满足正态分布的计量资料用均数±标准差(±s)表示,多组间比较采用单因素方差分析,经方差齐性检验满足方差齐的数据采用Dunnett-t 检验进一步进行组间两两比较,以P<0.05 为差异有统计学意义。
2 方法与结果
2.1 辣椒素含量测定方法
2.1.1 色谱条件 色谱柱:Diamonsil C18(250 mm×4.6 mm,5 μm);流动相:乙腈-水(80:20);流速:1.0 ml/min;检测波长:280 nm;进样量:10 μl。
2.1.2 对照品储备液的配制 精密称取5 mg 辣椒素加入到10 ml 容量瓶中,乙腈定容,摇匀,即制得辣椒素对照品储备液,浓度为500 μg/ml。
2.1.3 标准曲线的建立 将辣椒素对照品储备液配制成系列浓度的辣椒素对照品溶液,按“2.1.1”项下色谱条件,测定各个浓度的辣椒素对照品溶液,记录其峰面积[17]。 以相应进样浓度(X)为横坐标和峰面积(Y)为纵坐标进行线性回归,得辣椒素低浓度和高浓度标准曲线方程分别为:低浓度Y=3528.4X-339.3,R2=0.9999;高浓度Y=7110.3X-1191,R2=0.9994。结果表明, 辣椒素在检测浓度0.502~25.1 μg/ml和检测浓度50.2~150.6 μg/ml 范围内,其线性关系良好。
2.1.4 精密度试验 按“2.1.1”项下色谱条件,考察日内精密度,分别制备低浓度为0.5 μg/ml、中浓度为50 μg/ml、高浓度为100 μg/ml 的辣椒素对照品溶液各3 份,过0.22 μm 滤膜后进行进样测定其峰面积,见表1。结果显示,3 种浓度峰面积RSD 分别为1.93%、0.78%、0.94%(n=3),提示日内精密度均良好。
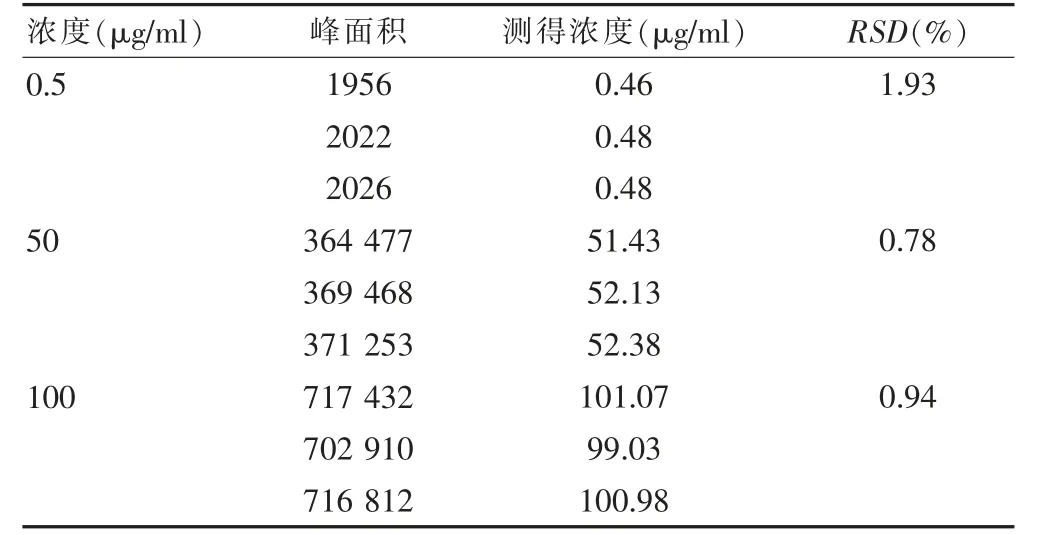
表1 精密度试验结果
2.1.5 稳定性试验 按“2.1.1”项下色谱条件,取油包油型辣椒碱乳剂接受液7 份, 分别于制备后0、2、4、8、12、24 和36 h 进样测定其峰面积,见表2。 结果显示,辣椒素峰面积RSD 为1.0%(n=7), 提示辣椒素溶液在36 h 内比较稳定。
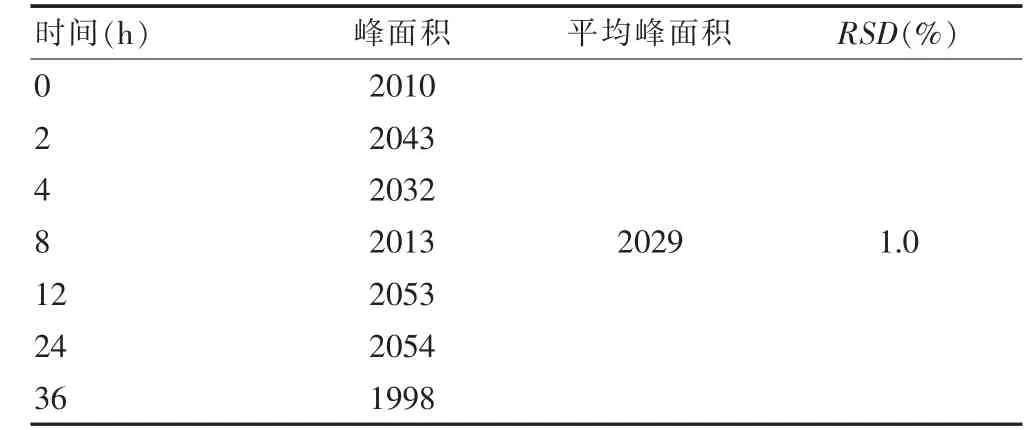
表2 稳定性试验结果
2.1.6 加样回收率试验 按处方量制备空白油包油乳剂,精密量取空白油包油乳剂的接收液1 ml 置10 ml容量瓶中,共6 份,分别精密加入辣椒素对照品储备液100 μl,用乙腈溶液定容,摇匀,按“2.1.1”项下色谱条件各进样10 μl 测定其峰面积,得到待测成分的含量,计算回收率,结果见表3。 结果表明游离药物的回收率符合要求。

表3 加样回收率试验结果
2.1.7 专属性试验 按“2.1.1”色谱条件,将“2.1.2”项下制备得到的辣椒素对照品溶液和空白油包油乳剂接受液进行高效液相色谱分析,结果见图1。
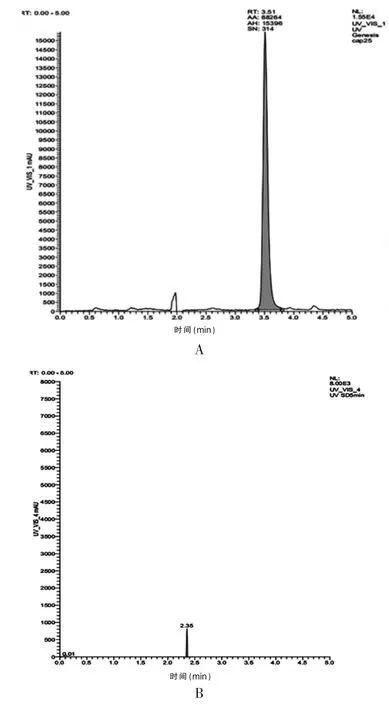
图1 辣椒素对照品与空白油包油乳剂接受液的高效液相色谱图
2.2 油包油型辣椒素乳剂的制备
通过高压均质法,以蓖麻油为内相,硅油为外相,Triton X100 为乳化剂,制备油包油型辣椒素乳剂。 具体操作:精密称量适量蓖麻油和Triton X100,水浴加热至75℃,搅拌条件下加入0.5 g 辣椒素使其溶解;加入适量硅油,高速剪切5 min;随后140 bar 条件下高压均质3 个循环,既得均匀的乳白色油包油型辣椒素乳剂,放入4℃冰箱保存,备用。
2.3 亲水性辣椒素乳膏的制备
将十六十八醇(6%~8%)、硬脂酸(4.0%~12.0%)、凡士林、维生素E(0.5%)混匀,加热至溶解;然后将十二烷基硫酸钠(0.5%~2%)和丙二醇(10%)溶解在热水中,边搅拌边将水相缓缓加入油相中,制成两亲性乳膏。 将10%(w/w)的辣椒素乙醇溶液加入90%(v/v)的丙二醇水溶液中,制成1%的亲水性辣椒素乳膏。
2.4 体外透皮实验
2.4.1 离体大鼠皮的前处理 取皮肤完好的大鼠,称重,检疫观察3 d,第3 天颈部脱臼法处死大鼠。用电动剃毛刀剔除老鼠腹部毛后, 将腹皮和鼠体钝性分离,刮去皮下脂肪组织、黏液组织和鼠毛,生理盐水冲洗干净后,涂上少量甘油,用锡纸包裹后,-20℃冷藏备用。
2.4.2 体外透皮试验 固定大鼠腹部皮肤在供给池与接受池之间,并将皮肤角质层面向供给池,使皮肤下层恰好接触液面, 保证皮肤与接受液液面之间无气泡。Franz 扩散池面积为3.14 cm2,接收池体积为7 ml,(32±1)℃恒温水浴, 接受液为30%乙醇-生理盐水溶液,搅拌速度为500 r/min。 将0.3 g 的油包油型乳剂涂抹在大鼠皮肤表面,在扩散池上封上封口膜,分别于18、20、22、24、26、28 h 取接收液1 ml,同时补充1 ml等温的接收液。
经0.22 μm 微孔滤膜过滤,取续滤液按“2.1.1”进样检测药物浓度Cn,并按照以下公式算出药物单位面积累积渗透量(Qn,μg/cm2)和稳态扩散速率[Js,μg/(cm2·h)][18]。
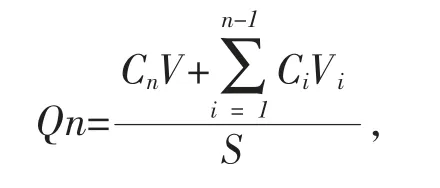
其中Cn、Ci分别为第n、i 个取样点测得的药物浓度(μg/ml);V 为接受液体积;Vi为第i 个取样点体积,S 为扩散渗透面积(3.14 cm2)。 以时间t 为横坐标,单位面积累积渗透量Qn 为纵坐标作图,对曲线的直线部分进行线性回归, 所得斜率即为稳态扩散速率Js[μg/(cm2·h)][19-20]。
2.4.3 稳定性 分层的快慢是衡量乳剂稳定性的重要指标。以1000 r/min 离心5 min,加速油包油型辣椒素乳剂分层,一定时间内观察油包油型辣椒素乳剂是否分层。结果显示,不分层,说明本研究制备油包油型辣椒素乳剂稳定。
2.5 油包油型辣椒素乳剂处方优化
油包油型辣椒素乳剂制备工艺的正交试验,考察了蓖麻油体积∶硅油体积(A)、硅油黏度(B)、Triton X100 用量(C)三个因素对辣椒素体外释放和稳定性的影响。设计3 因素3 水平的L9(33)正交试验表(表4)对乳剂的制备工艺进行优化, 以稳态扩散速率Js 和离心稳态性为指标进行研究,结果见表5。
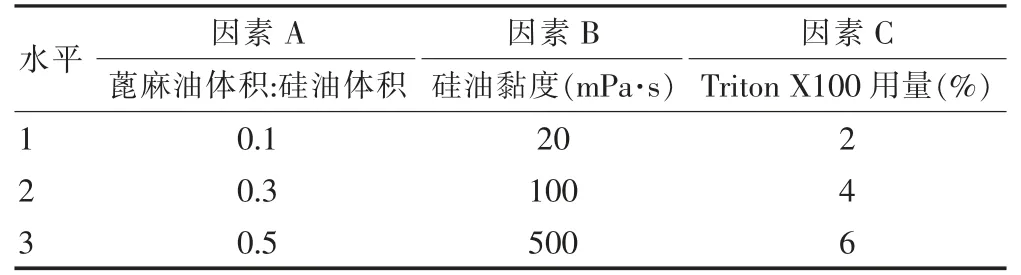
表4 因素水平表
由表5 中的极差值R,得知油包油型辣椒素乳剂处方制备工艺3 个影响因素顺序依次为:B>A>C,说明影响依次减弱顺序为:硅油黏度、相体积比、Triton X100 用量,油包油型辣椒素乳剂处方的最优处方为:A3B3C1。即油包油型辣椒素乳剂的最佳处方:相体积比为0.5,硅油黏度为500 mPa·s,Triton X100 用量为2%。
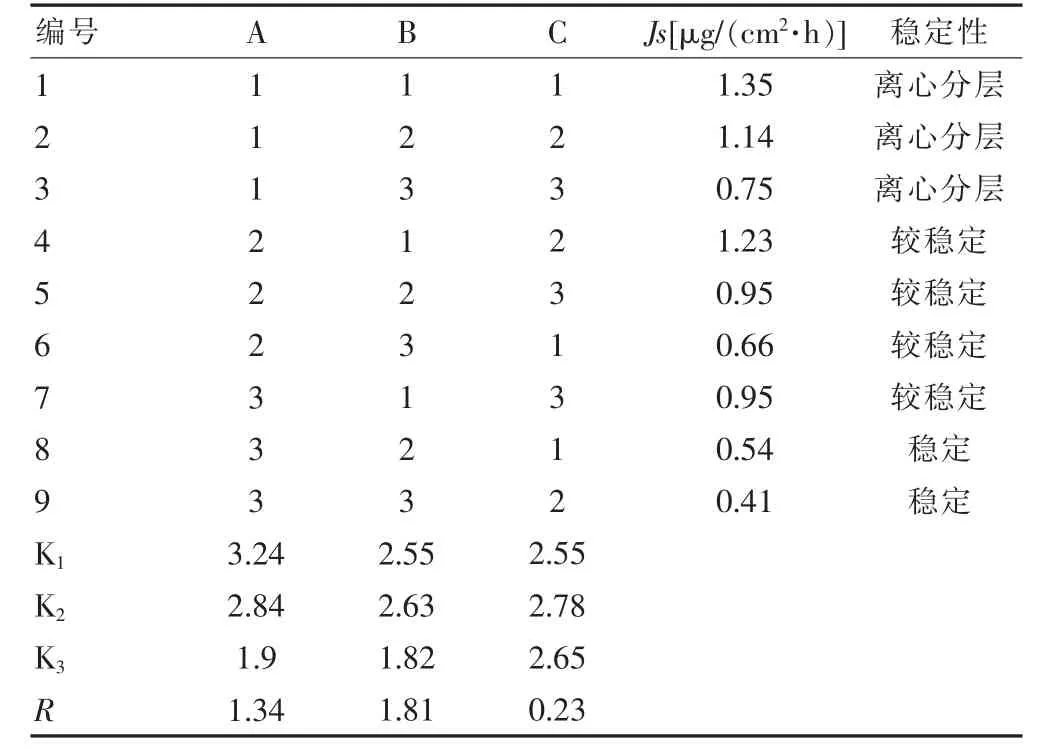
表5 正交试验结果
2.6 体外透皮实验比较
选择1%亲水性辣椒素乳膏和油包油型辣椒素乳剂的最优处方A3B3C1,按“2.4”项下方法进行体外透皮实验,实验结果见图2。 结果显示,亲水性辣椒素乳膏和油包油型辣椒素乳剂的单位面积累积渗透量Q 和时间成正比,亲水性辣椒素乳膏的渗透速率快,油包油型辣椒素乳剂的渗透速率低于亲水性辣椒素乳剂。Js 为(0.380±0.012)μg/(cm2·h)。
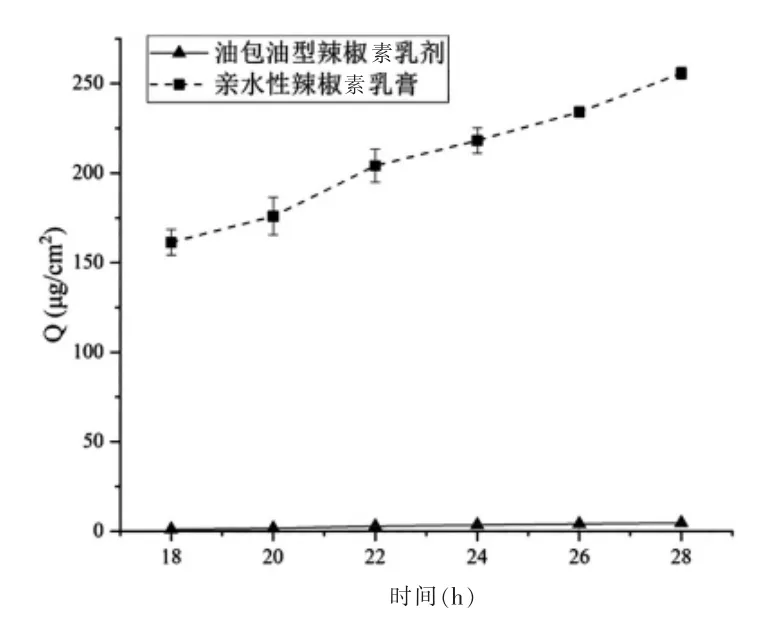
图2 油包油型辣椒素乳剂和亲水性辣椒素乳膏的体外透皮吸收曲线(n=3)
2.7 瘙痒动物模型的疗效研究
为研究油包油型辣椒碱乳剂治疗瘙痒的效果,将昆明小鼠24 只,随机分为3 组,雌雄各半,每组8 只(分别为受试组、市售组和空白对照组)。 实验前24 h用脱毛膏脱除小鼠背毛,避免损伤皮肤,观察有无红肿以及皮肤破损。 在受试组、市售组小鼠背部皮肤分别给予油包油型辣椒素乳剂与市售辣椒素软膏,每天1 次, 连续3 d。 空白对照组小鼠给予等容积生理盐水。末次给药后用生理盐水洗去药物。受试组、市售组和空白对照组小鼠按1.25 mg/kg 尾静脉注射0.025%右旋糖酐-40。以小鼠前肢抓头部、后肢抓躯体以及嘴咬全身各部位作为瘙痒指征, 记录30 min 内小鼠的瘙痒次数和潜伏时间,结果见表6 及图3。
结果显示,受试组的潜伏时间长于空白对照组和市售组,瘙痒次数少于空白对照组和市售组,差异有统计学意义(P<0.05)。 市售组的潜伏时间长于空白对照组,差异有统计学意义(P<0.05)(表6、图3)。

图3 油包油型辣椒素乳剂对右旋糖酐诱导小鼠瘙痒模型的影响(±s,n=8)
表6 油包油型辣椒素乳剂对右旋糖酐诱导小鼠瘙痒模型的影响(±s)

表6 油包油型辣椒素乳剂对右旋糖酐诱导小鼠瘙痒模型的影响(±s)
注 F 潜伏时间=80.66,P 潜伏时间<0.05,F 瘙痒次数=19.07,P 瘙痒次数<0.05;与空白对照组比较,aP<0.05;与市售组比较,bP<0.05
组别 潜伏时间(s) 潜伏时间的95%置信区间 瘙痒次数(次) 瘙痒次数的95%置信区间空白对照组(n=8)市售组(n=8)受试组(n=8)36.75±13.34 57.75±12.42a 121.88±15.91ab 25.60~47.90 47.37~68.13 108.58~135.17 37.00±10.03 31.13±9.34 11.50±6.05ab 28.62~45.38 23.32~38.93 6.44~16.56
3 讨论
本研究通过高压均质法制备出一种含有辣椒素的油包油型乳剂,并通过正交实验,优化了油包油型辣椒素乳剂的处方,本研究结果显示,油包油型辣椒素乳剂处方制备工艺3 个影响因素顺序依次为:B>A>C,说明影响依次减弱顺序为:硅油黏度、相体积比、Triton X100 用量, 油包油型辣椒素乳剂处方的最优处方为:A3B3C1,该结果表明,相体积比和硅油黏度对于油包油乳剂的扩散系数影响大。随着蓖麻油和硅油体积比的增加,硅油量减少,分散相降低,扩散速率增加,但会影响透皮速率。 不同黏度的硅油对扩散系数也具有显著影响,随着硅油黏度越高,扩散系数显著降低,辣椒素扩散越慢,有利于辣椒素的缓慢释放,且对乳剂的稳定性起到了关键影响,所以选择高黏度硅油。 表面活性剂Triton X100 对扩散系数基本无影响,但对于稳定性具较大的影响,而且随着硅油黏度增加,乳剂稳定性显著增加。 按照最优条件制备油包油乳液,验证其处方工艺,测得Js 和稳定性。 结果优于以上各处方,确定处方为:相体积比为0.5,硅油黏度为500 mPa·s,Triton X100 用量为2%为油包油型辣椒素乳剂的最佳处方组合。选用以上优化的最佳处方与1%亲水性辣椒素乳膏进行体外透皮实验, 结果显示,亲水性辣椒素乳膏和油包油型辣椒素乳剂的单位面积累积渗透量Q 和时间成正比, 亲水性辣椒素乳膏的渗透速率快,油包油型辣椒素乳剂的渗透速率明显低于亲水性辣椒素乳剂,证明油包油型辣椒素乳剂释放缓慢,可以达到持续释放的效果;最后,选择右旋糖酐致小鼠瘙痒模型研究市售辣椒素软膏和油包油型辣椒素乳剂的疗效, 各组小鼠30 min 内潜伏时间和瘙痒次数的比较结果显示,市售组和受试组小鼠的潜伏时间显著延长,且受试组小鼠瘙痒次数下降更显著,提示油包油型的辣椒素乳剂相比于普通辣椒素乳剂,能更有效地减少其瘙痒次数,表现出更好地缓解瘙痒的治疗效果。
本研究成功制备了一种含有二甲基硅油和蓖麻油的油包油型辣椒素乳剂, 并对其进行处方优化,确定了最优处方,并以右旋糖酐致小鼠瘙痒模型测定其药效。 相比于传统乳剂,该制剂具有剂量高、释放缓慢、依从性好和有效降低瘙痒次数的特点。 油包油型乳剂是一种有效利用辣椒素治疗慢性瘙痒的制剂方法,该方法可能会适用于其他具有皮肤刺激性和需长期给药的药物制剂制备。
