血清25-羟基维生素D3水平与儿童糖尿病肾病的相关性研究
2022-04-08吕洋
吕 洋
(鞍山市中心医院/小儿内分泌科 辽宁 鞍山 114001)
据估计2040年全球将有6.42亿糖尿病患者[1]。糖尿病的主要特征是高血糖,而高血糖引起的急性症状多少见,因此糖尿病的主要危害来自于高血糖引起的并发症,糖尿病的并发症可分为急性并发症和慢性并发症。急性并发症包括急性严重代谢紊乱和感染性疾病,而慢性并发症则包括血管性病变、神经系统损害等,其中血管性病变又可分为微血管病变和大血管病变[2]。微血管病变主要体现在视网膜、肾脏等处的毛细血管基底膜增厚,这些该病能够引起眼底组织、肾脏组织局部血管粥样硬化从而导致失明、肾功能衰竭。糖尿病肾病即是糖尿病的一种慢性并发症,其属于糖尿病并发症中的微血管性并发症。调查显示,近年来糖尿病肾病的发病率呈逐年上升趋势,这与着糖尿病发病率日渐上升的趋势有着紧密的联系,同时与人们对糖尿病肾病的关注度不高有关。糖尿病发病率的增加,给患者家庭、全社会都带来了沉重的经济负担,因此早期对糖尿病肾病进行正确诊断,并及时延缓其进展有着重要的意义[3]。研究发现,维生素D不足和缺陷与糖尿病有关;伴随着糖尿病肾病的发生,血清25-羟维生素D浓度的进一步下降[4]。而儿童的代谢又更具特征性,本研究即选取儿童糖尿病患者作为研究对象,探究25(OH)D3与儿童糖尿病肾病的相关性。
1 资料与方法
1.1 一般资料
选取我院收治的40例糖尿病肾病患儿作为研究对象,依据患儿所患糖尿病类型不同分为1型糖尿病肾病组和2型糖尿病肾病组,再纳入同期我院体检的正常儿童作为对照组。详细资料统计如下表1:
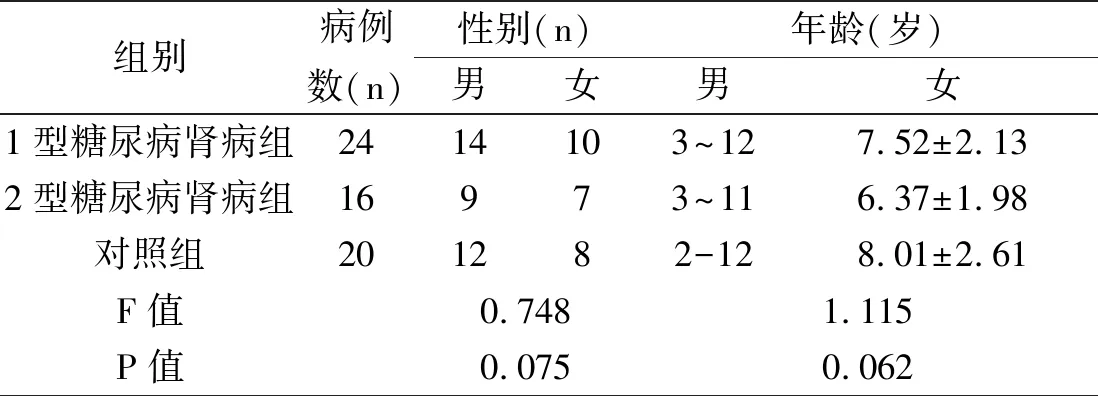
表1 两组患儿基本资料统计表
1.2 纳入标准与排除标准
本次研究所纳入患者均需符合以下要求方可纳入研究:①所有患者需明确诊断为糖尿病,诊断标准参考下文所示的1999年WHO关于糖尿病的诊断标准;②符合糖尿病肾脏病的诊断标准,诊断标准参见2007年版 NKF/KDOQI相关诊断标准;③所有入选者年龄在2-14岁之间。④所有对象签署知情同意书,同时对本研究内容有一定了解。
本次研究所纳入患者若符合以下几项中任意一项者则不予以纳入研究:①不符合纳入标准者;②入选者术前肾脏手术史者;④糖尿病患者伴发有糖尿病急性并发症者;⑤糖尿病合并妊娠者;⑥如患者近 3 月有外伤史、输血史或手术史;⑦近3月使用过糖皮质激素、免疫抑制剂、镇痛剂等药物。
1.3 方法
1.3.1病例的收集
①所有入选病例必须由主管医生完成统计表表的填写,统计表中所有项目均须完成。所填写的项目不得涂改,如需修改,应先将填错的数据用一短横线划掉,然后在其上方填上正确的结果,并在旁边签名和注明修改日期。主管医生在填写完成后应认真检查核对所有数据,并在表中签名,表明已检查过,务必保证数据填写的真实性、准确性。完成的数据收表经审查后进行保管,进行数据录入与管理工作。②在本研究开始前,参与研究的医生与人员必须经过统一的培训,统一记录方式与判断标准。在研究过程中,由负责人定期对研究进行监查访问及审核,以保证研究方案中的所有内容得到严格遵守、填写表格的正确以及填写数据的真实性、准确性。③保密原则:所有涉及本研究的全部资料应遵守保密性原则,并妥善保管。④在进行数据收集、整理时,应每隔3天对所收集、整理的数据进行简单复核,每周应进行一次抽样检查,以便于减少数据收集、整理发现的错误,同时改进数据收集、整理过程中的错误。⑤印刷版医疗记录审查:首先,向有丰富临床经验的临床医生请教,以了解如何在临床检验学指标方面审查医疗记录。第二,审查所有提取的打印版本的糖尿病肾病患者的医疗记录。审查结果将被记录在计算机上。第三,计算并提取相关指标,根据过程指标与结果指标,计算病历相关指标信息。⑥定期进行组内会议,主要对数据收集、整理、分析过程中遇到的问题进行分析、讨论,当遇到疑难问题时应咨询内分泌科与统计学相关领域内的专家。
1.3.2相关指标的检测
所有受试对象过夜空腹8 h以上,测定患者炎症指标(C反应蛋白、血沉、降钙素原)、代谢指标(FPG、TC、TG、HDL-C、LDL-C)及25-羟基维生素 D3[25(OH)D3]的水平。上述指标的检测均由我院检验科完成。
1.4 统计学方法
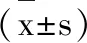
2 结果
2.1 三组儿童间的25(OH)D3水平比较
经测定,1型糖尿病肾病儿童的25(OH)D3水平为(12.70±4.02)ng/mL,2型糖尿病肾病儿童的25(OH)D3水平为(16.36±4.89)ng/mL,而对照组儿童的25(OH)D3水平为(26.12±7.27)ng/mL,三组儿童的25(OH)D3两两比较存在统计学差异(P<0.05)。
2.2 糖尿病肾病儿童的25(OH)D3与代谢指标、炎症指标间的相关性分析
采用Pearson相关系数分析发现,在糖尿病肾病患儿中,25(OH)D3与炎症指标无相关性(P>0.05),与FPG存在着相关性(P<0.05)、与其他代谢指标无显著相关性(P>0.05)。详细见下表2:
(C反应蛋白、血沉、降钙素原)、代谢指标(FPG、TC、TG、HDL-C、LDL-C)

指标相关性系数rP值C反应蛋白1.8760.234血沉1.9730.253降钙素原1.6340.197FPG-0.3520.021TC-1.8230.273TG-1.3810.174HDL-C1.1920.318LDL-C-1.2230.117
3 讨论
随着经济的发展和人们生活方式的改变,糖尿病的发病率日趋增加,据国际糖尿病联盟的调查数据显示,2015年成人的糖尿病全球总例数为4.15亿,此外还有将近2亿患者患有糖尿病却未被明确诊断,而糖耐量受损作为糖尿病的前期阶段,具有极高的进展为糖尿病的风险,据估计全球有超过3亿人处于糖耐量受损阶段,由此可见糖尿病已成为当下的一种常见病、多发病[5]。据估计2040年全球将有6.42亿糖尿病患者,约平均每六秒钟就有一个人死亡于糖尿病并发症[1]。糖尿病是一类胰岛素相对或绝对缺乏的慢性代谢性疾病,以高血糖作为主要特征,同时可能会伴有多尿、多饮、多食及体重减轻,上述被即典型的“三多一少”症状,当糖尿病持续进展时可出现多种急、慢性并发症,如酮症酸中毒、糖尿病足、糖尿病肾病等。更为重要的是糖尿病作为一种代谢性疾病,在进展过程中能够引起其他系统的相关性疾病。我国方家追[6]在对糖尿病患者引起的其他疾病进行分析时发现,600例患者中有44%的患者患有高血压,而有37%的患者血脂代谢异常,大动脉粥样硬化的发病率则约为28%,所有患者的慢性并发症发病率约为80%。此外,其还对这600例患者的典型糖尿病慢性并发症进行了分析,结果发现糖尿病视网膜病变和糖尿病肾病的患病率分别为28.31%和23.12%;周围神经病变41.04%,由此可见糖尿病伴发的其他系统非典型并发症疾病的发病率要远远高于糖尿病引起的典型并发症。
血管病变是2型糖尿病常见的慢性并发症之一,而其中糖尿病肾病是糖尿病血管并发症中较为常见且重要的并发症。2型糖尿病患者发病时间往往不能确定,缺乏长期的临床随访资料,难以对其进行准确的分期,目前国内外专家多参考T1DM的糖尿病肾病分期方法将其分为五个阶段:①Ⅰ-Ⅱ期:患者病变无临床征象,无法采用临床现有的检验学指标进行检测,大多数患者也为此阶段患者;②Ⅲ期:Ⅲ期被称为为糖尿病肾病的“高危期”,患者在此阶段出现微量白蛋白尿,目前规定Ⅲ期糖尿病肾病患者的尿白蛋白排泄率(urinary albumin excretion rate ,UAER)在 20~200g/min,24小时尿白蛋白排泄率在 30~300mg;③Ⅳ期:Ⅲ期患者继续进展为Ⅳ期,Ⅳ期也被称为临床肾病期,目前规定尿白蛋白排泄率>200g/min,24小时尿微量白蛋白>300mg,当患者进入到临床肾病期时往往会进展到终末期肾衰;④Ⅴ期:Ⅴ期即为终末期肾衰竭期肾小球滤过率(Glomerular filtration rate,GFR)<10%,此期需要进行肾脏替代治疗。研究显示在糖尿病肾病Ⅱ期以前给予积极干预能够延缓糖尿病肾病的进展,提高患者预后,因此故早期诊断早期治疗糖尿病肾病,有非常重要的意义。
肾病的发病机制复杂,尚未完全阐明,但有研究发现糖尿病患者低浓度血清 1,25(OH)2D3 与ACR、eGFR 较高具有相关性,说明 1,25(OH)2D3缺乏与肾病进展有关。糖尿病患者的高血糖状态可激活 RAAS(肾素-血管紧张素-醛固酮)系统升高肾小球内血压,从而加速其纤维化,促进生长因子、炎性因子的趋化,加速免疫细胞的渗透,破坏足细胞,增加细胞外基质的合成,而维生素D可能是 RAAS 系统的负内分泌调节因子,阻断肾组织内肾素合成、血管紧张素系统活化,达到降低血压,改善肾灌注,保护糖尿病肾病的发生、发展。而儿童期又可能发生维生素D的缺乏,因此更有可能发生糖尿病肾病。本次研究发现1型糖尿病肾病组、2型糖尿病肾病组及健康儿童的25(OH)D3存在统计学差异(P<0.05);在糖尿病肾病患儿中,25(OH)D3与炎症指标无相关性(P>0.05),与FPG存在着相关性(P<0.05)、与其他代谢指标无显著相关性(P>0.05)。
综上所述,25(OH)D3在儿童糖尿病肾病中起着重要的作用,但与炎症反应无显著关联性。
