靶向溶酶体新型次氯酸荧光探针的合成及性能
2022-04-08杜宇婷王宏亮赵三虎王桂林
杜宇婷,王宏亮,赵三虎,王桂林
(忻州师范学院 化学系,山西 忻州 034000)
0 引言
次氯酸(HClO),过氧化氢(H2O2),羟基自由基(HO·)和超氧阴离子自由基被称为活性氧(ROS),它们能够引起细胞内的氧化应激,与许多生理和病理过程相关[1-4]。其中,HClO吸引了很多人的关注,是因为它显示出关键的抗菌特性[5],以及它在生物、化学、环境及人体免疫防御系统中起着重要作用[6-7]。在生物体内,内源性的HClO是由过氧化氢和氯离子在髓过氧化物酶(MPO)的催化作用下产生[8],HClO的产生在生物体内是一把双刃剑。好的一方面,次氯酸能够保护生物体通过杀死入侵免疫系统中的病原体和细菌[9]。但是,另一方面,越来越多的证据表明,过量的HClO可能会导致蛋白质、核酸和脂质等生物分子被氧化,从而导致组织损伤、炎症以及一系列疾病,比如炎症甚至癌症[10-13]。溶酶体pH值是维持溶酶体正常消化功能的参数,不同原因导致的溶酶体pH值改变可能会影响溶酶体蛋白酶的多种生理过程,进而影响细胞正常功能。因此,基于以上原因,发展一种高选择性和高灵敏性,用于溶酶体中次氯酸检测方法具有重要意义。
在过去的几十年里,传统的HClO检测手段比如化学发光法、电化学分析、比色法和质谱法等[14-15],但是其存在耗时长、操作繁琐、检测限低等局限性。由于HClO在人体生理中发挥着重要作用,因此需要设计新的方法来精确的测定体内次氯酸根的含量。与这些传统的分析方法相比,荧光检测技术因其易于操作、响应快速和灵敏度高等优点,广泛应用于生物医学中[16-17]。近几年报道有关次氯酸的反应型荧光探针[18-19],主要是基于次氯酸的强氧化性,比如对席夫碱、不饱和碳碳双键、硫化物、硫缩酮和对甲氧基苯酚的氧化等[20-24]。
2008年,陈课题组报道了利用次氯酸的氧化性,将二苯甲酰肼氧化成罗丹明的二苯甲酰二亚胺[25]。2014年,Goswami 等发现了罗丹明类似物可以用于次氯酸的比率型检测[26]。2015年,Lee 等报道了一个基于罗丹明和丹磺基部分被次氯酸氧化的荧光探针[27]。2020年,詹和他的同事发现了一个罗丹明螺旋环的一个次氯酸的检测方法[28]。次氯酸对氟硼类衍生物的氧化也可以用于它的检测[29-30]。
众所周知,次氯酸可以把“C=C”和“C=N”氧化断键[16,31]。因此,本文设计并合成了一种以3-(溴甲基)苯甲醛为原料,吗啉作为溶酶体的靶向基团,分两步合成了一种检测溶酶体中次氯酸的荧光探针BMOA(图1)。研究发现探针BMOA 对次氯酸检测时具有超快的反应时间(150 s),高的灵敏度和选择性。探针对次氯酸的最低检出限仅为4.13 nmol/L和的特点。因此,本研究为次氯酸的检测提供了一种简单且有效的分析方法。高分辨质谱机理验证表明,荧光探针BMOA的“C=N”被次氯酸氧化而发生断裂,释放出MOB,从而使得荧光发生淬灭。

图1 探针BMOA 对次氯酸的识别机理
1 实验部分
1.1 试剂与仪器
3-(溴甲基)苯甲醛、N-Boc-1,4-苯二胺、吗啉购自安耐吉化学剂有限公司;无水乙醇(分析纯)、乙酸乙酯 (分析纯)、石油醚 (分析纯)、二氯甲烷 (分析纯)购自天津欧博凯化工有限公司购进;N,N-二甲基甲酰胺从天津市北辰方正试剂厂购进;三氯甲烷从成都市科隆化学品有限公司购进。200~300目柱层析硅胶(青岛海洋化工公司)。所用试剂均为分析纯,所用去离子水 (≥18 MΩ·cm) 由 Milli-Q 纯化系统制备。
SHZ-D(Ⅲ)予华牌循环水真空泵;RE-2000B旋转蒸发器;GKDL-20小型冷却水循环装置;DF-101S型集热式恒温磁力搅拌器(巩义市予华仪器有限责任公司);PHS-3C型pH计(上海雷磁仪器厂);ZF7三用紫外分析仪(上海予名仪器设备有限公司);UV-2550型紫外可见分光光度计(日本岛津公司);Bruker AVANCE-600 MHz超导核磁共振波谱仪(德国);赛默飞高分辨质谱仪;FS5荧光光谱仪(英国)。
1.2 探针BMOA的合成
探针分子 BMOA 的有机合成参考文献[32]。首先化合物MOB的合成,取原料3-(溴甲基)苯甲醛1.0 g(5 mmol)、吗啉环0.52 g(6 mmol)和碳酸钾1.54 g(10 mmol)溶解于适量的溶剂DMF,在70 ℃加热条件下反应,溶液由无色透明变为黄色,TCL监测,8 h后反应结束。加入40 mL蒸馏水淬灭,用乙酸乙酯萃取三次,减压蒸馏得到黄色油状物(溶剂DMF因沸点高无法旋出),柱层析乙酸乙酯作为洗脱剂,得到黄色晶状固体1.06 g(5 mmol)产率96.96%。1H NMR(400 MHz, DMSO-d6) δ 10.18, 10.02, 8.25, 7.85, 7.85,7.83, 7.83, 7.82, 7.81, 7.81, 7.80, 7.69, 7.67, 7.67,7.65, 7.65, 7.59, 7.57, 7.56, 7.12, 4.37, 3.60, 3.58,3.57, 3.56, 3.42, 2.42。探针BMOA的合成,取MOB 11.0 g(4 mmol)与N-Boc-1,4-苯二胺1.05 g (5 mmol)溶解于三氯甲烷中,加入催化量的哌啶,在70 ℃回流,TCL监测,12 h后反应结束。加入40 mL水淬灭,CH2Cl2萃取,减压蒸馏得到黑棕色油状物,柱层析(V(石油醚)∶V(乙酸乙酯)=6∶1)分离,最终得到探针BMOA黄色粉末0.21 g (0.5 mmol),产率为56.6%。1H NMR(400 MHz, DMSO-d6), δ 9.43 (s, 1H), 8.63 (s, 1H),7.87 (s, 1H), 7.83-7.77 (m, 1H), 7.51 (d,J= 8.3 Hz,2H), 7.45 (d,J= 7.4 Hz, 2H), 7.29-7.20 (m, 2H),3.58 (t,J=4.5 Hz, 4H), 3.52(s, 2H), 2.38(d,J=5.1 Hz,4H), 1.49 (s, 9H)。13C NMR (100 MHz, DMSO-d6), δ 159.1, 152.8, 147.0, 136.7, 136.4, 132.1, 129.3, 129.2,128.7, 127.8, 121.7, 121.7, 121.6, 119.3, 80.6, 66.9, 63.1,53.7, 53.6, 28.4。HR-MS, C23H29N3O3-,实测值 (计算值),m/z:394.2116[M-H-]-。探针 BMOA 的合成路线见图2所示。

图2 探针BMOA的合成路线
1.3 荧光探针BMOA的光谱性能测
在光谱测试前,首先用DMSO溶解探针固体,配制母液为10 mmol/L 探针。再用二蒸水配制10 mmol/L PBS 缓 冲 液 (pH=7.4)及 各 待 检 测 物 (Cys,ClO-,储备液(100 mmol/L)。测试时,用移液枪取BMOA的储备液,使测试的探针BMOA 浓度为5 mmol/L(VCH3CN/VPBS=1∶1)。不同浓度的待检测物依据实验需要按照类似的方法取其储备液进行配制。探针与各待检测物混合均匀后,室温振荡5 min后测试荧光光谱。所用的激发波长为292 nm,激发/发射狭缝宽度为5.0 nm/5.0 nm。响应时间的测定:使用荧光仪测定探针BMOA与次氯酸钠(120 mmol/L)反应的反应时间。机理验证的测定:在去离子水的体系中,加入5 mmol/L的探针BMOA,随后加入24倍当量的次氯酸钠,反应5 min后利用高分辨质谱分析。
2 结果与讨论
2.1 探针分子BMOA对次氯酸钠的光谱研究
在CH3CN/PBS 缓冲体系(pH=7.4,VCH3CN/VPBS=1∶1)中,如图3(a)所示,单独探针BMOA的紫外吸收波长是263 nm和333 nm,当向体系中分别加入不同浓度的 NaClO(50,80,120 mmol/L)后,探针原有的紫外吸收波长消失,在292 nm 处出现新的吸收峰,说明探针确实与次氯酸根离子发生反应,并且有新的物质生成。图3(b)所示,当向5 mmol/L的探针溶液中加入0~120 mmol/L的NaClO溶液后,探针BMOA 的荧光发射强度在544 nm处逐渐减弱,说明探针与次氯酸根离子发生反应,并且是淬灭型荧光探针。
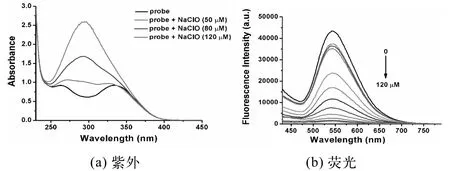
图3 图2探针BMOA对次氯酸钠的紫外和荧光变化
2.2 探针分子BMOA对次氯酸钠的滴定实验和反应时间
为了测试不同浓度的次氯酸根与探针BMOA的相互作用,进行滴定实验,如图4所示。随着次氯酸根离子浓度的增大,F544值在NaClO浓度为0~70 mmol/L呈现良好的线性关系,线性系数为0.997。根据检出限计算公式(LOD=3σ/k,σ为白样品连续测定10次的标准偏差,k为标准曲线斜率)[33],得到方法检出为 4.13 nmol/L。上述结果说明BMOA可以高灵敏、定量检测次氯酸。为了探究探针与次氯酸根离子的反应时间,考察了探针BMOA 与次氯酸混合后荧光强度随时间的变化情况。Figure 2B显示,反应体系的发射波长在544 nm处快速减弱,150 s后荧光强度基本不再变化。图4(a)所示为探针BMOA对NaClO的滴定实验、(b)所示为探针BMOA的荧光强度随时间的变化关系图。
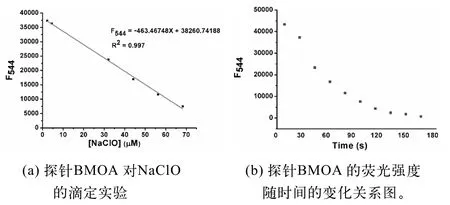
图4 不同浓度的次氯酸根与探针BMOA的相互作用随时间的变化关系
2.3 探针分子BMOA对次氯酸根离子的选择性和pH值的影响
在对探针BMOA光谱性能研究的基础上,进一步评估了探针的选择性,如图5所示。加入NaClO响应之后,在最大发射波长544 nm处,荧光几乎完全淬灭,但是加入其他分析物荧光强度没有变化。由此证明,探针BMOA对次氯酸根离子具有较好的选择性。如图5(b)所示,没有加入次氯酸根离子时,探针的荧光强度在pH=3~10的范围内,基本保持稳定,说明探针BMOA在生理pH环境下可以应用。当加入次氯酸根离子后,在pH=5.0~7.5的范围内,荧光强度的变化不明显,这说明该探针在生理条件下能够检测生物样品中的次氯酸根离子。

图5 探针BMOA对次氯酸根离子的选择性实验和pH对探针BMOA的影响
2.4 探针分子BMOA对次氯酸检测的机理研究
为了进一步验证推测的机理,即探针BMOA被次氯酸氧化释放MOB(如图6a是所示),运用高分辨质谱进行验证。在去离子水的体系中,加入5 mmol/L的探针BMOA,随后加入24倍当量的次氯酸钠,反应之后利用高分辨质谱分析。如图6b所示,检测到了MOB的峰(m/z 206.95),即探针被次氯酸氧化断裂,释放出MOB。这为探针BMOA按上述机理进行反应提供了有力的依据。

图6 探针BMOA对次氯酸根离子的识别机理和与次氯酸钠反应后的高分辨质谱
3 结语
本文通过利用3-(溴甲基)苯甲醛为原料,吗啉作为溶酶体靶向基团,设计合成了一种可以检测溶酶体中次氯酸的荧光探针BMOA。该探针BMOA可以快速灵敏、选择性地识别次氯酸根离子,并且其荧光信号在0~70 mmol/L次氯酸浓度范围内呈现良好的线性关系,其检测限仅为4.13 nmol/L。同时,探针BMOA对次氯酸根离子的响应时间仅为150 s。利用高分辨质谱深入探讨了该荧光探针的响应机理即荧光探针BMOA的“C=N”被次氯酸氧化而发生断裂,从而使得荧光发生淬灭。
