含锰废水为原料制备MnO2/Fe3O4及对Cu2+的吸附研究
2022-04-08胡波年欧金花
谭 鸿 黎 妮 胡波年 欧金花
(湖南工学院材料科学与工程学院,湖南 衡阳 421002)
0 引言
重金属离子污染可对人体产生严重的毒理效应,如皮肤病变、高血压、器官衰竭等。其中,铜离子是重金属离子中常见的污染源。目前,重金属离子的处理技术有吸附法、生物沉淀法、电解法等。在这些方法中,吸附法因其操作简便、价格低廉、无二次污染等优势被广泛研究。因此,开发高效、无毒、低成本的重金属离子吸附剂具有重要意义。
近年来,电絮凝技术以其操作简单、效率高、环境友好、成本低等优点,引起了广大科研工作者的关注。目前,电絮凝技术的工艺参数(如电极材料、电流密度等)已被广泛研究,但主要集中在如何提高去除率、降低能耗等方面,关于对絮凝体的调控和再利用的相关研究却很少。在高效处理重金属废水的前提下,降低污泥量或将其循环利用是电絮凝技术需要解决的问题之一。
针对上述问题,采用“以废治废”的理念,该文以含锰废水为原料,制备了一种MnO/FeO复合材料。在高效处理含锰废水的前提下,研究了MnO/FeO的结构、形貌以及其对铜离子的吸附性能。
1 试验部分
1.1 试验药品
铁片(2×50×60)mm购买于飞跃金属制品有限公司。模拟废水由5mol/L NaSO、0.22mol/L MnSO·HO组成,所用化学药品均购买于Sigma-Aldrich。
1.2 MnO2/Fe3O4的制备
采用数字脉冲电源对500mL含锰废水进行电絮凝试验。电絮凝工艺参数为脉冲频率为50Hz、电极间距为15mm、有效电极面积40cm、平均电流密度为5mA/cm。电絮凝试验结束后,离心收集絮凝沉淀,烘干。通过控制电解时间(10min、20min和30min),获得不同的絮体试样。随后,将收到的絮凝体试样在350℃的氮气气氛下煅烧3h,制得MnO/FeO复合材料,分别命名为MnO/FeO4-10,MnO/FeO-20,MnO/FeO-30。
1.3 吸附性能和吸附热力学、动力学研究
将20mg MnO/FeO加入30 mg/L, 100mL的铜离子溶液中,然后置于30℃的恒温水浴锅搅拌。提取样品并按预定间隔离心,通过紫外-可见分光光度法测定铜离子的含量。q为时间时的铜离子吸附量,q=(C-C)/,q为平衡时的铜离子吸附量,q=(C-C)/,其中C和C分别是铜离子的初始浓度和平衡浓度。C为时刻铜离子浓度,为铜离子体积,为所用MnO/FeO的质量。
2 结果与讨论
2.1 MnO2/Fe3O4的结构和形貌
采用X射线衍射仪(XRD)对含锰絮凝体和煅烧后样品进行了检测分析,如图1所示。首先,测试了含锰絮凝剂的结构,其特征峰与文献报道的氢氧化铁数据完全一致,它是由电解过程中产生的Fe和OH通过水合作用和络合作用形成。其中,37.1°、36.3°、46.9°、60.7°的峰分别代表氢氧化铁(JCPDS No.44-1415)的(210)、(301)、(20)和(321)面。絮凝体中没有发现锰化合物的特征峰,说明锰离子主要通过吸附的形式存在于絮凝体中。同时,对絮凝物煅烧后的样品进行检测。图中未见二氧化锰的特征吸收峰,说明MnO为无定型结构。其中,30.1°、35.4°、43.1°、56.9°和62.5°的峰分别代表FeO(JCPDS No.190629)的(220)、(311)、(400)、(511)和(440)面。通过以上数据结果分析可知,以含锰废水为原料,电絮凝处理制得吸附锰的铁氢氧化物,热处理后制得MnO/FeO材料。

图1 含锰絮凝体和MnO2/Fe3O4的XRD
采用扫描电镜(SEM)对样品进行了形貌表征,如图2所示。MnO/FeO-10,MnO/FeO-20,MnO/FeO-30样品中都可以观察到球形颗粒,大小为50nm~100nm。从图2(a)~图2(c)中可以发现,随着电解时间的延长,颗粒逐渐增大,这可能与电解过程中絮凝物的聚集和生长有关。电解时间越长,前驱体絮凝物颗粒越大,从而MnO/FeO颗粒越大。采用透射电镜(TEM)对样品进行更详细的形貌和晶形研究,如图2(d)所示。TEM进一步证实了样品的球形颗粒形貌并且从高分辨的TEM图中可观察到间距为0.25nm的晶格,这与FeO的(311)晶格数据一致。

图2 SEM 图
2.2 锰离子的去除效果
为了达到“以废治废”的目的,确保含锰废水得到有效处理,采用脉冲电源对含锰废水进行了电絮凝处理并检测了其去除效果。测试了电解过程中,锰的去除效率和残留浓度,见表1。从表1中可以看出,利用脉冲电絮凝法去除锰离子,含锰废水中锰离子的含量随着电解时间的增加而迅速降低,5min锰离子去除率即可达到92.37%,当电解时间超过10min后,锰离子的去除率可达到99.92%,此时锰离子浓度已降至0.1mg/L以下,达到国家锰离子废水排放标准。继续延长电解时间至30min,此时含锰废水中已不能检测到锰离子,去除率达到100%。以上数据说明,在成功制备的MnO/FeO同时,含锰离子得到了有效去除。

表1 不同电絮凝时间的去除效率及剩余锰离子含量
2.3 MnO2/Fe3O4对铜离子的吸附性能研究
为了表征样品的吸附能力,测试了不同MnO/FeO样品对铜离子溶液(20 mg/L)的去除效果。从图3(a)可知,MnO/FeO-10的去除率为92.5%, 优于MnO/FeO-20(78.6%)和MnO/FeO-30 (45.3%)。分析认为,MnO/FeO-10的优异性能归功于分散的球形纳米颗粒,因为其可提供较大的比表面积和吸附活性位点。而MnO/FeO-20 (78.6%)和MnO/FeO-30 (45.3%)的吸附性能下降是由于球形颗粒趋于团聚,比表面积和吸附活性位点下降所致。
众所周知,吸附容量与铜离子的初始浓度有关系。因此,用MnO/FeO-10对不同浓度的铜离子溶液进行了吸附研究。如图3(b)所示,当铜离子浓度为由10mg/L增至60mg/L时,吸附平衡时间由2h~3h增至3h~4h。10mg/L和20mg/L铜离子溶液的去除率分别为94.1%和92.5%,而60mg/L铜离子溶液的去除率仅为55.2%,由此说明当铜离子的初始浓度较高时,其吸附量已接近饱和。当铜离子初始浓度从10mg/L增加到60mg/L时,平衡吸附量从25.1mg/L增加到67.2mg/L。分析认为这是由于铜离子溶液浓度较高时,驱动力较大,因此克服了吸附剂与吸附质之间的传质阻力。
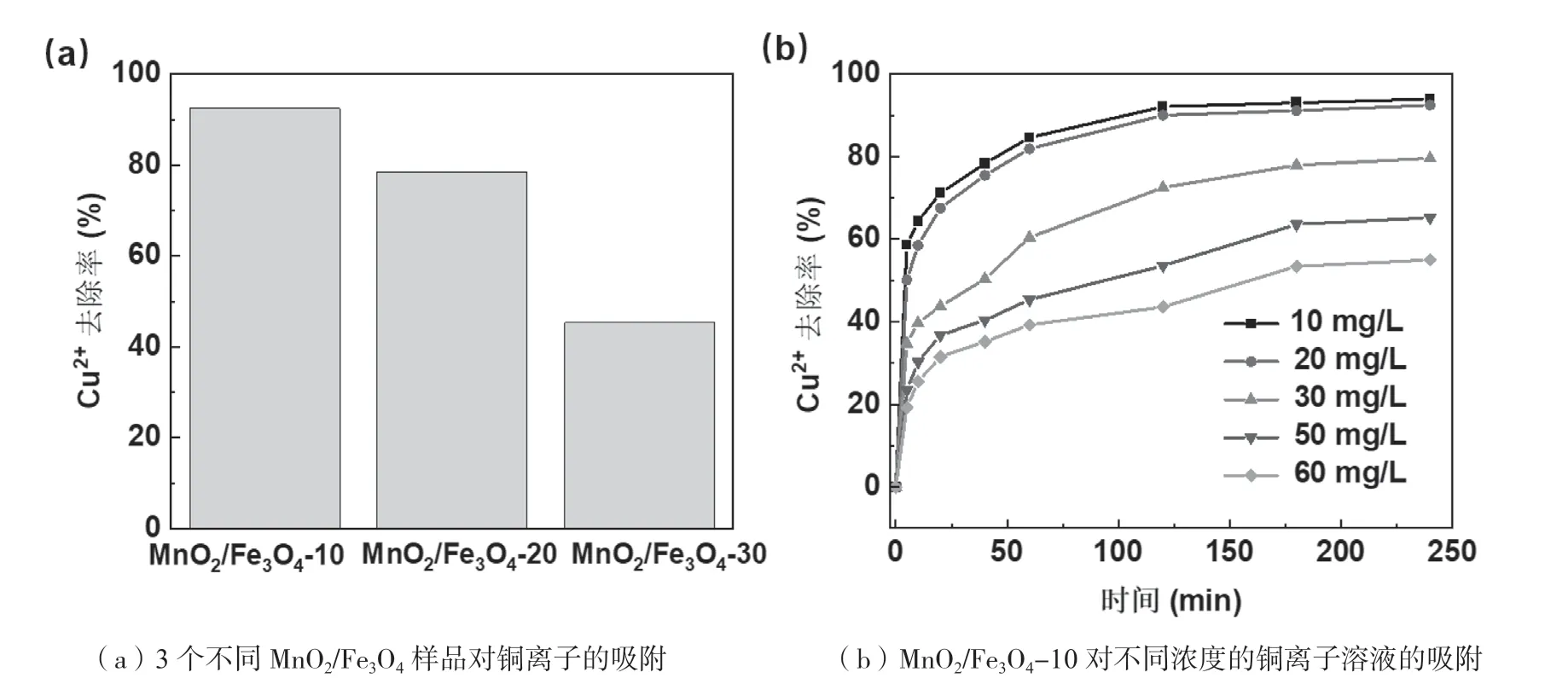
图3 对铜离子的吸附图
2.4 MnO2/Fe3O4对铜离子的吸附热力学、动力学研究
吸附等温线是指恒定环境温度下饱和吸附容量(q)与平衡浓度(C)之间的关系。采用Langmuir吸附等温线公式( 1)和Freundlich吸附等温线公式(2)分析了MnO/FeO-10对铜离子的吸附特征。

其中,为理论最大吸附量,K为Langmuir吸附平衡常数,K为Freundlich吸附平衡常数,=1,2,3…。图4(a)为Langmuir模型拟合数据图,图4(b)为Freundlich模型的拟合数据图。从图4(a)和图4(b)可知,Langmuir吸附等温线和Freundlich吸附等温线拟合的相关系数分别为0.9984和0.8197,这表明MnO/FeO-10对铜离子的吸附更符合Langmuir等温吸附,是一种单层吸附模式。另外,根据Langmuir模型计算可知,线形图的斜率为1/,因此MnO/FeO-10对铜离子的理论最大吸附量为72.5mg/g(1/0.138)。从理论最大吸附量数据可知,MnO/FeO-10对铜离子具有优异的吸附性能。
吸附动力学模型可表明吸附剂的吸附速率以及吸附过程可能的反应机理。因此,采用MnO/FeO-10对30mg/L铜离子溶液进行了吸附动力学研究。图4(c)和图4(d)分别为准一级动力学模型公式(3)和准二级动力学模型公式(4)的线性拟合图。

图4 数据图

其中,为拟一级动力学模型的速率常数,为拟二级动力学模型的速率常数。从图4(c)和图4(d)可知,准一级动力学模型和准二级动力学模型拟合的相关系数分别为0.9546和0.9966,这说明准二级动力学模型更符合MnO/FeO-10对铜离子的吸附特征。另外,试验平衡吸附量(qexp=62.1mg/g)与准二级动力学模型的计算值(qcal=60.6mg/g)接近,进一步说明了准二级动力学模型的匹配性。
3 结论
该研究首次以含锰废水为原料,采用了“以废治废”的策略,通过电絮凝技术及热处理,成功制备了MnO/FeO,同时有效处理了含锰废水。所制得的MnO/FeO-10对铜离子具有优异的吸附效果,理论最大吸附量为72.5 mg/g,其热力学吸附过程符合Freundlich模型,动力学吸附过程符合准二级动力学模型。表征分析认为,MnO/FeO-10的优异性能归功于分散的球形纳米颗粒形貌,因为其可提供较大的比表面积和较多的吸附活性位点。该文为电絮凝过程中污泥的回收利用提供了一种新的策略,扩展了重金属离子吸附剂的制备。
