正交试验筛选牛大力最佳切制工艺
2022-03-30李健王倩周改莲
李健 王倩 周改莲


【摘 要】 目的:通过正交试验筛选牛大力最佳切制工艺。方法:采用正交试验设计设置加工牛大力条件,通过紫外分光光度法、浸出物测定法等方法进行牛大力多糖、总黄酮和煎出物等指标的测定,制定综合评价规则进行结果分析。结果:3个因素对牛大力切制工艺影响程度依次为:A(蒸润时间)>B(切片厚度)>C(干燥温度),而各个因素不同水平的影响程度依次为:A1>A2>A3,B3>B2>Bd1,C2>C3>C1。结论:牛大力最佳切制工艺应为A1B3C2,即蒸润10 min,切3 mm片,60 ℃烘干。
【关键词】 切制工艺;正交试验;牛大力
【中图分类号】R283 【文献标志码】 A 【文章编号】1007-8517(2022)02-0040-04
Screening the Best Cutting Processing of Millettia speciosa Champ by Orthogonal Experimental Design
LI Jian1 WANG Qian2 ZHOU Gailian2*
1. School of Traditional Chinese Medicine Affiliated to Guangxi University of Traditional Chinese Medicine,
Nanning 530022, China;2.Guangxi University of Traditional Chinese Medicine, Nanning 530200, China
Abstract:Objective To screening the best Processing Conditions of Millettia speciosa Champ by orthogonal test. Methods Orthogonal design was used to set the processing conditions of Millettia speciosa Champ, the contents of polysaccharides, total flavonoids and decoctions were determined by UV spectrophotometry and extraction method, and made comprehensive evaluation rules to analyze the results.Result The influence of the three factors on the processing of Millettia is in the order of A (steaming time)>B (slice thickness)>C (drying temperature),and The influence degree of each factor at different levels is: A1>A2>A3, B3>B2>B1,C2>C3>C1. Conclusion The best cutting process of Millettia is A1B3C2, which is processing Millettia steaming for 10 min, cutting into 3 mm and drying at 60 ℃.
Key words:Cutting Process; Orthogonal Experimental Design; Millettia speciosa Champ
牛大力為豆科植物美丽崖豆藤Millettia speciosa Champ.的干燥块根[1],别名山莲藕、血藤、牛古大力、九龙串珠、大力薯[2],分布于广东、广西、海南等地,在广西梧州、玉林、百色、南宁、钦州等地均有产[3],也是广西壮族和仫佬族民间常用的草药[4]。炮制是处理中药的一种传统技术,也是中医用药的特点,目前对于牛大力炮制的研究和记载甚少。药材进行炮制时必须具合适炮制的形态,而牛大力根是根茎类药材,进行炮制处理时一般切片,切片薄,在炮制过程中易破碎,从而影响饮片外观和价格。反之,切片厚,在炮制处理过程中又难达到所需的效果,导致药材炮制不均匀,影响药材疗效。现在市面上牛大力多以整根和斜段为主,少见适用于炮制处理的片,因此对牛大力切制工艺进行探索具有重要意义,也能为今后牛大力饮片生产和炮制研究提供理论和实验依据。
1 仪器与材料
1.1 仪器 UV-1780型紫外可见分光光度计(岛津仪器有限公司);CPA225D型和SQP型电子天平(赛多利斯科学仪器有限公司);KQ5200B型超声波清洗器(昆山市超声仪器有限公司);HWS-26型电热恒温水浴锅(上海齐欣科学仪器有限公司);DHG-9140A型电热恒温鼓风干燥箱(上海齐欣科学仪器有限公司);DFY-500型中药粉碎机(温岭市林大机械有限公司)。
1.2 材料 硫酸(批号:20161202,成都金山化学试剂有限公司);乙醇(批号:2017122101,成都市科隆化学品有限公司);亚硝酸钠(批号:2016040191)和氢氧化钠(批号:2017102003)天津市致远化学试剂有限公司;硝酸铝(批号20170514,天津市科密欧化学试剂有限公司);芦丁对照品(批号:wkq16101104)和葡萄糖对照品(批号:wkq16082202)购自四川省维克奇生物科技有限公司;牛大力原药材购自玉林市玉州区喜运中药材购销部。
2 方法
2.1 供试品溶液制备
2.1.1 牛大力多糖供试品溶液制备 取牛大力样品0.5 g,精密称定,置于500 mL圆底烧瓶中,加入80%乙醇100 mL,冷凝回流1 h,过滤,取滤渣和滤纸置于圆底烧瓶中,加入100 mL水,沸水浴1 h,过滤,取滤液25 mL置于50 mL容量瓶中,定容至刻度,即得牛大力多糖供试品溶液。
2.1.2 牛大力总黄酮供试品溶液制备 取牛大力样品1.0 g,精密称定,置于25 mL具塞锥形瓶中,称重,精密移入60%乙醇10 mL,密封,超声45 min,取出,放至室温,60%乙醇补重,摇匀后抽滤,取滤液,即得牛大力总黄酮供试品。
2.1.3 牛大力煎出物供试品制备 取牛大力样品2 g,精密称定,置于250 mL具塞锥形瓶中,精密加入纯水50 mL,称定重量,静置1 h,接入冷凝回流装置,加热至沸腾,保持微沸状态1 h,取出,放置室温,用水补重,摇匀,过滤,精密移取滤液25 mL,置于干燥恒重的蒸发皿中,沸水浴挥干,即得牛大力煎出物。牛大力煎出物的测定参照药典通则2201(浸出物测定法之水溶性浸出物测定法:热浸法)[5]。
2.2 对照品溶液的制备
2.2.1 葡萄糖标准品溶液制备 精密称取葡萄糖对照品33.30 mg,置于100 mL洁净容量瓶中,加入适量水,超声溶解,放置室温后,加水定容至刻度,既得浓度为0.33 mg/mL葡萄糖对照品溶液。
2.2.2 芦丁标准品溶液制备 精密称取芦丁对照品25.15 mg,置于25 mL洁净容量瓶中,先加入适量60%乙醇,超声溶解后,放置室温,加60%乙醇定容刻度,既得浓度为1.01 mg/mL芦丁对照品溶液。
2.3 显色法及最大吸收波长选择
2.3.1 牛大力多糖供试品显色法及吸收波长的选择 取葡萄糖对照品溶液和牛大力多糖供试品溶液,各1 mL,分别置于10 mL具塞试管中,加水至2 mL,摇匀,加入0.2%蒽酮-硫酸溶液至10 mL,摇匀,冷却后沸水浴10 min,取出,立即冰水浴10 min;以相对应溶液为空白对照,在200~700 nm范围内进行全波长扫描,牛大力多糖供试品在波长583 nm处有最大吸收,因此选择583 nm作为测定波长。
2.3.2 牛大力总黄酮供试品显色法及吸收波长的选择 取芦丁对照品溶液和牛大力总黄酮供试品溶液,各3 mL,分别置于25 mL容量瓶中,加入浓度为5%的NaNO2溶液1 mL,混匀,静置6 min,加入浓度为10% 的Al(NO3)3溶液1 mL,混匀,静置6 min,加入浓度为4% 的NaOH溶液10 mL,再用30%乙醇溶液定容至刻度,混勻,静置15 min;以相对应溶液为空白对照,在200~700 nm范围内进行全波长扫描。牛大力总黄酮供试品溶液在409 nm处有吸收峰,因此选择483 nm作为牛大力总黄酮测定波长。
2.4 线性关系考察
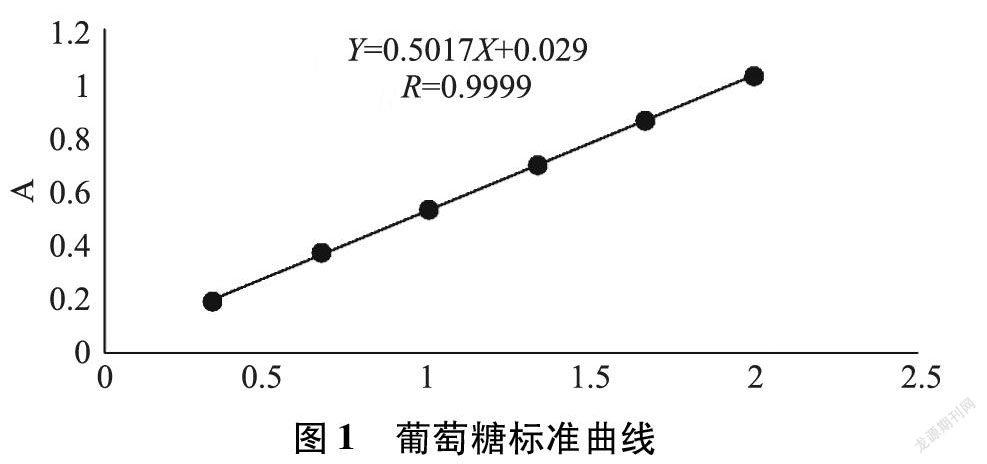
2.4.1 葡萄糖标准曲线绘制 精密移取“2.2.1”项下葡萄糖对照品溶液0.1 mL、0.2 mL、0.3 mL、0.4 mL、0.5 mL和0.6 mL,分别置于10 mL洁净具塞试管中,加水至2 mL,按“2.3.1”项下显色法显色,以相对应溶液为空白对照,在波长583 nm处测定其吸光度分别为0.1893、0.3711、0.5309、0.6977、0.8639、1.0298,以葡萄糖对照品浓度为横坐标X,吸光度值为纵坐标Y,绘制标准曲线如图1,得到标准曲线回归方程Y=0.5017X+0.029(R=0.9999),即浓度在0.3330~1.9980 mg/mL范围内,葡萄糖浓度与吸光度呈良好线性关系。
2.4.2 芦丁标准曲线绘制 精确移取“2.2.2”项下芦丁对照品溶液0.5 mL、1.0 mL、1.5 mL、4.0 mL、6.0 mL和8.0 mL,分别置于10 mL洁净的容量瓶中,用60%乙醇定容至刻度,摇匀,即得不同浓度的芦丁对照品溶液。分别取3 mL不同浓度对照品溶液分别置于25 mL容量瓶中,按“2.3.2”项下显色方法显色,以相对应溶液为空白对照,在波长483 nm处测定吸光度值分别为0.0654、0.1377、0.2123、0.5346、0.8334、1.0881,以芦丁对照品浓度作为横坐标x,吸光度值作为纵坐标y,绘制标准曲线如图2,得到标准曲线回归方程y=1.3576x+0.0006(R=0.9998),即浓度在0.0503~0.8048 mg/mL范围内,芦丁浓度与吸光度呈良好线性关系。
2.5 药材处理 鉴于中药材切制过程中可能会影响到药材有效成分含量的三个主要因素分别是蒸润时间、切片厚度和干燥温度,结合前期单因素分析结果,采用正交试验对蒸润时间(A)、切片厚度(B)和干燥温度(C)进行考察,因素水平表如1,选择了L9(34) 正交表,并按照正交表进行样品处理条件如表2。
2.6 多糖、总黄酮和煎出物测定
2.6.1 多糖含量测定 称取不同处理牛大力粉末,每个样品取3份,每份0.5 g,精密称定,共27份,按“2.1.3”项下供试品制备方法进行牛大力多糖供试品制备,再按 “2.3.1”项下显色方法显色,在波长582 nm处测定其吸光度,通过绘制的葡萄糖标准曲线计算器多糖含量,同一份样品取平均值作为该样品多糖含量,得出1~9号样品中多糖含量依次为41.46%、46.95%、40.16%、35.50%、36.17%、39.14%、36.30%、35.17%和35.86%。
2.6.2 总黄酮含量测定 称取不同处理牛大力粉末,每个样品取3份,每份1.0 g,精密称定,共27份,按“2.1.2”项下供试品制备方法进行牛大力总黄酮供试品制备,再按“2.3.2”项下显色方法显色后,在波长483 nm处测定其吸光度,通过绘制的芦丁标准曲线计算其总黄酮含量,同一份样品取平均值作为该样品总黄酮含量,得出1~9号样品中总黄酮含量依次为0.45%、0.48%、0.44%、0.38%、0.33%、0.34%和0.32%。
2.6.3 煎出物含量测定 称取不同处理牛大力粉末,每个样品取3份,每份2.0 g,精密称定,共27份,按“2.1.3”项下煎出物含量测定方法进行测定,同一份样品取平均值作为该样品煎出物含量,得出样品1~9号样品中煎出物含量依次为13.46%、11.00%、18.35%、11.54%、8.18%、11.09%、10.95%、10.40%和14.95%。
3 结果分析
3.1 测定指标的综合评分规则及综合评分结果 通过对文献统计,发现牛大力成分的研究主要集中在总黄酮和多糖类化合物的研究方面,且药理研究方面也主要以总黄酮、多糖和水煎液的药理活性研究为主,考虑到水煎液中含有总黄酮和多糖成分,因此设置权重系数为:多糖权重系数0.4、总黄酮权重系数0.4和煎出物权重系数0.2,综合评价指标按以下方法进行计算:
综合评分=M1(M1′ )×40%+M2(M2′ )×40%+M3(M3′)×20%)×100
M1为牛大力中多糖含量;
M1′为牛大力中多糖含量最大值;
M2为牛大力中总黄酮含量;
M2′为牛大力中总黄酮含量最大值;
M3为牛大力煎出物含量;
M3′为煎出物含量最大值。
根据上述计算公式,结合多糖、总黄酮和煎出物含量三个指标,对正交条件下处理的9个样品进行综合评分,得出1~9号样品综合得分依次为87.49、 92.25、 90.88、 74.49、 72.33、 77.10、 70.36、 69.63和73.51。
3.2 正交结果 基于对正交条件处理后9个牛大力样品中多糖、总黄酮和煎出物含量的测定及综合评分结果绘制牛大力切制正交试验结果表(表3),通过IBM SPSS Statistics 21进行方差分析结果如表4。
由表3可知,3个因素对牛大力切制工艺影响程度依次为:A(蒸润时间)>B(切片厚度)>C(干燥溫度),而各个因素不同水平的影响程度依次为:A1>A2>A3,B3>B2>B1,C2>C1>C3。由表4可知,因素A(蒸润时间)对牛大力切制工艺测定指标的综合性评分有显著性影响(P<0.05),而因素B(切片厚度)和C(蒸润时间)对牛大力切制工艺测定指标的综合性评分没有显著性影响(P>0.05),结合上述正交试验结果分析,牛大力最佳切制工艺应为A1B3C2,即蒸润10 min,切3 mm片,60 ℃烘干。
参考文献
[1]
广西壮族自治区食品药品监督管理局.广西壮族自治区壮药质量标准[M].南宁:广西科学技术出版社,2008:61.
[2]黄泰康,丁志遵,赵守训,等.现代本草纲目(上册)[M].北京:中国医药科技出版社,2008:504.
[3]广西壮族自治区卫生厅.广西中药材标准[M].南宁:广西科学技术出版社,1992:159-160.
[4] 黄燮才.广西民族药简编[M].南宁:广西壮族自治区卫生局药品检验所,1980:135.
[5] 国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015:202.
(收稿日期:2021-05-25 编辑:刘 斌)
