刺苞老鼠簕的化学成分及其抗炎和抗氧化活性研究
2022-03-29贾慧珍鲁建美许又凯
贾慧珍,孙 朋,鲁建美,吴 敏,许又凯
1中国科学院西双版纳热带植物园 热带植物资源可持续利用重点实验室,勐腊 666303;2中国科学院大学,北京 100049
爵床科(Acanthaceae)约有229属,3 450种[1]。我国约有68属311种,以云南地区种类最多。老鼠簕属(Acanthus)全球有30余种,其中有三种分布在中国,分别为老鼠簕Acanthusilicifolius,刺苞老鼠簕A.lecucostachyus和小花老鼠簕A.ebracteatus。在泰国传统医药中,老鼠簕属植物常被用作泻下、抗炎、治疗风湿性关节炎、退热、抗脓肿、抗溃疡等,其叶子被用于治疗风湿病、蛇咬、麻痹和哮喘,也可与胡椒一起作为滋补剂使用[2]。刺苞老鼠簕A.lecucostachyus,又名蛤蟆花,产云南南部且主要分布于西双版纳海拔550~1150米的密林中潮湿处,中南半岛及印度也有分布[3]。傣名为“帕夯喃”,是传统的傣药,在多部傣医药经书中均有记载[4,5],主要用于治疗肾结石。据《中国傣药志》[4]中记载刺苞老鼠簕气微,味淡,凉,入水、土塔,归肾、膀胱经,全草入药具有清热解毒,利尿化石的功效,并与盾翅藤、水红木和肾茶等共同煎服治疗慢性肾炎。傣医使用刺苞老鼠簕治疗疾病已有上千年历史,并有明确疗效,已收入2005年版第三册傣族药《云南省中药材标准》[5]中的法定药材,是傣医常用草药之一,具有重要的药用价值。Huo等[6]综述国内外老鼠簕属植物的化学成分多为木脂素类、苯乙醇苷类、黄酮类、三萜类等。Babu等[7]通过药理实验表明老鼠簕叶子具有抗氧化和抗肿瘤等活性。虽然刺苞老鼠簕已列为云南省法定药材,但《云南省中药材标准》[5]只做了药材的生药鉴定和薄板层析等,刺苞老鼠簕的化学成分和药理活性仍为空白。因此,本文对刺苞老鼠簕的化学成分进行了研究,并对其化合物进行抗氧化和抗炎活性筛选,为刺苞老鼠簕的药用提供依据。
1 材料与方法
1.1 仪器与材料
AVANCE III 500MHz核磁共振波谱仪(德国Bruker公司);Avance III 600MHz核磁共振波谱仪(瑞士布鲁克公司);UPLC-IT-TOF液相-离子阱飞行时间色谱质谱联用仪(岛津制作所);多功能荧光酶标仪+摇床Varioskan Flash(美国Thermofisher);Waters 600型高效液相色谱仪配备Waters 2996二极管阵列紫外检测器(美国Waters公司),色谱柱为YMC-Pack ODS-A(300 mm×10 mm,S-5 μm)半制备柱(TMS作内标);柱层层析硅胶(200~300目)和GF254薄层色谱硅胶购自青岛海洋化工厂分厂;薄层层析硅胶(10~40 μm)购自青岛美高化工有限公司;Sephadex LH-20(40~70 μm)购自瑞典GE Healthcare Bio-Sciences AB公司;EYELA油浴锅OSB-2100 和旋转蒸发仪N-1100(上海爱朗仪器有限公司);倒置生物显微镜NIB-100(宁波永新光学股份有限公司);台式离心机TDL-40B(上海安亭科学仪器厂);生物安全柜BSC-1100IIB2-X 和CO2细胞培养箱QP-80(济南鑫贝西生物技术有限公司);小鼠单核巨噬细胞RAW 264.7(中科院上海细胞库);DMEM培养基和胎牛血清(BI公司);Griess Reagent、LPS及对照药物L-NMMA(Sigma公司);乙酸乙酯、甲醇、二氯甲烷、石油醚、浓硫酸等试剂均为分析纯购自天津市大茂化学试剂厂。
刺苞老鼠簕全草A.lecucostachyus于2019年8月采自于云南省西双版纳傣族自治州勐腊县勐腊镇补蚌村,经中科院西双版纳热带植物园肖春芬高级实验员鉴定,标本(No.60099)存放于中科院西双版纳热带植物园标本馆。
1.2 实验方法
1.2.1 提取分离
取干燥的刺苞老鼠簕全草3.8 kg,粉碎,室温下用甲醇浸泡浸提3次(七天/次),合并提取液,滤过,减压浓缩得总浸膏515 g。将总浸膏加适量纯水混匀,使其充分溶解,用乙酸乙酯萃取8次,减压浓缩得到乙酸乙酯部位(186 g)。乙酸乙酯部位经大孔树脂(纯水、30%、60%、90%、丙酮)洗脱,得到5个组分(Fr.1~5)。Fr.3经硅胶(200~300目)柱色谱(二氯甲烷-甲醇梯度)洗脱后,得到3个部分(A.1、A.2、A.3),其中A.1经薄层层析硅胶柱色谱,反复硅胶柱色谱(石油醚-乙酸乙酯梯度)洗脱以及重结晶得到化合物1(461.8 mg)。A.2经反复硅胶柱色谱,再经SephadexLH-20凝胶柱色谱分离纯化,甲醇洗脱,得到化合物2(1.3 mg)。A.3经硅胶柱(200~300目)分离,再经硅胶柱(10~40 μm)分离,用不同溶剂体系(二氯甲烷-甲醇,石油醚-乙酸乙酯)洗脱,得到化合物3(2.6 mg)、4(13.5 mg)和5(13.0 mg)。A.3组分经反复硅胶柱色谱得到化合物6(9.0 mg)和7(1.6 mg)。Fr.4经硅胶柱色谱(二氯甲烷-甲醇)洗脱,洗脱物经SephadexLH-20凝胶色谱,TLC检测合并相同部分,再经薄层层析硅胶柱色谱洗脱得到化合物8(2.8 mg)和9(45.7 mg),过半制备HPLC(乙腈-纯水40∶60)分离得到化合物10(12.5 mg)。Fr.2经硅胶柱(200~300目)色谱分离,TLC检测并合并相同馏分,经反复硅胶柱色谱层析分离,得到化合物11(6.8 mg)、12(5.9 mg)和13(2.9 mg)。
1.2.2 活性筛选
通过DPPH自由基清除实验对分离得到的化合物进行抗氧化活性筛选,准备好与化合物对应的EP管,终浓度为100 μM,在96孔板进行分组,每组设置三个复孔,空白对照组加入100 μL无水乙醇,实验组加入100 μL待测化合物,将DPPH工作液分别加入96孔板分组中,避光反应30 min后,在517 nm处测吸光值。
将RAW 264.7细胞接种在96孔板,用1 μg/mL LPS进行诱导刺激,同时加入待测化合物处理至50 μM,设置不含药物组和L-NMMA阳性药物组为对照。对细胞进行培养后,取培养基检测NO生成,在570 nm处测定吸光值。在剩余的培养基加入MTS进行细胞存活率检测,排除化合物毒性影响。
NO生成抑制率=(OD非药物处理组-OD样品组)/
OD非药物处理组× 100%
2 实验结果
2.1 结构鉴定
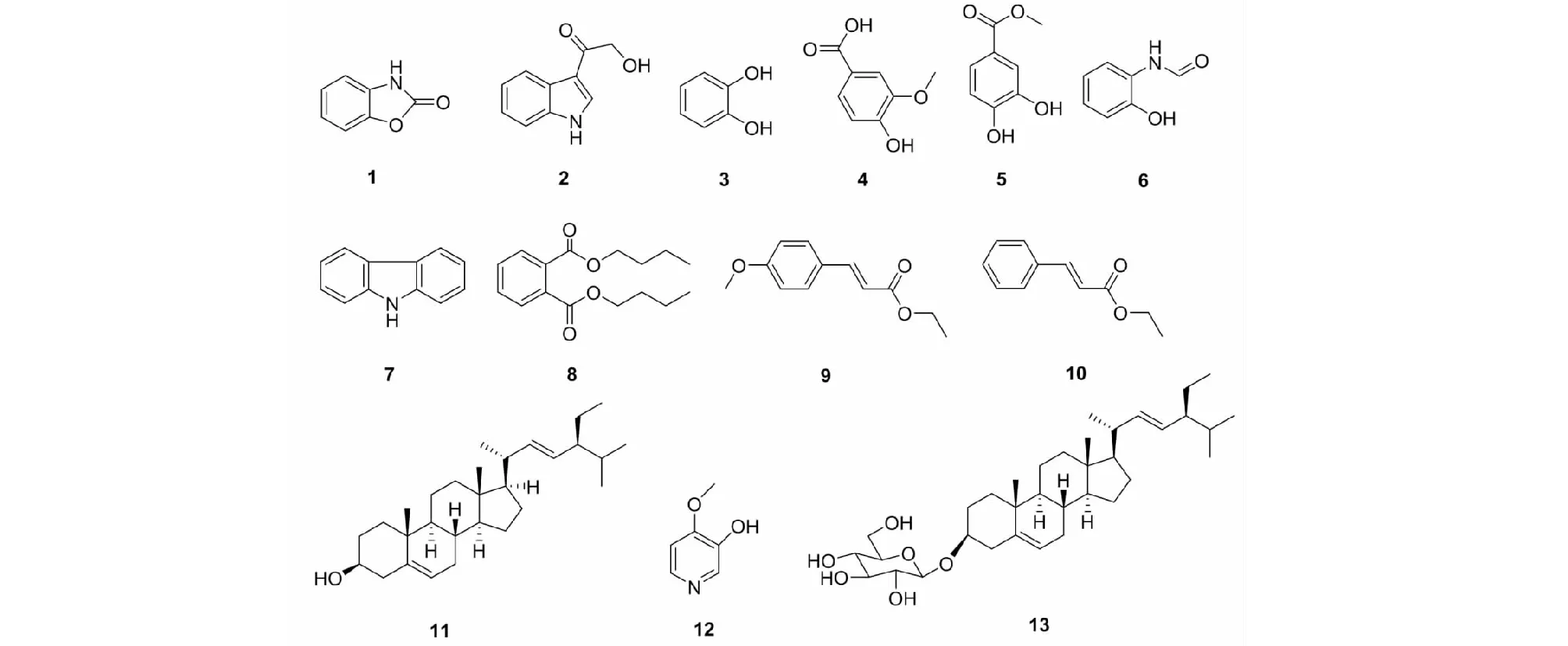
图1 化合物1~13的化学结构Fig.1 The chemical structures of compounds 1-13
化合物1白色粉末,可形成晶体(甲醇);EI-MS:m/z136 [M+H]+,分子式为C7H5NO2。1H NMR(500 MHz,CD3OD)δ:7.21~7.18(1H,m,H-7),7.14(1H,dd,J= 7.6,1.0 Hz,H-4),7.10(1H,dd,J= 7.8,1.2 Hz,H-6),7.06(1H,dd,J= 4.7,4.1 Hz,H-5);13C NMR(125 MHz,CD3OD)δ:157.2(C-2),123.4(C-4),110.9(C-5),110.7(C-6),125.1(C-7),131.6(C-8),145.4(C-9)。以上数据与文献[8]基本一致,故鉴定为2-苯并噁唑啉酮(结构见图1)。
化合物2浅黄色晶体(甲醇);ESI-MS:m/z176 [M+H]+、174 [M-H]-,分子式为C10H9NO2。1H NMR(500 MHz,CD3OD)δ:8.23(1H,s,H-2),8.19(1H,d,J= 8.0 Hz,H-4),7.45(1H,d,J= 8.0 Hz,H-7),7.22(2H,s,H-5,H-6),4.72(2H,s,H-9);13C NMR(125 MHz,CD3OD)δ:195.8(C-8),137.9(C-7a),134.1(C-2),127.1(C-3a),124.3(C-6),123.3(C-5),122.7(C-7),115.0(C-4),113.0(C-3),65.7(C-9)。以上数据与文献[9]基本一致,故鉴定为3-羟基乙酰基吲哚。
化合物3无色针晶(甲醇);ESI-MS:m/z109 [M-H]-,分子式为C6H6O2。1H NMR(500 MHz,CD3OD)δ:6.75(2H,m,H-3,H-5),6.65(2H,m,J= 9.5,3.5 Hz,H-4,H-6);13C NMR(125 MHz,CD3OD)δ:146.4(C-1,C-2),120.9(C-4,C-5),116.4(C-3,C-6)。以上数据与文献[10]基本一致,故鉴定为儿茶酚。
化合物4白色片状结晶(甲醇);ESI-MS:m/z167 [M-H]-,分子式为C8H8O4。1H NMR(500 MHz,CD3OD)δ:7.57(1H,d,J= 1.9 Hz,H-2),7.47(1H,dd,J= 8.2,1.9 Hz,H-6),6.75(1H,d,J= 8.2 Hz,H-5),3.87(3H,s,-OCH3);13C NMR(125 MHz,CD3OD)δ:175.6(C = O),150.1(C-3),148.2(C-4),130.5(C-6),124.1(C-1),115.0(C-2),114.2(C-5),56.4(-OCH3)。以上数据与文献[9]基本一致,故鉴定为香草酸。
化合物5无色粉末;EI-MS:m/z169 [M+H]+,分子式为C8H8O4。1H NMR(500 MHz,CD3OD)δ:7.54(1H,dd,J= 8.2,1.9 Hz,H-6),7.52(1H,d,J= 1.9 Hz,H-2),6.82(1H,d,J= 8.2 Hz,H-5),3.88(3H,s,-OCH3);13C NMR(125 MHz,CD3OD)δ:170.0(C = O),152.7(C-1),148.7(C-3),125.2(C-6),123.1(C-4),116.0(C-2),113.90(C-5),56.4(-OCH3)。以上数据与文献[11]基本一致,故鉴定为methyl 3,4-dihydroxy-benzoate。
化合物6淡黄色粉末;ESI-MS:m/z138 [M+H]+,分子式为C7H7NO2。1H NMR(500 MHz,CD3OD)δ:8.27(1H,s,H-8),7.97-7.92(1H,dd,J= 8.1,1.3 Hz,H-5),6.97-6.92(1H,dt,J= 1.5,8.1 Hz,H-3),6.83(1H,dd,J= 8.1,1.3 Hz,H-4),6.80-6.76(1H,dt,J= 8.1,1.5 Hz,H-2);13C NMR(125 MHz,CD3OD)δ:161.9(C-8),148.6(C-4),126.8(C-5),126.2(C-2),122.6(C-1),120.4(C-6),116.3(C-3)。以上数据与文献[12]基本一致,故鉴定为N-(2-hydroxyphenyl) formamide。
化合物7白色粉末;ESI-MS:m/z168 [M+H]+,分子式为C12H9N。1H NMR(500 MHz,CD3OD)δ:8.05~8.01(2H,dt,J= 8.1,0.9 Hz,H-1,H-9),7.42(2H,dt,J= 8.1,0.9 Hz,H-3,H-12),7.34(2H,ddd,J= 8.2,7.1,1.2 Hz,H-4,H-11),7.13(2H,ddd,J= 8.0,7.1,1.0 Hz,H-5,H-10);13C NMR(125 MHz,CD3OD)δ:141.5(C-2,C-13),126.7(C-7,C-8),124.3(C-4,C-11),121.1(C-1,C-9),119.5(C-5,C-10),111.7(C-3,C-12)。以上数据与文献[13]基本一致,故鉴定为咔唑。
化合物8无色油状物;ESI-MS:m/z279[M+H]+,分子式为C16H22O4。1H NMR(500 MHz,CD3OD)δ:7.68~7.65(2H,m,H-2,H-5),7.56(2H,dt,J= 5.8,2.9 Hz,H-3,H-4),4.23(4H,t,J= 6.6 Hz,H-13,H-16),1.71~1.62(4H,m,H-14,H-15),1.44~1.3(4H,m,H-17,H-20),0.93(6H,t,J= 7.1 Hz,H-18,H-19);13C NMR(125 MHz,CD3OD)δ:169.3(C-7,C-10),133.6(C-1,C-2),132.4(C-4,C-5),129.9(C-3,C-6),66.7(C-13,C-16),31.7(C-14,C-15),20.3(C-17,C-20),14.1(C-18,C-19)。以上数据与文献[14]基本一致,故鉴定为邻苯二甲酰正二丁酯。
化合物9无色针晶;ESI-MS:m/z207 [M+H]+,分子式为C12H14O3。1H NMR(500 MHz,CD3OD)δ:7.68(2H,d,J= 10 Hz,H-2,H-6),6.89(3H,m,overlapped,H-1′,H-3,H-5),5.81(1H,d,J= 12.8 Hz,H-2′),4.16(2H,q,J= 7.1 Hz,H-1′′),3.80(3H,s,-OCH3),1.25(3H,t,J= 7.1 Hz,H-2′′);13C NMR(125 MHz,CD3OD)δ:168.4(C-3′),161.8(C-4),144.3(C-1),133.3(C-1′),117.8(C-2,C-6),114.2(C-3,C-5),61.1(C-1′′),55.8(-OCH3),14.1(C-2′)。以上数据与文献[15]基本一致,故鉴定为ethylp-methoxy-trans-cinnamate。
化合物10白色蜡状物;ESI-MS:m/z177 [M+H]+,分子式为C11H12O2。1H NMR(500 MHz,CD3OD)δ:7.67(1H,d,J= 16.0 Hz,H-7),7.59(2H,m,H-2,H-6),7.40(3H,dd,J= 9.5,6.0 Hz,H-3,H-4,H-5),6.51(1H,dd,J= 16.0,1.1 Hz,H-8),4.23(2H,q,J= 7.1 Hz,H-10),1.30(3H,m,H-11);13C NMR(125 MHz,CD3OD)δ:168.7(C-9),146.1(C-7),135.7(C-1),131.5(C-4),130.0(C-3,C-5),129.2(C-2,C-6),119.0(C-8),61.6(C-10),14.7(C-11)。以上数据与文献[16]基本一致,故鉴定为肉桂酸乙酯。
化合物11白色针状晶体(氯仿);ESI-MS:m/z413 [M+H]+,分子式为C29H48O。1H NMR(500 MHz,CDCl3)δ:5.34(1H,dd,J= 3.4,1.8 Hz,H-6),5.15(1H,dd,J= 15.2,8.6 Hz,H-22),5.02(1H,dd,J= 15.2,8.7 Hz,H-23),3.52(1H,ddd,J= 15.2,10.9,4.5 Hz,H-3),1.01(3H,q,J= 6.5 Hz,H-19),0.90(3H,d,J= 6.5 Hz,H-21),0.86~0.78(3H,overlapped,H-26,H-27,H-29),0.68(3H,d,J= 9.2 Hz,H-18);13C NMR(125 MHz,CDCl3)δ:140.8(C-5),138.4(C-22),129.4(C-23),121.9(C-6),71.9(C-3),57.0(C-14),56.1(C-17),51.4(C-9),50.2(C-24),42.4(C-4,C-13),40.6(C-20),39.7(C-12),37.4(C-1),36.7(C-10),32.0(C-7,C-2,C-25),31.8(C-8),29.0(C-16),25.5(C-28),24.5(C-15),21.3(C-21),21.1(C-11,C-27),19.6(C-26),19.1(C-29),12.3(C-19),12.1(C-18)。以上数据与文献[17]基本一致,故鉴定为豆甾醇。
化合物12无色油状物;ESI-MS:m/z126 [M+H]+,分子式为C6H7NO2。1H NMR(500 MHz,CD3OD)δ:7.57(1H,s,H-2),7.47(1H,dd,J= 8.2,1.8 Hz,H-6),6.76-6.73(1H,m,H-5),3.87(3H,s,CH3);13C NMR(125 MHz,CD3OD)δ:150.2(C-4),148.1(C-3),124.2(C-6),115.4(C-2),114.0(C-5),56.2(-OCH3)。以上数据与文献[18]基本一致,故鉴定为3-hydroxy-4-methoxypyridine。
化合物13浅黄色粉末;ESI-MS:m/z592 [M+NH4]+、597[M+Na]+,619[M+COOH]-,分子式为C35H58O6。1H NMR(500 MHz,CDCl3∶CD3OD = 3∶1)δ:5.30(1H,s,H-6),5.08(1H,dd,J= 15.1,8.6 Hz,H-22),4.95(1H,dd,J= 15.2,8.8 Hz,H-23),4.34(1H,d,J= 7.8 Hz,H-1′),3.51(1H,m,H-3),1.19(3H,s,H-21),0.94(3H,s,H-19),0.77(3H,d,J= 6.1 Hz,H-26),0.63(3H,s,H-18);13C NMR(125 MHz,CDCl3∶CD3OD = 3∶1)δ:140.2(C-5),138.4(C-22),129.2(C-23),122.3(C-6),101.1(C-1′),79.2(C-3),76.3(C-3′),75.7(C-5′),73.5(C-2′),70.2(C-4′),61.9(C-6′),56.8(C-14),56.1(C-17),51.2(C-9),50.2(C-24),42.2(C-13),40.5(C-12),39.6(C-20),38.7(C-4),37.2(C-1),36.8(C-10),31.9(C-7),31.9(C-8),31.9(C-25),29.7(C-2),28.9(C-16),25.4(C-28),24.3(C-15),21.2(C-11),21.1(C-21),19.3(C-27),19.2(C-19),18.9(C-26),12.2(C-29),12.0(C-18)。以上数据与文献[19]基本一致,故鉴定为豆甾醇-3-O-β-D-吡喃葡萄糖苷。
2.2 活性筛选
清除DPPH自由基[20]初筛实验结果表明(见表1),化合物1~13均具有一定的抗氧化活性,其中化合物3和6的DPPH自由基清除率较高,表现出较好的抗氧化活性。对其进一步复筛,计算其IC50值,分别为105.18、299.89 μM。
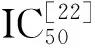
3 讨论与结论
本研究对刺苞老鼠簕的化学成分进行分析,从刺苞老鼠簕全草甲醇提取物的乙酸乙酯部位中分离鉴定了13个化合物,其中包括5个生物碱(其中1、6为苯并噁唑啉酮类生物碱,2为吲哚类生物碱,7为β-卡波林类生物碱、12为吡啶类生物碱)、2个苯丙素类及2个甾醇类化合物。苯并噁唑啉酮类生物碱为老鼠簕属的主要和特征性成分,与文献报道的同属植物的化学成分相同[23]。在自然条件下,苯并噁唑嗪酮也可降解为苯并噁唑啉酮,是禾本科作物中重要的次生代谢产物,可通过抑制叶绿体的光合磷酸化抑制一些幼苗生长,其作为除草剂的研制开发具有广阔的应用前景[24]。咔唑生物碱为首次在老鼠簕属植物中分离得到。咔唑是芸香科植物的主要成分,不仅可插入DNA,还能抑制端粒酶和调节蛋白磷酸化,其在天然产物抗癌治疗中扮演着重要的角色[25]。化合物中儿茶酚(3)不仅显示了较好的清除DPPH自由基的能力,而且体外抗炎实验中也显示了较好的活性。Ramalingam等[26]研究中也表明儿茶酚衍生物具有较好的抗氧化活性,其治疗慢性肾炎的作用机制还需要进一步研究探讨。

表1 化合物1~13的抗氧化活性筛选Table 1 Screening of antioxidant activities of the compounds 1-13

表2 化合物1~10的抗炎活性筛选Table 2 Anti-inflammatory activity screeningof the compounds 1-10
