恩替卡韦联合阿德福韦酯在乙型肝炎肝硬化失代偿期患者中的应用分析
2022-03-27毕丽霞
毕丽霞

摘 要:目的 探究乙型肝炎肝硬化失代偿期患者应用恩替卡韦联合阿德福韦酯的治疗效果。方法 选取2019年1月~2021年4月中国人民解放军联勤保障部队第九六零医院淄博医疗区感染科收治的100例乙型肝炎肝硬化失代偿期患者为研究对象,以随机数表法分为对照组和观察组,每组50例。两组患者均接受基础治疗,抗病毒治疗中分别应用阿德福韦酯、恩替卡韦联合阿德福韦酯,持续治疗6个月后,比较两组患者治疗效果、治疗前后肝功能指标[谷丙转氨酶(ALT)、总胆红素(TBIL)、白蛋白(ALB)、凝血酶原时间(PT)]、乙型肝炎病毒表达相关指标[乙肝病毒DNA(HBV-DNA)、乙肝病毒e抗原(HBeAg)]水平、肝硬化相关指标[透明质酸(HA)、人粘连蛋白(LN)、Ⅲ型前胶原氨基端肽(PⅢNP)、Ⅳ型胶原(CⅣ)]及不良反应发生率。结果 观察组治疗总有效率高于对照组,差异有统计学意义(P<0.05);治疗前,两组ALT、TBIL、ALB、PT水平相近,差异均无统计学意义(P>0.05);治疗后,观察组ALT、TBIL、PT水平均低于对照组,ALB水平高于对照组,差异均有统计学意义(P<0.05);治疗前,两组HBV-DNA、HBeAg水平相近,差异均无统计学意义(P>0.05);治疗后,观察组HBV-DNA、HBeAg水平均低于对照组,差异均有统计学意义(P<0.05);治疗前,两组HA、LN、PⅢNP、CⅣ水平相近,差异均无统计学意义(P>0.05);治疗后,观察组HA、LN、PⅢNP、CⅣ水平均低于对照组,差异均有统计学意义(P<0.05);观察组不良反应发生率与对照组相近,差异无统计学意义(P>0.05)。结论 对乙型肝炎肝硬化失代偿期患者应用恩替卡韦联合阿德福韦酯抗病毒治疗,与单纯应用阿德福韦酯治疗相比,可进一步提升治疗效果,改善肝功能指标、抑制病毒基因表达、改善肝硬化程度,且治疗安全性良好。
关键词:乙型肝炎肝硬化;失代偿期;抗病毒治疗
中图分类号:R512.62 文献标识码:A 文章编号:1009-8011(2022)-6-0-04
乙型肝炎肝硬化失代偿期为消化内科常见疾病,主要特征为肝脏慢性弥漫性结缔组织增生、肝细胞坏死、肝小叶结构损伤,并出现门静脉高压、肝功能减退等症状,严重时会引发消化道出血、腹腔积液,威胁患者生命安全[1-2]。在对乙型肝炎肝硬化失代偿期患者常规治疗中,以控制感染、保护患者肝脏功能为主,在此基础上,需联合抗病毒治疗,以清除乙肝病毒,减少患者肝功能损伤。阿德福韦酯为单磷酸腺苷无环核苷类似物,通过抑制乙型肝炎病毒(HBV)DNA多聚酶工作过程,以抑制HBV逆转录过程,但单一用药存在一定耐药性[3]。恩替卡韦为乙型病毒性肝炎常见治疗药物,通过抑制HBV活性、抑制乙型肝炎复制,以抑制病毒表达、减轻其肝功能损伤,且耐药性低[4]。为此,本研究选取中国人民解放军联勤保障部队第九六零医院淄博医疗区感染科收治的100例乙型肝炎肝硬化失代偿期患者为研究对象,分析上述两种抗病毒药物联合的治疗价值。
1 资料与方法
1.1 一般资料
选取2019年1月~2021年4月中国人民解放军联勤保障部队第九六零医院淄博医疗区感染科收治的100例乙型肝炎肝硬化失代偿期患者为研究对象,以随机数表法分为对照组和观察组,每组50例。对照组男29例,女21例;年龄31~70岁,平均年龄(48.76±6.15)岁;病程3~14年,平均病程(8.76±1.10)年。观察组男26例,女24例,年龄32~75岁,平均年龄(49.11±5.88)岁;病程5~18年,平均病程(8.83±1.23)年。两组患者一般资料比较,差异无统计学意义(P>0.05)。两组患者均对本研究内容知情,并签署知情同意书,通过中国人民解放军联勤保障部队第九六零医院淄博医疗区感染科医学伦理委员会批准。
1.2 纳入与排除标准
纳入标准:①均符合《慢性乙型肝炎防治指南(2015年版)》[5]乙型肝炎肝硬化失代偿期诊断标准:乙肝肝硬化病史≥3年,谷丙转氨酶(ALT)为31~400 U/L;②年龄18~75岁;
③近6个月内未接受抗病毒治疗。
排除标准:①合并甲状腺疾病者;②有既往精神病史、癫痫史者;③合并其他病毒感染者;④合并自身免疫系统疾病者;⑤2度以上肝昏迷者;⑥α2-抗胰蛋白酶缺乏者;⑦心肾等脏器严重功能障碍者;⑧肝豆状核变性者;⑨研究期间退出者。
1.3 方法
两组患者均接受基础治疗:①甘草酸二铵(生产企业:正大天晴药业集团股份有限公司,国药准字H10940190,规格:10 mL/50 mg)静脉滴注,150 mg甘草酸二铵+250 mL 10%葡萄糖注射液缓慢静脉滴注,1次/d;②還原型谷胱甘肽(生产企业:上海复旦复华药业有限公司,国药准字H20031265,规格:0.6 g/瓶)静脉滴注,0.6 g还原型谷胱甘肽+100 mL 0.9%氯化钠注射液静脉滴注,1次/d;③结合患者药敏结果实施抗感染治疗,并结合其实际情况实施利尿、滴注血浆等治疗。
对照组在基础治疗中,应用阿德福韦酯片(生产企业:福建广生堂药业股份有限公司,国药准字H20070198,规格:10 mg/片)口服,10 mg/次,1次/d。
观察组在对照组治疗基础上,应用恩替卡韦分散片(生产企业:海南中和药业股份有限公司,国药准字H20100064,规格:0.5 mg/片)口服,0.5 mg/次,1次/d。
两组口服药物均持续治疗6个月后,进行疗效评价。
1.4 观察指标
①比较两组治疗有效率:参考孙海英等[6]文献中相关标准。显效:临床体征消失,凝血功能、肝功能等指标均改善,无复发;有效:临床体征改善,凝血功能、肝功能指标缓解,无复发;无效:未能达到上述标准。总有效率=(显效+有效)例数/总例数×100%。
②比较两组患者治疗前后肝功能指标:谷丙转氨酶(ALT)、总胆红素(TBIL)、白蛋白(ALB)、凝血酶原时间(PT)。以全自动生化分析仪(生产企业:迈瑞公司,型号:BS280)检验、全自动凝血分析仪(生产企业:普利生公司,型号:C2000-A)检验。
③比较两组患者治疗前后乙型肝炎病毒表达相关指标水平:包括乙肝病毒DNA(HBV-DNA)、乙肝病毒e抗原(HBeAg),以荧光定量分析仪(生产企业:博日公司,型号:9600)检验。
④比较两组患者治疗前后肝硬化相关指标水平:包括透明质酸(HA)、人粘连蛋白(LN)、Ⅲ型前胶原氨基端肽(PⅢNP)、Ⅳ型胶原(CⅣ),以化学发光检测仪(生产企业:北京滨松光子公司,型号:BHP9507)。
⑤比较两组治疗不良反应发生率。不良反应包括头痛、眩晕、恶心、腹部不适等。不良反应发生率=(头痛+眩晕+恶心+腹部不适)例数/总例数×100%。
1.5 统计学分析
采用SPSS 22.0统计学软件处理研究数据,计量资料用(x±s)表示,采用t检验比较;计数资料用[n(%)]表示,采用字2检验比较,P<0.05表示差异具有统计学意义。
2 结果
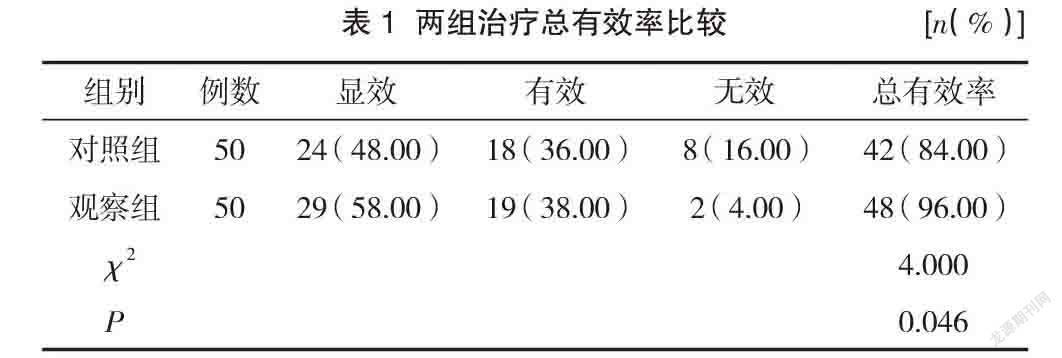
2.1 两组治疗总有效率比较
观察组治疗总有效率高于对照组,差异有统计学意义(P<0.05)。见表1。
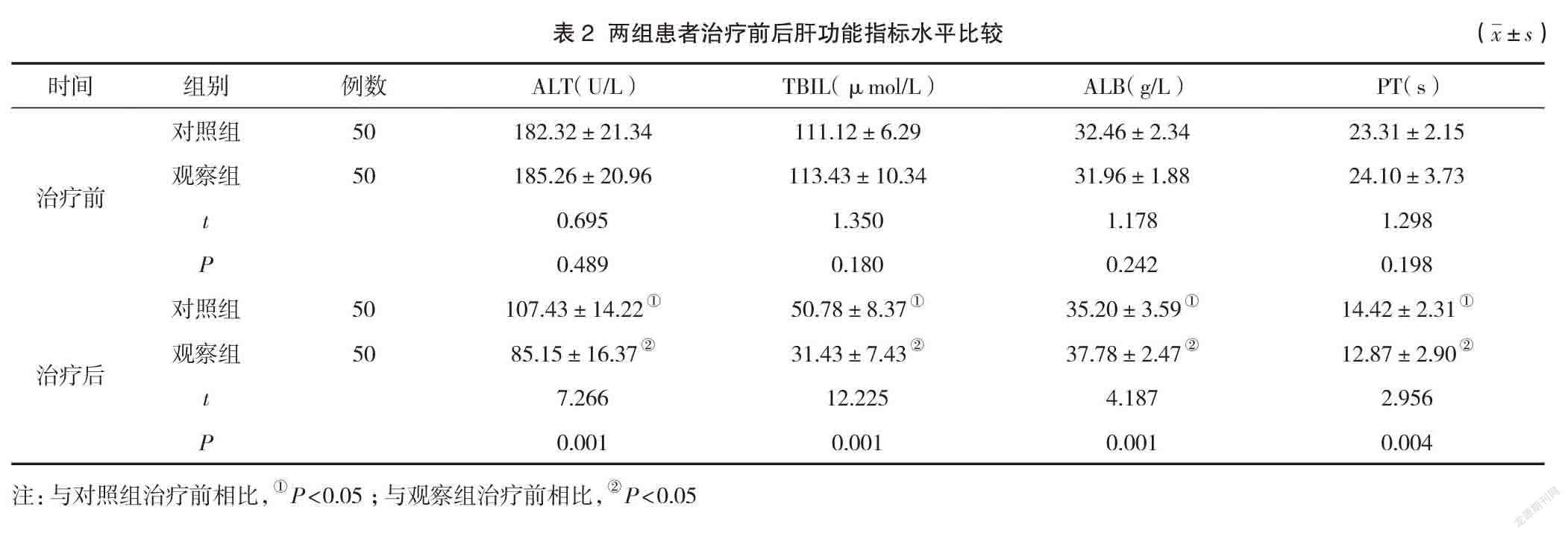
2.2 两组患者治疗前后肝功能指标水平比较
治疗前,两组患者肝功能指标水平相近,差异均无统计学意义(P>0.05);治疗后,观察组患者ALT、TBIL、PT水平均低于对照组,ALB水平高于对照组,差异均有统计学意义(P<0.05)。见表2。
2.3 两组患者治疗前后乙型肝炎病毒表达相关指标水平比较
治疗前,两组患者乙型肝炎病毒表达相关指标水平相近,差异均无统计学意义(P>0.05);治疗后,观察组患者HBV-DNA、HBeAg水平均低于对照组,差异均有统计学意义(P<0.05)。见表3。
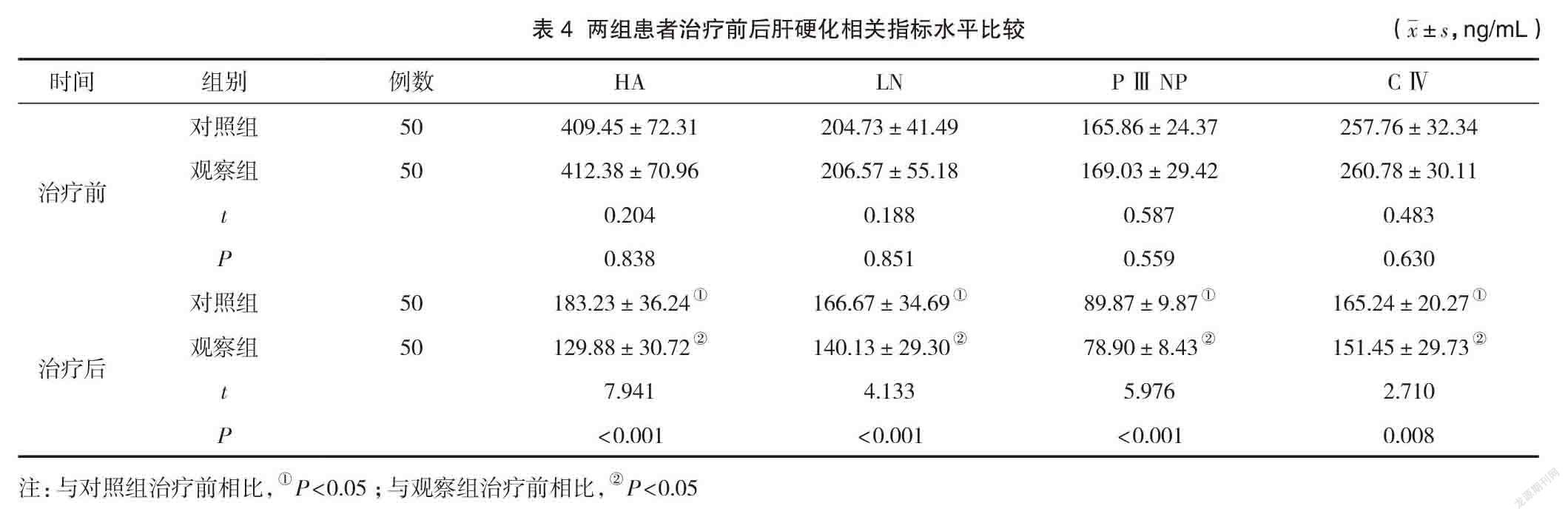
2.4 两组患者治疗前后肝硬化相关指标水平比较
治疗前,两组患者肝硬化相关指标水平相近,差异均无统计学意义(P>0.05);治疗后,观察组HA、LN、PⅢNP、CⅣ水平均低于对照组,差异均有统计学意义(P<0.05)。见表4。
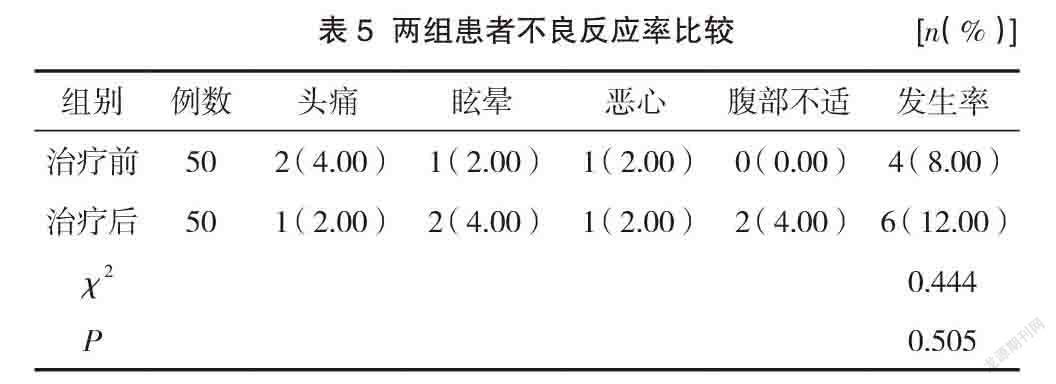
2.5 两组患者不良反应发生率比较
观察组不良反应发生率与对照组相近,差异无统计学意义(P>0.05)。见表5。
3 讨论
抗病毒治疗为乙肝肝硬化失代偿期重要的治疗方案[7]。其中阿德福韦酯为常见治疗药物,口服用药治疗后,通过与自然底物脱氧腺苷三磷酸竞争及整合至病毒DNA后引起病毒DNA链延长两种方式,影响HBV逆转录过程,抑制HBV活性,减少病毒对肝脏细胞功能的影响[8-9]。但长期使用该药治疗,可能会发生耐药性,影响治疗效果。因此考虑对乙型肝炎肝硬化失代偿期患者应用抗病毒药物联合治疗。
恩替卡韦为鸟嘌呤核苷类似物,可通过磷酸化生成有活性的三磷酸盐,在与HBV-DNA多聚酶天然底物三磷酸脱氧鸟嘌呤核苷竞争后,通过抑制HBV多聚酶启动、mRNA逆转录、DNA正链合成过程,以全面性抑制HBV-DNA复制、合成过程,满足乙型病毒性肝炎抗病毒治疗效果,但单一用药同样存在一定耐药发生风险[10]。本研究中,对观察组患者应用上述两种药物联合治疗,结果显示,观察组治疗总有效率明显高于对照组(P<0.05),且治疗后肝功能指标水平显著改善,乙型肝炎病毒表达相关指标水平明显低于对照组(P<0.05),说明对乙肝肝硬化失代偿期患者应用两种药物联合治疗后,可显著抑制HBV-DNA转录过程,减少HBV对患者肝脏细胞损伤影响,促进患者肝脏功能修复,考虑原因为,单独应用阿德福韦酯治疗中,通过抑制HBV逆转录过程以改善其肝功能指标,但长时间治疗可能会增加耐药性,影响肝功能改善质量;阿德福韦酯联合恩替卡韦治疗后,可在单纯抑制HBV活性基础上,通过影响HBV多聚酶启动、mRNA逆转录及DNA正链合成过程,以强化药物对HBV增殖抑制作用,且两种药物联合后,对HBV基因干扰能力增强,减少病毒对患者肝脏细胞功能的影响,促进其肝脏细胞自我功能修复;同时两种药物联合后,可避免单一用药出现耐药情况,维持抗病毒治疗效果稳定性,提升治疗效果[11]。本研究结果显示,治疗后观察组肝脏细胞纤维化指标水平均明显低于对照组,考虑原因为,肝脏细胞纤维化为肝硬化患者主要病变表现,出现HA、LN、PⅢNP、CⅣ水平升高症状,影响患者肝功能代偿能力;两种药物联合后,通过提升HBV控制能力,抑制病毒对其肝脏细胞持续性毒性干扰,并随病毒清除,患者肝脏细胞自我修复能力增强,可降低肝脏纤维化程度,改善患者肝功能指标,提升治疗效果,证实两种药物联合后积极治疗价值[12]。研究结果显示,观察组不良反应发生率与对照组相近,说明两种药物联合治疗后并未增加药物不良反应,提示联合治疗安全性理想。
综上所述,对乙肝肝硬化失代偿期患者抗病毒治疗中,应用阿德福韦酯联合恩替卡韦治疗,与单纯应用阿德福韦酯治疗相比,可进一步提升治疗效果,改善肝功能指标、抑制病毒基因表达、改善肝硬化程度,且安全性良好,效果显著。
参考文献
[1]李宇,张平,郑渝梁,等.失代偿期乙型肝炎肝硬化并发慢加急性肝衰竭患者危险因素分析[J].肝脏,2019,24(6):718-719.
[2]宋景春,张海涛,刘斌,等.前列地尔联合核苷类抗病毒药物对HBV感染失代偿期肝硬化患者肝功能、肝纤维化指标及血清炎性因子的影响[J].海南医学院学报,2019,25(8):593-597.
[3]范丽,张婷.拉米夫定、阿德福韦酯、恩替卡韦治疗失代偿期乙型肝炎肝硬化临床研究[J].陕西医学杂志,2019,48(7):939-941.
[4]袁媛,陈洁,杨雪梅,等.国产恩替卡韦对HBeAg阳性代偿期乙肝肝硬化患者HBV复制的抑制效果,血清球蛋白及补体C3,C4的影响研究[J].川北医学院学报,2020,35(3):432-435,449.
[5]中华医学会肝病分会,中华医学会感染病分会.慢性乙型肝炎防治指南(2015年版)[J].中華实验和临床感染病杂志,2016,21(4):219-235.
[6]孙海英,刘桂清.恩替卡韦治疗慢性乙型肝炎肝硬化失代偿期患者的疗效探讨[J].中国实用医药,2020,15(4):100-101.
[7]骆长玲,曹颖,谢雯.抗病毒治疗促进失代偿期乙型肝炎肝硬化再代偿研究进展[J].中国实用内科杂志,2020,40(6):457-460,465.
[8]嵇笑笑,李丽,傅涓涓,等.不同病毒学应答状态对失代偿期乙型肝炎肝硬化患者预后的影响[J].临床肝胆病杂志,2020,36(5):1033-1037.
[9]徐静,陶琳琳,叶娇娇,等.替比夫定联合阿德福韦酯治疗失代偿期乙型肝炎肝硬化患者疗效及其对肾功能的影响[J].实用肝脏病杂志,2019,22(1):89-92.
[10]张笛,李贞茂,王治兰,等.不同抗病毒药物治疗前后乙肝肝硬化失代偿期患者血清IL-17的观察[J].四川医学,2019,40(10):990-992.
[11]刘小莹,郑宏波,王山军,等.恩替卡韦单药方案维持对初始行拉米夫定+阿德福韦酯方案治疗慢性乙型肝炎及慢性乙型肝炎后肝硬化疗效影响[J].陕西医学杂志,2020,49(4):502-505.
[12]刘玮,连晶晶,李洁.恩替卡韦联合治疗对慢性乙型肝炎患者炎性反应,肝功能及肝纤维化的影响[J].临床误诊误治,2019,32(1):35-39.
