NGF/ TrKA 信号通路在膝骨关节炎疼痛中的研究进展
2022-03-23李明超王培民殷松江黄正泉邢润麟
李明超 王培民 殷松江 张 力 黄正泉 邢润麟
1.江苏省昆山市第三人民医院骨科,江苏昆山 215300;2.南京中医药大学附属医院骨伤科,江苏南京 210029
膝关节骨关节炎(knee osteoarthritis,KOA)是引起膝关节疼痛的主要原因[1],60 岁以上人群中,约9.6%的男性和18.0%的女性患有症状性骨关节炎[2],该病已成为公共卫生的挑战[3]。目前尚无有效阻止该病进展的治疗方法[4-5]。阻断神经生长因子(nerve growth factor,NGF)对减轻KOA 疼痛有较好疗效,引起了临床对NGF及其主要功能受体原肌球蛋白受体激酶A(tropomyosin receptor kinase A,TrKA)和下游分子的关注。NGF 激活疼痛伤害感受的疼痛信号,引起疼痛和痛觉敏化。阻断NGF及其受体后,疼痛减轻。本文围绕NGF/TrKA 通路及其下游分子与KOA 疼痛的关系作一综述。
1 KOA 疼痛机制
疼痛伤害感受器广泛分布于皮肤、肌肉、关节,可对机械、温度、化学刺激等产生应答,并将信息传递到中枢神经。长期慢性疼痛使神经纤维激活的阈值降低,在较低的炎症刺激时即可被激活,引起痛觉敏化。KOA 疼痛包括炎症性疼痛和神经病理性疼痛,其神经生物学机制尚未阐明,但两者之间相互影响[6]。
2 NGF/TrKA 通路与KOA 疼痛
NGF 可调节神经元的生长发育,对慢性疼痛、KOA 疼痛有重要作用。TrKA 是NGF 的特异性高亲和力受体。NGF与TrKA 结合激活Ras/MAPK、PI3K/Akt、PLCγ 等多种信号通路[7](图1A),对神经元的发育和存活以及痛觉具有重要作用。缺乏NGF 会导致深度痛觉丧失;缺乏TrKA 时不仅对疼痛刺激没有反应,还伴有无汗和智力低下[8]。
有研究发现,向大鼠后足局部注射NGF,会引起痛觉过敏,注射促进TrKA 激活的非NGF 因子也会引起痛觉过敏;而使用TrKA 抑制剂可阻止NGF 引起的痛觉过敏[9]。NGF 呈TrKA 依赖性地诱导的膝关节痛觉敏感性[10],这表明NGF 通过TrKA 诱导疼痛和痛敏反应。
当膝关节局部机械应力增加或受到刺激时,免疫细胞合成NGF 增多,刺激肥大细胞表达组胺、5-羟色胺(5-hydroxytryptamine,5-HT)、H+及释放更多的NGF,形成正反馈环路(图1A)。NGF 又可进一步激活瞬时感受器电位香草酸受体1(transient receptor potential vanilloid 1,TRPV1)和其他离子通道,导致膝关节痛觉过敏[11]。
3 NGF/TrKA 通路与KOA 疼痛相关病理变化
KOA 早期,疼痛为活动后加重,休息可缓解;中期,疼痛时间增加,出现夜间痛;晚期,多为持续疼痛、静息性疼痛。这种不同时期的不同疼痛表现,可能与病理变化不同有关。KOA 患者关节液和血液中NGF与TrKA 的表达也随疾病进展而增加[12],提示NGF/TrKA 通路与KOA 疼痛相关的病理变化有关。
3.1 痛觉敏化
痛觉敏化是KOA 疼痛的主要原因之一[13],分为外周敏化和中枢敏化。NGF、TrKA 结合后,一方面促进Ca2+内流传导疼痛,调节TRPV1 过表达;另一方面,NGF/TrKA 复合体转运至背根神经节(dorsal root ganglion,DRG),影响DRG 神经元中TRPV1 的表达和激活,触发电压门控钠通道、缓激肽受体、酸敏感离子通道,参与DRG 中伤害感受器表面受体的表达,引发外周敏化[14](图1B)。同时,NGF/TrKA 通路可促进神经末梢释放降钙素基因相关肽(calcitonin gene-related peptide,CGRP)、P 物质(SP)、痛觉肽等。这些神经肽又与中枢神经元相关受体结合,产生中枢敏化(图1C)。
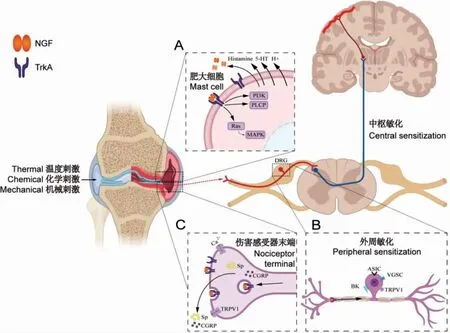
图1 NGF/TrKA 信号通路与KOA 疼痛、痛觉敏化的关系
3.2 炎症
膝关节镜检查中,50%以上的KOA 患者有滑膜炎表现[15]。滑膜组织含有较多的TrKA 阳性神经纤维,因此,NGF/TrKA 通路可能通过滑膜炎症引起痛觉敏化。Neogi 等[13]在对KOA 的研究中,证明KOA 中的滑膜炎可导致广泛的痛觉敏化。
白细胞介素1β、转化生长因子β 等炎症因子,可直接作用于疼痛伤害感受器,产生炎症性疼痛;持续的炎症性疼痛引起外周敏化,敏化的神经末梢又可引起促炎因子分泌增加,形成恶性循环。这种炎症性疼痛与神经病理性疼痛之间的相互作用,可能是晚期KOA 疼痛反复发作、难以治愈的原因。
3.3 血管生成
血管生成,即从先前存在的血管生长出新的血管,是急性炎症向慢性炎症转变的关键步骤。在KOA患者的滑膜和软骨交界处可观察到血管生成和感觉神经分布,这些新生血管周围的神经纤维含有SP 和CGRP,具有促进血管形成和引起疼痛双重作用。
NGF/TrKA 通路促血管生成作用表现在:①NGF与内皮细胞表面TrKA 受体结合刺激内皮细胞增殖和毛细血管形成;②促进感觉神经末梢SP 和CGRP的释放,刺激血管生成;③NGF与巨噬细胞上的TrKA结合可释放血管内皮生长因子,刺激血管生成。见图2。

图2 NGF 的促血管生成作用
3.4 神经芽生
NGF 可诱导外周和中枢神经纤维芽生。研究发现,NGF/TrKA 通路可影响骨软骨交界处的感觉神经密度,通过抑制TrKA 可以减少骨软骨交界处的感觉神经密度[16]。用MRI 对骨髓损伤区域的微阵列分析显示,骨髓损伤区域促神经生长和炎症的相关基因均上调,最终神经与新血管生长并穿透关节软骨,使正常无神经支配的软骨结构有了新的疼痛感受器[16]。
3.5 软骨损伤
软骨退变是KOA 的基本病理改变,KOA 早期患者软骨中NGF 水平较低,而晚期NGF 水平升高[17]。NGF 和TrKA 的表达随KOA 阶段进展而增加。NGF通过增加硫酸黏多糖和基质金属蛋白酶的释放,增加软骨内基质的降解,参与软骨退变[18]。
4 NGF/TrKA 通路相关药物
4.1 西药进展
许多学者希望通过靶向NGF/TrKA 通路缓解疼痛[19]。目前,阻断该通路主要有以下方式:①NGF 抑制剂,可同时阻止NGF与TrKA 和p75NTR 两种受体的作用[19];②抑制NGF与TrKA 结合;③选择性抑制TrKA[20]。
4.2 中药进展
部分天然药物也可通过抑制NGF/TrKA 通路下游信号分子TRPV1 起到止痛作用,如蜂毒能通过抑制大鼠DRG 中TrkA/TRPV1 通路起到镇痛作用[21]。但选择性TRPV1 拮抗剂多具有体温增高等不良反应[22-23],局部外用药未出现该类效应[24],具有更好的安全性。
5 结论及展望
目前,仍没有可以逆转KOA 病理进程的药物或方法。KOA 疼痛机制复杂,涉及多种关节结构[25]。有学者将KOA 分类为炎症表型、疼痛表型和代谢表型,这种分类有助于确定不同病理特征[4]、制订个体化治疗方案[26],对于炎症表型为主者,以抑炎药物为主;对伴有神经病理性疼痛者,可结合阻断痛觉敏化的药物。
X 线检查可反映KOA 的病程进展,但与KOA 疼痛程度相关性较弱[27]。随着MRI 应用,发现滑膜炎症、骨髓损伤、关节积液等病理改变与疼痛程度相关性较高[13,28],两种检查的影像主要在滑膜、软骨、骨髓水肿、积液等病理改变的成像中有差异,其中滑膜组织大多表达TrKA,骨髓水肿时NGF、TrKA 表达增加,由此可以发现MRI 能评估疼痛可能与NGF/TrKA通路有关。
NGF 通过促进炎症因子分泌和诱导神经元敏化来增加疼痛[28]。由于大分子抗NGF 单克隆抗体同时抑制NGF与P75NTR 受体的生理功能,存在安全隐患,增加关节置换机会[19],因此美国食品药品监督管理局一度停止了抗NGF 的临床试验[29]。通过选择性抑制TrKA 或其下游信号通路[30],可有效地缓解疼痛和痛觉敏化,又不阻断NGF与p75NTR 结合的生理功能,具有安全性上的优势。
综上所述,KOA 疼痛与炎症和痛觉敏化有关。炎症主要表现为滑膜炎,可促进KOA 病程进展[31],通过治疗可减轻炎症性疼痛[32];NGF/TrKA 信号通路与外周敏化关系密切,可加重炎症环境,是晚期KOA 疼痛反复发作的关键点。目前针对NGF/TrKA 信号通路开发的药物表现出较好的缓解疼痛作用,同时暴露出一些副作用,对该类药物的研发仍不成熟,对该通路进一步研究,可能为减轻KOA 疼痛、研发新型药物等提供新的思路。
