H5 亚型2.3.4.4 分支禽流感病毒HA 基因重组质粒的免疫保护效力研究
2022-03-22李炯颉梁真洁陈普成曾显营柳金雄邓国华姜永萍陈化兰
李炯颉,梁真洁,陈普成,曾显营,柳金雄,邓国华,姜永萍,陈化兰
(中国农业科学院哈尔滨兽医研究所兽医生物技术国家重点实验室,黑龙江 哈尔滨 150069)
高致病性禽流感(Highly pathogenic avian influenza,HPAI)是由正粘病毒科流感病毒属A 型流感病毒引发的一种传播快、死亡率高的禽类烈性传染病。HPAI 不仅对家禽造成严重危害,也对人类健康构成严重威胁,近年来该类病毒感染人的事件时有发生。血凝素(HA)是流感病毒囊膜纤突的重要组成部分,是参与禽流感病毒(Avian influenza virus,AIV)与细胞表面受体结合的主要蛋白[1]。因此,HA 蛋白是保护性免疫应答的主要靶抗原,针对HA 蛋白的抗体能够阻止病毒吸附和病毒侵入宿主细胞,从而保护机体免受病毒的感染[2]。
接种疫苗一直是控制AIV 传播最有效的手段,基于基因工程技术的不断发展,各种新型疫苗相继研发并投入使用。DNA 疫苗是将编码相关抗原蛋白的基因插入到质粒载体中,将重组质粒直接注射动物,通过在宿主细胞内表达相关抗原基因诱导机体产生免疫应答。DNA 疫苗能真实地呈现外源基因编码蛋白的抗原性,并能同时激发细胞与体液免疫应答反应;递呈的免疫源单一,免疫持续期长、可以反复加强免疫;免疫接种与自然感染动物可以利用特异性诊断试剂进行鉴别,具有长远的开发前景[3]。2018年,由中国农业科学院哈尔滨兽医研究所研制的H5 亚型禽流感DNA 疫苗获得了国家一类新兽药证书,是中国首个获得批准的禽流感DNA 疫苗。
AIV HA 抗原基因不断进化导致的抗原变异是影响原有疫苗无法提供完全免疫保护的主要原因,因此需要实时构建并更新疫苗株[4]。流行病学监测结果表明,H5 亚型2.3.4.4d 分支是目前影响我国部分地区养禽业的主要AIV,根据抗原性和遗传演化分析结果,本研究选择A/Duck/Guizhou/S4184/2017(H5N6)(简称DK/GZ/S4184/2017(H5N6))株作为2.3.4.4d 分支代表AIV,以其HA 基因构建重组质粒并进行免疫效力评估,为防控该分支AI 提供有效的疫苗储备。
1 材料与方法
1.1 主要实验材料pCAGGs 质粒、攻毒用H5 亚型高致病性AIV(HPAIV)DK/GZ/S4184/2017(H5N6)、HPAIV DK/GD/S1110/2019(H5N6)、HPAIV DK/GX/1/2018(H5N6)、HPAIV DK/HuN/SE0110/2018(H5N6)株及其标准抗原和对应的H5N6 AIV 多克隆抗体、293T 细胞均由中国农业科学院哈尔滨兽医研究所国家禽流感参考实验室保存;E. coliDH5α 感受态细胞购自北京全式金生物技术有限公司;Q5 高保真酶和内切酶EcoR I/XhoI 等均购自NEB 公司;Lipofectamin 3000 转染试剂购自Invitrogen 公司;兔抗鸡IgGFITC 购自Sigma 公司;兔抗GAPDH 单克隆抗体(MAb)购自Santa Cruz Biotechnology 公司;鼠抗兔IgG-DyLight800、驴抗鸡Ig(H+L)-Dylight800 抗体购自Odyssey 公司。引物均由库美公司合成。
1.2 重组质粒的构建与PCR 鉴定将DK/GZ/S4184/2017(H5N6)株HA 基因的密码子优化为鸡体所偏嗜的密码子,并由南京金斯瑞生物科技有限公司合成。优化的HA 基因经EcoR I/XhoI 双酶切后定向克隆至pCAGGs 载体,构建的重组质粒采用载体引物进行PCR 和测序鉴定后,命名为pCA-S4184。
1.3 目的蛋白表达的间接免疫荧光试验(IFA)及western blot 鉴定待293T 细胞状态良好、密度约为8×105个/mL 时,利用Lipofectamine 3000 转染试剂分别将重组质粒pCA-S4184 及对照质粒pCAGGs 转染至293T 细胞。转染48 h 后采用4%多聚甲醛固定细胞30 min,以H5N6 AIV 多克隆抗体(1∶300)为一抗,兔抗鸡IgG-FITC(1∶1 000)为二抗经IFA 检测。另外收集细胞后经RIPA 裂解,以H5N6 AIV 多克隆抗体(1∶300)为一抗,以驴抗鸡Ig(H+L)-Dylight800(1∶5 000)为二抗经western blot 鉴定,分析HA 蛋白的表达情况,并以GAPDH 作为293T 细胞基因正常表达的对照。以上试验均设未转染质粒的细胞作为空白对照。
1.4 SPF 鸡的免疫试验设计将重组质粒pCAS4184 以肌肉注射的方式免疫3 周龄SPF 鸡,免疫以及分组情况见表1,并在首次免疫及攻毒后每周采血,采用红细胞凝集抑制试验(HI)检测HI 抗体水平(HI 抗体滴度为1∶4 以上为阳性)。
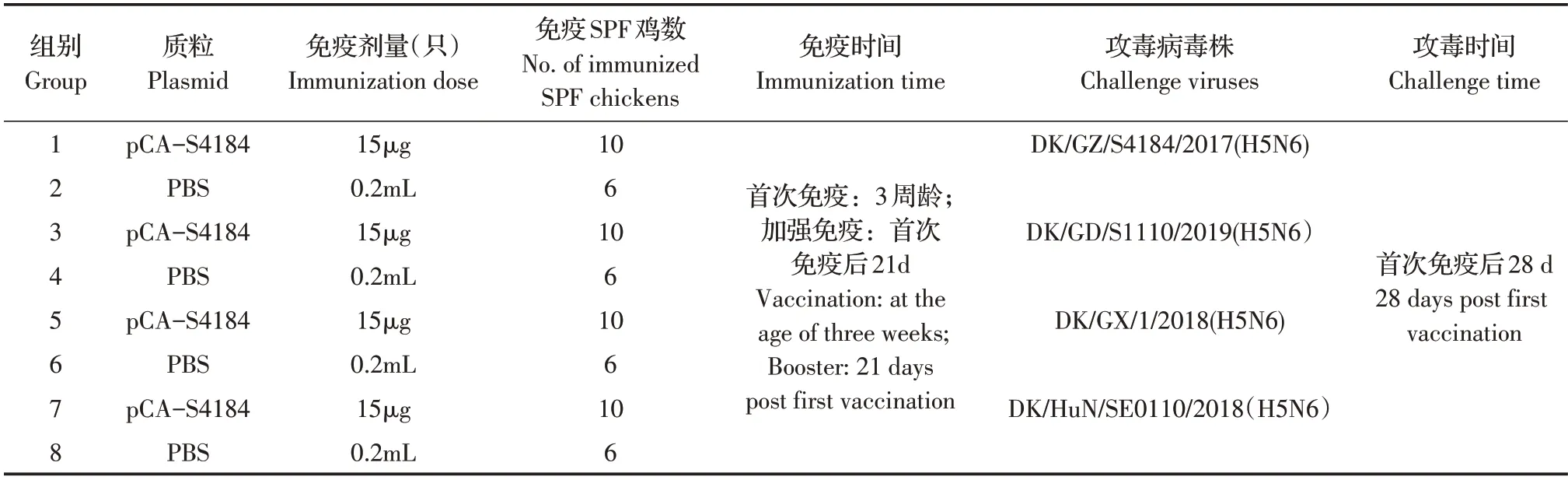
表1 SPF鸡的免疫试验设计Table 1 Experimental design of SPF chickens
1.5 攻毒保护试验加强免疫后一周(首免后28 d),分别经滴鼻途径感染105EID50/0.1 mL/只的1 株同源HPAIV DK/GZ/S4184/2017(H5N6)株、3 株同分支异源HPAIV DK/GD/S1110/2019(H5N6)、DK/GX/1/2018(H5N6)、DK/HuN/SE0110/2018(H5N6)株,攻毒后在14 d 的观察期内每天记录免疫组和对照组鸡的发病和死亡情况。
1.6 攻毒后实验鸡的排毒检测分别于攻毒后的3 d、5 d 和7 d 无菌采集各组鸡的喉头和泄殖腔棉拭子,置于含氨苄青霉素和链霉素的无菌PBS中,取100 μL 10 倍倍比稀释后接种9 日龄~11 日龄鸡胚,37 ℃孵化48 后经血凝试验检测鸡胚尿囊液的HA 效价,加入50 μL 1%红细胞悬液,并根据Reed-Meunch 法计算所分离病毒的滴度。
1.7 抗体持续期试验将构建的重组质粒pCAS4184 以15 μg/只两次免疫3 周龄SPF 鸡,免疫组30只,对照组15 只。免疫后每隔2 周采集其翅静脉血检测HI 抗体,分析HI 抗体的动态消长规律,评估该重组质粒的免疫保护期;分别在首免后第12 周和24 周,随机选取8 只免疫鸡,连同日龄相同的8 只对照组鸡分别用105EID50/0.1 mL/只剂量攻击同源HPAIV DK/GZ/S4184/2017(H5N6)株,攻毒后14 d 观察期内每天记录各组鸡的发病和死亡情况;分别在攻毒后的3 d、5 d 和7 d 采集每只鸡的泄殖腔拭子和喉头拭子进行病毒的分离与滴定,检测攻毒后各组鸡的排毒情况。
2 结 果
2.1 重组质粒pCA-S4184 的构建与鉴定结果将DK/GZ/S4184/2017(H5N6)株HA 基因的密码子优化后经公司合成,并克隆至pCAGGS 载体中。构建的重组质粒经PCR 鉴定,结果显示扩增的目的条带均正确(图1),并且测序结果与预期完全符合。表明正确构建了重组质粒pCA-S4184。
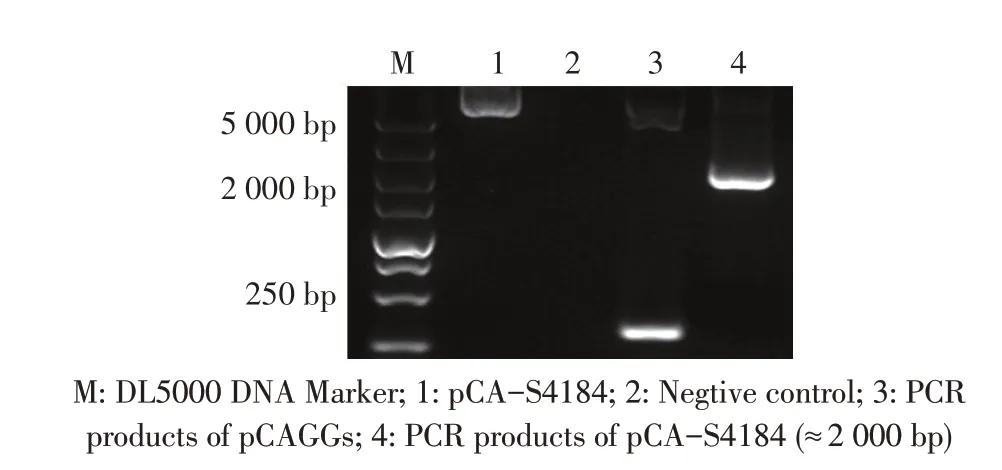
图1 重组质粒pCA-S4184的PCR鉴定结果Fig.1 Identification of pCA-S4184 by PCR
2.2 目的蛋白表达的IFA 及western blot 鉴定结果分别将重组质粒pCA-S4184 和空载体pCAGGs 质粒转染293T 细胞48 h 后,分别经IFA 和western blot 鉴定。IFA 结果显示,pCA-S4184 转染的细胞中可观察到绿色荧光,而空载体转染的细胞和未转染质粒的空白细胞中则无绿色荧光(图2A);Western blot 结果显示,pCA-S4184 转染的细胞中出现约74 ku 的特异性条带,空载体转染的细胞与空白对照细胞中均无该特异性条带。但不同载体转染的293T 细胞及空白细胞中均检测到了GAPDH 的表达(图2B),以上结果表明DK/GZ/S4184/2017(H5N6)株HA 基因在293T 细胞中获得了表达,且具有良好的反应原性。
图2 HA基因在293T细胞中表达的IFA(A)及western blot(B)鉴定结果Fig.2 Identification of HA gene expression by IFA(A)and western blot(B)
2.3 重组质粒免疫后的HI 抗体检测结果将pCAS4184 以15 μg/只免疫SPF 鸡,3 周后加强免疫,一周后,分别经滴鼻感染同源或同分支异源病毒。免疫及攻毒后每周采血检测HI 抗体水平。结果显示,加强免疫之前各组免疫鸡针对DK/GZ/S4184/2017(H5N6)抗原的HI 抗体均维持在较低水平;加强免疫后一周,4 组免疫鸡针对该抗原的HI 抗体平均水平分别为1∶11、1∶11、1∶8、1∶11,PBS 对照组鸡的HI 抗体均为0。所有免疫鸡的HI 抗体水平在攻毒后1 周均有明显升高,平均HI 抗体在1∶16 左右(图3)。表明,重组质粒pCA-S4184 具有良好的免疫原性,可以诱导SPF 鸡产生相应的HI 抗体。
图3 免疫鸡HI抗体检测结果Fig.3 Results of the HI antibodies in vaccinated chickens
2.4 攻毒后各组鸡发病、死亡及排毒检测结果首免后28 d,分别用致死剂量的1 株同源和3 株同分支异源HPAIV 攻击后,在14 d 的观察期内每天记录各组鸡的发病和死亡情况并在攻毒后的不同时间采集各组鸡的喉头和泄殖腔棉拭子进行检测。结果显示,4组对照鸡在攻毒后2 d~5 d全部发病死亡,并大量排毒;攻击DK/GZ/S4184/2017(H5N6)、DK/GX/1/2018(H5N6)和DK/HuN/SE0110/2018(H5N6)株病毒的所有免疫鸡均健活,无发病也无排毒,攻击DK/GD/S1110/2019(H5N6)株病毒的免疫组中虽有个别鸡有低剂量的一过性排毒,但均获得了100%的免疫保护率(表2)。上述结果表明,重组质粒pCA-S4184 的免疫效果良好,15 μg/只的剂量即可对SPF 鸡提供100%的抵抗同源和同分支异源病毒攻击的能力,而且能显著降低攻毒后的排毒量。
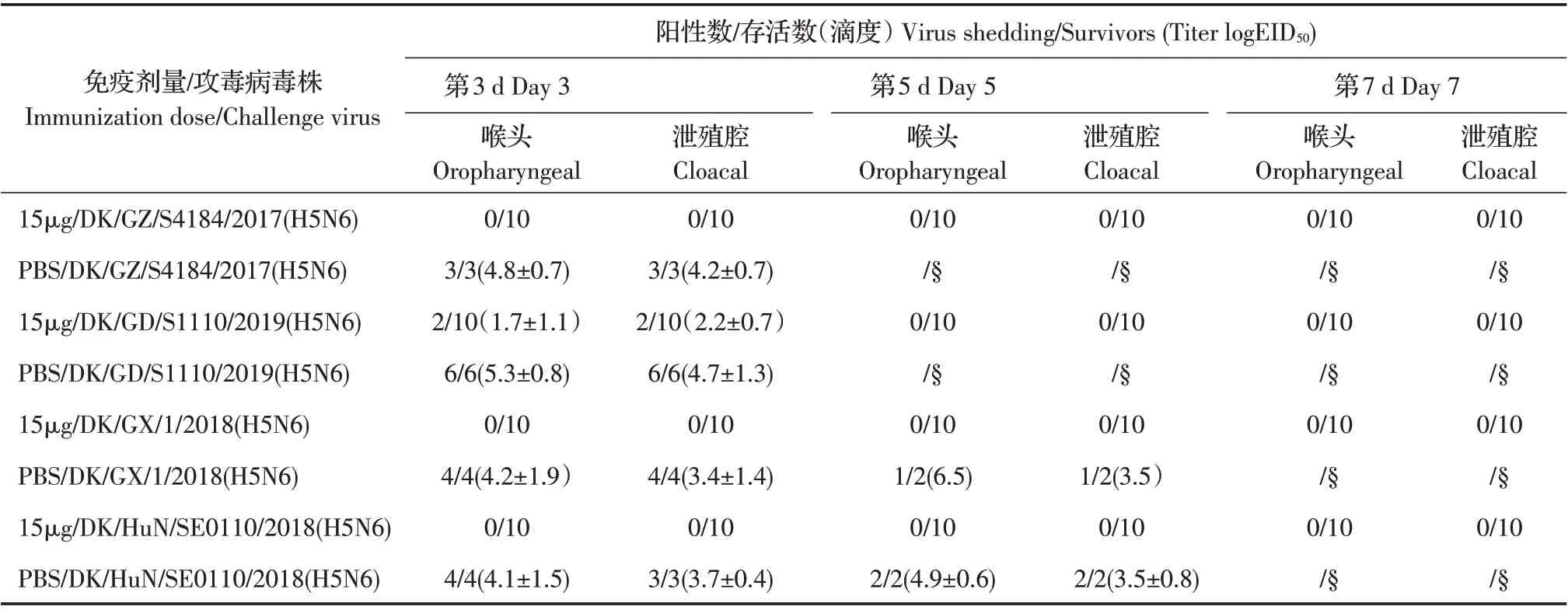
表2 各组鸡攻击H5N6 AIV 后的排毒检测结果Table 2 Virus shedding from SPF chickens infected with H5N6 AIV
2.5 重组质粒免疫SPF 鸡后的HI 抗体持续期检测结果重组质粒pCA-S4184 以15 μg/只免疫SPF 鸡,3周后加强免疫,免疫后每周采血,检测HI 抗体并分析其动态消长规律。结果显示,首免后3 周,免疫鸡的平均HI抗体为1∶4,加强免疫后2周,平均HI抗体可上升至1∶37,其后平均HI 抗体保持在1∶11~1∶64,免疫后25 周,免疫鸡平均HI 抗体水平还可达1∶11,对照组鸡的HI 抗体始终为0(图4)。结果表明,重组质粒pCA-S4184 所诱导的HI 抗体可持续25 周以上。

图4 HI抗体持续期检测结果Fig.4 Results of the HI antibody duration
2.6 重组质粒免疫SPF 鸡后的持续期攻毒试验结果首免后的第12 周和24 周,分别随机选取8 只免疫鸡及8 只对照组鸡分别用致死剂量的同源病毒攻击,在14 d 观察期内每天记录试验鸡的发病和死亡情况;分别在攻毒后的不同时间采集每只鸡的泄殖腔和喉头拭子进行病毒的分离与滴定。结果显示,免疫鸡在攻毒后均存活,可完全抵御HPAIV DK/GZ/S4184/2017(H5N6)的攻击,且无排毒现象(表3)。上述结果表明,重组质粒pCA-S4184 的免疫持续保护期较长,在首免后第24 周仍可以抵御同源病毒的致死性攻击。
表3 免疫持续期内SPF鸡攻击H5N6 AIV 后的排毒检测结果Table 3 Virus shedding from SPF chickens infected with H5N6 AIV in HI antibody duration
3 讨 论
近年来,H5N6 亚型AIV 逐渐取代H5N1 亚型AIV,成为我国家禽和活禽市场中流行的主要AIV[5-7]。H5 亚型AIV 的高突变率和死亡率,对禽类养殖业以及公共卫生安全,乃至社会的稳定都造成了很大的影响。疫苗免疫是防制AI 的主动措施和关键环节,而疫苗的免疫效率取决于流行株与疫苗株之间的抗原性匹配程度,鉴于流感病毒的高突变率,只有抗原性匹配的疫苗才能为动物机体提供坚实有效的免疫力[8]。2017 年底以来的流行病学监测结果显示,H5亚型2.3.4.4分支AIV已在19个省份分离到,并可进一步分为2.3.4.4b 分支、2.3.4.4c 分支、2.3.4.4d分支,其中以2.3.4.4d分支为主[9]。因此有必要研制和更新针对2.3.4.4分支AIV的禽流感DNA疫苗。
经过多年研究,本实验室建立了系统的禽流感DNA 疫苗研制平台,构建了一系列不同抗原分支的AIV DNA 疫苗,但不同抗原分支AIV HA 基因的免疫原性有差异,动物试验表明,10 μg 及以上相应质粒的免疫剂量可诱导产生较高的HI 抗体水平,并可抵御同源病毒的致死性攻击[10-12]。本研究根据鸡的偏嗜性对HPAIV S4184(H5N6)株的HA 基因优化并合成后插入到pCAGGs 载体中,构建了表达2.3.4.4 分支AIV代表株DK/GZ/S4184/2017(H5N6)HA 基因的重组质粒pCA-S4184,IFA 和western blot 鉴定结果显示,该HA 基因可以在293T 细胞中表达,为了评价其免疫保护效果,进行了一系列免疫效力评估试验:以15 μg 剂量免疫3 周龄SPF 鸡,首免后3 周以同样剂量和方式加强免疫,1 周后分别用105EID50/0.1 mL/只同源HPAIV DK/GZ/S4184/2017(H5N6)和同分支异源HPAIV DK/GD/S1110/2019(H5N6)、DK/GX/1/2018(H5N6)、DK/HuN/SE0110/2018(H5N6)株通过鼻腔途径攻击。结果表明,重组质粒pCA-S4184 免疫后SPF 鸡可以产生抵抗同源及同分支异源病毒攻击的能力,对SPF 鸡的保护率均可达100%。免疫持续期试验结果显示,以15 μg/只免疫SPF 鸡后HI 抗体持续期可达25 周以上,在加强免疫后至25 周,平均HI 抗体滴度保持在1∶11~1∶64;在免疫后第12 周和24 周的攻毒保护试验中,免疫鸡均100%抵御了同源HPAIV DK/GZ/S4184/2017(H5N6)的攻击。另外,重组质粒pCA-S4184 以15 μg/只的剂量免疫后虽然能抵御同源以及同分支异源病毒的致死性攻击,但平均HI 抗体水平在免疫后初期以及免疫后21 周左右均低于1∶16,考虑到HI 抗体水平检测标准以及现地应用的复杂性,临床免疫效果可能会与实验室试验结果有一定差距,因此建议该重组质粒的免疫剂量应适当提高。本研究结果表明,表达H5N6 亚型AIV HA 基因的重组质粒pCA-S4184 免疫效果良好,有望成为预防我国当前流行的H5 亚型2.3.4.4 分支HPAIV 的储备DNA 疫苗。
