线性和非线性定量在同位素稀释质谱法中应用的比较*
2022-03-18马妍慧皇甫昱婵周韵斓沈立松
马妍慧,皇甫昱婵,周韵斓,沈立松
上海交通大学医学院附属新华医院检验科,上海 200092
质谱(MS)定量通常使用稳定同位素标记(SIL)的分析物作内标(IS),并通过分析物和IS峰面积比值进行定量。IS用于校正样品制备、进样、电离和仪器性能的变化,加入IS的定量方法能够提高方法的准确度和精度。
稳定同位素标记的内标在MS准确定量定性方面具有很大的实用性。然而,在某些情况下,分析物天然存在的同位素或者内参标准品中存在没有被标记的目标分析物,均对二者信号存在一定“串扰”。对于富含同位素的化合物,例如含有硫、氯或溴的化合物,或是相对分子质量更大的化合物,以及分析物或内标浓度比高的化合物,这种现象变得更加明显[1-2]。这可能会导致非线性响应的情况出现,影响定量结果[3]。在这些情况下,如果使用非线性回归,通过实验确定每个分析物或内标组合的可调校准参数(如确定一个或两个常数),数据拟合可能会更准确。因存在分析物中稳定同位素的信号,非线性拟合在基于MS测定中提供更准确的定量[2]。相反,它亦可校正同位素内标中分析物作为杂质的存在情况。本文利用已获得的同位素稀释质谱法检测伊立替康(CPT-11)及其代谢产物的数据[4],分析了线性和非线性拟合[5]的比较与实际应用。
1 材料与方法
1.1仪器与试剂 仪器:高效液相色谱(HPLC)仪Agilent 1260(美国Agilent公司)、三重串联四级杆质谱API 3200及电喷雾离子源。试剂:CPT-11(纯度≥97%)、SN-38(纯度≥98%)、SN-38G(纯度≥97%)均购自美国Sigma-Aldrich公司;APC(纯度≥97%)和IS CPT-11 D10、SN-38 D3、SN-38G D3和APC D3购自Toronto Research Chemicals,Inc(图1);乙腈和醋酸(HPLC级),二甲基亚砜(DMSO)购自德国Merck公司,去离子水制备自美国Milli-Q Plus纯水系统。从上海交通大学医学院附属新华医院检验科实验室的7例健康志愿者那里收集空白EDTA血浆,混合后制备标准品和质量控制(QC)样品。
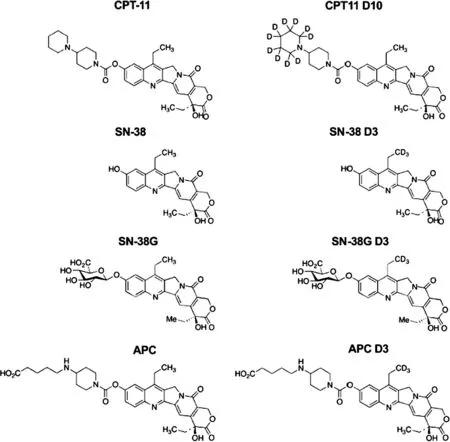
图1 标准品及相应同位素内标结构式
1.2液相色谱条件 色谱柱菲罗门反相C18色谱柱 (4.6 mm×50 mm,2.6 μm),柱温30 ℃;流动相A为水(含0.1%醋酸,V/V),B为乙腈(含0.1%醋酸,V/V),流速300 μL/min,进样量为15 μL。采用梯度洗脱,前1 min为95%流动相A,>1~7 min为95%流动相A至5%流动相A,>7.0~7.5 min为5%流动相A,>7.5~8.0 min为5%流动相A至95%流动相A,并持续此梯度至9 min,总时间为9 min。质谱条件:电喷雾离子源,正离子扫描模式,毛细管电压4 500 V,干燥气为氮气(N2),温度180 ℃,流速4 L/min,雾化气压力0.4 bar;碰撞气为N2,碰撞能量为8 eV;扫描质量范围为质荷比(m/z) 50~1 000。采用多离子反应监测模式,定量离子通道选择m/z CPT-11 m/z 587.216>124.3,SN-38 m/z 393.3>349.2,SN-38G m/z 569.2>393.3,APC m/z 619.2>393.3,CPT-11 D10 m/z 597.3>133.3,SN-38 D3 m/z 396.2>352.3,SN-38G D3 m/z 572.1>396.2,APC D3 m/z 622.3>396.2。
1.3试剂、校准曲线和QC样本制备 所购买试剂均为1 mg,CPT-11、CPT-11 D10和SN-38、SN-38 D3溶于DMSO获得终质量浓度分为5 000、1 000、100、1 000 μg/mL储存液,SN-38G、SN-38G D3和APC、APC D3溶于DMSO∶甲醇(50∶50)获得终浓度分为100、1 000、5 000、1 000 μg/mL储存液。储备液均分装于2 mL离心管中,-80 ℃冰箱保存备用。在混合人血浆中准确加入4种标准品和内参储备液,-80 ℃冰箱保存备用。制作校准曲线时,溶解后漩涡混匀,2倍稀释后得到CPT-11和APC浓度为2 500、1 250、625、312.5、156.3、78.1、39.1、19.5、9.8、4.9 μg/mL,SN-38和SN-38G浓度为1 000、500、250、125、62.5、31.3、15.6、7.8、3.9、2.0、1.0 ng/mL的混合标准溶液。制备200×混合内参储存液,工作液终浓度分别为CPT-11 100 ng/mL、APC 100 ng/mL、SN-38 50 ng/mL、SN-38G 100 ng/mL。制备高、中、低3种浓度QC血浆样本,CPT-11为80、400、1 000 ng/mL;SN-38 和 SN-38G为15、100、400 ng/mL;APC为40、200、400 ng/mL,所有QC样本制备后分装,-80 ℃冰箱保存备用。
1.4样本前处理 准确吸取200 μL EDTA-K2抗凝血浆样本,加入5 μL混合内标工作液(200×),加入795 μL乙腈蛋白沉淀,振荡混匀后4 ℃ 16 000 g高速离心10 min,吸取900 μL 上清,置于35 ℃ N2吹干,再以100 μL 0.1% 醋酸水和乙腈(50∶50)溶液复溶,15 μL进样分析。样本重复检测5次,取均值。
1.5标准曲线分析 以Excel中LINEST拟合分析功能分析线性回归、曲线回归(二次函数和三次函数)和有理多项式逼近函数Padé[1,1]近似,y=(a0+ a1x)/(1-a2x)。

表1 LINEST常用分析
2 结 果
2.1同位素稀释质谱法分析CPT-11及其代谢产物和内参色谱结果 在本实验条件下,4种物质(1 μg/mL)的混合标准溶液,采用正离子模式电喷雾离子化后,根据保留时间依次出峰时间分别为SN-38G(4.61 min)、APC(4.65 min) CPT-11(4.72 min)和SN-38(5.16 min),与各相应同位素内参保留时间一致,见图2A。标准品单独分析时,SN-38和SN-38 D3洗脱峰在5.16~5.21 min,其他时间没有峰出现(图2A和2B)。但混合标准品和内参后,在SN-38G D3(50 ng/mL)色谱结果中提取到SN-38碎片离子峰(图2C),CPT-11 D10中亦可提取SN-38离子峰。考虑SN-38主要结构均存在于CPT-11、SN-38G和APC分子结构中,发生源内裂解时可能存在部分交叉。
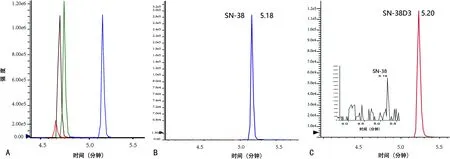
图2 CPT-11及其代谢产物色谱图和SN-38、SN-38 D3 提取m/z 393.3>349.2离子色谱图
2.2数据分析 实验室对CPT-11的校准范围是4.9~2 500.0 ng/mL,方法线性定量范围9.8~1 250.0 ng/mL。应用LINEST分析4种标准曲线,外推校准曲线见图3。4种计算公式分别为:线性函数y=91.51x-48.59;二次函数y=0.167x2+83.02x-19.40;三次函数y=-0.009 3x3+0.88x2+71.10x-0.55;Padé[1,1]y=(-19.60+83.32x)/(1-0.001 8x),R2均>0.999。二次函数、三次函数曲线回归和Padé[1,1]近似3种浓度QC计算结果偏差10%以内(表2)。

表2 基于同位素稀释质谱法的4种标准曲线计算CPT-11 QC样本偏差
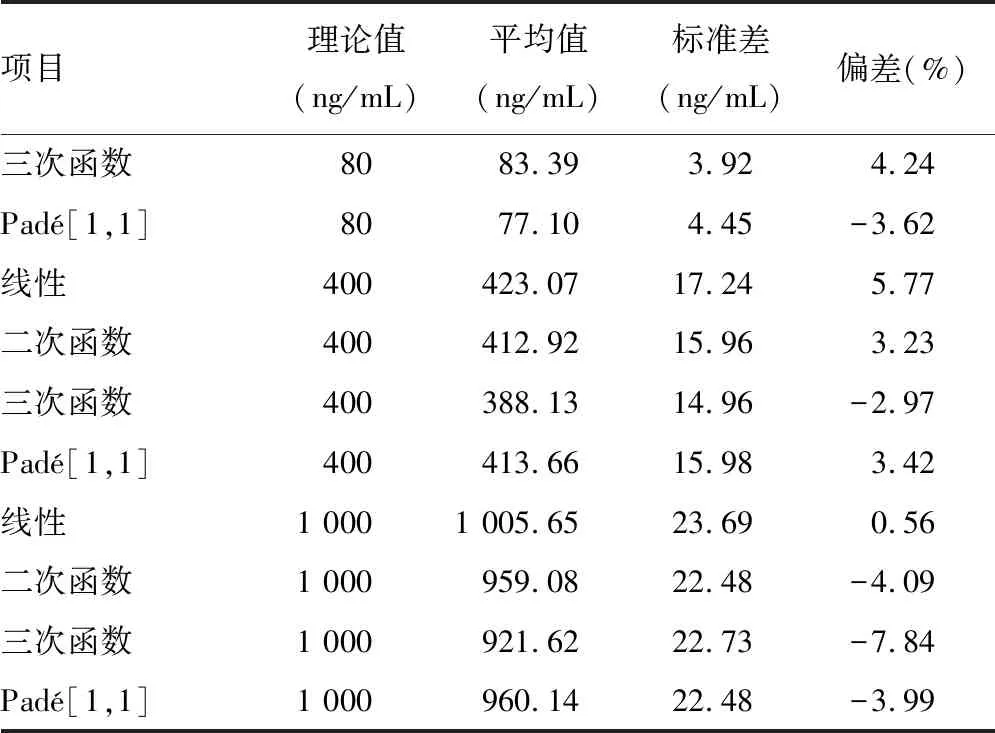
续表2 基于同位素稀释质谱法的4种标准曲线计算CPT-11 QC样本偏差
对SN-38的校准范围是1.0~1 000.0 ng/mL,方法线性定量范围2.0~500.0 ng/mL。应用LINEST分析4种标准曲线,外推校准曲线,见图4。SN-38 4种计算公式分别为:线性函数y= 133.3x-4.22;二次函数y=0.018x2+133.24x-4.2;三次函数y=-3.99x3+21.16x2+109.44x-1.5;Padé[1,1]Y=(-4.13+132.93x)/(1-0.000 8x),R2均>0.999。线性回归、二次函数曲线回归和Padé[1,1]近似3种浓度QC计算结果偏差10%以内(表3)。
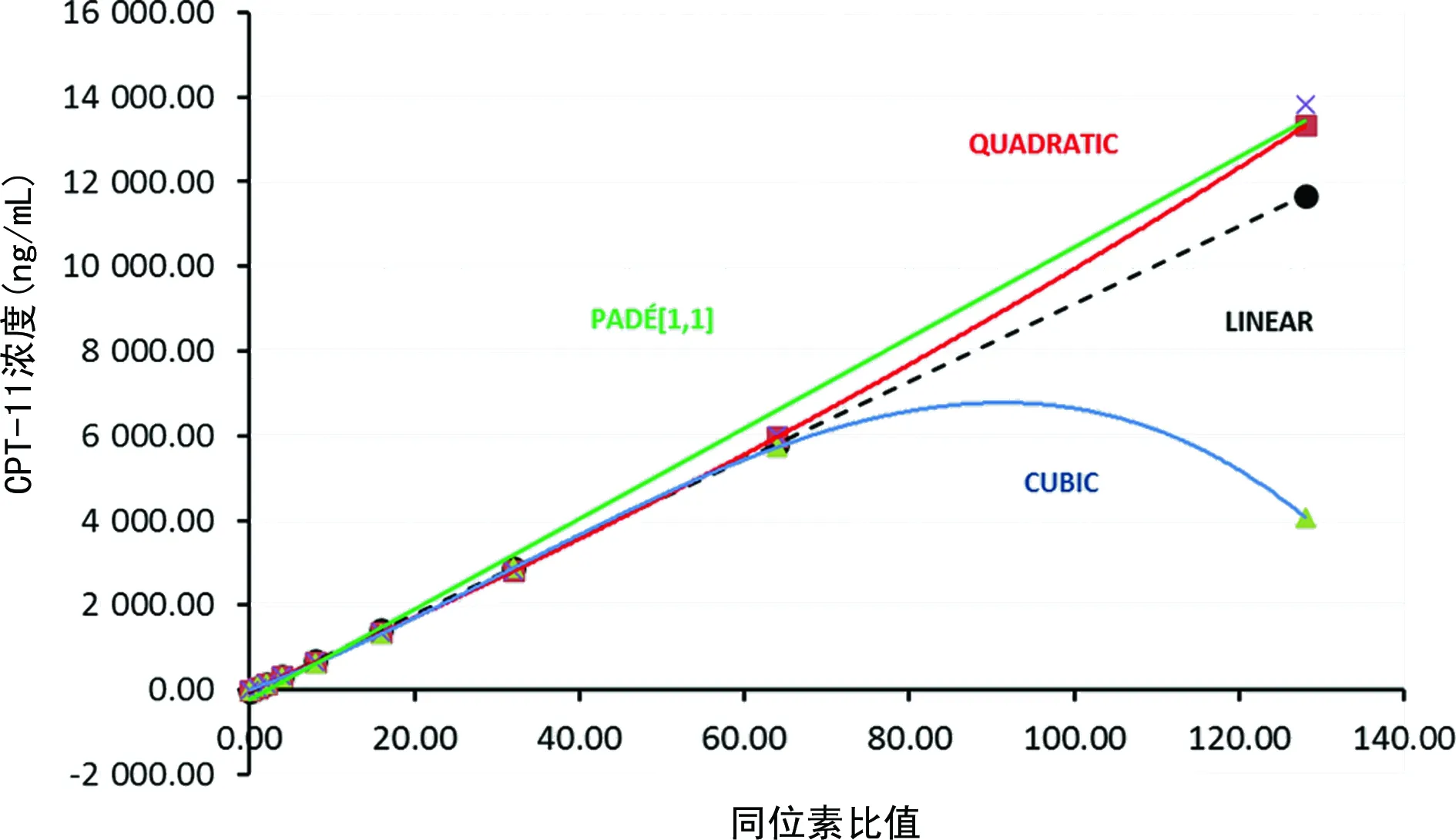
注:黑色虚线为线性方程,正方形表示曲线为二次函数,三角形表示曲线为三次函数,十字曲线为Padé[1,1]近似。
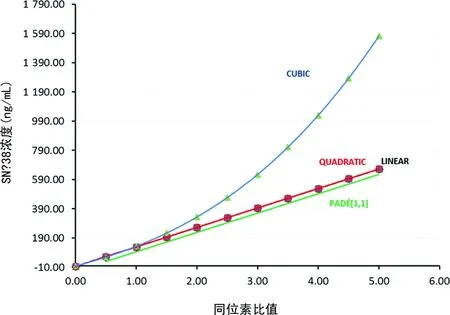
注:黑色虚线为线性方程,正方形表示曲线为二次函数,三角形表示曲线为三次函数,十字曲线为Padé[1,1]近似。
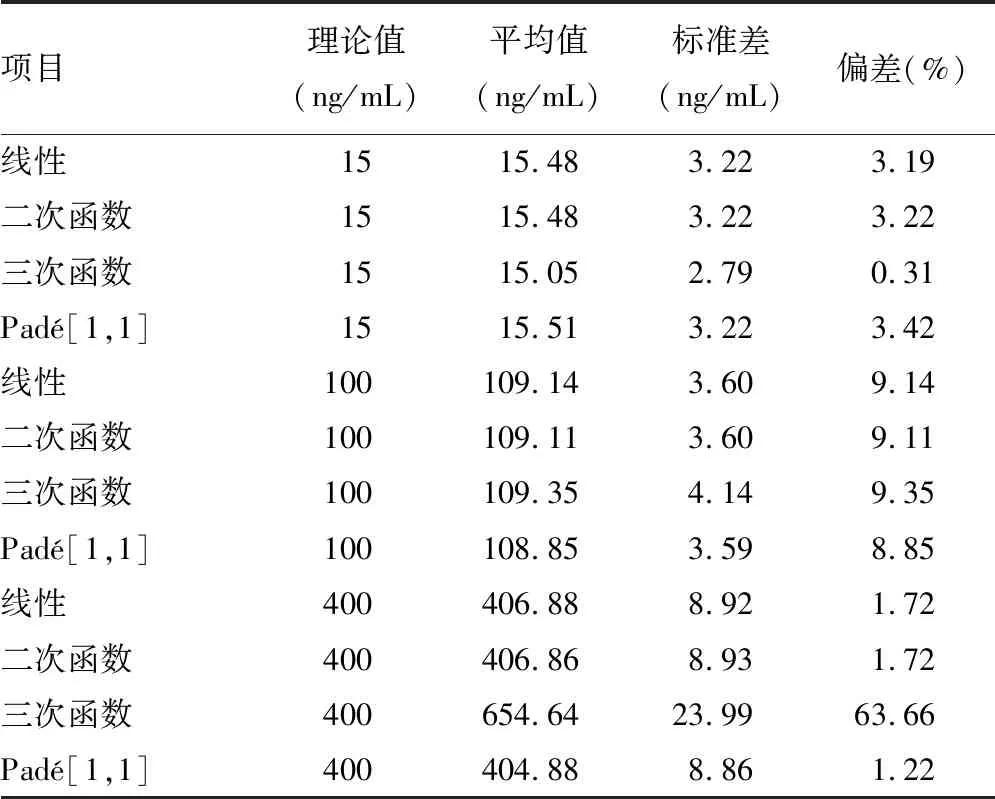
表3 基于同位素稀释质谱法的4种标准曲线计算SN-38 QC样本偏差
对SN-38G的校准范围是1.0~1 000 ng/mL,方法线性定量范围2.0~500.0 ng/mL。应用LINEST分析4种标准曲线,外推校准曲线,见图5。SN-38G 4种计算公式分别为:线性函数y=41.91x-9.15;二次函数y=1.62x2+24.62x+4.64;三次函数y=0.25x3-2.53x2+40.57x-2.04;Padé[1,1]y=(3.3+27.7x)/(1-0.031 4x),R2均>0.999。二次函数和三次函数曲线回归,Padé[1,1]近似3种浓度QC计算结果偏差15%以内(表4)。
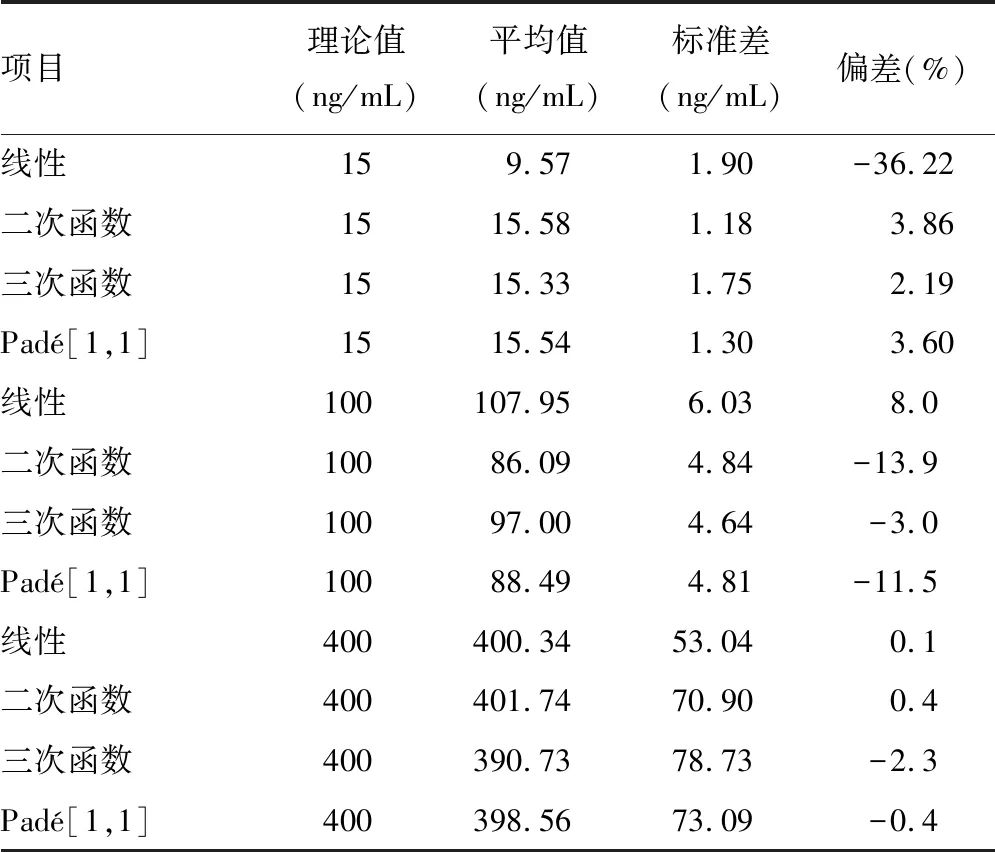
表4 基于同位素稀释质谱法的4种标准曲线计算SN-38G QC样本偏差
对APC的校准范围是4.9~2 500.0 ng/mL,方法线性定量范围9.8~625.0 ng/mL。应用LINEST分析4种标准曲线,外推校准曲线见图6。4种计算公式分别为:线性y=123.85x-211.96,R2=0.989;二次函数y=2.65x2+32.45x+40.96;三次函数y=0.071 5x3-1.204x2+80.81x-27.67;Padé[1,1]y=(-2.71+60.54x)/(1-0.014 7x),R2均>0.999。只有Padé[1,1]近似3种浓度QC计算结果偏差10%以内(表5)。

注:黑色虚线为线性方程,正方形表示曲线为二次函数,三角形表示曲线为三次函数,十字曲线为Padé[1,1]近似。

注:黑色虚线为线性方程,正方形表示曲线为二次函数,三角形表示曲线为三次函数,十字曲线为Padé[1,1]近似。

表5 基于同位素稀释质谱法的4种标准曲线计算APC QC样本偏差
3 讨 论
复杂物质组分含量的定量分析是当前医学检验研究中的重要问题之一,而质谱分析技术在生物医学领域的迅速应用无疑提供了强有力的分析手段。校准曲线的准确度也决定了样本定量的准确度。在生物分析和临床化学领域中,通常以线性拟合用于校准曲线,非线性的校准并不常用[6-8]。但同位素稀释质谱法常常存在非线性响应,当实验者观察到非线性响应时,通常会采用经验多项式(一般以二次函数曲线拟合为主)来表示观察到的曲率,而忽略非线性的物理基础。尽管所有二次函数都是非线性的,但并非所有非线性方程都是二次的,且对于重要的校准数据,某些非二次非线性方程可以适当地用作校准函数。为探讨此问题,本实验采用同位素稀释质谱法对伊立替康及其3种主要代谢产物进行检测,进行线性和非线性拟合,以及一种非二次非线性拟合方程对数据进行分析。
本文对每种化合物均使用了IS,用以更好地完成校准曲线和(或)校正基质效应等影响因素。同时,本文发现CPT-11 D10中存在相对少量的SN-38(SN-38 D3中的程度较小)会导致SN-38的校准曲线出现问题,推测SN-38检测下限(LLMI)应该不低于2.0 ng/mL,代谢产物APC亦存在类似情况。本文初步实验中没有发现该方法存在其他重要问题,无残留效应,批内和批间精密度CV<10%[9],QC样品的加标回收率准确性,以及基质效应和样本回收率均根据MATUSZEWSKI等[10]确定的比例都在80%~120%,多数在85%~115%。
实验中所有的拟合分析是利用Excel中LINEST函数公式完成,线性拟合未采用加权最小二乘法分析,因此可见CPT-11、SN-38G和APC 3种分析物低浓度时偏差>15%,但如果采用1/x2加权系数,可能意味着高浓度QC样本结果出现偏差>15%。SN-38是CPT-11的活性代谢产物,APC和SN-38G是其无活性代谢产物,4种分析物共享主要结构(SN-38),而且现有商品化标准品种纯度不可能达到100%。从4种分析物的4种校准曲线拟合分析结果看,不同的分析物对线性函数、二次函数、三次函数和Padé[1,1]近似4种方程的偏向性存在不同。总体而言,在不采用加权系数分析时,Padé[1,1]近似获得的校准曲线中,高中低3种QC偏差相对更小且稳定。
对于分析物定量分析而言,尤其是采用稳定同位素作为内参时,并非所有的分析方法都符合线性响应函数。因此,不同的实验室为避免基于同位素的定量分析中的非线性校正亦采用不同的分析方法,包括:忽略非线性部分的数据,使用反比建立线性函数[11];应用偏最小二乘回归统计加权方案来抵消非线性的影响[11]或将坐标变换对数值。但在同位素稀释质谱方法中,尤其对于多种结构相似分析物及其同位素内标物的混合物,这两种物质的同位素比和质量比之间的一般关系既不是线性也不是多项式。相反,它是两个线性函数的比率[5]。本文建议实验中优先以线性拟合校准曲线,但同位素稀释校准曲线拟合时,线性或曲线可能会引入不必要的误差,此时可应用有理Padé[1,1]近似方程和线性最小二乘拟合来避免这些误差。
