三元体系Na2CO3-NaF-H2O 298.15 K和318.15 K相平衡研究
2022-03-11卢子钰柳召刚吴锦绣胡艳宏刘兴宇
卢子钰,柳召刚,吴锦绣,胡艳宏,刘兴宇
(1.内蒙古科技大学材料与冶金学院,内蒙古包头 014010;2.轻稀土资源绿色提取与高效利用教育部重点实验室;3.内蒙古自治区稀土湿法冶金与轻稀土应用重点实验室;4.内蒙古大学化学与化工学院)
氟化钠是一种无色发亮晶体或白色粉末,溶于水和氢氟酸,微溶于醇;其水溶液呈弱碱性,主要用于农业杀菌剂、杀虫剂、木材防腐剂等[1]。包头混合稀土矿中含有6.3%的氟和3.4%的磷(均以质量分数计)[2],经过酸浸、碱溶、水洗处理其中的氟、磷均被集中到水洗液中。这些废水处理起来难度很大,可以对其中的氟通过水盐相图的方法以氟化钠的形式进行分离回收。
近年来水盐相图的研究得到很高的关注。张杰等[3]从水盐体系相平衡实验和理论研究两个方面综述了国内外相关的研究进展及研究方法。而含有NaF和Na2CO3的多元水盐体系也被中外学者多次报道。NaF作为一种常见的化合物,单独含有NaF的水盐体系有很多,比如:NIZOMOV等[4]做了NaFNaHCO3-H2O体系在25℃的相平衡研究;李红霞[5]做了四元体系NaF-Na3PO4-NaOH-H2O及其子体系离子浓度测定方法的探究。为使各离子的测量值更加准确,故他们针对水盐体系中各离子浓度的测定方法进行了研究。Na2CO3与NaF同时在水盐体系中的研究也较常见,比如:WANG等[6]研究了308.15 K和323.15 K下Na-F-CO3-HCO3-H2O体系溶解度的测定及Na-F-Cl-SO4-CO3-HCO3-H2O体系Pitzer平衡模型的建立;FELMY等[7]研究了氟化物和磷酸盐成分在环境模拟程序(ESP)中Pitzer模型的增强型热力学数据库的开发。上述两篇文献都包含了对氟化物和磷酸盐Pitzer模型的研究,通过对实验值和计算值的对比,大大提高了数据的准确性。郝晴等[8-9]研究了Na2CO3-NaF-H2O三元水盐体系在313.15 K和343.15 K的相平衡。虽然前人的研究已经积攒了很多关于NaF和Na2CO3的实验数据,但是想要系统地研究这两种物质的水盐相平衡,必须单独研究该体系,并且得到该体系更多温度的实验数据,使研究更完整、更具有说服力。
1 实验部分
1.1 试剂和仪器
试剂:氟化钠和碳酸钠(均为分析纯);盐酸标准溶液(浓度为0.1 mol/L);氟离子标准溶液(浓度为0.100 0 mol/L);氟离子强度调节剂(TISAB,pH=5.0~5.5);氯化钾溶液(浓度为3.0 mol/L,20℃);酚酞指示剂;甲基橙指示剂。实验用水是由自来水电渗析和混合床离子交换处理得到的去离子水,pH=6,呈弱酸性,电导率小于0.6×10-4S/m。
仪器:MP523型pH/离子浓度测量仪;PHS-3E型pH计;MP5002电子天平;D8 ADVANCE X射线衍射仪(XRD);HH-4恒温水浴锅;JJ-1精密磁力搅拌器。
1.2 实验方法
采用等温溶解平衡法对Na2CO3-NaF-H2O在298.15 K和318.15 K的三元水盐体系饱和NaF固液平衡进行研究。主要研究不同温度下的溶解度变化,所以在控制实验温度的基础上,其他实验条件不变。为研究氟化钠和碳酸钠之间的盐析作用关系,需要先做一个对照实验进行定性分析,再根据对照实验结果进行下一步实验。对照实验分为两组:第一组,往饱和碳酸钠溶液中加入梯度质量的氟化钠固体;第二组,往饱和氟化钠溶液中加入梯度质量的碳酸钠固体。将试样放入298.15 K的恒温水浴锅中持续保温7 d使其达到稳定平衡状态。实验结果发现:第一组实验,饱和碳酸钠溶液的质量分数随着氟化钠质量分数的增加略有降低,但变化非常微弱,而氟化钠的质量分数很低且基本保持恒定;第二组实验,饱和氟化钠溶液的质量分数随着碳酸钠质量分数的增加明显降低。所以针对第二组实验做详细研究。
实验过程:取11个硬质聚乙烯塑料瓶,往每个塑料瓶中分别加入50 mL去离子水和5 g氟化钠粉末,充分摇匀得到饱和氟化钠初始溶液。往饱和氟化钠溶液中分别加入以饱和碳酸钠溶液溶质质量的10%为梯度的碳酸钠固体直到最终饱和,最后一个为纯饱和碳酸钠溶液,共11个样品。将11个塑料瓶置于298.15 K的恒温水浴锅中保温,把磁力转子放入水浴锅中使其自由搅动,保证水浴锅中各区域的温度保持一致。在此状态下保持7 d,使瓶中的固液混合物充分反应,达到平衡状态。到达时间后磁力转子停止搅动,持续保温48 h使溶液得到有效静置。在保温状态下取上清液,分析溶液的物理化学性质和各组分浓度,当分析结果显示化学组成保持恒定时说明反应达到平衡。318.15 K的实验方法和过程同上。
1.3 分析方法
对湿固相和液相分别进行分析。分离后的液相和湿固相中含有氟离子、碳酸根,应用化学定量法对各离子进行检测,得到其在溶液中的浓度。采用pH/离子浓度测量仪测定氟含量;采用盐酸滴定法[10]测定碳酸根含量;采用密度瓶法[11]测定溶液密度。采用X射线衍射仪对平衡固相进行物相分析。
2 结果与讨论
2.1 实验结果
三元体系Na2CO3-NaF-H2O在298.15 K的溶解度对照实验数据见表1。表1数据显示,当在饱和氟化钠溶液中加入少量碳酸钠时,溶液中的氟化钠含量降低;当溶液中碳酸钠含量逐渐增加时,氟化钠的含量呈现线性下降的趋势;当溶液中碳酸钠逐渐达到饱和时,氟化钠的含量微乎其微,且基本保持不变。

表1 三元体系Na2CO3-NaF-H2O 298.15 K溶解度对照实验数据Table1 Comparative experimental dataof the solubility of ternary systemof Na2CO3-NaF-H2Oat 298.15 K
由于没有三元体系Na2CO3-NaF-H2O在318.15 K时的文献数据,所以只能对298.15 K的文献数据进行对比。表2为三元体系Na2CO3-NaF-H2O在298.15 K时共饱点的文献值和实验值数据。对实验值与文献值数据进行了误差分析,结果表明实验值数据精确到平均值为±1.06%以内。说明实验数据在误差范围内,数据真实有效。

表2 三元体系Na2CO3-NaF-H2O 298.15 K共饱点文献值和实验值Table 2 Literature and experimental values of co-saturation point of ternary systemof Na2CO3-NaF-H2Oat 298.15 K
实验测定了三元体系Na2CO3-NaF-H2O在298.15 K和318.15 K的溶解度数据,结果见表3和表4。表4的溶液数据与表3略有不同,前几个样品中的氟化钠含量迅速下降,且大部分氟化钠已经析出;当碳酸钠含量逐渐增加时氟化钠含量有所下降,但变化不大且含量很低。此实验数据说明,当碳酸钠浓度相同时,温度越高氟化钠的析出量越大。证明了升高温度可以加速氟化钠的析出。将该体系在两个温度下的共饱点溶解度数据进行比较(表3~表4中E点为共饱点),其中298.15K下NaF和Na2CO3的质量分数分别为1.81%和20.91%,318.15 K下NaF和Na2CO3的质量分数分别为0.49%和27.01%。由表3~表4中平衡固相可知,该体系在两个温度下的共饱点均未生成固溶体和复盐,该处存在的固相均为NaF和Na2CO3·H2O。但是,318.15 K比298.15 K的共饱点明显后移,298.15 K共饱点的碳酸钠质量分数低于318.15 K的数值,而298.15 K氟化钠的质量分数高于318.15 K的数值。说明随着温度的升高共饱点的固相物质未发生变化,却可以增加Na2CO3的质量分数,使反应加速,使溶液更快地达到平衡状态。

表3 三元体系Na2CO3-NaF-H2O 298.15 K固液平衡组成Table 3 Solid-liquid equilibriumcomposition of ternary systemof Na2CO3-NaF-H2Oat 298.15 K

表4 三元体系Na2CO3-NaF-H2O 318.15 K固液平衡组成Table 4 Solid-liquid equilibriumcomposition of ternary systemof Na2CO3-NaF-H2Oat 318.15 K
根据表3和表4数据,并参考《水盐体系相图及应用》[12]绘图方法,绘制了三元体系Na2CO3-NaFH2O在298.15 K和318.15 K的等温溶解度图,见图1。由图1可知,L区域为全液相区,该区域溶液中包含大量的NaF和Na2CO3·H2O(见表3和表4);S1+L区域为NaF单盐结晶区,该区域本身存在NaF固体,当该区域溶液溶解度达到饱和时会有NaF固体析出;S2+L区域为Na2CO3·H2O单盐结晶区,与NaF结晶区变化一致(298.15 K相图的S2+L区域大于318.15 K相图的S2+L区域);S1+S2+L区域为NaF和Na2CO3·H2O混合结晶区,该区域沉淀中包含NaF和Na2CO3·H2O固体,液相中也存在NaF和Na2CO3·H2O,当达到固相析出条件时液相中的NaF和Na2CO3·H2O同时析出;S1+S2+Na2CO3区域为NaF、Na2CO3·H2O和Na2CO3结晶区,此区域为全固相区。相图中均包含1个共饱点E,此点的平衡固相为Na2CO3·H2O和NaF的混合物。相图中还包含3条单变量溶解度曲线分别为AE、CE和AC,其中AE是单盐结晶区(S1+L)和混合结晶区(S1+S2+L)的分界线,从单盐结晶区(S1+L)到混合结晶区(S1+S2+L)会逐渐有Na2CO3·H2O析出;CE是单盐结晶区(S2+L)和混合结晶区(S1+S2+L)的分界线,从单盐结晶区(S2+L)到混合结晶区(S1+S2+L)会逐渐有NaF析出;AC是混合结晶区(S1+S2+L)和全固相区(S1+S2+Na2CO3)的分界线,这条线内全为固相,其中包含了Na2CO3固体。

图1 三元体系Na2CO3-NaF-H2O 298.15 K(a)和318.15 K(b)相图Fig.1 Phase diagrams of ternary systemof Na2CO3-NaF-H2O at 298.15 K(a)and 318.15 K(b)
2.2 物化性质研究
2.2.1 密度分析
由表3和表4中三元体系Na2CO3-NaF-H2O在298.15 K和318.15 K的密度数据绘制出两个温度的密度曲线图,见图2。由于最后一个数据为饱和碳酸钠溶液,所以取前10组密度数据进行分析。从图2看出:298.15 K时碳酸钠质量分数在20%之前液相密度呈现线性增加的趋势,但是在碳酸钠质量分数为20.0%~22.5%时液相密度出现了一个指数级的增加,增加量为0.05 g/mL,之后的区域密度基本没有变化;318.15 K时碳酸钠质量分数在约27%之前密度曲线呈现线性增加的趋势,但是在碳酸钠质量分数达到30%时曲线有明显的爬升,但基本稳定在此区域,与对应相图对比发现碳酸钠的质量分数已达到共饱点。说明液相密度与碳酸钠的质量分数成正相关,液相密度随碳酸钠质量分数的增加而增大,但是到达共饱点时液相密度有明显的增大,之后基本不变。对比两温度下的密度曲线发现,液相密度与温度密切相关,当温度升高时溶液的密度增大。
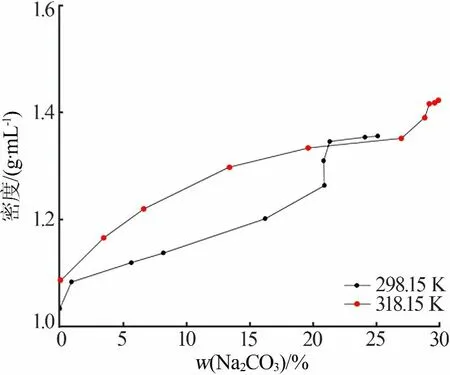
图2 三元体系Na2CO3-NaF-H2O 298.15 K和318.15 K密度Fig.2 Density of ternary systemof NaF-Na2CO3-H2O at 298.15 K and 318.15 K
2.2.2 pH分析
图3为三元体系Na2CO3-NaF-H2O在298.15 K和318.15 K的pH曲线图。从图3看出,两个温度的pH均随碳酸钠质量分数的增加线性增大。曲线的首尾数据分别为饱和氟化钠溶液及饱和碳酸钠溶液的pH。298.15 K时饱和氟化钠溶液pH=10.01、饱和碳酸钠溶液pH=12.02;318.15 K时饱和氟化钠溶液pH=9.89、饱和碳酸钠溶液pH=11.87。两个温度下同种溶液的pH不同,但变化趋势相同,pH均随着温度的升高而减小。通过实验结果分析得出,氟化钠和碳酸钠均为强碱弱酸盐,强碱弱酸盐溶液会随着温度的升高促进水解[13],溶液中电解出来的[H+]会随温度的升高而不断增加,而pH与[H+]呈负相关,所以温度越高pH越小。

图3 三元体系Na2CO3-NaF-H2O 298.15 K和318.15 K pHFig.3 pH of ternary systemof NaF-Na2CO3-H2O at 298.15 K and 318.15 K
2.2.3 共饱点XRD分析
图4为三元体系Na2CO3-NaF-H2O在298.15 K和318.15 K共饱点E平衡固相的XRD谱图。通过与Na2CO3·H2O和NaF的标准XRD谱图对比可以看出,湿渣中存在Na2CO3·H2O和NaF。
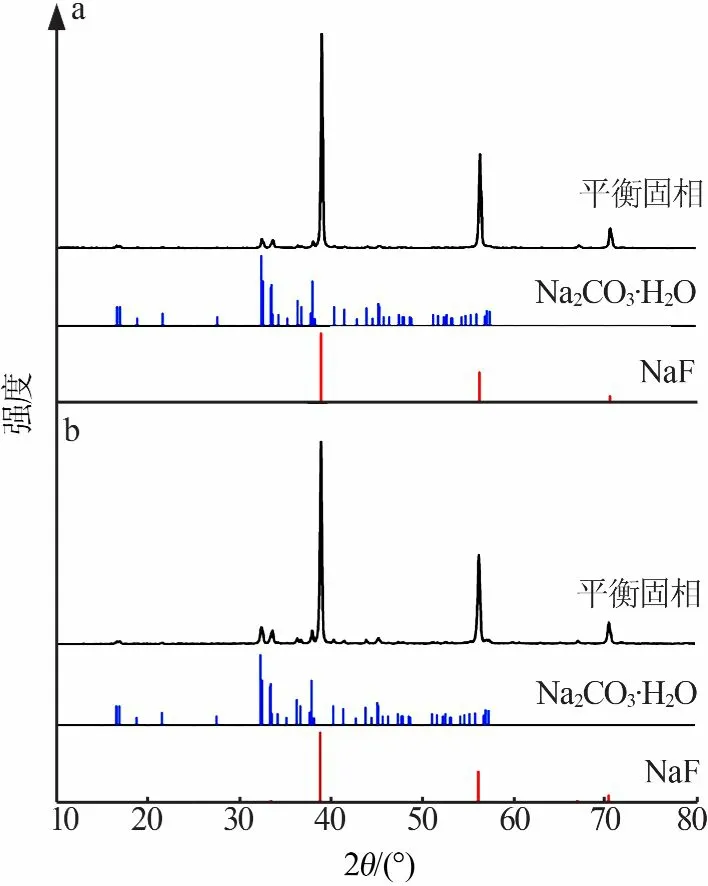
图4 三元体系Na2CO3-NaF-H2O 298.15 K(a)和318.15 K(b)共饱点平衡固相XRD谱图Fig.4 XRDpatterns of co-saturation pointsof ternary systemof Na2CO3-NaF-H2Oat 298.15 K(a)and 318.15 K(b)
3 结论
采用等温溶解平衡法研究了三元体系Na2CO3-NaF-H2O在298.15 K和318.15 K的固液相平衡与相图,得出以下结论。1)氟化钠和碳酸钠互有盐析作用,但碳酸钠对氟化钠的盐析作用强,氟化钠对碳酸钠的盐析作用微弱。2)NaF对Na2CO3的溶解度影响不大,而Na2CO3会降低NaF的溶解度。该体系属于简单共饱型,未生成复盐和固溶体。两个相图所表示的区域大致相同,相图中均包含1个全液相区域(L)、2个单盐结晶区(NaF和Na2CO3·H2O)、1个混合结晶区(NaF+Na2CO3·H2O)和1个全固相区(NaF+Na2CO3·H2O+Na2CO3),以及3条单变量溶解度曲线(AE、CE和AC)和1个共饱点E(NaF+Na2CO3·H2O)。3)当温度不变时,液相密度随着碳酸钠质量分数的增加而增大、溶液pH随着碳酸钠质量分数的增加而增大;当液相组成不变时,液相密度随着温度的升高而增大、溶液pH随着温度的升高而减小。
