参芪扶正注射液联合CapeOX 方案治疗IIB~IV 期胃癌患者的临床疗效
2022-03-10宋亚熙
宋亚熙
新乡市中心医院,新乡医学院第四临床学院,河南 新乡 453000
国际癌症研究中心(IARC) 2018 年统计,全世界胃癌死亡78.32 万例,在恶性肿瘤病死率中居第3 位,新发103.41 万例,在恶性肿瘤发病率中居第5 位,消化道恶性肿瘤中胃癌发病率居高不下[1-2]。现阶段化疗仍是治疗胃癌的重要策略,其中CapeOx方案即卡培他滨+奥沙利铂可杀灭癌细胞,使患者获益,但会不同程度影响患者免疫功能,增加感染、肿瘤免疫逃逸等风险,因此改善患者免疫功能至关重要[3-4]。参芪扶正注射液具有益气扶正的功效,且体外试验表明,其能通过肿瘤相关巨噬细胞提高癌细胞对铂类化疗的敏感性,逆转癌细胞铂类耐药性,故推测参芪扶正注射液联合CapeOX 方案可能有助于增强疗效[5-6]。本研究探讨参芪扶正注射液联合CapeOX 方案治疗IIB~IV 期胃癌的临床应用价值,为临床提供参考,报告如下。
1 资料和方法
1.1 一般资料
选取2016 年5 月至2019 年10 月新乡市中心医院收治的70 例IIB~IV 期胃癌患者,随机双盲法分为参照组、试验组,各35 例。其中试验组女18 例,男17 例,年龄(45.49±4.06)岁,年龄范围38~57岁,体质量指数(22.89±0.98)kg/m2,体质量指数范围18~25 kg/m2;肿瘤T 分期IIB 期11 例,III 期15 例,IV 期9 例,分化程度低分化5 例,中分化14例,高分化16 例;参照组女16 例,男19 例,年龄(45.98±4.24)岁,年龄范围39~58 岁;体质量指数(22.95±1.01)kg/m2,体质量指数范围19~26 kg/m2;肿瘤T 分期IIB 期11 例,III 期17 例,IV 期7 例,分化程度低分化7 例,中分化18 例,高分化10 例。两组一般资料均衡可比(P>0.05)。本研究经新乡市中心医院,新乡医学院医学伦理委员会批准(伦理号:伦理20220364)。
1.2 纳排标准
(1)纳入标准:符合胃癌诊断标准[7];肿瘤T分期为IIB~IV 期;Karnofsky 功能状态(KPS)评分>70 分[8];患者及近亲属知晓本研究,并签署同意书。(2)排除标准:存在相关药物过敏史者;合并其他系统原发性恶性肿瘤者;预估生存期<3 个月者;心肾肝功能严重不全者;合并急性感染者。
1.3 方法
两组均给予CapeOX 方案治疗,卡培他滨片(齐鲁制药有限公司,国药准字H20133361,规格:0.5 g)口服,1 000 mg/m2,2 次/d,d1~d14;注射用奥沙利铂(先声药业有限公司,国药准字H20093899,规格:50 mg),静脉滴注,130 mg/m2,d1;21 d 为1 周期,共治疗2 个周期。试验组加用参芪扶正注射液(丽珠集团利民制药厂,国药准字Z19990065,规格:250 mL)250 mL/次,1 次/d,静滴,21 d 为一个周期,共2 个周期。
1.4 观察指标
(1)临床疗效。化疗效果评估根据Revised Response Criteria for Lymphoma 标准[9]。进展(PD):出现新病灶或者靶病灶绝对值增加≥5 mm,同时至少最大径之和增加20%;稳定(SD):靶病灶最大径之和增加<20%或减少<20%;部分缓解(PR):靶病灶最大径之和减少<20%且维持时间不低于30 d;完全缓解(CR):肿瘤标志物正常,无新病灶出现,所有靶病灶完全消失,维持时间>30 d。疾病控制率(DCR)=(CR+PR+SD)/35×100%。(2)肿瘤标志物。比较两组治疗前后癌胚抗原(CEA),糖类抗原724(CA724),糖类抗原199(CA199)水平,采用全自动电化学发光免疫分析仪检测。(3)T 细胞亚群。比较两组治疗前后CD3+、CD4+、CD4+/CD8+水平,采用流式细胞仪检测。(4)环状RNA CD2AP(circCD2AP)、微小RNA-4286(miR-4286)。比较两组治疗前后circCD2AP、miR-4286 水平,采用实时荧光定量PCR 法检测。(5)两组毒副反应。
1.5 统计学方法
2 结果
2.1 疗效
试验组疾病控制率(60.00%)与参照组(54.29%)比较,差异无统计学意义(P>0.05)。见表1。

表1 两组疗效比较[例(%)]
2.2 肿瘤标志物
两组治疗后CA724、CA199、CEA 均低于治疗前,且试验组低于参照组(P<0.05)。见表2。
表2 两组肿瘤标志物比较()
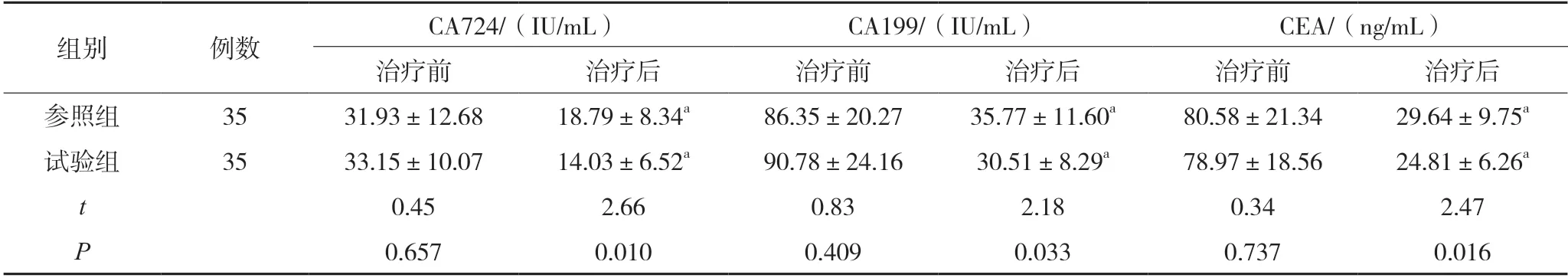
表2 两组肿瘤标志物比较()
注:与本组治疗前相比,aP<0.05。CA724为糖类抗原724;CA199为糖类抗原199;CEA为癌胚抗原。
2.3 免疫功能
试验组治疗后CD4+/CD8+、CD3+、CD4+水平高于治疗前,参照组治疗后CD4+/CD8+、CD3+、CD4+水平低于治疗前(P<0.05);与参照组比较,试验组治疗后CD4+/CD8+、CD3+、CD4+水平较高(P<0.05)。见表3。
表3 两组免疫功能比较()

表3 两组免疫功能比较()
注:与本组治疗前相比,aP<0.05。
2.4 circCD2AP、miR-4286
两组治疗后circCD2AP、miR-4286 均低于治疗前,且试验组低于参照组(P<0.05)。见表4。
表4 两组circCD2AP、miR-4286比较()
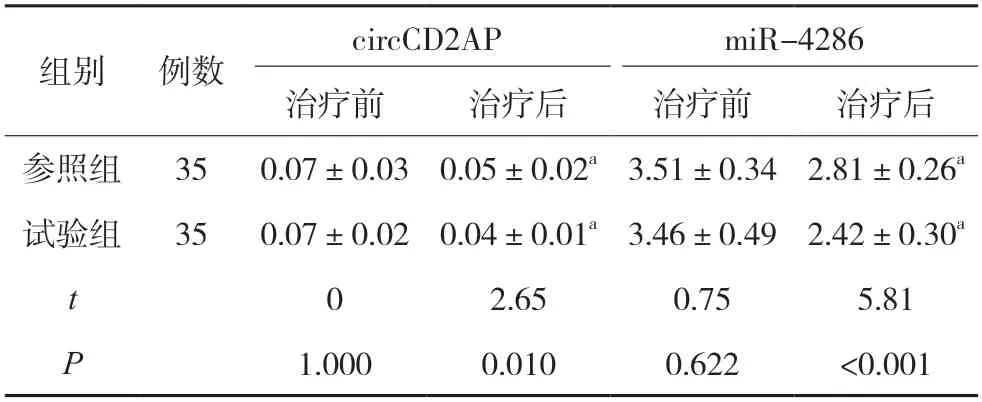
表4 两组circCD2AP、miR-4286比较()
注:与本组治疗前相比,aP<0.05。
2.5 毒副反应
两组毒副反应均为Ⅰ~Ⅱ级,无Ⅲ、Ⅳ级。参照组发生恶心呕吐15 例,骨髓抑制9 例,腹泻3 例;试验组发生恶心呕吐12 例,骨髓抑制2 例,腹泻1例。试验组恶心呕吐、腹泻发生率(34.29%、2.86%)与参照组(42.86%、8.57%)比较,差异无统计学意 义(χ2=0.54、0.27,P=0.461、0.607);试 验 组骨髓抑制发生率为5.71%,低于参照组的25.71%(χ2=5.29,P=0.022)。
3 讨论
胃癌起病隐匿性强,多数胃癌患者错失手术根治时机,就诊时已进展至中晚期[10]。晚期胃癌主要治疗手段是化疗,CapeOX 方案中卡培他滨发挥抗肿瘤作用是在肿瘤组织转化为氟尿嘧啶时胞苷脱氨酶代谢成5'-脱氧-5'氟尿苷,同时经肠黏膜可迅速被吸收,属于氟尿嘧啶类口服药物[11]。临床研究证实,CapeOX 方案影响治疗依从性,毒副反应显著是此化疗方案共性问题,优点是疗效在晚期胃癌治疗中还算稳定[12-13]。因此目前中晚期胃癌的治疗仍是临床棘手问题。根据既往资料,CapeOX 方案化疗治疗胃癌的总有效率为32.50%,仍存在较大提升空间,故考虑联合疗法,以实现增效减毒效果[14-15]。
中医学中,胃癌属于“胃脘痛”“胃积”等范畴,病机多因饮食失节,脾胃受损,运化失司,气结痰凝,气、痰、瘀、毒互结,于正气虚弱时形成肿瘤,日久损耗,又加重气虚症状,故宜治以益气扶正[16-17]。胃癌晚期患者机体多呈失养之象,气血亏虚、脾胃虚弱。中医理论认为,胃癌发病是多种病因如瘀血阻络、正气亏虚、情志不畅、毒聚胃腑等综合作用的结果。故治疗之首选祛邪为佐,以扶正为主的方针。参芪扶正注射液具有扶正固本、益气补虚的功效,属于中成药制剂,药物组成有党参、黄芪等。参芪扶正注射液经现代药理研究发现,其中党参可增强患者的免疫抵抗力,调节免疫系统,其中所含人参皂苷能够提高抗肿瘤活性;黄芪成分黄芪多糖可以调节免疫功能,提高NK 细胞的毒活性,增强网状内皮的吞噬作用[18]。
本研究显示,试验组疾病控制率与参照组相似,但治疗后CA724、CA199、CEA 低于参照组,CD3+、CD4+、CD4+/CD8+水平高于参照组,提示参芪扶正注射液联合CapeOX 方案化疗治疗IIB~IV 期胃癌,能在一定程度上增强癌细胞杀灭效应,提高机体细胞免疫功能。试验组各肿瘤标志物水平较低,考虑与联合参芪扶正注射液时,获得完全缓解、部分缓解患者数量相对较多有关。参芪扶正注射液重用党参、黄芪,可益气补虚,扶正固本,从而实现祛邪效果。现代医学认为,参芪扶正注射液能活化T 细胞,增强巨噬细胞吞噬能力,提高机体对肿瘤监视效应,并能增强自然杀伤细胞杀伤力,同时还可调节细胞内代谢和微循环,增加化疗敏感性[19]。另有资料[20]显示,参芪扶正注射液可提高骨髓造血干细胞的增殖分裂能力,本研究显示试验组骨髓抑制发生率低于参照组,可能与这一机制有关。circCD2AP、miR-4286 在胃癌患者中表达显著升高,其中circCD2AP 与肿瘤浸润深度、临床分期等病理特征相关,miR-4286 与肿瘤细胞分化程度有关[21]。本研究显示,参芪扶正注射液联合CapeOX 方案化疗,能降低circCD2AP、miR-4286,有利于患者病情的控制与改善,但其详细分子机制尚不明确,有待后续的进一步探讨。
综上所述,参芪扶正注射液联合CapeOX 方案化疗治疗IIB~IV 期胃癌,能在一定程度上增强癌细胞杀灭效应,提高机体细胞免疫功能,减少骨髓抑制毒副反应的发生。
