Fenton氧化法与电絮凝法对水中盐酸四环素的去除
2022-03-10杨晓婷邱海燕谯梦丹兰贵红
杨晓婷,邱海燕,谯梦丹,石 宇,徐 波,*,兰贵红,高 虹
(1.西南石油大学化学化工学院,四川成都 610500;2.吉林油田分公司油气工程研究院,吉林松原 138000)
抗生素是一种具有抑制和杀灭病菌及致病微生物能力的化学物质,近年来被普遍使用,导致其使用量非常大甚至出现滥用。据统计,我国36种抗生素向环境的总排放量为53 800 t,其中46%会排放进入河流,54%会被土壤吸收[1]。环境中抗生素的大量残留会导致耐药基因和细菌的大量产生[2-3],造成水体、沉积物和土壤的污染。盐酸四环素(tetracycline hydrochloride,TC)作为医疗和畜牧业常用抗生素,在水体、土壤等介质中大量残留。在水环境中,残留的TC不仅会影响水中微生物的组成与活性,还会对水生生物产生毒害作用,从而破坏水环境的生态平衡,给人类健康和生态系统带来影响[4]。
目前,物化法[5-7]和生物法[8-9]是处理抗生素废水的常用方法,但这些方法各有局限。高级氧化技术(AOPs)作为一种降解废水中难降解有机物的方法,包括臭氧氧化法[10]、湿式氧化法[11]、光催化氧化法[12]等。在AOPs中,Fenton氧化法作为处理抗生素废水的传统方法,因其氧化效率高且操作简单而得到普遍应用[13-14]。同样,电絮凝法(electroflocculation,EF)因为处理成本低廉、效率高、不会造成二次污染以及污泥产量少等优点而应用于抗生素废水的处理[7,15]。然而,报道这两种方法单独运用于抗生素处理的研究虽多,但缺乏两种方法同做比较的研究。
本试验以TC溶液为处理对象,研究Fenton氧化法的H2O2投加量、FeSO4·7H2O投加量、初始pH、反应时间和初始TC浓度对TC去除效果的影响,以及EF中电流强度、极板距离、电解时间和初始TC浓度对TC去除效果的影响,并比较Fenton氧化法与EF对TC去除中哪一种效率更高,为去除水中TC的实际应用提供参考。
1 试验材料和方法
1.1 试验试剂及仪器
试验试剂:TC;柠檬酸三钠(分析纯);FeSO4·7H2O(分析纯);H2O2(30%);Na2SO4(分析纯);NaOH(分析纯);浓H2SO4(98%)。其余试剂均为分析纯,试验过程中所有水溶液均使用超纯水配制。
试验仪器:电解槽;多用电泳仪(DYY-10C型电泳仪);磁力搅拌器(78-1);COD消解仪(COD-571-1);紫外分光光度计(UV-1800);PHS-3C型精密pH计。
试验装置:电絮凝装置如图1所示。电絮凝反应体系由电解槽、金属电极、磁力搅拌器和多用电泳仪组成,其中反应器大小为100 mm×100 mm×100 mm,有效容积为0.9 L。

图1 电絮凝试验装置Fig.1 Experimental Setup of EF Process
1.2 试验水质
试验用水采用TC(100 mg/L)和柠檬酸三钠(50 mg/L)混合配制的溶液,其CODCr含量为(246.4±20.0) mg/L,pH值为5.4±0.2。
1.3 试验方法
1.3.1 Fenton氧化试验方法
室温下量取100 mL配制溶液于250 mL烧杯中,用一定浓度的NaOH和H2SO4调节pH至指定范围,然后在磁力搅拌器的搅拌下加入一定量的FeSO4·7H2O,待其溶解后加入一定体积的H2O2(30%),反应一定时间后,静置一段时间,取滤清液测定TC去除率、CODCr去除率。
1.3.2 电絮凝试验方法
每次试验在电解槽中加入300 mL待处理配制溶液,并加入适量的Na2SO4(100 mg/L)作为电解质。将金属电极(铝、铁电极)插入电解槽中连接电源,电极板(尺寸为96 mm×100 mm,厚为3 mm)每次使用前用砂纸打磨至光滑并用稀盐酸(0.1 mol/L)清洗,每块极板的有效尺寸为19 mm ×100 mm,电极间距根据试验所需用电解槽内的小卡槽调节,电流强度由多用电泳仪调节。反应一定时间,取样过滤后测定TC去除率、CODCr去除率。
1.4 分析项目与测定
(1)CODCr:重铬酸盐法(HJ 828—2017)。
(2)TC:所取水样经0.45 μm水系滤膜过滤后进行各项参数测定。TC用紫外可见分光光度计于276.4 nm波长(此波长下柠檬酸三钠无吸收)下进行定量测定,该波长为TC在200~400 nm的最大吸收波长(图2)。配制TC质量浓度为0、1、2、4、6、8、10、20、40、60 mg/L,用紫外分光光度计在276.4 nm下测量不同TC质量浓度的吸光度A,绘制标准曲线并得到线性回归方程A=0.035 8cTC-0.009 3,相关系数R2=0.999 61,利用线性回归方程可计算不同吸光度下TC的浓度,TC浓度-吸光度标准曲线如图3所示。

图2 TC紫外扫描图谱Fig.2 UV Scanning Spectrum of TC

图3 TC浓度-吸光度标准曲线Fig.3 Standard Curve of TC Concentration-Absorbance
1.5 降解效率评估计算
试验中主要测定的是CODCr和TC含量,根据得到的试验数据可以计算出CODCr及TC去除率,去除率的计算如式(1)和式(2)。
(1)
(2)
其中:η1——TC去除率;
η2——CODCr去除率;
c0——TC模拟废水中原始TC的质量浓度,mg/L;
ci——TC模拟废水经处理后TC的质量浓度,mg/L;
C0——TC模拟废水原始CODCr的质量浓度,mg/L;
Ci——TC模拟废水经处理后CODCr的质量浓度,mg/L。
1.6 电能耗计算
试验中降解所需的电耗能计算如式(3)。
(3)
其中:W——降解1 L抗生素所需要消耗的电能,kW·h/L;
t——电解时间,h;
V——溶液体积,L;
U——平均电压,V;
I——电流强度,A。
2 结果和讨论
2.1 Fenton氧化法对水中TC的去除
2.1.1 H2O2投加量的影响
H2O2是反应过程中·OH的来源,因此,·OH的产生量与Fenton试剂的投加量相关[16]。试验初始TC质量浓度为100 mg/L,初始pH值为5.4,FeSO4·7H2O投加量为2.323 g/L,反应时间为20 min。设置H2O2投加量为0.8、1.0、1.5、2.0、2.5、3.0 mL/L这6个梯度,探究不同H2O2投加量对TC及CODCr去除效果的影响,结果如图4所示。

图4 H2O2投加量对TC及CODCr去除效果的影响Fig.4 Effect of H2O2 Dosage on TC and CODCr Removal
结果表明,TC和CODCr去除率随着H2O2投加量的增加先增加后减少,当H2O2投加量为2.0 mL/L时,TC和CODCr去除率分别为76.74%和60.00%,当H2O2投加量大于2.0 mL/L时,TC和CODCr去除率有减小的趋势。因此,在Fe2+含量一定的条件下,降解效率主要取决于H2O2的投加量[17]。因为在酸性情况下,Fe2+会催化H2O2生成·OH,随着H2O2投加量增加,·OH生成量不断增加并被全部用于降解,故TC和CODCr去除率不断增加;但当H2O2投加量超过一定值时,过多的H2O2部分自身分解,且过多的H2O2与Fe2+反应生成Fe3+,Fe3+会抑制·OH的生成[18],同时过多的H2O2会增加其对·OH的捕获而产生·O2H,·O2H氧化能力低于·OH[19]。因此,当H2O2投加量继续增加时,TC和CODCr去除效果受到微弱抑制。综上,确定最佳H2O2投加量为2.0 mL/L。
2.1.2 Fe2+投加量的影响
试验初始TC质量浓度为100 mg/L,初始pH值为5.4,根据2.1.1确定H2O2投加量为2.0 mL/L,反应时间为20 min。设置FeSO4·7H2O投加量为1.158、1.544、2.316、4.634、5.790、9.264、23.160 g/L这7个梯度,探究不同FeSO4·7H2O投加量对TC及CODCr去除效果的影响,结果如图5所示。

图5 FeSO4·7H2O投加量对TC及CODCr去除效果的影响Fig.5 Effect of FeSO4·7H2O Dosage on TC and CODCr Removal
结果表明,TC及CODCr去除率会随FeSO4·7H2O投加量的增加先增大后减小,当FeSO4·7H2O投加量为4.634 g/L时,TC及CODCr去除率最大,分别为78.46%、70.00%。这是因为在一定范围内,当FeSO4·7H2O投加量少时,Fe2+催化H2O2产生的·OH较少,对TC及CODCr去除效果不好;当FeSO4·7H2O投加量增加时,产生的·OH相应增加,对TC及CODCr去除效果相应提高;但当FeSO4·7H2O投加量超过某一投加量后,过量的Fe2+会消耗H2O2和·OH生成Fe3+,使·OH的产生速率和数量下降,从而使TC及CODCr去除效果降低[18,20]。综上,确定最佳FeSO4·7H2O投加量为4.634 g/L。
2.1.3 初始pH的影响
试验初始TC质量浓度为100 mg/L,根据2.1.1和2.1.2确定H2O2和FeSO4·7H2O投加量分别为2.0 mL/L、4.634 g/L,反应时间为20 min。设置初始pH值为1.0、3.0、5.0、7.0、9.0、11.0这6个梯度,探究不同初始pH对TC及CODCr去除效果的影响,结果如图6所示。
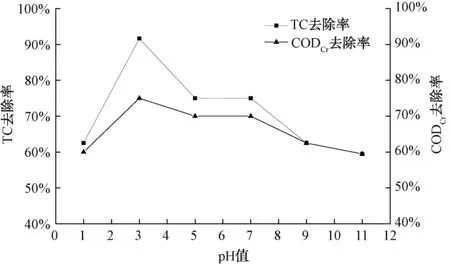
图6 初始pH值对TC及CODCr去除效果的影响Fig.6 Effect of Initial pH Value on TC and CODCr Removal
2.1.4 反应时间的影响
试验初始TC质量浓度为100 mg/L,根据2.1.1、2.1.2、2.1.3确定H2O2投加量为2.0 mL/L、FeSO4·7H2O投加量为4.634 g/L、初始pH值为3.0。设置反应时间为3、5、10、15、20、25、35、45 min这8个梯度,探究不同反应时间对TC及CODCr去除效果的影响,结果如图7所示。

图7 反应时间对TC及CODCr去除效果的影响Fig.7 Effect of Reaction Time on TC and CODCr Removal
结果表明,在反应前20 min内,TC及CODCr去除率随时间的延长而增加;当反应时间为20 min时,TC及CODCr去除率达到最大值,分别为91.67%、75.00%;当反应时间大于20 min时,CODCr去除率随时间的延长而趋于稳定,TC去除率虽然有所下降但下降很少,整体趋势趋于稳定。Fenton氧化法处理废水反应从反应时间可分为2个反应过程,一个是Fe2+的催化降解反应。一个是Fe3+的催化降解反应。·OH和·O2H都有降解有机物质的能力,但·O2H的氧化能力远远小于·OH,且·O2H的产生速率远远小于·OH的产生速率,故在反应初期内可达到较好的处理效果[24];随着反应时间的延长,去除TC的·OH生成量会因为Fenton试剂的逐渐消耗而逐渐减少,使TC去除率最终趋于稳定[20]。可见,最佳反应时间为20 min。
2.1.5 初始TC浓度的影响
试验以100 mL配制溶液计算,由2.1.1、2.1.2、2.1.3、2.1.4确定H2O2投加量为2.0 mL/L、FeSO4·7H2O投加量为4.634 g/L、初始pH值为3.0、反应时间为20 min。设置初始TC质量浓度为80、100、120 mg/L这3个梯度,探究不同初始TC浓度对TC及CODCr去除效果的影响,结果如图8所示。
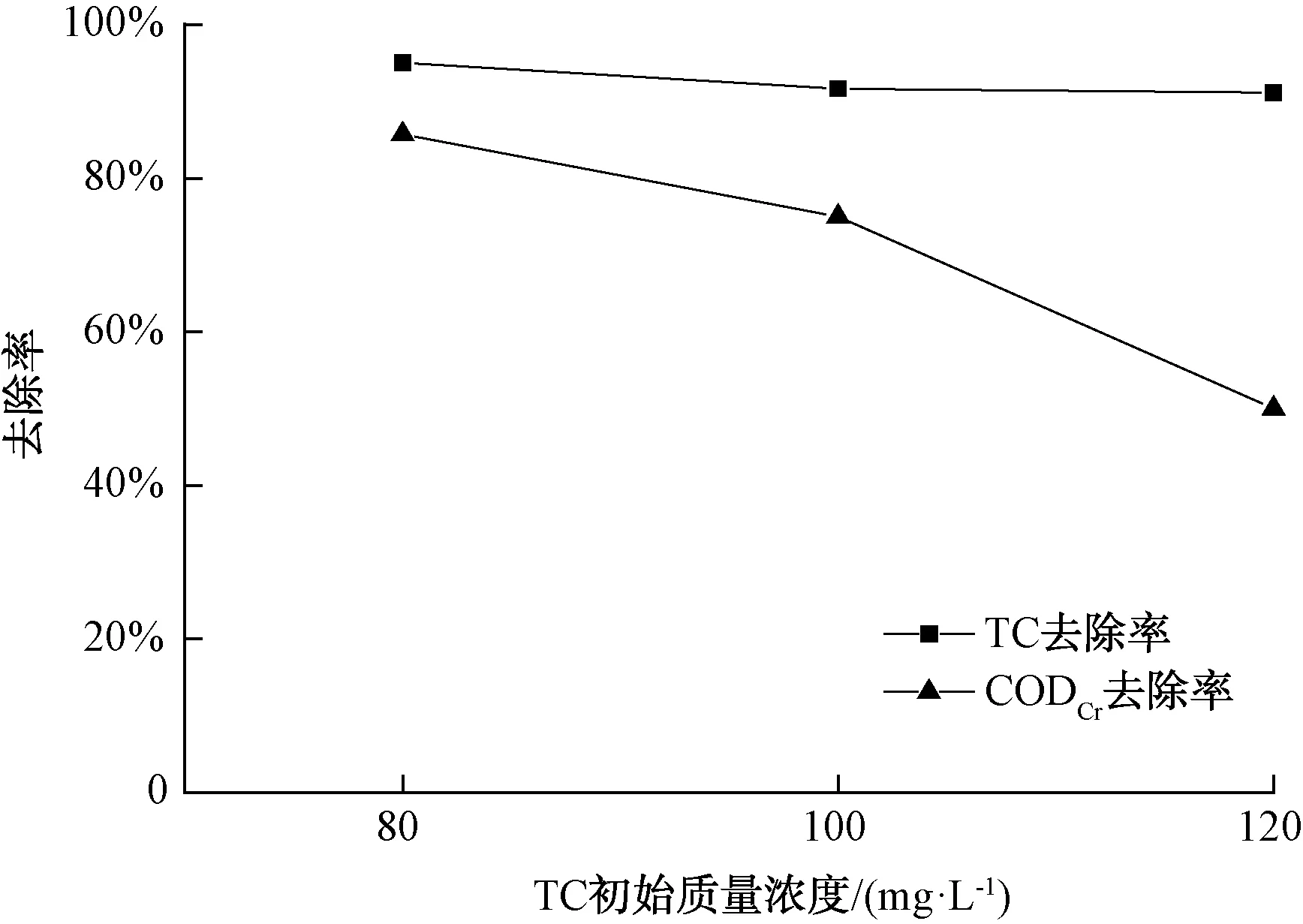
图8 初始TC浓度对TC及CODCr去除效果的影响Fig.8 Effect of Initial Concentration of TC on TC and CODCr Removal
结果表明,在一定浓度范围内,随初始TC浓度的增大,TC及CODCr去除率减小。当初始TC质量浓度从80 mg/L增大到100 mg/L时,TC去除率从95.01%降到91.67%,CODCr去除率从85.71%降到75.00%;当初始TC质量浓度继续增大到120 mg/L时,TC去除率下降了0.53%,CODCr去除率下降了20.00%。因为在Fenton试剂产生·OH的量一定的情况下,能氧化降解TC的量是一定的,但单位体积TC分子数量增大,与·OH反应的TC分子增多,所以TC去除率虽有所下降但下降得不多。此外,由于在给定条件下·OH生成速率恒定,达到相同的矿化度需要更长的处理时间,故100 mg/L时的CODCr去除率比80 mg/L时的CODCr去除率下降了10.71%[25]。因此,当TC浓度逐渐增大时,TC和CODCr去除率会随浓度的增加而减小。可见,TC溶液初始质量浓度为100 mg/L时,虽去除率不是最高的,但却是最合适的。
2.2 电絮凝法对水中TC的去除
2.2.1 电流强度的影响
试验选定铁和铝为电极,初始TC质量浓度为100 mg/L,电极间距为34 mm,电解反应时间为30 min。设置电流强度为0.05、0.10、0.15、0.20、0.30 A这5个梯度,探究不同电流强度对TC及CODCr去除效果的影响,结果如图9所示。
马来酸氟吡汀联合美洛昔康用于前正中开胸二尖瓣置换术患者术后镇痛的临床观察 …………………… 林 涛等(22):3142

图9 电流强度对电絮凝反应体系的影响Fig.9 Effect of Current Intensity on EF Reaction System
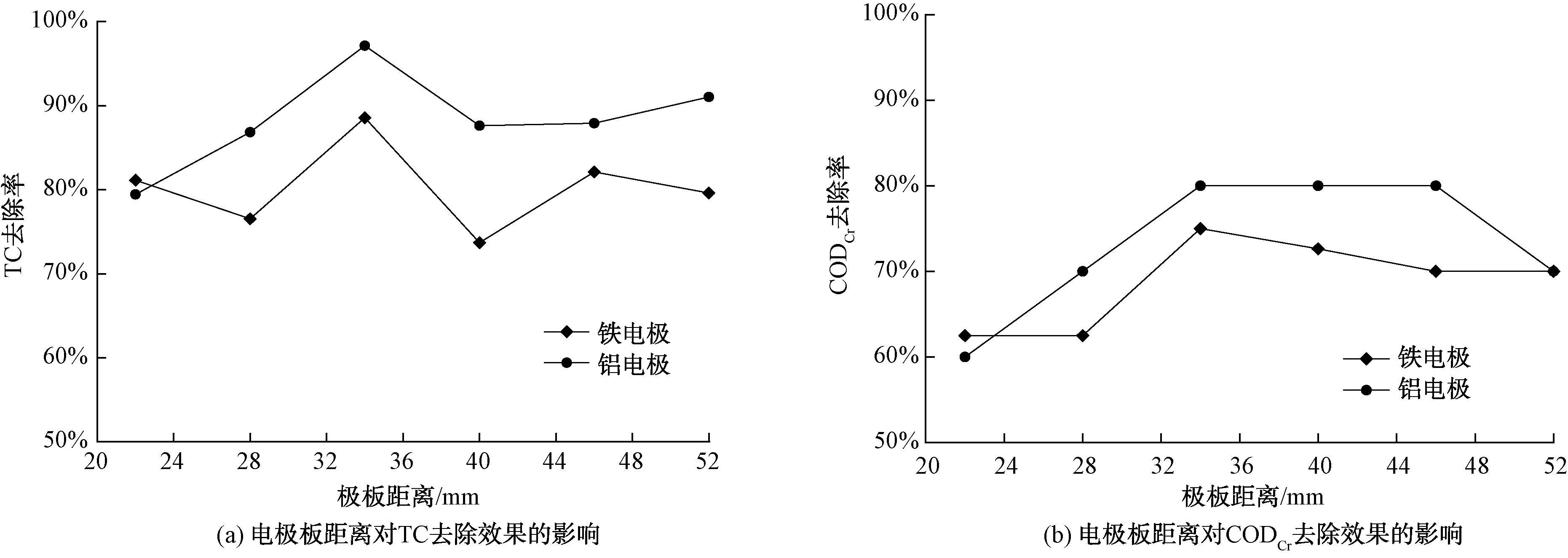
图10 电极板距离对电絮凝反应体系的影响Fig.10 Effect of Inter-Electrode Distance on EF Reaction System
图9表明,当电流强度小于0.20 A时,铝和铁电极的TC和CODCr去除率随着电流强度增大而增大;当电流强度为0.20 A时,铝电极的TC、CODCr去除率分别为97.14%、80.00%,铁电极的TC、CODCr去除率分别为88.57%、75.00%;当电流强度增大到0.30 A时,铝电极的TC去除率下降到87.74%,铁电极的TC去除率不再变化,铝和铁电极的CODCr去除率都保持不变。因此,铝电絮凝对TC的絮凝作用比铁电絮凝更好。因为随着电流强度的增加,金属氧化物量增加,电极板产生处理废水的絮凝剂增多,使胶体颗粒失稳,共同形成更多的沉淀,同时阳极氧化作用也随电流强度的增加而增强,最终促使TC及CODCr的去除率上升[26-27];单质铝的还原性比单质铁强,随着电流的增加,铝会先于铁生成金属离子,使金属离子量多于铁,金属铝离子和OH-之间的碰撞率高于金属铁离子,因此,铝电絮凝会优于铁电絮凝[28]。然而在电流强度增大的同时,可能会产生水氧化和金属氧化的竞争,从而降低TC及CODCr去除效率,还会使电极板的钝化程度加重,带来一些损耗[29]。综上,确定最佳电流强度为0.20 A。
2.2.2 电极板距离的影响
试验选定铁和铝为电极,初始TC质量浓度为100 mg/L,根据2.2.1确定电流强度为0.20 A,电解反应时间为30 min。设置电极间距为22、28、34、40、46、52 mm这6个梯度,探究不同电极板距离对TC及CODCr去除效果的影响,结果如图10所示。
图10表明,在极板距离为22~52 mm时,铁和铝电极的TC和CODCr去除率随着电极板间距增大而先增大后减小。当电极间距为34 mm时两电极的去除率均取得最大值,铁电极的TC、CODCr去除率分别为88.57%、75.00%,铝电极的TC、CODCr去除率97.14%、80.00%。这可能是因为此时电极板产生的大量氢氧化物絮体有充足的空间与废水中的TC接触反应,去除率较高。当电极板间距过小时,虽然此时板间电阻较小、耗能少且氢氧化物絮体大量生成,但过小的电极板间距会影响电解反应中电子和离子的扩散[30];而随着电极板间距增加,电阻也增加,电解反应中电子和离子迁移的速度变慢,离子和羟基聚合物之间的相互作用减少,使去除效果较差[27]。因此,最佳电极板距离确定为34 mm。
2.2.3 电解时间的影响
试验选定铁和铝为电极,初始TC质量浓度为100 mg/L,根据2.2.1、2.2.2确定电流强度为0.20 A、电极间距为34 mm。设置电解反应时间为5、8、13、16、20、30、35 min这7个梯度,探究不同电解时间对TC及CODCr去除效果的影响,结果如图11所示。
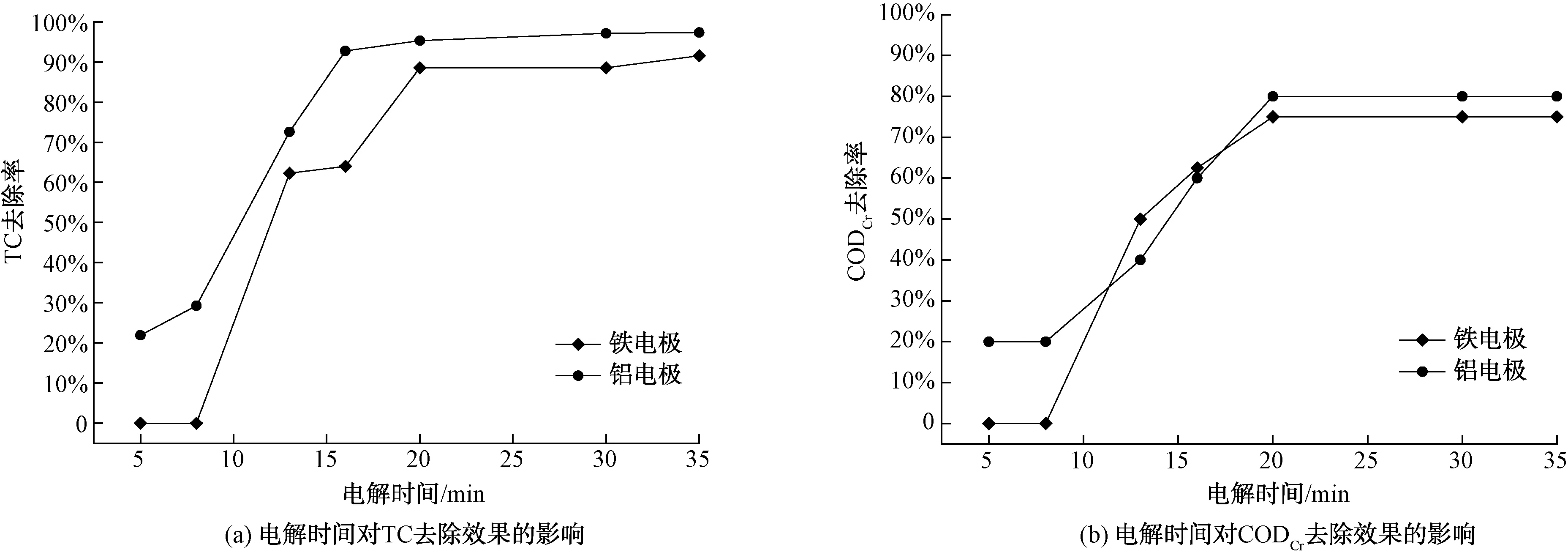
图11 电解时间对电絮凝反应体系的影响Fig.11 Effect of Electrolysis Time on EF Reaction System
图11表明,铁和铝电极的TC和CODCr去除率都随着电解时间的延长先增加后趋于稳定。当电解时间为20 min时,铁电极的TC、CODCr去除率分别为88.57%、75.00%,铝电极的TC、CODCr去除率分别为95.32%、80.00%。而当电解时间大于20 min时,铁和铝电极的TC去除率虽然在增大但增加的趋势减缓,CODCr去除率则变化不大。这是因为随着时间的增加,更多的絮凝剂被释放到水中[31]。根据法拉第方程可知,当电流强度一定时,电解反应过程中金属电极失去电子形成金属离子的质量与电解时间成正比,电解时间增加,电极释放出的金属离子数量随之增加,与·OH形成更多的氢氧根化物絮凝体,吸附更多的污染物颗粒,如式(4)[32]。
ΔM=MIt/(nF)
(4)
其中:ΔM——产生的离子质量,kg;
M——物质的摩尔质量,kg/mol;
I——反应电流,A;
t——反应时间,min;
n——化合物中正化合价总数的绝对值;
F——法拉第常数,9.65×104C/mol。

2.2.4 初始TC浓度的影响
试验选定铁和铝为电极,以300 mL配制溶液计算,根据2.2.1、2.2.2、2.2.3确定电流强度为0.2 A、电极间距为34 mm、电解时间为20 min。设置初始TC质量浓度为80、100、120 mg/L这3个梯度,探究不同初始TC浓度对TC及CODCr去除效果的影响,结果如图12所示。
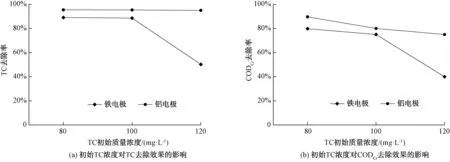
图12 初始TC浓度对电絮凝反应体系的影响Fig.12 Effect of Initial Concentration of TC on EF Reaction System

2.3 Fenton氧化法与电絮凝法对水中TC的去除比较
试验以300 mL配制溶液计算,分别采用电絮凝法和Fenton氧化法处理,其中电絮凝法分别选定铁和铝为电极,在电流强度为0.2 A、平均电压U=135 V、电极间距为34 mm、电解时间为20 min下电絮凝降解100 mg/L的TC溶液,Fenton氧化法以H2O2投加量为0.19 mL/L、FeSO4·7H2O投加量为0.441 7 g/L、反应时间为20 min降解100 mg/L的TC溶液,探究不同体系对TC及CODCr去除效果的影响。结果如图13所示。
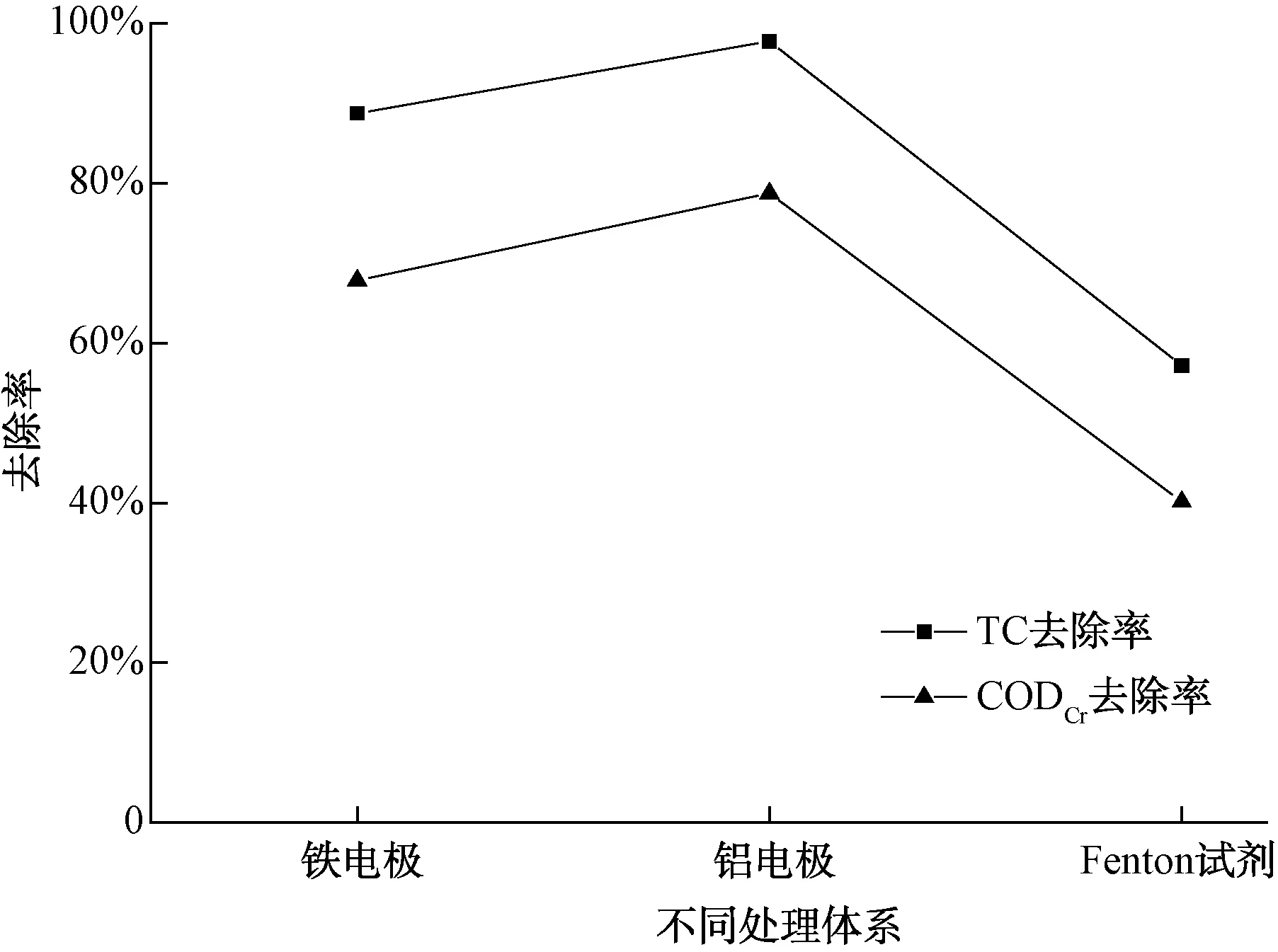
图13 两种体系对TC及CODCr去除效果的影响Fig.13 Effect of Two Systems on TC and CODCr Removal
图13表明,在相同能耗与成本下,铝电极的TC、CODCr去除率分别为97.75%、78.74%,铁电极的TC、CODCr去除率比铝电极小,分别为88.74%、67.83%,Fenton氧化法的TC、CODCr去除率分别为57.18%、40.14%。由此可知,在能耗或成本相同下铝电絮凝对100 mg/L的TC溶液的TC及CODCr去除效果更好。并且从铝电絮凝对TC及CODCr的高去除率可以推断出TC溶液经过电絮凝处理后可能被分解成分子小碎片,提高了废水的生物可降解性。根据相关文献,实际生产废水中生化法对TC有较高的去除效果(表1),去除效果最高可达97%,但能去除的初始TC浓度都很低,而本试验铝电絮凝法虽然处理的是TC溶液,但能去除初始TC浓度高于生化物法的几十倍,且TC去除率高达97.75%,故本试验处理100 mg/L的TC溶液时铝电絮凝法比生化法更优。
对铝电絮凝20 min后的TC溶液进行GC-MS检测(图14),结果表明电絮凝之后的一部分TC产物为含有喹啉、多环等新官能团化合物,而不同新官能团化合物会有不同的毒性,故TC溶液电絮凝后的毒性可能不会遵循下降趋势[39-40]。

表1 生产废水中TC的去除Tab.1 Removal of TC in Production Wastewater
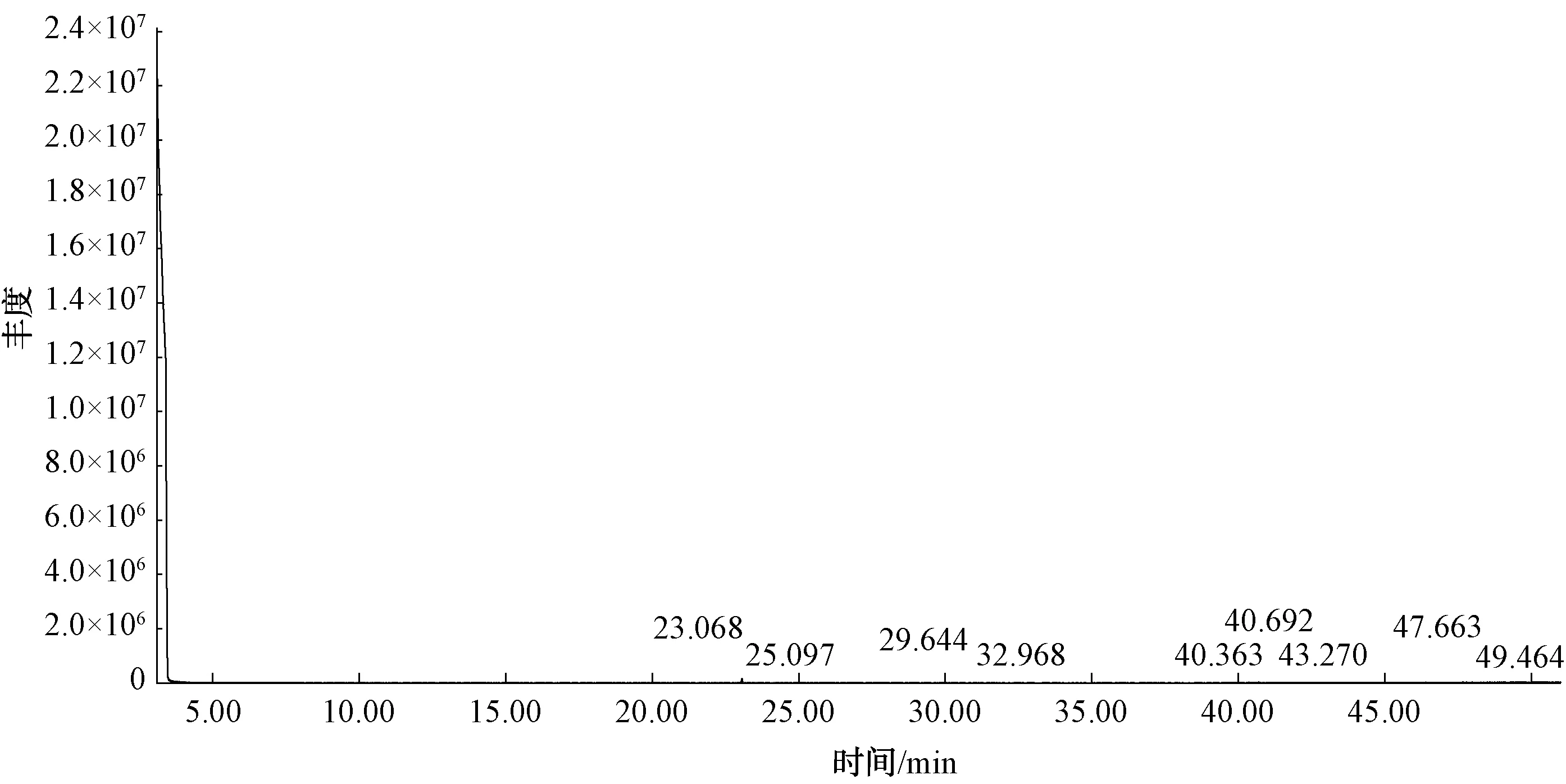
图14 TC溶液电解20 min后产物GC-MS谱图Fig.14 GC-MS Spectrum of Product after 20 min of Electrolysis of TC Solution
试验处理300 mL配制溶液,电絮凝体系所消耗电能为0.03 kW·h/L,根据成都市平均电价为0.491 3元/(kW·h),电费价格为14.74元/(t水),Fenton氧化法中H2O2价格为0.024元/mL,FeSO4·7H2O价格为0.023 04元/g,Fenton氧化法处理成本为14.74元/(t水),但不包括pH调节和回调的费用。
综上,铝电絮凝法只有在处理高浓度的TC溶液时才有使用的价值,在处理低浓度的TC溶液时采用生化法较为经济。
3 结论
(1)100 mg/L的TC溶液分别在Fenton氧化法和EF降解最优条件下的处理效果:Fenton氧化法对TC、CODCr去除率分别为91.67%、80.00%;铁电极的TC、CODCr去除率分别为88.57%、75.00%;铝电极的TC、CODCr去除率分别为95.32%、80.00%。铝电极处理TC的效率高于铁电极和Fenton氧化法。
(2)Fenton氧化法处理100 mg/L的TC溶液,Fe2+催化H2O2生成大量的·OH氧化降解废水中的TC,反应速率快,处理效果好,但处理后的溶液中含有Fe2+、Fe3+,使废水色度大、矿化度高,且当处理溶液中的有机物质时,可能会有H2O2药品的浪费,这会增加一定的投资成本。而EF处理100 mg/L的TC溶液,不用添加药剂,电解时极板会生成含有絮凝作用的物质,将溶液中的细小颗粒进行沉淀,且处理后的TC溶液色度小、矿化度低,此外EF具有设备简单、操作方便、占地面积小、容易实现自动化的优点。
