二氧化钛紫外光(UV/TiO2)降解2,4,6-三氯酚的多因素影响
2022-03-10王希诚高乃云
王希诚,高乃云
(1.同济大学污染控制与资源化研究国家重点实验室,上海 200092;2.水发规划设计有限公司,山东济南 250100)
氯酚类物质是一类化学稳定的有机化合物,被大量应用于印刷、造纸、印染、皮革、制药等行业,在水体表面、底泥沉积物和土壤中广泛存在,并有可能通过生物体富集作用进入人体[1]。氯酚类物质毒害性较高,是公认的有毒有害污染物。其中,2,4,6-三氯酚(2,4,6-TCP)作为一种典型的氯酚类物质,在地下水、废水以及土壤中都可以检测到[2-3]。目前,中、美、德等国等将其列入控制污染物,世卫组织规定三TCP在饮用水中的允许含量不超过200 μg/L[3-4]。
氯酚类污染物的降解和去除可以采用生物法[5-6]、物理化学法[2,7]、化学还原法[8]、高级氧化法[9]、电极吸附[10]及离子交换[11]等技术,其中高级氧化法由于氧化能力强、处理效果好等优点,是目前研究的热点。UV/TiO2作为一种常见的高级氧化工艺,具有无毒、节能、高效等优点,目前在有机污染物、无机污染物去除方面的研究已经取得了较大的进展[12-16],被认为是一种极具前途的深度净化技术。
本试验基于UV/TiO2高级氧化技术,以纳米TiO2为光催化剂,对配制于水溶液中的2,4,6-TCP进行降解,研究催化剂(TiO2)投加量、2,4,6-TCP初始质量浓度、pH等因素以及不同阴离子对其降解情况的影响,初步探讨2,4,6-TCP的水处理动力学模型。
1 试验
1.1 试验示意图
图1为试验示意图,反应器上部的紫外灯管置于密闭的黑色套筒中,灯管激发紫外线对下方的反应皿照射,同时,在反应皿中加入已知浓度的TiO2和所需浓度的2,4,6-TCP溶液,通过转子与磁力搅拌器将两者混合均匀,从而实现UV/TiO2对目标反应物2,4,6-TCP的高级氧化。
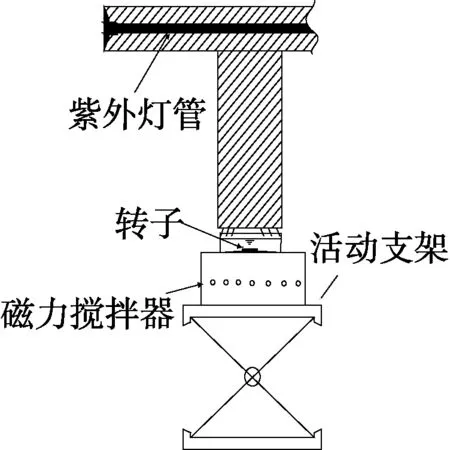
图1 试验示意图Fig.1 Schematic Diagram of Experiment
1.2 试验药剂
使用超纯水将2,4,6-TCP粉末(Sigma公司,纯度>98%)配置为质量浓度为100 mg/L的储备液,根据需要稀释后使用。TiO2(纳米级);流动相甲醇、冰醋酸(Sigma公司,HPLC级);H2SO4、NaOH溶液(分析纯)调节pH;Na2SO4、NaCl、NaHCO3、Na2CO3、NaNO3溶液(分析纯,摩尔浓度均为10 mmol/L)调节阴离子浓度。
1.3 仪器参数及分析方法
紫外灯管(功率为75 W,主波长为253.7 nm,强度为154 μW/cm2);降解反应在室温下[(20±2)℃]进行;飞鸽牌(TGL-16C型)离心机(上海安亭科学仪器厂)。2,4,6-TCP的浓度测定仪器为岛津LC-2010 AHT的高效液相色谱仪;检测波长n=289 nm;色谱柱为Shim-pack VODS(250.0 mm×4.6 mm);流动相V(甲醇)∶V[水(含质量分数为1%的乙酸)]=80∶20;流动相流速为1.0 mL/min;柱温T=40 ℃;分析时间t=10 min。
1.4 试验方法
称取一定量纳米级TiO2于烧杯中,配制成20.0 g/L的悬浊液,使用磁力搅拌器及转子连续搅拌,混合1 h以上,使其充分混合均匀。按照光催化剂(TiO2)所需用量,使用移液枪将配制好的TiO2悬浊液加入反应皿中,使其与2,4,6-TCP反应液避光混合均匀,30 min后置于紫外灯下进行反应。分别选取反应时间为5、10、15、20、30、40、50、60、75、90、120 min的水样离心分离,将不同反应时间取出的水样滴加过量亚硫酸钠(10%)终止反应后,使用台式高速离心机进行离心分离9 min,取上层清液[17-18]进行HPLC检测。
2 结果与讨论
2.1 UV/TiO2与2,4,6-TCP反应动力学分析
TiO2光催化主要反应的历程如下:TiO2的能带是不连续的,由低能的价带[电子(e-)氧化还原电位为-0.5 eV]和高能的导带[空穴(h+)氧化还原电位为2.7 eV]构成,两者之间带隙能为3.2 eV,以λ≤387.5 nm的光波照射TiO2表面,当光子能量≥TiO2的带隙能时,处于价带的e-被激发到导带生成h+,h+与吸附于TiO2表面的OH-或H2O反应,生成羟基自由基(·OH),如式(1)~式(3)[13]。
2TiO2+hv→TiO2(e-)+TiO2(h+)
(1)
TiO2(h+)+OH-→TiO2+·OH
(2)
TiO2(h+)+H2O→TiO2+H++·OH
(3)
此外,还存在UV直接辐射水中的OH-,而在水溶液中激发生成·OH,如式(4)~式(5)。
H2O→H++OH-
(4)
OH-+hv→·OH
(5)
生成的·OH可以在催化剂表面及水体中使有机物矿化为CO2、H2O等小分子无机物,如式(6)。
2,4,6-TCP+·OH→降解产物+H2O
(6)
由于反应过程中生成的·OH在水中寿命极短,小于1 μs,无法进行直接定量计算。目前,常用的做法是采用拟一级动力学方程进行表征。因此,在以下各节各试验影响参数的讨论中,采用式(7)具体阐述TiO2投加量、2,4,6-TCP初始质量浓度、紫外光照强度、pH、阴离子对降解过程的影响作用。
-dC/dt=kOHC0COH
(7)
其中:C——2,4,6-TCP的摩尔浓度,mol/L;
t——反应时间,min;
kOH——·OH氧化2,4,6-TCP的速率常数,L/(mol·min);
C0——2,4,6-TCP的初始摩尔浓度,mol/L;
COH——·OH的摩尔浓度,mol/L。
对于均质反应器,如式(8)。
(8)
本试验光照强度为常量,使用磁力搅拌器可以将催化剂TiO2快速均匀地分布于水中,可以认为此反应装置为均质反应器,·OH在水体表面均匀存在。UV光照强度及TiO2浓度稳定,所以·OH也一直稳定存在于反应体系中。因此,式(7)中COH为一常数,可认为UV/TiO2光催化降解2,4,6-TCP的反应符合一级动力学,其中k为准一级动力学反应常数,式(8)可以简化为式(9)。
(9)
2.2 反应条件对光催化降解2,4,6-TCP的影响
2.2.1 TiO2投加量的影响
取200 mL初始质量浓度为5 mg/L的2,4,6-TCP溶液,在pH值=5.02的条件下反应90 min,考察TiO2投加量对光催化降解2,4,6-TCP的降解率影响,结果如图2所示。将试验数据进行积分处理,拟合In(C/Co)与t的变换规律,查看不同TiO2投加量对光催化降解2,4,6-TCP的反应动力学拟合,结果如图3所示。其k(速率常数)、t1/2(半衰期)和R2(相关系数)如表1所示。
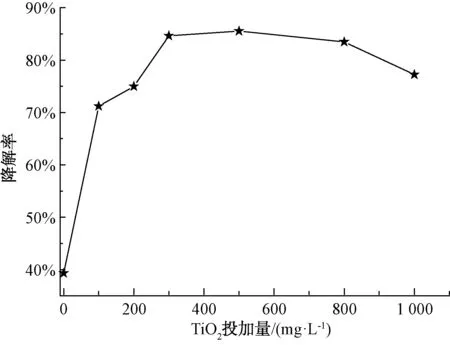
图2 TiO2投加量对光催化降解2,4,6-TCP的影响Fig.2 Effect of TiO2 Dosage on Photocatalytic Degradation of 2,4,6-TCP

图3 TiO2投加量对光催化降解2,4,6-TCP的影响Fig.3 Effect of Dosages of TiO2 on Photocatalytic Degradation of 2,4,6-TCP
由图2可知,2,4,6-TCP的降解在300~800 mg/L时催化降解效果较好,且当TiO2投加量为500 mg/L时,90 min后2,4,6-TCP的降解率最高,为85.5%。同时,由图3和表1可知,当TiO2投加量为500 mg/L时,2,4,6-TCP的光催化降解速率较其他投加量时都较快。这是由于当催化剂用量较少时,光源产生的光子不能在催化剂表面被完全转化为化学能,光子能量利用率较低,适量增加催化剂用量就可以产生更多·OH,提高光催化降解的效率;但是当催化剂用量超过一定程度时,过多的粒子会使光散射,减弱有效光强度,从而降低光的吸收[17-18]。本次试验最佳TiO2投加量为500 mg/L。

表1 不同TiO2投加量下光催化降解2,4,6-TCP的准一级动力学模型的拟合参数Tab.1 Fitting Parameters of Kinetics Models of Quasi-First-Order Dynamic Model on Photocatalytic Degradation of 2,4,6-TCP under Different Dosages of TiO2
2.2.2 2,4,6-TCP初始质量浓度的影响
固定TiO2的投加量为500 mg/L,取200 mL不同初始质量浓度的2,4,6-TCP溶液,在pH值=5.0的条件下反应120 min,考察不同2,4,6-TCP初始质量浓度对光催化降解的影响,将试验数据拟合In(C/Co)与t的变换规律,查看不同2,4,6-TCP初始质量浓度对光催化降解的反应动力学影响,结果如图4所示。其k、t1/2和R2如表2所示。
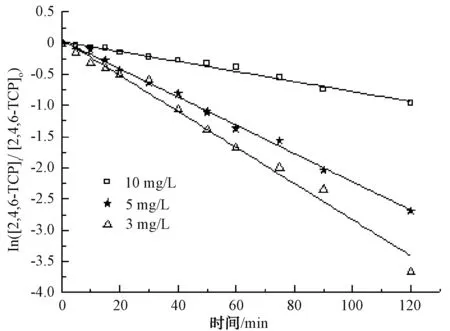
图4 初始质量浓度对光催化降解2,4,6-TCP的影响Fig.4 Effect of Initial Concerntrations on Photocatalytic Degradation of 2,4,6-TCP

表2 不同初始质量浓度下光催化降解2,4,6-TCP的准一级动力学模型的拟合参数Tab.2 Fitting Parameters of Kinetics Models of Quasi-First-Order Dynamic Model on Photocatalytic Degradation of 2,4,6-TCP under Different Initial Concentrations
结果表明,随着2,4,6-TCP初始质量浓度的增加,其降解速率明显降低。这是因为在紫外光强以及TiO2量不变的情况下,单位时间内紫外光在TiO2表面所激发出的·OH不变,反应物的初始质量浓度增加,一定时间内单位反应物所获得·OH的概率降低,一定时间内反应物的去除率将明显降低。当2,4,6-TCP的初始质量浓度由3 mg/L增加到10 mg/L时,UV/TiO2对2,4,6-TCP的降解速率也由0.029 0 min-1降低到0.008 0 min-1,降低了将近4倍。
2.2.3 不同pH条件对2,4,6-TCP降解的影响
固定TiO2的投加量为500 mg/L,取200 mL初始质量浓度为5 mg/L的2,4,6-TCP溶液,调节反应液的pH后放置紫外线下反应120 min。本试验各个工况的pH实测值分别为2.62、5.05、6.82、8.96、10.80,考察不同pH对光催化降解的影响,将试验数据拟合In(C/Co)与t的变换规律,查看不同pH条件下对光催化降解的反应动力学影响,结果如图5所示。其k、t1/2和R2如表3所示。
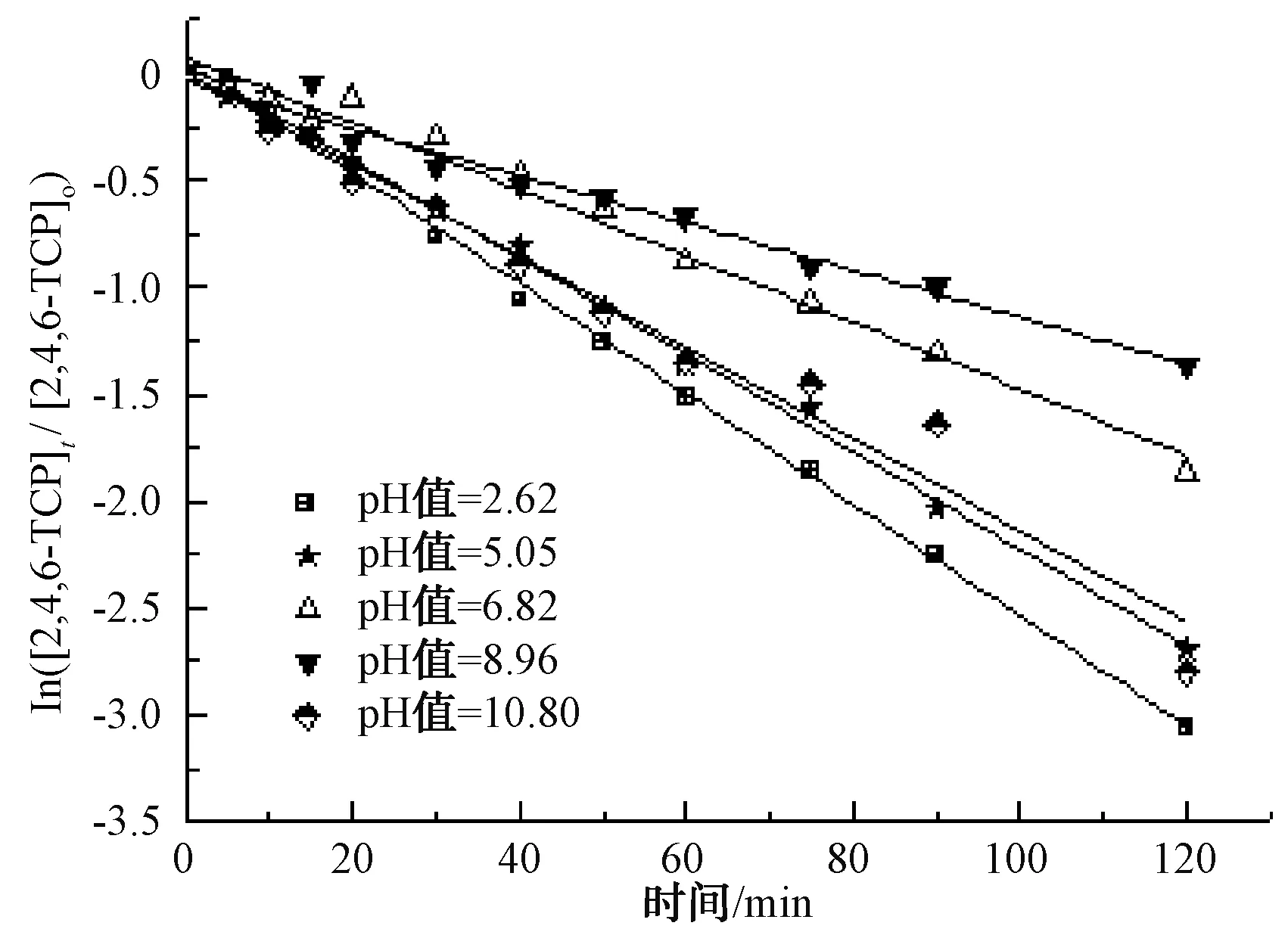
图5 pH对光催化降解2,4,6-TCP的影响Fig.5 Effect of pH Value on Photocatalytic Degradation of 2,4,6-TCP

表3 不同pH条件下光催化降解2,4,6-TCP的准一级动力学模型的拟合参数Tab.3 Fitting Parameters of Kinetics Models of Quasi-First-Order Dynamic Model on Photocatalytic Degradation of 2,4,6-TCP under Different pH Value
根据Tajik等[19]的研究,光催化活性受到pH的影响,是因为光催化剂的表面电荷或者目标污染物的表面电荷可以发生变化,从而改变两者之间的吸附力。2,4,6-TCP是一种弱酸,电离平衡常数为6.1[20-21],当溶液pH值≤6.1时,溶液中的2,4,6-TCP主要以分子形式存在,当溶液pH值>6.1时,溶液中的2,4,6-TCP主要以离子态存在,且pH越高,其离子态的含量越高。另外,根据Muneer[22]等的研究,催化剂TiO2作为两性氧化物,等电点≈6.6,因此,当pH值≤6.6时,催化剂TiO2表面带正电荷,反之当pH值>6.6时,催化剂TiO2表面带负电荷。
根据UV/TiO2处理2,4,6-TCP的基本原理分析,产生·OH主要有两种途径:①通过紫外激发吸附于TiO2表面的OH-或H2O生成;②通过紫外直接激发存在水溶液中的OH-生成。UV/TiO2在酸性(pH值≤6.82)条件下,pH越低,2,4,6-TCP的降解速率越高,且pH的变化对降解速率的影响程度很大。pH值由2.62升至6.82,2,4,6-TCP的降解速率k由0.025 9降到0.015 5,pH值=2.62时的降解速率是pH值=6.82的近2倍。这可能是在此pH下TiO2的表面带正电荷,更易吸收分子态和负离子态的2,4,6-TCP,因此,途径①是主要的降解方式。表现为在酸性及中性条件下,pH越低,吸附于TiO2表面的分子态2,4,6-TCP越多,从而更有利于TiO2表面产生的·OH与其反应。
在中性及弱碱性条件下,即pH值为6.82~8.92时,2,4,6-TCP的降解速率k由0.015 5降至0.010 7,pH升高不利于降解反应的进行;而在强碱性条件下,即pH值为8.96~10.80时,降解速率k由0.010 7升至0.021 4,pH值=10.80时的降解速率是pH值=8.96的2倍,pH的升高有利于降解反应的进行。根据马艳等[21]的研究,单独UV方式处理2,4,6-TCP时,溶液的pH越高,越易被降解。这是由于在中性或碱性(pH值>6.82)条件下,随着pH的升高,催化剂TiO2表面带负电荷的粒子逐渐增多,且溶液中的2,4,6-TCP逐渐开始以负离子态存在,被吸附于TiO2表面被去除的可能性越低,表现为途径①作为主方式的逐渐降低,途径②开始逐渐增强。在中性及弱碱性(6.82 2.2.4 不同光强条件对2,4,6-TCP降解的影响 固定TiO2的投加量为500 mg/L,取200 mL初始质量浓度为5 mg/L的2,4,6-TCP溶液,在pH值=5.0但光强不同的条件下反应,120 min后考察不同的光强条件对2,4,6-TCP降解的影响,将试验数据拟合In(C/Co)与t的变换规律,查看不同光强对光催化降解的反应动力学影响,结果如图6所示。其k、t1/2和R2如表4所示。 图6 紫外光照强度对光催化降解2,4,6-TCP的影响Fig.6 Effect of UV Intensity on Photocatalytic Degradation of 2,4,6-TCP 结果表明,随着紫外光照强度的降低,2,4,6-TCP的降解速率明显降低。这是因为紫外光是UV/TiO2产生·OH的主要来源,紫外光照强度的降低,必然引起·OH产量的降低,单位反应物所获得·OH的概率降低,反应物的去除率降低。当紫外光照强度由154 μW/cm2降低至38.5 μW/cm2时,UV/TiO2对2,4,6-TCP的降解速率也由0.022 7 min-1降低至0.005 5 min-1。这是由于在UV/TiO2体系中,紫外光照强度是激发体系降解活性的重要参数。增加光照强度可以大大提高单位时间、单位反应体积内的活化物质分子数,从而提高反应速率。马艳等[21]采用UV辐照降解水中的有机物,也得到了和本试验类似的结论。 表4 不同紫外光照强度下光催化降解2,4,6-TCP的准一级动力学模型的拟合参数Tab.4 Fitting Parameters of Kinetics Models of Quasi-First-Order Dynamic Model on Photocatalytic Degradation of 2,4,6-TCP under Different UV Intensity 2.2.5 不同阴离子对2,4,6-TCP降解的影响 图7 阴离子对光催化降解2,4,6-TCP的影响 摩尔浓度均为5 mmol/L)Fig.7 Effect of Anions on Photocatalytic Degradation of 2,4,6-TCP (Concentrations of Cl-, and are all 5 mmol/L) 表5 不同阴离子条件下光催化臭氧降解2,4,6-TCP的准一级动力学模型的拟合参数Tab.5 Fitting Parameters of Kinetics Models of Quasi-First-Order Dynamic Model on Phtocatalytic Degradation of 2,4,6-TCP under Different Anions (10) Cl-对反应的影响较复杂[21,25],在紫外的照射下会产生一定量的·OH,产生量与Cl-浓度有关,对反应具有促进作用;但是同时也会消耗一部分·OH,对反应起抑制作用,反应如式(11)~式(12)。 (11) (12) (1)采用UV/TiO2高级氧化技术对2,4,6-TCP进行降解试验,结果表明,UV/TiO2高级氧化工艺能有效降解2,4,6-TCP,且符合准一级动力学模型,相关系数均在0.96以上。 (2)催化剂(TiO2)投加量对UV/TiO2高级氧化降解有机物的效果影响很大。当TiO2投加量为0~1 000 mg/L时,反应90 min后通过2,4,6-TCP去除率和降解速率可知,TiO2的最佳投加量为500 mg/L。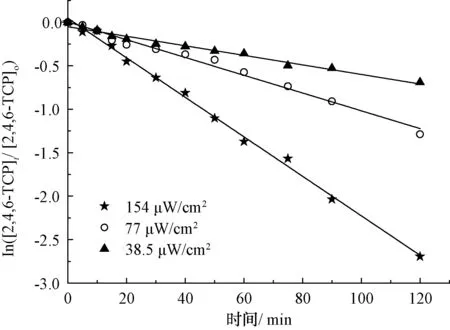
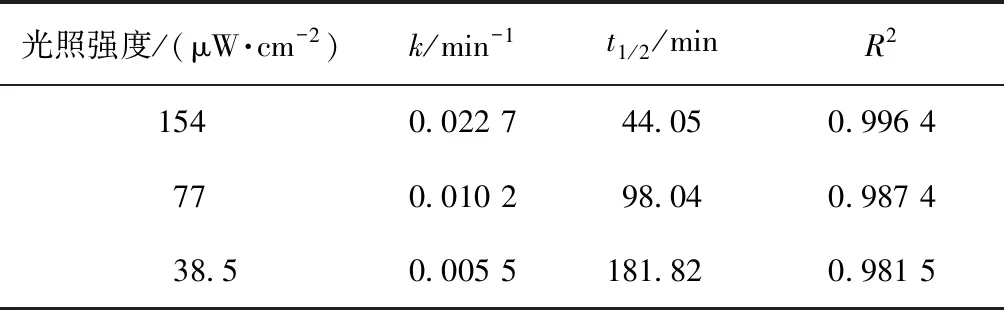



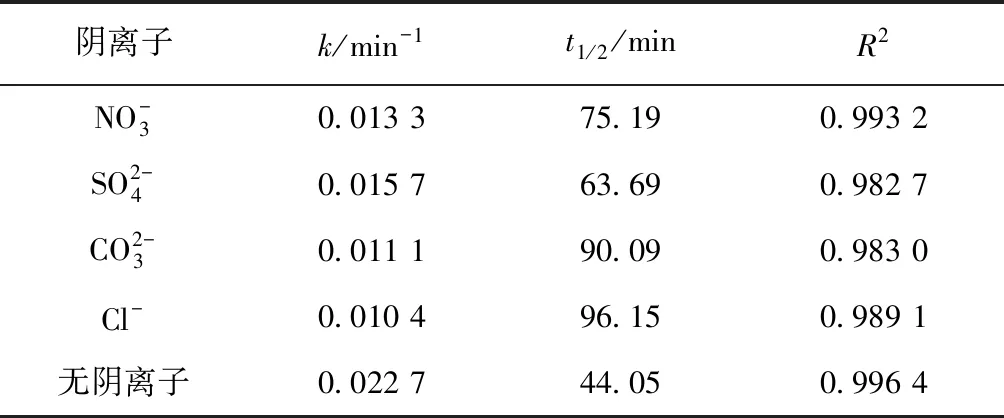
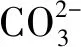




3 结论

