碱改性凹凸棒石对土壤中镉化学形态及环境风险的影响
2022-03-10陶玲仝云龙余方可杨万辉王艺蓉王丽任珺
陶玲, 仝云龙, 余方可, 杨万辉, 王艺蓉, 王丽, 任珺*
(1.甘肃省黄河水环境重点实验室, 兰州交通大学, 甘肃 兰州 730070;2.兰州交通大学环境与市政工程学院环境生态研究所, 甘肃 兰州 730070;3.甘肃瀚兴环保科技有限公司, 甘肃 兰州 730070;4.陕西科技大学环境科学与工程学院, 陕西 西安 710021)
土壤是极其珍贵的自然资源,是人们生存生活必不可少的物质循环基础[1]。目前,受到人类活动的影响,大部分污染物直接或间接进入土壤,造成土壤污染。土壤无机污染中最突出的污染问题就是重金属污染[2]。一项关于土耳其农业土壤的研究表明,由于交通运输和工农业污染物排放的原因,研究区域的土壤显示出中度甚至高度的砷和铅污染[3]。2010—2012年间,中国科学院20多位院士经过考察和调研形成的一份关于中国土壤中重金属的污染和防治的调研报告指出,中国重金属污染现状和趋势非常严重。相比于其他重金属,镉元素因其在土壤-植物系统中具有更高的可迁移性[4],极易影响植物的生长,同时容易通过食物链进入人体,增加人体肾功能失调、骨质软化、致癌等风险而备受关注[5]。
土壤中重金属的危害不仅仅与它在土壤中的总量有关,更取决于它在环境中的化学形态及所占比例[6]。针对重金属难降解、高迁移率、赋存形态不同而毒性不同的特性,土壤钝化修复技术通过加入钝化材料降低重金属在土壤中的有效含量或改变重金属的化学形态从而降低其毒性[7],因其价格低廉、操作方便、不影响土壤正常使用等优点,成为治理重金属污染土壤的重要手段[8]。现阶段,常用的钝化剂可分为无机钝化剂(黏土矿物、工业废弃物等)、有机钝化剂(有机肥、生物炭等),有机-无机复配钝化剂(污泥、堆肥等)[9-10]。黏土矿物在中国资源丰富且种类繁多,因其经济实惠、绿色环保、具有较大的比表面积以及较强的吸附和离子交换性能,被广泛应用于重金属污染的修复治理[11-12]。其中,凹凸棒石(Attapulgite,ATP)是一种链层状结构的含水镁铝硅酸盐矿物,晶层由两个硅氧四面体晶片与一个铝氧八面体晶片构成,属于2∶1型结构。因凹凸棒石具有孔道丰富、廉价易得、稳定性好、可负载其他材料、富含矿物质营养元素等特点,被广泛应用于重金属污染土壤修复领域[13]。谭科艳等[14]利用凹凸棒石对重金属污染土壤进行修复试验,凹凸棒石的添加改善了矿区的土壤环境条件,对Cu和Cd的平均修复率分别达到31.50%和34.92%。然而,由于天然凹凸棒石的基本结构单元棒晶较为粗大,呈现的显微结构较为致密、不松散,其吸附和离子交换性能难以完全发挥出来,因此需要对凹凸棒石进行改性,使其更具有应用价值。陈展祥等[15]利用凹凸棒石和生化黄腐酸改性凹凸棒石,研究其对生菜体内Cd含量的影响,结果显示两者均可显著降低植物体内Cd的含量,且改性材料的作用优于未改性材料。也有研究表明在酸活化条件下凹凸棒石对土壤中重金属Zn的最大钝化容量提高了2.94倍[16]。碱改性作为化学改性的主要方法之一,王金明等[17]使用质量分数为8%的氢氧化钠对凹凸棒石进行改性,发现改性后材料面网间距增加,吸附性能提高。余树荣等[18]使用氧化钙与凹凸棒石复合,制成有吸附催化作用的材料,也提高了凹凸棒石的吸附性。然而,除了吸附性能的提高,利用碱改性凹凸棒石对土壤中重金属进行钝化效果研究的报道却相对较少。有必要对氢氧化钠改性凹凸棒石对土壤中重金属的钝化效果开展深入研究,对于修复重金属污染土壤有着重要的意义。
本文采用氢氧化钠对凹凸棒石进行改性,利用表征实验(扫描电镜、X射线衍射和红外光谱)分析改性前后凹凸棒石的变化规律,通过钝化实验探究氢氧化钠改性凹凸棒石对Cd污染土壤的理化性质以及Cd化学形态的影响,以期为氢氧化钠改性凹凸棒石修复Cd污染土壤及后续研究提供理论支持,同时为进一步广泛、高效地应用甘肃省储量丰富的凹凸棒石资源提供帮助。
1 实验部分
1.1 供试材料
供试土壤采用甘肃省兰州市安宁区兰州交通大学校园土配制的模拟Cd污染土壤。采用五点梅花式取样法,采集校园表层土(0~20cm)。土壤去除大块杂质,经自然风干后,进行Cd污染土壤的制备,将水合氯化镉以水溶液的形式添加至未受污染的校园土中。模拟Cd污染土壤的基本理化性质如下:pH值为7.29,电导率(EC)为329μS/cm,有机质含量(OM)为1.60%,阳离子交换量(CEC)为22.79cmol/kg,速效磷、速效氮和速效钾含量分别为20.96mg/kg、22.75mg/kg和18.25mg/kg,土壤中Cd总量为15.50mg/kg。模拟Cd污染土壤平衡1个月后备用。
凹凸棒石由甘肃瀚兴环保科技有限公司提供,采自甘肃省临泽县板桥镇。主要成分为:凹凸棒石29.7%,石英21.8%,长石14.6%,白云石6.3%,蒙脱石5.3%,石膏5.1%,海泡石4.9%,绿泥石4.8%,云母4.2%,方解石3.2%[19]。钝化材料以凹凸棒石为原材料,经破碎,先水洗纯化,再进行酸洗活化的预处理。烘干后,将氢氧化钠与凹凸棒石按照1∶2、1∶4、1∶6、1∶8、1∶10的质量比(分别记为NP12、NP14、NP16、NP18、NP110),在固液比为1∶10的条件下,采用浸渍法于加热搅拌器上搅拌2h,期间保持反应温度为70℃。搅拌完成后超声30min,然后用去离子水冲洗材料,洗涤至材料上清液pH值为8左右,再在烘箱中于105℃下烘干,研磨后过200目筛,封存于密封袋中备用。经过预处理而未进行改性的凹凸棒石记为NP01。
1.2 钝化实验
准确称取1.2kg模拟Cd污染土壤于不同的塑料盆中(直径20cm),然后将6种钝化材料按照40g/kg的添加量分别加入土壤中,以未添加钝化材料的Cd污染土壤为对照(CK),充分混合搅拌,加入去离子水使土壤含水率保持在70%田间持水量,在自然条件下钝化30d。然后测定土样理化性质、土壤中Cd化学形态,计算土壤中Cd的风险评价指数和潜在风险指数,每种处理重复3次。
1.3 指标测定
土壤pH值按照土水比为1∶2.5(m/V)混合振荡离心,使用pH计(pHS-3C型)测定。土壤EC值按照土水比为1∶5(m/V)混合振荡离心,使用电导率仪(DDS-307A型)测定。使用硫酸亚铁滴定法测定土壤OM氯化钡-硫酸强迫交换法测定土壤CEC值。碳酸氢钠浸提-钼锑抗比色法(722可见分光光度计)测定土壤速效磷。碱解扩散法测定土壤速效氮。乙酸铵浸提-火焰光度法(6400A火焰光度计)测定土壤速效钾。采用欧洲共同体标准物质局(The European Community Bureau of Reference)提出的BCR连续提取法测定土壤中Cd的化学形态[20]。采用盐酸-硝酸-氢氟酸-高氯酸四酸进行消解,火焰原子吸收分光光度计(TAS-990)测定土壤中总Cd含量。
采用高分辨场发射扫描电子显微镜(ZEISS GeminiSEM 500型,德国卡尔·蔡司公司)分析材料的微观形貌变化;使用X射线衍射仪(MiniFlex600型,日本理学公司)分析材料的晶体结构;采用傅里叶变换红外光谱仪(VERTEX 70型,德国布鲁克公司)分析材料的官能团。
1.4 钝化效果评估方法
作为对BCR法结果的检查,在下面的公式(1)中对四种形态的总和与土壤中重金属总量进行比较[21]。
(1)
式中:PR(percentage recovery)为Cd的回收率(%);S1表示酸溶态Cd含量;S2表示还原态Cd含量;S3表示氧化态Cd含量;S4表示残渣态Cd含量;TC为土壤中重金属的总量(mg/kg)。若4种形态与重金属总量吻合良好,则PR值为95%~105%。
通过比较潜在的活跃形态(S1+S2+S3)和稳定形态(S4),可以用式(2)计算Cd的潜在风险指数(potential risk index,PRI)[22-23]。其中,T为单一重金属的毒性影响因子,定义TCd=30。PRI值可分为五个等级:低风险,PRI<40;中等风险,PRI值在40~80之间;较高风险,PRI值在80~160之间;高风险,PRI值在160~320之间;极高风险,PRI≥320。
(2)
通过将BCR法连续提取得到的S1含量与S1、S2、S3、S4含量之和进行比较,可以用公式(3)计算Cd的风险评价指数(risk assessment code,RAC)[23]。RAC的五种分类为:无风险,RAC值低于1%;低风险,RAC值在1%~10%范围内;中等风险,RAC值在10%~30%范围内;高风险,RAC值在30%~50%范围内;极高风险,RAC值高于50%。
(3)
1.5 数据处理
所得数据均为3次重复实验的平均值,采用Microsoft Excel 2016对数据进行整理,并用Statistica 7.0和SPSS 23.0软件进行差异显著性分析(P<0.05)和Person相关性分析,利用Origin 2019b进行制图。
2 结果与讨论
2.1 氢氧化钠改性凹凸棒石的表征
2.1.1氢氧化钠改性凹凸棒石的SEM分析结果
凹凸棒石的晶体结构可分为基本结构单元,即棒晶;由棒晶紧密平行聚集而成的棒晶束;以及晶束间相互聚集而形成的各种聚集体。凹凸棒石原矿结构密实,形态不对称,表面光滑,多为聚集体形式存在。如图1所示,NP12和NP14改性材料展现出更多细小甚至呈球状颗粒分布的棒晶,且表面变得粗糙,交叉出现更多孔道,使得接触表面积变大。NP16改性材料的SEM图可以清楚地看到细长、多平行排列的棒晶。而NP18和NP110改性凹凸棒石中,聚集体数量减少,出现一些相互交杂且形态粗大的棒晶。氢氧化钠能与凹凸棒石结构的Si发生反应,在一定范围内随着氢氧化钠浓度的增大,反应更加彻底,使得凹凸棒石表面被侵蚀而变得粗糙,增加适合吸附重金属的活性位点;原矿中多数存在的聚集体(0.01~0.1mm数量级)经反应后生成棒晶束和棒晶(0.1~1μm数量级),提高其有效表面积。

图1 氢氧化钠改性凹凸棒石的扫描电镜图像Fig.1 Scanning electron micrographs of attapulgite modified by NaOH
2.1.2氢氧化钠改性凹凸棒石的XRD和FTIR分析结果
经过碱改性,对比改性凹凸棒石与未改性凹凸棒石NP01,采用XRD对晶体结构进行分析可发现,在2θ=27.01°处,凹凸棒石中的水硼锶石在添加氢氧化钠改性凹凸棒石后特征峰消失,说明该杂质经改性后消失,提高了凹凸棒石的吸附性;在2θ=26.68°处,石英的特征衍射峰强度减弱,表明石英杂质在改性过程中转化为活性的非晶硅酸盐,有利于提高改性凹凸棒石的吸附性能[24];在2θ=35°附近,凹凸棒石特征衍射峰的强度降低,可能是因为在改性过程中硅氧四面体被分解,氢氧化钠处理打开Si—O—Si键,形成Si—O-,进而有利于提高改性凹凸棒石的表面负电位,增加其吸附位点;除NP110外,经氢氧化钠改性后,改性材料中出现的可能是方沸石的特征峰[25],说明经过氢氧化钠改性,凹凸棒石的Si与Al溶出(图2a)。

图2 氢氧化钠改性凹凸棒石的X射线衍射图谱和傅里叶变换红外光谱图Fig.2 X-ray diffraction patterns and Fourier transform infrared spectroscopy spectra of attapulgite modified by NaOH
通过FTIR对材料官能团的分析表明,在3617cm-1处存在吸收峰为Al—OH—Al的伸缩振动,此处吸收峰减弱或消失的原因可能在于氢氧化钠改性过程中,发生化学反应,使得Al—OH—Al键断开[26];3550cm-1处的吸收峰归属孔道中的结晶水;由于Al—Mg—OH伸缩振动,在3405cm-1处存在吸收峰[27]。随着改性过程中氢氧化钠浓度的增加,这3个吸收峰逐渐变弱甚至消失。1615cm-1处的吸收峰是沸石水弯曲振动[28];1490cm-1和1363cm-1处存在吸收峰是由于C—H2的伸缩振动;最强吸收带于1037cm-1处,对应连接两个反向四面体的Si—O—Si键的伸缩振动;由于Si—O的伸缩振动,792cm-1和477cm-1处存在吸收峰;对应519cm-1处的吸收峰由Al—O—Si的伸缩振动,随着改性过程中氢氧化钠浓度的增加有减小的趋势(图2b)。
2.2 氢氧化钠改性凹凸棒石对土壤理化性质的影响
pH和CEC是影响土壤重金属生物有效态和形态分布的重要参数[29]。与CK相比,添加氢氧化钠改性凹凸棒石后,土壤pH、CEC和EC值均显著增加(表1)。添加NP12钝化材料的土壤pH值由CK的7.29升高至8.14,显著高于其他处理组,而NP14、NP16、NP18、NP110钝化材料则分别提高土壤pH值0.81、0.74、0.70、0.69个单位。除CK和NP01,NP18和NP110处理组间差异不显著外,其他各处理之间差异显著。
表1氢氧化钠改性凹凸棒石钝化Cd污染土壤的pH值、阳离子交换容量(CEC)和电导率(EC)
Table 1 The pH, cation exchange capacity (CEC), electrical conductivity (EC) of Cd polluted soil stabilized with attapulgite modified by NaOH
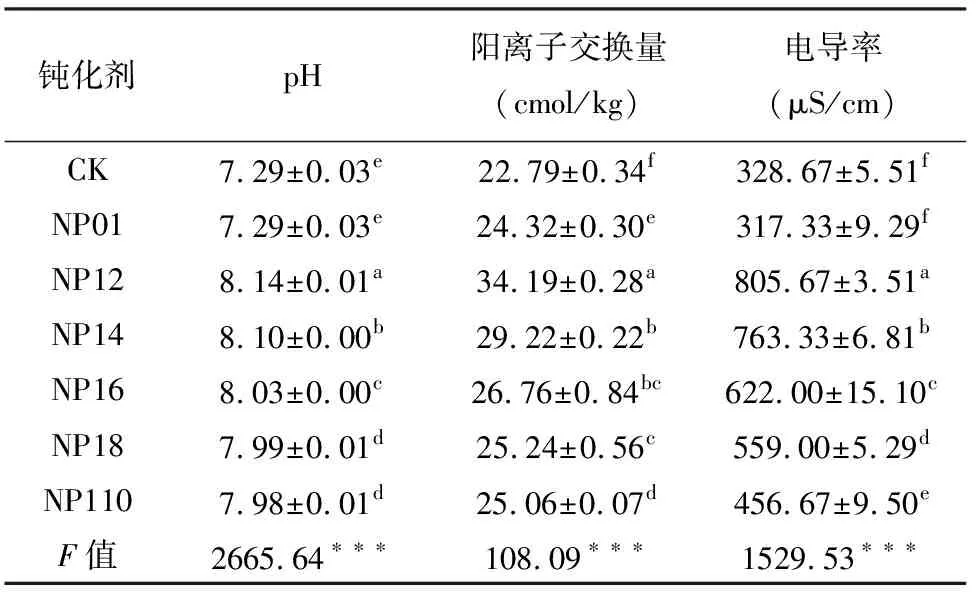
钝化剂pH阳离子交换量(cmol/kg)电导率(μS/cm)CK7.29±0.03e22.79±0.34f328.67±5.51fNP017.29±0.03e24.32±0.30e317.33±9.29fNP128.14±0.01a34.19±0.28a805.67±3.51aNP148.10±0.00b29.22±0.22b763.33±6.81bNP168.03±0.00c26.76±0.84bc622.00±15.10cNP187.99±0.01d25.24±0.56c559.00±5.29dNP1107.98±0.01d25.06±0.07d456.67±9.50eF值2665.64∗∗∗108.09∗∗∗1529.53∗∗∗
注: 同列不同小写字母(a、b、c、d)本身没有具体的含义,是通过相互之间的比较来体现差异是否显著(P<0.05),字母不同表示两者差异显著,差异性显著表明数据变化较为明显(本文其他表格和图内的a、b、c、d含义同此)。F值后的“***”表示在0.001水平上差异显著。
与对照相比,添加未改性凹凸棒石NP01的土壤CEC升高最少,为24.32cmol/kg,但显著高于对照组;添加氢氧化钠改性凹凸棒石均可显著提高土壤CEC。其中,添加NP12钝化材料后土壤CEC由22.79cmol/kg升高至34.19cmol/kg,显著高于其他处理。对于6种钝化材料,添加NP14和NP16以及NP16和NP18钝化材料后土壤CEC之间差异不显著,其余处理之间差异显著。
与CK相比,添加未改性凹凸棒石NP01钝化土壤后,土壤EC值降低,但不显著;添加改性凹凸棒石土壤EC值均显著升高,且添加NP12改性材料后土壤EC值升高最多,显著高于其他处理。添加氢氧化钠改性凹凸棒石后,各处理之间差异显著。

土壤CEC值的增加,首先是因为凹凸棒石自身具有很高的CEC,加入土壤当中使得土壤CEC值升高;其次可能是凹凸棒石具有很强的吸附性和黏性,一方面吸收更多矿物元素,另一方面其自身存在的自由颗粒与土壤胶体颗粒反应形成复合体或团聚体,从而提高土壤CEC值[32]。
较对照处理,施用氢氧化钠改性凹凸棒石能显著提高土壤pH和CEC值,说明改性后的凹凸棒石可改良碱性土壤。且已有研究表明,土壤的pH和CEC值的升高,有助于抑制土壤中重金属的溶解释放,从而增加重金属在土壤中的稳定性[33]。
2.3 氢氧化钠改性凹凸棒石对土壤中Cd的化学形态影响
根据BCR连续提取法的分类,土壤中酸溶态和还原态重金属活性较高,易发生迁移被植物利用;氧化态和残渣态重金属稳定性较强,环境风险较低。CK土壤中酸溶态和还原态Cd含量的占比分别为37.01%和45.36%,这可能是因为人为添加至土壤中的Cd主要以较为活跃的形式存在于土壤当中[34],氧化态和残渣态Cd含量分别占比5.68%和12.77%(图3)。

图3 氢氧化钠改性凹凸棒石钝化土壤中Cd的化学形态分布Fig.3 Chemical speciations distribution of Cd in soil stabilized with attapulgite modified by NaOH
与CK相比,添加氢氧化钠改性凹凸棒石钝化土壤后,酸溶态和还原态Cd含量均显著降低,氧化态和残渣态Cd含量显著升高。随着改性材料中氢氧化钠比例的升高,土壤中酸溶态Cd含量逐渐下降,降幅最大由CK的37.01%降至19.88%(NP12),其他处理组酸溶态含量依次为27.74%(NP14)<29.24%(NP18)<29.66%(NP16)<32.04%(NP110)<34.00%(NP01);其中,添加NP12材料钝化土壤后,土壤中酸溶态含量显著低于其他处理。与CK相比,各处理下还原态Cd含量均显著降低,由45.36%(CK)最大降低至37.41%(NP16);添加NP16材料钝化土壤后土壤中还原态Cd含量与NP18、NP110之间差异不显著,但显著低于其他处理组。氧化态Cd含量由5.68%最高增至17.42%(NP110);与CK相比,各处理下氧化态Cd含量均显著增加;其中,添加NP110材料钝化土壤后,土壤中氧化态Cd含量与NP18处理组之间差异不显著,但显著高于其他处理组。与CK相比,残渣态Cd含量可由CK的12.77%最高升至25.36%(NP12),其他处理下残渣态Cd含量分别为17.41%(NP14)、15.69%(NP16)、13.86%(NP18)、13.32%(NP110)、13.21%(NP01);其中,添加NP12材料钝化土壤后残渣态Cd含量显著高于其他处理。6组处理以及对照组中Cd的回收率均满足95%~105%的要求(表2)。
表2氢氧化钠改性凹凸棒石钝化土壤中Cd的BCR连续萃取态含量和回收率
Table 2 BCR sequential extractions and percentage recovery of Cd in soil stabilized with attapulgite modified by NaOH

钝化剂酸溶态Cd(mg/kg)还原态Cd(mg/kg)氧化态Cd(mg/kg)残渣态Cd(mg/kg)Cd回收率(%)CK5.73±0.31a7.03±0.20a0.88±0.14e1.97±0.14d100.82NP015.27±0.14ab6.63±0.00b1.24±0.20d2.04±0.36d98.04NP123.08±0.57d6.06±0.11cd2.19±0.00c3.93±0.11a98.55NP144.30±0.52c6.16±0.11c2.11±0.27c2.69±0.08b98.57NP164.59±0.21bc5.63±0.07e2.29±0.09bc2.43±0.07bc96.52NP184.53±0.32c5.79±0.26de2.59±0.30ab2.14±0.13cd97.27NP1104.96±0.29bc5.89±0.26cde2.70±0.17a2.06±0.05d100.84F值15.29∗∗∗24.07∗∗∗36.91∗∗∗50.74∗∗∗
注: 同列不同小写字母(a、b、c、d)表示处理之间差异显著(P<0.05)。F值后的“***”表示在0.001水平上差异显著。
土壤中不同形态的重金属其生态毒性不同。添加氢氧化钠改性凹凸棒石后,重金属Cd由活跃形态向稳定形态转化,生态风险降低,这是因为氢氧化钠改性凹凸棒石具有更粗糙的表面积以及特殊的晶体结构,一方面通过吸附作用将Cd2+吸附,另一方面在吸附的同时还可以将其固定在晶格当中,或者是在吸附的同时通过离子交换作用改变Cd2+的存在形态[35-36]。也可能是加入钝化剂导致土壤pH值升高,增加土壤胶体负电荷量,使活跃形态的Cd2+通过配位、沉淀等作用形成硅酸盐或氢氧化物等沉淀,从而转化为稳定的残渣态被固定下来[37-38];以及加入氢氧化钠改性凹凸棒石后,土壤CEC值的升高增加了土壤阳离子吸附位点,促进土壤对重金属的吸附与固定[39]。陈哲等[40]利用天然及改性凹凸棒研究其对稀土尾矿土壤中重金属Pb的钝化效果,结果也显示施用天然及改性凹凸棒石能够使活跃的酸溶态重金属转化为稳定的残渣态重金属。
2.4 土壤中Cd的环境风险评价
添加氢氧化钠改性凹凸棒石钝化土壤后,Cd的RAC值和PRI值均显著降低(F=24.31,P<0.001;F=19.97,P<0.001)(图4)。
Cd的RAC值由CK的36.70%最多可降至20.08%(NP12),添加NP12处理后Cd由高风险范围降至中等风险范围,RAC值显著低于其他处理组,说明该钝化剂具有明显钝化效果。NP14处理后Cd的RAC值为28.09%,也处于中等风险范围,但是NP12与NP14处理组之间的差异显著。其他处理下,Cd的RAC值均大于30%,仍然处于高风险范围内,且组间差异不显著。可能是因为配制的Cd污染土壤浓度为15.50mg/kg,且人工配制的Cd污染土壤中Cd主要以活跃的形式存在于土壤当中。
土壤中Cd的PRI值在添加氢氧化钠改性凹凸棒石钝化后,由CK的207.90最多可降至86.40(NP12),降幅最多为58.44%,由高风险降低至较高风险的范围,NP12处理后土壤中Cd的PRI值显著低于其他处理。与CK相比,NP12、NP14、NP16处理组的PRI值均显著降低,其中,NP14处理组可降至139.81,NP16处理组可降至154.82,风险均显著降低。NP01、NP18、NP110处理组与CK之间无显著性差异,但PRI值仍有降低,NP01处理组可降至196.51,NP18处理组可降至181.20,NP110处理组可降至197.11。

不同小写字母(a、b、c、d)表示处理之间差异显著(P<0.05)。
图4氢氧化钠改性凹凸棒石钝化土壤中Cd的风险评价指数和潜在风险指数
Fig.4 Risk assessment code and potential risk index of Cd in soil stabilized with attapulgite modified by NaOH
2.5 相关性分析
相关性分析结果(表3)表明,土壤pH与酸溶态Cd、还原态Cd、土壤RAC和PRI值均呈极显著负相关;与氧化态Cd和残渣态Cd均呈极显著正相关,说明pH值是控制Cd活性的关键因素之一,随着pH值的升高,土壤中酸溶态Cd含量显著降低,残渣态Cd含量显著升高,Cd活性显著降低[41-42]。土壤EC与酸溶态Cd、还原态Cd、土壤RAC和PRI值均呈极显著负相关;与氧化态Cd呈显著正相关,与残渣态Cd呈极显著正相关(P<0.01)。土壤CEC与酸溶态Cd、土壤RAC和PRI值均呈极显著负相关;与还原态Cd呈显著负相关,而与氧化态Cd呈正相关,但是相关性不强,说明CEC是影响Cd活性的重要因素之一,随着CEC的升高,土壤中酸溶态和还原态Cd含量显著降低,残渣态Cd含量显著升高,Cd活性显著降低,这与迟荪琳等[43]的研究结论相同。
表3钝化土壤的理化性质与Cd化学形态和环境风险指数之间的相关系数
Table 3 Correlation coefficients among physiochemical traits of the stabilized soil, chemical speciation and environmental risk factors of Cd in soil
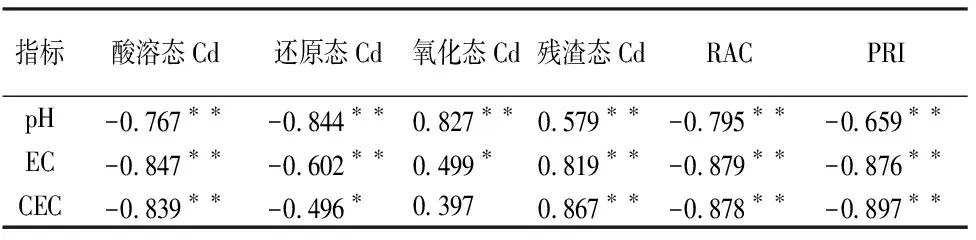
指标酸溶态Cd还原态Cd氧化态Cd残渣态CdRAC PRIpH-0.767∗∗-0.844∗∗0.827∗∗0.579∗∗ -0.795∗∗-0.659∗∗EC-0.847∗∗-0.602∗∗0.499∗0.819∗∗ -0.879∗∗-0.876∗∗CEC-0.839∗∗-0.496∗0.3970.867∗∗ -0.878∗∗-0.897∗∗
注: “*”表示相关系数达到显著水平(0.01 “**”表示相关系数达到极显著水平(0.001 本文使用氢氧化钠作为改性剂,对凹凸棒石进行改性,分析改性前后凹凸棒石的结构特征与物质组成,通过钝化实验研究改性材料对重金属污染土壤中土壤理化性质与重金属Cd形态变化的影响。当氢氧化钠与凹凸棒石质量比为1∶2时改性效果最好。经反应,部分聚集体(0.01~0.1mm数量级)生成棒晶束和棒晶(0.1~1μm数量级),Si—O—Si键与Al—OH—Al键断裂,Si与Al得到释放,凹凸棒石表面出现更多孔道及吸附位点,有效表面积与吸附性能显著提高。氢氧化钠改性凹凸棒石能改变部分土壤理化性质,显著提高土壤pH值、CEC和EC值,改善土壤环境。添加氢氧化钠改性凹凸棒石能不同程度地促进土壤中Cd由活性高的酸溶态向稳定性强的残渣态转化,使Cd转变为硅酸盐或氢氧化物等沉淀,显著降低Cd的活性,使土壤中Cd的风险评价指数和潜在风险指数均降低一个风险等级,从而降低了土壤中Cd的环境风险。碱改性凹凸棒石对土壤中重金属Cd具有良好的钝化作用。 本研究为氢氧化钠改性凹凸棒石钝化土壤中重金属Cd提供了数据支持,为开发高效凹凸棒石土壤修复剂提供了新的思路和理论依据,但仍需要进一步的研究来探讨氢氧化钠改性凹凸棒石在不同环境条件下的最佳钝化效果。3 结论
