左心功能相关参数及左右心室内径比值与中重度肺动脉高压患者预后的关系
2022-03-07胡文文刘倩倩李慕子万琳媛梁玉熊长明逄坤静
胡文文,刘倩倩,李慕子,万琳媛,梁玉,熊长明,逄坤静
肺动脉高压是一种常见的肺血管疾病,血流动力学诊断标准为:在海平面静息状态下,右心导管检查测定的肺动脉平均压≥25 mmHg(1 mmHg=0.133 kPa)[1-2];其病理生理学特点是肺血管结构或功能改变[3]引起肺循环压力和肺血管阻力进行性增加,进而导致肺血流量减少,右心压力负荷增大、右心功能不全甚至死亡[4-5]。尽管近年来靶向药物的应用为肺动脉高压的治疗带来了重要进展,但肺动脉高压仍然属于严重预后不良的一类心血管疾病[6]。早期识别肺动脉高压高危患者并尽早给予合理的治疗方案尤为重要。目前发表的对肺动脉高压危险因素的研究多集中在对右心功能的影像学评估方面,左心功能相关参数研究很少。本研究旨在探讨超声心动图无创测量左心功能相关参数以及左右心室内径比值与中重度肺动脉高压患者预后的关系。
1 资料与方法
1.1 研究对象
回顾性分析2019 年1 月至2020 年11 月我院心内科住院的中重度肺动脉高压患者90 例。同期记录患者基线资料:人口学特征、WHO 心功能分级、6分钟步行距离(6MWD)、入院首次实验室检查指标,包括血清白蛋白(ALB)、丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、N 末端B 型利钠肽原(NT-ProBNP)、血肌酐(CREA)、尿素氮(BUN)、动脉血氧分压(PO2)、动脉血氧饱和度(SO2)。肺动脉高压纳入标准:(1)符合2009 年欧洲心脏病学会与欧洲呼吸学会联合制定的《肺动脉高压的诊断和治疗指南》[1];(2)符合右心漂浮导管检查适应证。排除标准:(1)由于病情较重或其他原因不能完成本研究所要求的必查项目;(2)合并其他急、慢性器质性病变,如肝肾疾病等;(3)哺乳、妊娠。
1.2 仪器与方法
仪器:采用 Vivid E95 超声机(通用电气公司,Horten,美国),二维经胸探头S5-1,频率3.5 MHZ。
右心导管检查:检查均在局麻下完成,收集平均肺动脉压(mPAP)、肺血管阻力(PVR)、体循环血流量右心导管(CORHC)及心指数右心导管(CIRHC)。
超声心动图检查:所有患者均常规连接肢体导联心电图,左侧卧位采集图像。于左心室长轴切面:舒张末期测量左心室舒张末期内径(LVEDd)、右心室流出道近端内径(RVOT-prox),左心室流出道内径(D),连续测量三次取平均值,计算左心室流出道横截面积(A)[A=π×(D/2)2];于心尖四腔心切面:舒张末期测量左、右心室基底段左右径(LVTDd、RVTDd)、收缩末期和舒张末期二维描记右心室心内膜测得右心室收缩末、舒张末面积(ESA、EDA)、M 型测量舒张和收缩末期三尖瓣环纵向峰值瓣环位移(TAPSE);于心尖五腔心切面获得左心室流出道水平多普勒血流频谱,测量血流速度时间积分(VTI);分别计算左心输出量超声心动图(COEcho)=A×VTI×心率、左心指数超声心动图(CIEcho)=COEcho/体表面积(BSA)、LVEDd/RVOT-prox、RVTDd/LVTDd、右心室面积变化分数(RV FAC)[RV FAC(%)=100×(EDA -ESA)/EDA]。
1.3 随访
患者出院后每3 个月门诊或电话随访一次。每次随访记录患者病情变化、使用药物变化、再住院、死亡或肺移植的原因和具体时间,最后一次随访日期为2020 年11 月。以临床恶化发生为复合终点,根据不良心血管事件发生情况分为临床恶化组和无临床恶化组。临床恶化定义为:(1)全因死亡;(2)肺移植;(3)因肺动脉高压恶化再住院;(4)肺动脉高压治疗升级(增加口服靶向药物种类或增加剂量或增加皮下或静脉注射靶向药物)[7]。临床恶化的时间被定义为从超声心动图检查之日到上述第一次临床恶化事件的时间。
1.4 统计学方法
采用SPSS 25.0 统计软件。符合正态分布的连续变量用均数 ± 标准差表示,组间比较采用独立样本t检验;不符合正态分布的计量资料用中位数(P25,P75)表示,组间比较采用 Mann-Whitney U 检验 ;分类变量采用构成比表示,组间比较采用卡方检验。ROC 曲线分析确定最大AUC 和最佳截点值。采用Cox 比例风险回归模型(逐步分析法)、Kaplan-Meier 曲线进行生存分析。以P<0.05 定义为差异有统计学意义。相关性研究采用Pearson 相关分析。
2 结果
2.1 两组肺动脉高压患者的临床基线资料比较(表1)
表1 两组肺动脉高压患者的临床基线资料比较[,中位数(P25,P75)]
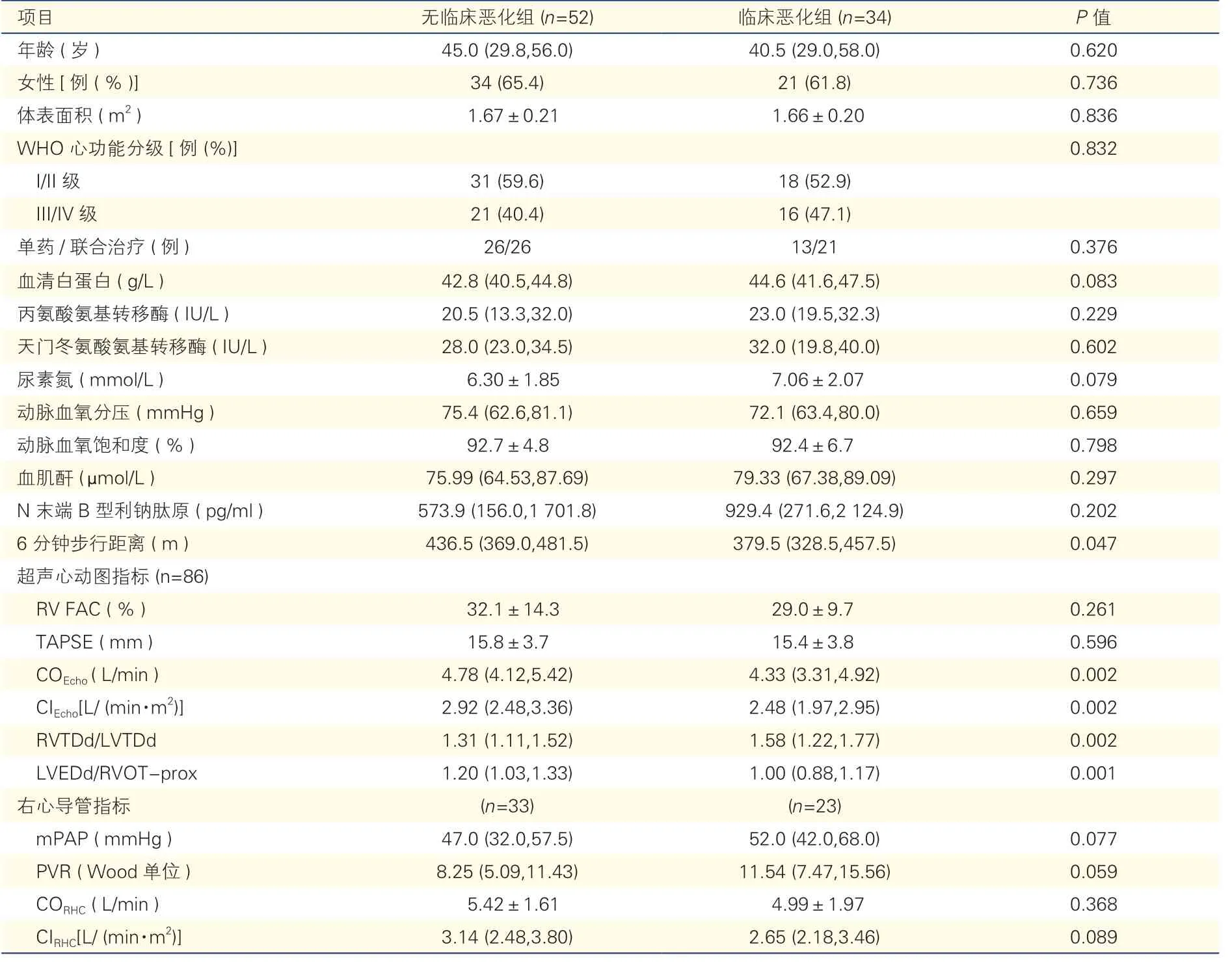
表1 两组肺动脉高压患者的临床基线资料比较[,中位数(P25,P75)]
注:mPAP:平均肺动脉压;PVR:肺血管阻力;CORHC:体循环血流量右心导管;CIRHC:心指数右心导管;COEcho:左心输出量超声心动图;CIEcho:左心指数超声心动图;LVEDd/RVOT-prox:左心室舒张末期内径/右心室流出道近端内径;RVTDd/LVTDd:右心室/左心室基底段左右径;RV FAC:右心室面积变化分数;TAPSE:三尖瓣环纵向峰值瓣环位移。1 mmHg=0.133 KPa
纳入的90 例肺动脉高压患者中,完成随访86例(95.6%),中位随访时间为12.1(9.1,14.3)个月。其中男性31 例(36%),女性55 例(64%);中位年龄43.5(29.0,56.3)岁。43 例为特发性肺动脉高压,33 例为慢性血栓栓塞性肺动脉高压,8 例为结缔组织病相关肺动脉高压,2 例为可遗传性肺动脉高压。最终34 例患者发生临床恶化(临床恶化组),无临床恶化52 例(无临床恶化组)。34 例临床恶化组患者中,2 例(2.3%)发生全因死亡、6 例(7.0%)因肺动脉高压恶化再住院、26 例(30.2%)肺动脉高压治疗升级。与无临床恶化组相比,临床恶化组的COEcho及CIEcho更低、RVTDd/LVTDd更大、LVEDd/RVOT-prox更小、6MWD 更短,差异均有统计学意义(P均<0.05)。
2.2 Cox 风险回归分析(表2)
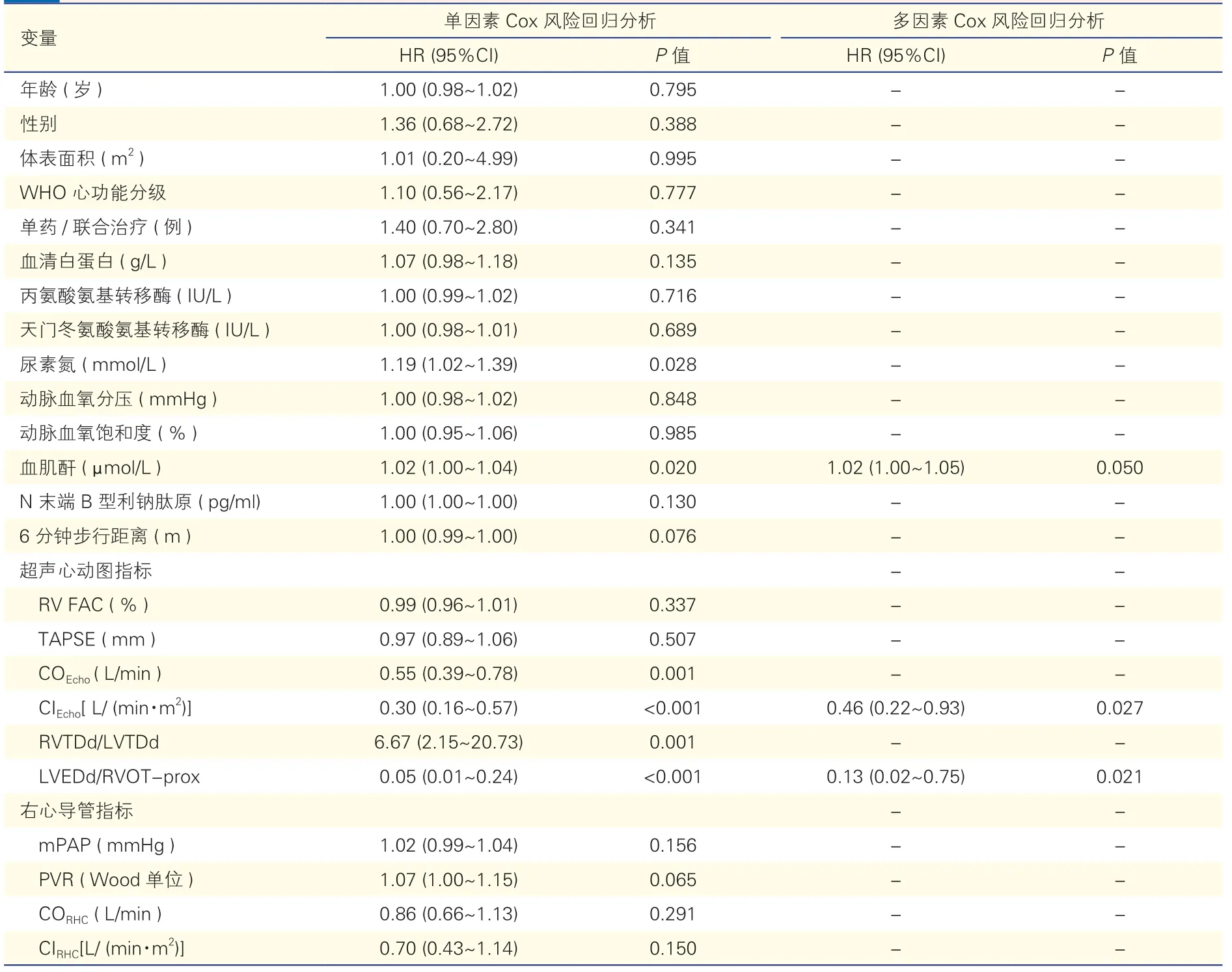
表2 单因素和多因素Cox 风险回归分析
单因素Cox 风险回归分析结果表明:BUN、CREA、COEcho、CIEcho、RVTDd/LVTDd、LVEDd/RVOTprox 均与肺动脉高压患者预后相关(P均<0.05)。将上述各参数纳入多因素Cox 风险回归模型,分析结果表明:CIEcho、LVEDd/RVOT-prox 是预测中重度肺动脉高压患者预后的独立指标(P=0.027、P=0.021)。
2.3 ROC 曲线分析
ROC 曲线分析表明:CIEcho<2.710 L/(min·m2)和LVEDd/RVOT-prox<1.064 是最佳截点值,CIEcho最大AUC 为0.70,95% CI:0.588~0.812,敏感度65.4%,特异度70.6%(P=0.002);LVEDd/RVOT-prox 最 大AUC 为0.72,95% CI:0.609~0.831,敏感度71.2%,特异度64.7%(P=0.001)。
2.4 Kaplan-Meier 生存曲线
CIEcho<2.710 L/(min·m2)者(n=42)的临床恶化发生率明显高于CIEcho≥ 2.710 L/(min·m2)者(n=44,P=0.001,图1)。LVEDd/RVOT-prox<1.064 者(n=37)的临床恶化发生率亦高于LVEDd/RVOT-prox ≥1.064 者(n=49,P=0.001,图2)。
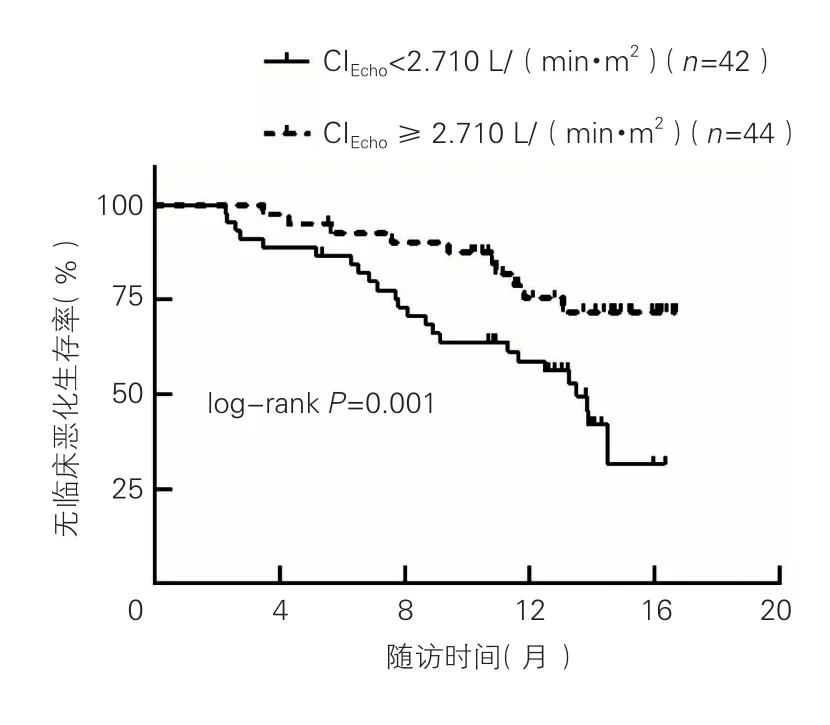
图1 CIEcho<2.710 L/(min·m2)和CIEcho ≥2.710 L/(min·m2)两者生存曲线

图2 LVEDd/RVOT-prox<1.064 和 LVEDd/RVOTprox ≥1.064 两者生存曲线
2.5 超声测量左心功能相关参数与临床指标的相关性
Pearson 相关分析结果表明:CIEcho与右心导管测量的CIRHC、CORHC具有相关性(r=0.68、r=0.58,P均<0.001);LVEDd/RVOT-prox 与NT-pro BNP弱相关(r=-0.5,P=0.001);CIEcho与NT-pro BNP、PVR、6MWD 呈弱相关(r=0.41、P<0.001,r=0.36、P=0.007;r=0.31、P=0.005);LVEDd/RVOT-prox 与CORHC呈弱相关(r=0.35,P=0.009)。
3 讨论
肺动脉高压是一类严重预后不良的心血管系统疾病,发病隐匿、病理机制复杂、病情进展迅速、内科药物治疗效果不理想。肺小动脉进行性狭窄或闭塞导致肺动脉压力及肺循环阻力增高,右心室后负荷增大,右心室收缩末期压力增高导致右心室壁肥厚、右心室腔扩大、三尖瓣关闭不全,最终右心功能衰竭导致多脏器功能减低[8-9]。同时,肺循环高阻力导致肺血流量减少,左心回心血流量减少,左心室前负荷减小。右心室收缩末期压力增高导致室间隔向左心室侧偏移会降低左心室容积,导致左心室心输出量下降[10-11],出现左心低心排出量。左心室心输出量的减低程度与肺动脉高压的病情严重程度应当是一致的,理论上可以预测肺动脉高压的不良预后。左心室舒张末期前负荷减低导致左心室容积减小,其减小的程度与右心室后负荷增大导致的右心室扩大程度应当一致,意味着右心室与左心室内径的比值与肺动脉高压的严重程度呈正相关,应当也具有不良预后的预测价值。为了验证这一理论假设,本研究回顾分析了随访完整的86 例肺动脉高压患者的超声心动图资料,通过测量上述相关参数,发现其对于肺动脉高压的临床恶化发生率具有良好的预测价值。
超声心动图测量指标CIEcho、LVEDd/RVOT-prox对于肺动脉高压预后的预测价值优于其它临床检查指标。临床恶化组相比于无临床恶化组肺动脉高压患者,所有实验室检查参数差异均无统计学意义(表1),只有临床恶化组的6MWD 短于无临床恶化组(P=0.047)。但超声心动图测量的左心室COEcho、CIEcho、RVTDd/LVTDd(P均=0.002),LVEDd/RVOT-prox(P=0.001)在两者间的差异均有统计学意义。说明超声心动图测量指标对于区别不良预后的肺动脉高压患者比实验室检查指标更为敏感。Cox 风险回归分析结果进一步验证了此结论。尽管单因素Cox 风险回归分析结果表明尿素氮、CREA、COEcho、CIEcho、RVTDd/LVTDd、LVEDd/RVOT-prox均与肺动脉高压患者预后相关(P均<0.05),将上述各参数纳入多因素Cox 风险回归模型后,只有CIEcho、LVEDd/RVOT-prox 是预测中重度肺动脉高压患者预后的独立指标(P=0.027、P=0.021)。ROC曲线分析发现CIEcho<2.710 L/(min·m2)和LVEDd/RVOT-prox<1.064 是最佳截点值。Kaplan-Meier 生存曲线分析证实了左心室CIEcho<2.710 L/(min·m2)者和LVEDd/RVOT-prox<1.064 者临床恶化发生率明显高(P均=0.001)。这与Weatherald 等[12]、McLaughlin 等[13]和Zeng 等[14]的研究结果相似。值得注意的是超声心动图测量的反映右心室功能的FAC(%)和TAPSE 在Cox 回归分析中并无显著性预测价值(P均>0.05),临床恶化组和无临床恶化组两个值的差异也无统计学意义。这提示,尽管肺动脉高压属于右心系统疾病,但反映右心室功能的超声心动图参数FAC(%)和TAPSE 对于肺动脉高压预后评估的敏感度却低于左心CIEcho和LVEDd/RVOTprox 两个指标。
左心CIEcho和LVEDd/RVOT-prox 与公认的反映肺动脉高压心功能的临床指标[15]具有一定的相关性。本研究通过Pearson 相关分析发现CIEcho和LVEDd/RVOT-prox 与NT-pro BNP、6MWD 均相关,说明这两个超声心动图指标与经过验证的临床指标一致性良好。左心室CIEcho与有创的右心导管测量结果CIRHC呈强相关,也表明超声心动图测量的左心室CIEcho准确性可靠。
本研究也存在一定的局限性。研究为单中心研究,样本量相对较少。肺动脉高压病因相对集中,并未涉及肺动脉高压的所有病因分类。随访时间较短,对于两个超声心动图指标对肺动脉高压远期临床恶化预测价值无法明确。另外本研究属于回顾性研究,右心导管检查与超声心动图检查时间不一致,影响两个检查测量指标一致性的对比结果。希望在未来的研究中弥补上述不足。
综上所述,对于中重度肺动脉高压患者,将超声心动图测量的左心室CIEcho<2.710 L/(min·m2)和LVEDd/RVOT-prox<1.064 作为不良预后的预测指标具有可靠性。相比右心功能相关指标,反映左心室功能的CIEcho以及LVEDd/RVOT-prox 对肺动脉高压患者病情判断及治疗效果评估更具有敏感性。
利益冲突:所有作者均声明不存在利益冲突
