热浸提法提取茶叶中茶多酚的方法优化
2022-03-07牟小凤
李 娟,牟小凤
(绵阳师范学院化学与化学工程学院,四川绵阳 621000)
0 引言
茶多酚(Tea Polyphenols)是一种混合物,它是茶叶中多酚类物质的总称,主要包括黄烷酮类、花色苷类、花白素类、黄酮醇类、酚酸和缩酚酸类等6类化合物[1],在茶叶中的含量一般在15%~20%,其中黄烷酮类含量最高,其次是黄酮类,而其他酚类物质存在的量相对较少[2].常见的茶多酚为白色不定型粉末,易溶于水,可溶于乙醇、丙酮、乙酸乙酯、甲醇,不溶于氯仿.目前研究报道绿茶中的茶多酚含量较高.
茶多酚作为茶叶中主要成分之一,不仅可以形成茶叶中的色香味,也可以使茶叶具有保健功能[3].自发现茶多酚以来,就对茶多酚进行了多种方面的研究,但是目前茶多酚的浸提工艺都还没达到成熟和稳定的条件,因此优化提取茶叶中茶多酚的工艺条件具有重要意义,同时也为进一步研究茶多酚在工业化生产和开发上提供了理论依据.目前,关于茶多酚含量测定的研究很多[4-8],有关提取茶叶中茶多酚的研究方法也很多,国内外提取茶多酚的方法大致可以分为四种[9-11]:有机溶剂萃取法、金属离子沉淀法、柱层析法和超临界流体萃取法.但是这些大多都是注重茶多酚的后处理阶段,只有较少人专门针对浸取工艺进行研究,而浸提是各种提取方法的前提,是必须的一个工艺步骤,浸提工艺对后续所需产品的纯度及产量都有十分重要的影响,因此优化浸提茶叶中茶多酚的工艺条件,对于提高产品的产率和纯度,具有非常重要的意义.本论文的目的是通过改变热浸提法提取茶叶中茶多酚的不同工艺条件,对不同影响因素设计正交试验表,再按正交试验表依次进行试验,最终获得提取茶叶茶多酚含量的最佳工艺条件.
1 实验部分
1.1 仪器
T6新世纪紫外可见分光光度计(北京普析通用仪器有限责任公司)DF-101S集热式恒温磁力搅拌器(河南省予华仪器有限公司)、FA2004电子天平(上海舜宇恒平科学仪器有限公司).
1.2 试剂
绿茶(联合利华食品(中国)有限公司)、没食子酸丙脂、酒石酸亚铁、磷酸氢二钠、磷酸二氢钾、95%的乙醇(分析纯,成都科龙试验厂).
1.3 含量测定原理、实验方法
1.3.1 研究的主要内容 根据茶多酚研究的现状,本文拟采用紫外可见分光光度技术研究立顿绿茶在不同热浸提工艺条件下茶多酚的提取率情况.实验内容如下:
通过改变不同的工艺影响因素:液固比、溶剂(乙醇)的浓度、浸提时间和提取温度,设计正交试验表,按照正交试验表依次提取茶叶中的茶多酚,利用酒石酸亚铁比色法,该方法也是测定茶多酚含量的国标方法,其测定原理是茶多酚类物质能与亚铁离子形成紫蓝色络合物,该溶液对540 nm可见光有最大吸收,故用紫外可见分光光度计测出其吸光度,利用标准曲线计算出茶水中茶多酚的含量,再通过比较茶多酚的提取率,最终获得最优的工艺条件.
1.3.2 绿茶中茶多酚的提取 称取0.500 0 g干燥且已被碾碎的茶叶,放进准备好的干净的250.00 mL圆底烧瓶中,将95%的乙醇按照所需浓度进行稀释,再用量筒取所需体积的溶剂倒入圆底烧瓶中,在恒温水浴锅里面进行回流提取,过滤,得到棕绿色液体,即可作为待测液.
1.3.3 茶多酚含量的测定 移取待测液1.00 mL于25.00 mL容量瓶中,加入5.00 mL酒石酸亚铁溶液,再加入4.00 mL蒸馏水,充分摇匀,最后用配制的pH为7.5的缓冲溶液定容至刻度线,以蒸馏水作为空白对照,在波长为540 nm处测定吸光度,根据标准曲线算出其没食子酸丙脂含量,然后乘上1.5的换算系数就是茶多酚的含量,根据稀释倍数计算出待测液中茶多酚的总含量,除以称取茶叶的总质量即为茶多酚的提取率.
1.3.4 没食子酸丙酯标准曲线的绘制 分别吸取浓度为1.000 0 mg·mL-1的没食子酸丙酯标准溶液0、0.25、0.50、0.75、1.00、1.25 mL于6个25.00 mL的容量瓶中,分别加入4 mL蒸馏水,再加入酒石酸亚铁溶液5 mL,用配制好的pH为7.5的磷酸缓冲溶液稀释至刻度,摇匀.用1 cm石英比色皿,在540 nm处以试剂空白作参比,用紫外分光光度计分别测量其吸光度.
根据实验,绘制出没食子酸丙脂标准溶液浓度与吸光度的标准曲线,如图1所示.

图1 没食子酸丙脂标准曲线图
可得出没食子酸丙脂标准溶液浓度与吸光度的标准曲线方程为:y=13.189x+0.002,相关系数为:R2=0.999 6.
2 结果与讨论
2.1 正交试验设计
查阅相关针对绿茶中茶多酚的提取工艺的研究发现,主要的研究方法有水浸提-膜分离提取茶叶中的有效成分的绿色节能的新型组合工艺[12]、超声浸提法[13,14]、微波浸提法[15]、复合酶辅助浸提[16]、有机溶剂浸提法、离子沉淀法等,之所以选择有机溶剂(乙醇)浸提,是考虑经济性和安全性的条件下的结果,并且本次所考察的液固比、溶剂浓度、浸提时间和提取温度这四个因素并没有在有关文献中同时查阅到,且针对各个影响因素所设计的水平数也考虑的较细致,因此通过这次实验找到较为合适的浸提条件.
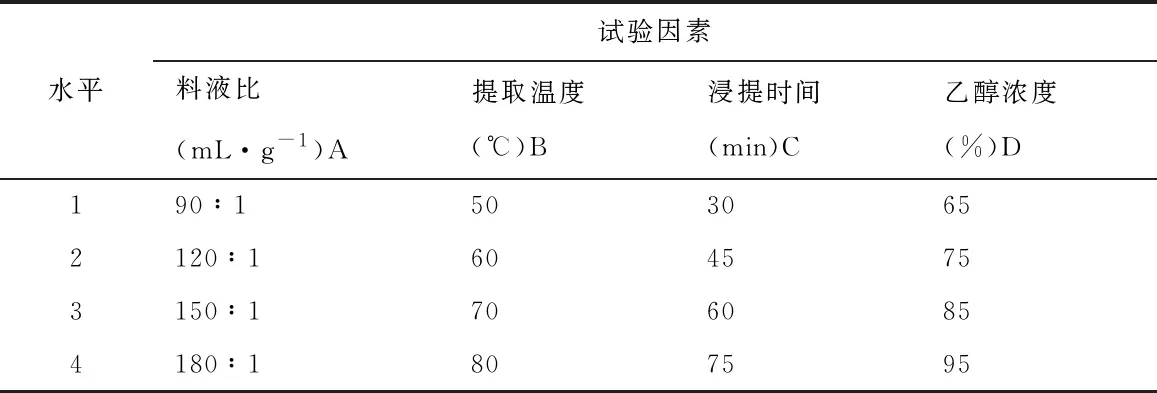
表1 正交水平因素列表
2.1.1 提取条件优化 本实验通过考察液固比、乙醇浓度、提取温度和浸提时间4个因素对茶多酚提取率的影响,为了优化有机溶剂法提取茶多酚的工艺条件,选用L16(45)的正交试验表,依次按表进行实验,考察的因素水平表和正交实验表如下所示.
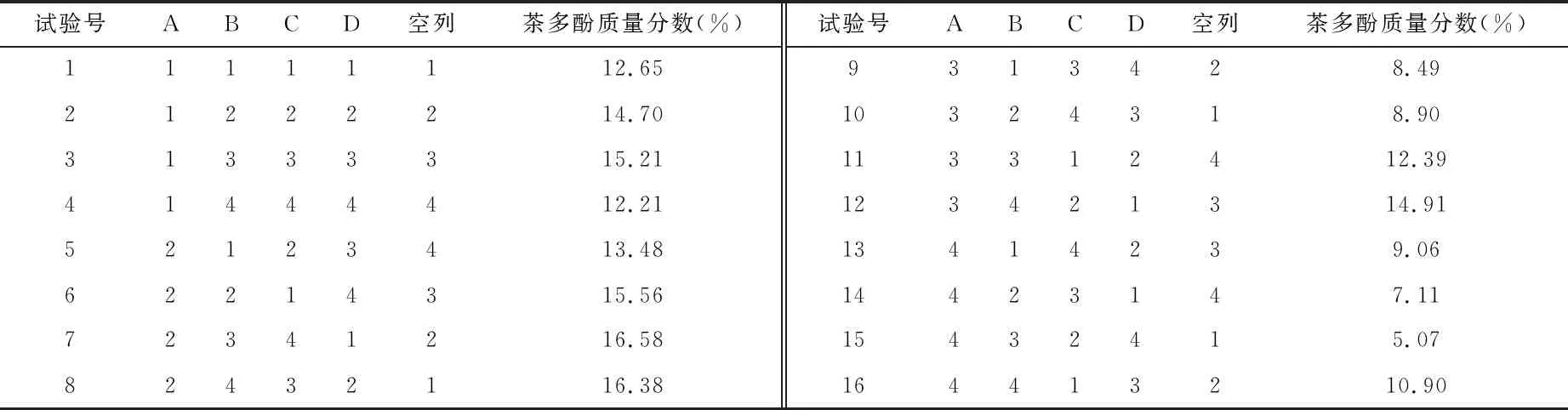
表2 正交试验列表及结果数据表
2.1.2 各因素对茶多酚提取率的影响效应曲线 根据正交试验结果分析表中各因素的k值,可以做出各因素对茶多酚提取率的影响因素曲线.
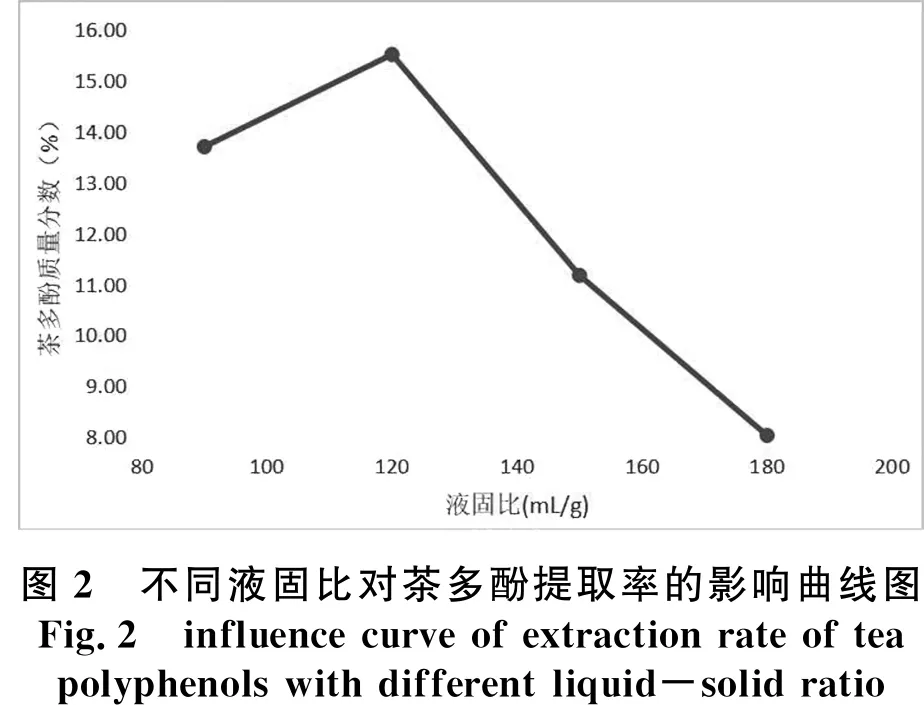
(1)由图2可得,增大液固比,即增加提取溶剂的量,茶多酚的提取率增加,但当增加至120∶1时,继续增加提取溶剂的量,茶多酚提取率反而下降,可见,提取茶叶中的茶多酚的液固比为120∶1比较合适.
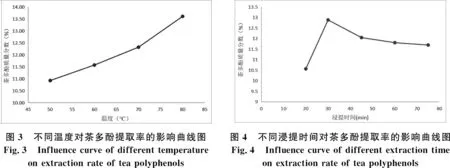
(2)由图3可得,升高温度,茶多酚提取率呈逐渐增加的趋势,且曲线在温度70 ℃至80 ℃之间时坡度最陡,由于溶剂乙醇的沸点为78 ℃,因此温度在70-80 ℃比较适合.
(3)由图4可得,在一定时间范围内,增加浸提时间,茶多酚提取率会提高,但随着浸提时间逐渐增加,茶多酚的浸提率会出现下降的情况,可见茶多酚提取时间在30 min比较合适.
(4)由图5可得,随着乙醇浓度的增加,茶多酚提取率先增加后逐渐减小,即当乙醇浓度为75%时,茶多酚提取率最高,可见提取茶多酚的乙醇浓度应在75%较合适.
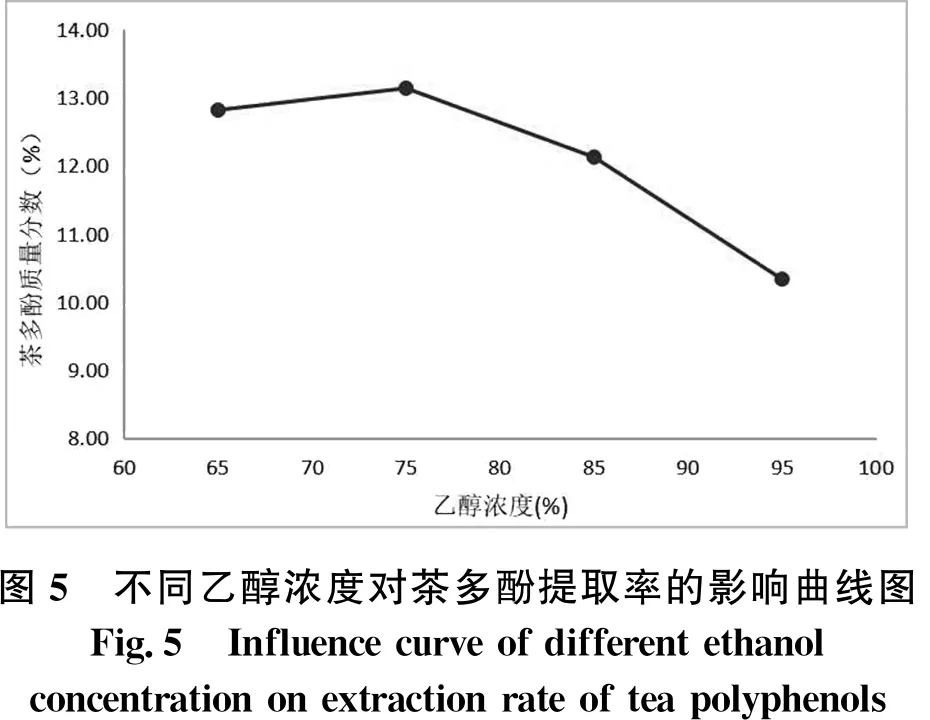
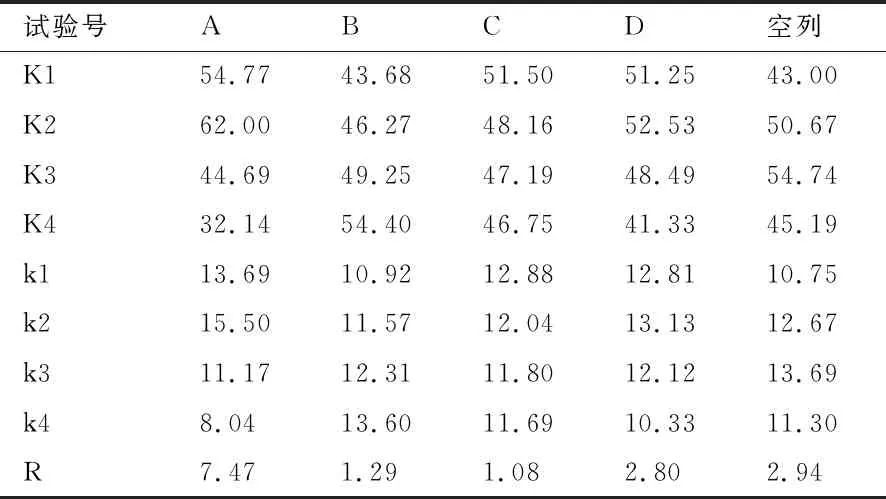
表3 正交试验结果分析表
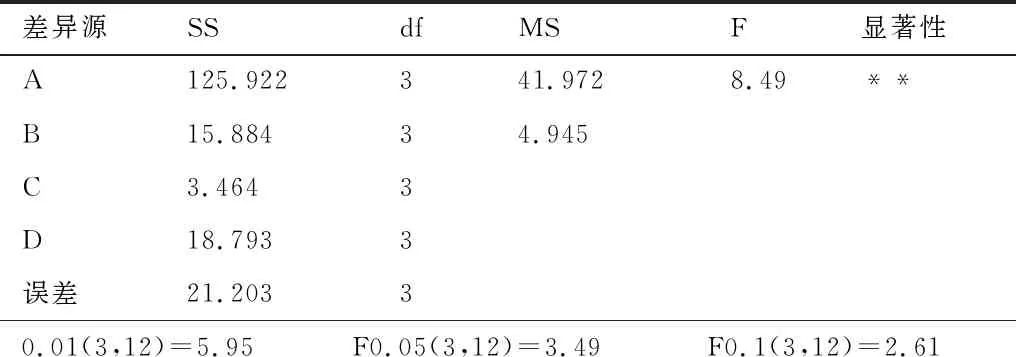
表4 方差分析表
2.1.3 试验结果的方差分析 在正交试验设计结果的方差分析中,计算各因素均方MS时,发现B、C、D三种因素的均方小于误差的均方,则说明提取温度、浸提时间和乙醇浓度对试验结果的影响较小,为次要因素,所以可以将它们都归为误差,这样误差的离差平方和、自由度和均方都会随之发生改变,因此重新计算后不需要计算B、C、D的F值,求得因素A的F值为8.49,可知因素液固比对试验结果有显著影响.
2.2 结果与分析
由表3和影响效率曲线分析可知,各因素对茶多酚提取率的影响大小依次为A>D>B>C,A的影响最大,C最小.最优条件为A2B4C1D2,即:液固比为120∶1、提取温度为80 ℃、浸提时间为30 min、乙醇浓度为75%.根据方差分析表也可以发现,因素液固比的影响最大,提取温度、浸提时间和乙醇浓度的影响较小.
不同液固比对茶多酚浸提率的影响主要考虑的是溶剂量的多少,茶叶要与溶剂乙醇有充分的接触,其中的茶多酚才能充分溶解在溶剂中,而在整个浸提过程中,主要是物质的物理扩散过程,增加溶剂体积可以在一定程度上增大细胞内外物质浓度差,从而提高茶多酚从茶叶细胞向溶液中扩散的能力.但是当液固比使扩散趋于饱和时,再增加溶剂量反而会降低溶液中茶多酚的浸提率.
茶叶中茶多酚的溶解量在一定时间范围内,会随着时间的增加而增加,但是因茶多酚热稳定性不好,提取时间过长,浸提液中的一部分茶多酚会被氧化,从而降低了溶液中茶多酚的浸提率.
在一定温度范围内,随着温度的增加,分子运动加剧,茶叶中茶多酚的溶解速度和溶解量都在增加,但是当温度增加到一定程度时,茶多酚已完全溶解,继续增加温度对茶多酚的含量也不会有太大影响.
在一定范围内,溶剂乙醇浓度的增加,茶叶与溶剂接触程度加大,且细胞内外浓度差增大,茶叶中茶多酚的溶解量在不断增加,但是当增加到某一程度时,茶叶与溶剂的接触程度反而降低,使溶液中茶多酚的浸提率降低.
3 结论
本文采用紫外可见分光光度技术研究立顿绿茶在不同热浸提工艺条件下茶多酚的提取率情况,利用酒石酸亚铁比色法测定溶液中茶多酚的含量,采用正交试验设计对液固比、溶剂(乙醇)浓度、浸提时间和提取温度这四个影响因素对茶多酚的提取效果进行研究,发现各因素对茶多酚提取率的影响大小依次为液固比、溶剂(乙醇)浓度、浸提温度和浸提时间,并且了解到各因素均应在一定范围进行实验最佳,最后通过比较茶多酚的提取率获得本实验最优的工艺条件,即液固比为120∶1、提取温度为80 ℃、浸提时间为30 min、乙醇浓度为75%,按最优工艺条件重复实验三次达到最佳效果,即茶多酚提取率达到最高17.23%.
