超声检查在心源性休克患者接受静脉- 动脉体外膜氧合治疗撤机中的应用价值
2022-03-06张威张维维通信作者
张威,张维维(通信作者)
赣州市人民医院重症医学科 (江西赣州 341000)
体外膜氧合(extracorporeal membrane oxygenation,ECMO)疗法最早在1976年被应用于对新生儿进行床旁心肺支持治疗[1]。经过多年发展,目前常采用的静脉-动脉体外膜氧合(vein-artery extracorporeal membrane oxygenation,V-A ECMO)技术已较为成熟,并且能够作为一种替代人体短期机械循环的辅助方法,被广泛用于治疗终末期扩张型心肌病、急性心肌梗死、病毒性心肌炎、心脏复苏、心源性休克等疾病患者,同时也被指南推荐为治疗难治性心源性休克的一线治疗方法。临床目前认为,当患者病情明显好转后应考虑及时脱离ECMO,在此过程中撤机成功与否对患者的预后具有重大影响[2]。目前虽有部分研究探讨了关于V-A ECMO 撤机的时机及评价标准[3],但仍未达成共识。本研究对心源性休克患者撤机前进行超声检查,根据患者结局进行分组并比较不同结局患者的超声检查指标,评价超声检查的应用价值,为临床提供一定参考。
1 资料与方法
1.1 一般资料
选择2016年5月至2020年9月于我院行V-A ECMO 治疗的心源性休克患者49例作为研究对象,根据撤机试验结果将患者分为两组,试验组撤机试验成功(37例),对照组撤机试验失败(12例)。试验组男19例,女18例;年龄47~69岁,平均(57.64±8.21)岁;体质量指数19.3~25.7 kg/m2,平均(22.68±4.28)kg/m2;心源性休克病因,心肌炎4例,扩张型心肌病12例,冠心病21例;V-A ECMO 治疗时间38~62 h,平均(51.21±5.27)h。对照组男6例, 女6例; 年龄43~62岁, 平均(56.39±7.84)岁;体质量指数18.6~24.8 kg/m2,平均(22.15±6.84)kg/m2;心源性休克病因,心肌炎1例,扩张型心肌病4例,冠心病7例;V-A ECMO 治疗时间42~65 h,平均(52.51±7.28)h。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会批准。
纳入标准:经诊断为左心室功能衰竭;均接受V-A ECMO 治疗;年龄>18周岁;均行有创机械通气。排除标准:合并心律失常患者;行主动脉内球囊反搏术的循环衰竭患者;合并右心功能障碍患者;主动脉瓣中度及以上反流的患者。
1.2 方法
采用美国Medtronic 公司生产的美敦力导管套装包,在局部麻醉患者右侧股动脉及股静脉后分别放置15~20 F 和19~22 F 的插管,静脉插管管道尖端位于下腔静脉内肝静脉出口的远心端1~2 cm 平面,动脉插管管道尖端位于腹主动脉中段;插管成功后在动脉插管的近心端放置1根6~8 F的灌注导管,导管头连接股动脉插管分流孔。患者均采用有创机械通气,呼吸机参数设置:采集血流动力学指标时调整为压力控制模式(潮气量设置为8~12 ml/kg),呼气末正压设置为5 cmH2O(1 cmH2O=0.098 kPa),呼吸频率(respiratory rate,RR)设置为15~20次/min。常规监测患者的生命体征,包括心率(heart rate,HR)、中心静脉压(central venous pressure,CVP)、肱动脉收缩压等。撤机标准:患者混合静脉血氧饱和度在70%以上,CVP<12 cmH2O,平均血压>60 mmHg(1 mmHg=0.133 kPa), 左心室射血分数(left ventricular ejection fraction,LVEF)≥40.00%。
所有患者在撤机试验开始前使用美国GE 公司生产的Vividi 超声仪对患者进行床旁超声检查,检查过程中采用1.8~6.0 MHz 凸阵探头进行扫描,获取患者心脏左室长轴观,并计算LVEF;获取患者心尖五腔观,在左室流出道放置脉冲取样容积,测量血流速度,记录心脏速度-时间积分(velocity-time integral,VTI),分别于患者通气吸气末及呼气末进行测量,得到极大值VTImax和极小值VTImin,计算主动脉速度-时间积分变异指数( △velocity-time integral variation index,△VTI),计算公式为△VTI=(VTImax-VTImin)/VTImax×100%。分别于患者通气吸气末及呼气末测量下腔静脉内径(diameter,D),测量部位为下腔静脉距肝静脉出口远心端约2 cm 处,得到极大值Dmax和极小值Dmin,计算得到下腔静脉呼吸变异指数(△respiratory variation index,△RVI),计算公式为△RVI=(Dmax-Dmin)/Dmax×100%,同时记录所有患者的静脉血氧饱和度(oxygen saturation in venous blood,SvO2)及心指数(cardiac index,CI)。在床旁超声检查过程中保持患者体征的平稳,检查由专人进行,结果取3次检测结果的平均值。
撤机试验:撤机试验由专业医师进行,患者取仰卧位,逐渐减小ECMO 血流量,减小流量速度为1 L/min,减小至1 L/min 时停止减小,观察患者生命体征,若患者在10~15 min 内出现肺水肿、容量过负荷、血压下降至60 mmHg 并持续、心律失常等情况时,判定为撤机失败。
1.3 观察指标
比较两组撤机试验前的各检测指标,包括LVEF、 △RVI、 △VTI、CVP、HR、SvO2及CI;分析撤机试验失败的影响因素。
1.4 统计学处理
采用SPSS 22.0统计软件进行数据分析,计量资料均符合正态分布,以±s表示,组间比较采用配对样本t检验;计数资料以率表示,采用χ2检验;多因素分析采用Logistic回归模型,P<0.05为差异有统计学意义。
2 结果
2.1 两组撤机试验前各指标比较
两组LVEF、 △RVI、CVP 及HR 比较, 差异均无统计学意义(P>0.05);试验组△VTI、SvO2及CI 均高于对照组,差异有统计学意义(P<0.05),见表1。
2.2 撤机试验失败的多因素Logistic 回归分析
将表1中差异有统计学意义的变量作为自变量,撤机失败与否作为因变量(撤机成功=0,撤机失败=1)进行多变量Logistic回归分析,结果显示,△VTI、SvO2及CI 是撤机失败的影响因素(P<0.05),见表2。
表1 两组撤机试验前各指标比较(±s)

表1 两组撤机试验前各指标比较(±s)
注:LVEF 为左心室射血分数,△RVI 为下腔静脉呼吸变异指数,△VTI 为主动脉速度-时间积分变异指数,CVP 为中心静脉压,HR 为心率,SvO2 为静脉血氧饱和度,CI 为心指数
组别例数LVEF△RVI(%) △VTI(%) CVP(mmH2O) HR(次/min)SvO2(%) CI[L/(min·m2)]对照组120.41±0.065.34±0.8211.35±2.528.39±1.28104.38±14.6881.39±8.242.16±0.61试验组370.42±0.085.17±0.7618.36±2.848.24±1.36105.74±11.2592.57±9.252.84±0.24 t 0.4610.6418.1140.3490.2973.9613.774 P 0.6540.5280.0000.7280.7690.0000.000
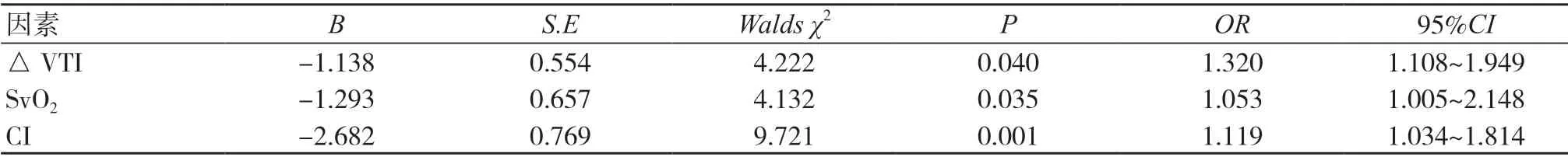
表2 撤机试验失败的多因素Logistic 回归分析
3 讨论
ECMO 可将人体的静脉血引流至体外,并使其变成动脉血再回输进入体内,故可在短期内替代心脏与肺的功能,是目前为心力衰竭或呼吸衰竭患者争取恢复心肺功能时间的常用方法,也是目前常用的体外生命支持方式。根据不同类型,ECMO 可分为多种,目前主要采用的为V-A ECMO,适用于治疗各种原因引起的终末期心力衰竭,为心脏移植或植入心室辅助装置赢得宝贵时间[4]。有研究表明,进行V-A ECMO 患者若无法成功脱机,其预后差、病死率高[5];也有部分研究表明,少数患者在脱机后可因心功能未完全恢复而需要再次治疗或死亡[6]。建立与脱离ECMO 的过程,均伴随着机体血流动力学的明显改变,尤其是在脱离过程中,会出现全身血管扩张、左心功能不全、右心功能不全等情况,致使心脏后负荷明显加重[7]。为了在脱离ECMO 后仍能维持较为平稳的血流动力学,在进行ECMO 脱离过程中应采用逐渐降低流量的方式进行试验,避免突然引起的低心排量导致的全身器官缺氧损伤。
目前,关于ECMO 脱离过程中的判定指标尚无统一标准,且存在一定争议,多数学者认为,脱离过程中若出现血流动力学指标的明显恶化,应及时停止脱离,而延长ECMO 维持时间可增加相关并发症发生风险[8]。研究显示,若ECMO 脱离时机体血流动力学指标变化剧烈,应采用超声进行密切监测[9]。在ECMO 开始过程中,需要700~1 000 ml 的启动液,这部分液体在脱离过程中会全部注入患者体内,加重心脏的前负荷,因此,应采用超声密切监测患者各项指标,判断其容量反应性,对撤机后循环容量的耐受力做出预测[10]。既往,临床常采用Swan-ganz 导管监测患者容量反应性,通过外周或中心静脉插入肺动脉或心脏右心系统监测患者心排血量、心脏及肺血管压力等指标[11]。但由于该方法在操作过程中容易遇到导管屈曲、嵌顿困难或气囊破裂等问题,患者易出现血栓、心律失常、感染等并发症[9]。本研究采用心脏超声进行实时监测,具有无创、操作简便等优点。有研究表明,心脏超声在监测机体容量反应性指标如△RVI 等方面具有重要作用[12]。本研究结果显示,两组LVEF、△RVI、CVP 及HR 比较,差异均无统计学意义(P>0.05)。分析后认为,静脉插管插入部位为下腔静脉,由于静脉插管具有一定的抽吸作用,对下腔静脉的直径产生一定影响,可能抵消了因呼吸作用引起的下腔静脉直径改变,故两组的△RVI 比较,差异无统计学意义。本研究结果还显示,试验组△VTI、SvO2及CI 均高于对照组,差异有统计学意义(P<0.05);多因素Logistic回归分析结果显示,△VTI、SvO2及CI 是撤机是否成功的影响因素。分析后认为,△VTI 更高提示患者的左心室心肌细胞处于Frank-Starling 曲线的上升支[13],其负荷潜能较大,在撤机后,能够适应额外启动液体的回输,故可成功撤机;而对照组△VTI 更小,说明患者心室细胞处于Frank-Starling 曲线的平台支[14],在增大循环血量时,心室细胞难以适应启动液的回输,故导致撤机失败;SvO2更高提示患者机体外周组织中的血液灌注情况更好,而更高的CI提示患者的心脏前负荷、后负荷均处于更佳的状态,患者心功能在一定程度上更好。
综上所述,超声检查在心源性休克患者接受V-A ECMO 治疗撤机中具有重要作用,△VTI、SvO2及CI 是撤机失败的影响因素,通过检测上述指标能够一定程度上判断患者对撤机是否耐受。
