以颅内出血为首发表现的增殖性脑血管病1例
2022-03-04马海波王建林屈茜茜赵修敏
马海波,王建林,屈茜茜,赵修敏
作者单位:250031济南,山东省立第三医院神经内科(马海波,赵修敏),急诊医学科(王建林);济南市中心医院中医科(屈茜茜)
增殖性脑血管病(CPA)是一种区别于经典脑动静脉畸形(AVM)的罕见脑血管病。目前国内尚无颅内出血为首发临床表现的报道,本文报道1例CPA致脑叶出血的患者如下。
1 病例患者,女,72岁,退役运动员,因“跌倒后意识丧失2 h”于2019年1月27日入住我院。患者入院前2 h被家属发现跌倒在地,意识清,能言语,约10 min后出现意识丧失。既往史:高血压病、2型糖尿病、冠状动脉粥样硬化性心脏病病史10年,平素应用药物控制尚可。无胸痛、胸闷、头痛、癫痫发作及脑血管病病史,既往无皮疹。无抗血小板聚集药物及抗凝药物使用史。无吸烟、饮酒史,无脑血管病家族史,配偶及两个女儿体健。神经系统查体:血压150/76 mmHg(1 mmHg=0.133 kPa),昏迷,双侧瞳孔等大等圆,直径约2.5 mm,对光反射消失,眼球向左凝视。双侧额纹对称,鼻唇沟对称,余颅神经不能配合。四肢无自主活动,刺激下四肢可见肢体肌肉回缩,四肢肌张力低,双侧Babinski征、脑膜刺激征阳性。全身肌肉无萎缩及震颤。其余神经系统查体不能配合。入院后头颅CT示右侧额叶、大脑镰旁及胼胝体体部出血,脑室积血,蛛网膜下腔出血,提示脑疝可能;右侧额顶叶、大脑镰旁混杂密度影,结合病史考虑动静脉畸形可能;中线结构局限性向左移位,双侧额叶及胼胝体膝部密度略减低(图1)。急诊给予气管插管、呼吸机辅助呼吸等对症治疗,尼莫地平注射液泵入改善血管痉挛。入院后以双侧额部为穿刺点,急症行双侧脑室硬通道穿刺外引流术以缓解脑疝症状。手术开始距发病3 h,术后昏迷状态。术后GCS评分5T(E1VTM4)。实验室检查:D-二聚体5.55 mg/L,糖化血红蛋白7.0%,空腹血糖14.4 mmol/L,低密度脂蛋白3.86 mmol/L。复查头颅CT及CTA(2019-01-29):(1)颅内出血范围缩小、可见低密度水肿影;(2)右侧额、顶叶混杂与正常脑组织同密度的高密度影,右侧大脑前动脉A2以远巨大血管团,部分跨过中线至对侧,远端累及右侧额、顶、枕部,考虑CPA;(3)右侧颈内动脉起始端狭窄;(4)双侧颈内动脉虹吸段均可见局限性隆起,左侧较大(0.35 cm);(5)左侧大脑前动脉A2以远端未见显示,左侧大脑中动脉及大脑后动脉纤细(图2)。患者于2019年2月7日意识状态好转,为嗜睡状态。查体:血压130/69 mmHg,气管切开,脑室外引流管夹闭,双肺呼吸音粗,有湿罗音。神经系统查体:嗜睡,双侧瞳孔2.5 mm,对光反射存在,眼球运动可。右侧肢体可自主活动,左侧肢体刺激下可见肌肉收缩,双侧Babinski征阳性。患者及家属拒绝行DSA检查,复查头颅CT(2019-02-09)示脑出血明显减少、第四脑室开通(图3),故拔除脑室引流管。诊断:CPA。患者于2019年2月22日出院,嗜睡状态,左侧肢体肌力Ⅰ级,右侧肢体肌力Ⅴ级。随访3个月,患者于其他医院神经外科行动脉瘤介入治疗术两次(术式不详),随访3个月时再次出现致命性脑出血,治疗后呈植物状态,随访9个月时死亡。
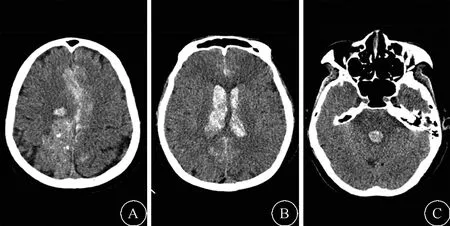
图1 头颅CT检查(2019-01-27) 右侧额叶出血、中线局限性向左偏移,脑室系统积血,右侧额、顶、枕叶多发高密度影,考虑畸形血管
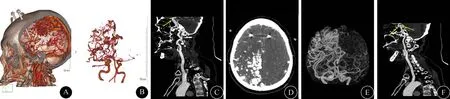
图2 头颈部CTA检查(2019-01-29) 双侧脑室的脑血管图像(A、D),横断面显示右侧额、顶、枕叶增生的脑血管影(D),去颅骨后颅内血管为巨大血管团,部分跨过中线至对侧,远端累及右侧额、顶、枕部,典型CPA影像学增生血管表现(B、E),右侧颈内动脉起始部狭窄、虹吸部小动脉瘤(C),左侧颈内动脉虹吸部动脉瘤(F)
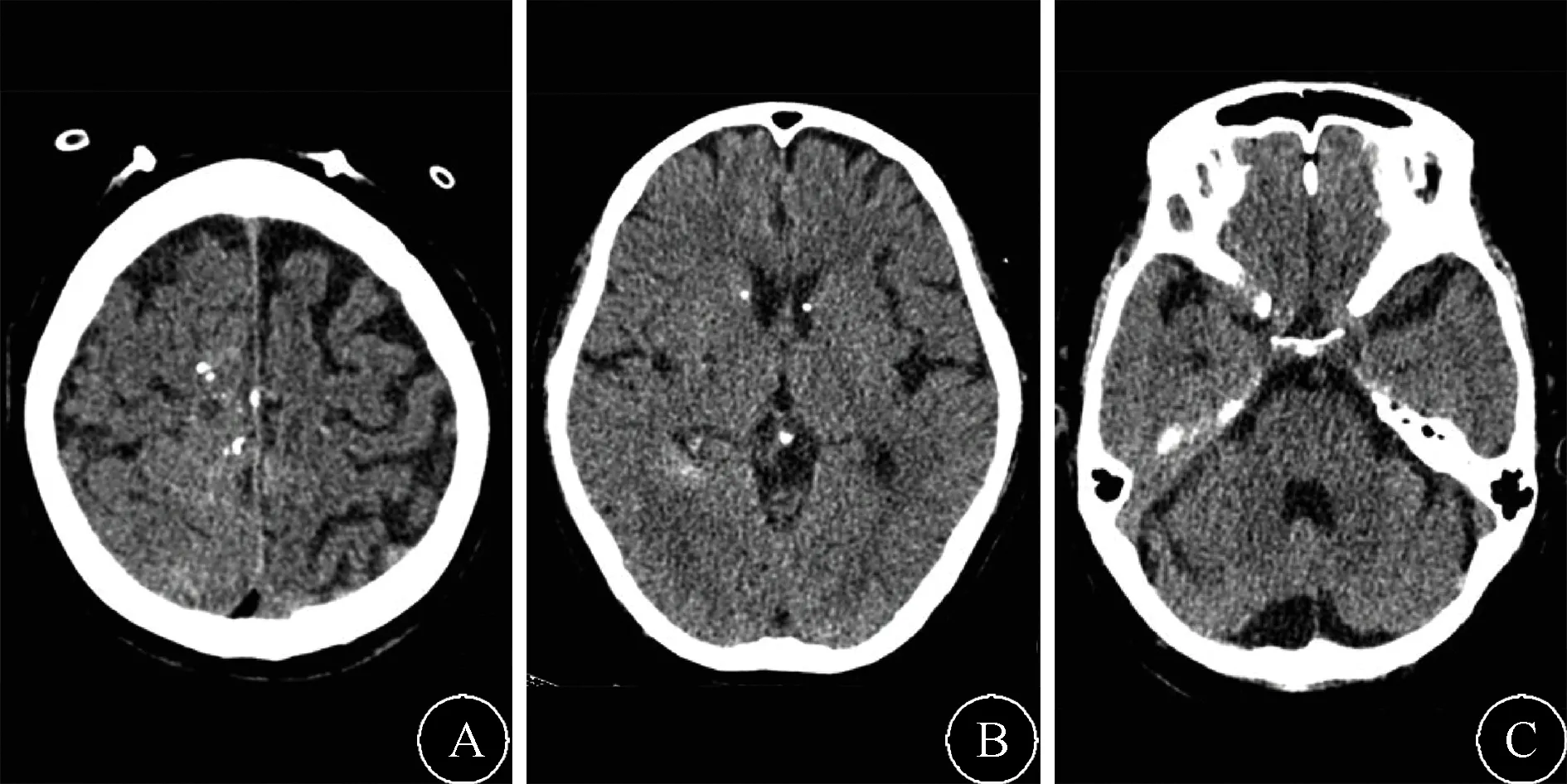
图3 头颅CT检查(2019-02-09) 脑室穿刺外引流术术后12 d,脑室出血基本完全引出,右侧脑叶仍有多发高密度影,考虑畸形血管影
2 讨论CPA具体发病机制未知,考虑缺血导致血管增殖可能,类似烟雾病。尸体研究[1]发现,CPA同时存在两种类型的血管病变——增殖性病变和血管畸形变,是增殖性病变和血管畸形变的一个中间过渡类型。本例患者既有血管增多、增粗,提示增殖性病变,又存在血管畸形表现,符合为CPA血管病变特点。
CPA患者多数较为年轻(平均年龄23岁),最常见的临床表现依次为头痛(44.9%)、癫痫发作(37.1%)和TIA(33.7%)[2],少见的临床表现包括合并面舌部血管瘤、侵蚀颅骨而出现头部搏动包块和视神经乳头水肿。CPA的脑出血发病率为18%,但脑出血的再出血率高达67%[2]。综合目前有详细临床报道的以脑出血作为CPA临床表现的文献报道发现,脑出血多为非首发症状,患者常以头痛、癫痫、脑缺血为首发症状[3],或为继发性脑出血[4]。本例虽为老年患者,既往有高血压病、糖尿病、冠状动脉粥样硬化性心脏病等脑血管病的危险因素,但患者右侧额叶大脑镰旁及胼胝体体部出血,与高血压性脑出血经典出血部位不符,与血管异常部位一致,考虑为非高血压性脑出血,结合后来的CTA表现,考虑为CPA,经微创手术等治疗患者病情平稳。提示除高血压性脑出血外,脑出血也可以由CPA等少见疾病导致,且脑出血急性期通过脑室硬通道外引流术治疗脑室积血是可行的。本例患者既往无头痛、癫痫及缺血性脑血管事件病史,脑出血为首发临床表现,属于CPA的少见类型。
影像学研究[1,5]显示,CPA异常血管网病灶内脑血容量(CBV)上升、达峰时间(TTP)轻度下降和平均通过时间(MTT)延长;病灶周围异常增殖的血管因“盗血”出现远超病灶形态学异常的大面积低灌注,表现为CBV下降和TTP上升,甚至累及整个脑叶。超病灶的低灌注及血流动力变化可以解释此病最常见的临床表现——缺血性脑卒中、癫痫及头痛发作。Saliou等[6]认为,脑出血风险与炎性反应通路基因多态性有关,与增殖无关,结合影像学MTT下降认为出血风险低与供血动脉近端狭窄导致病变血管压力低有关。而CPA脑出血患者再出血风险高,可能与脑出血患者存在血管脆弱区有关。本例患者既往无脑缺血发作、癫痫、头痛等低灌注常见的症状,首发症状为脑出血,随访中发现患者再次出血,为CPA少见病例,符合CPA再出血风险高的特点。本病例表现为出血与再出血,可能与患者颈内动脉近端狭窄程度轻有关,推测其血管可能存在脆弱区。
目前CPA尚无特效药物,以对症治疗为主。有学者[7]采用颅内外搭桥、钻孔等间接血运重建治疗改善CPA皮质及皮质下供血以治疗CPA,也有研究[5]采用脑-硬脑膜-颞浅动脉血管贴敷术融合术和肌肉血管吻合术等间接血运重建术治疗CPA取得成功,但术后可能并发脑出血,且缺乏长期随访证实。另外可以通过选择性栓塞来改善头痛和癫痫症状,但有导致脑缺血事件的风险,故需严格把握适应证。另外,本病也可采用伽马刀在非功能区脑组织进行放射治疗[8]。CPA引起的脑出血罕见,但再出血风险高,故出血后可以通过DSA识别急性和非急性脑出血患者的假性动脉瘤和动脉瘤,并通过氰基丙烯酸正丁酯等进行靶向栓塞来治疗脆弱责任血管,预防再出血[2]。
CPA为罕见病,目前病因、发病机制及治疗多基于个案报道,缺乏临床随机对照研究等循证医学证据。通过完善脑血管检查,诊断并不困难。相信随着对CPA不断探索,对病因、发病机制及治疗会有更深入的认识。
