西南喀斯特地区水体硝态氮时空分布特征及其来源解析
2022-03-02李冬丽贺海波
李冬丽, 贺海波
西南喀斯特地区水体硝态氮时空分布特征及其来源解析
李冬丽1, 2, 贺海波1, 3*
(1. 中国科学院 地球化学研究所 环境地球化学国家重点实验室, 贵州 贵阳 550081; 2. 天津大学 地球系统科学学院, 天津 300072; 3. 云南大学 云南省地球系统科学重点实验室, 云南 昆明 650500)
由于人类活动影响, 水体硝态氮污染已经成为世界范围内的环境问题。硝态氮污染不仅会造成水体富营养化, 长期摄入过量硝酸盐还会严重威胁人体健康, 控制并解决水体硝态氮污染是我国经济社会发展过程中亟待解决的重要环境问题。我国西南喀斯特地区是世界上面积最大、发育最典型和人地矛盾尖锐的岩溶连续分布带, 具有十分脆弱且高度敏感的生态系统。与非喀斯特地区相比, 这里水体硝态氮污染情况更为复杂和严重。因此, 明确西南喀斯特地区内硝态氮的时空分布特征并对其来源进行解析是有效治理的前提。本研究梳理了近几十年来西南喀斯特地区水体硝态氮的现代监测结果, 探讨了水体硝态氮时空分布特征、来源及受控机制等问题, 发现: (1)区域内地表水硝态氮平均检出质量浓度不高, 地下水检出质量浓度波动范围较大; (2)近几十年来, 地表水硝态氮质量浓度整体呈现小幅增长趋势, 而地下水检出质量浓度随时间的变化存在地域差异; (3)降水的稀释和冲携作用对区域内硝态氮质量浓度及分布的影响不容忽视, 而人类活动导致的土地利用变化带来的影响可能成为未来的主控因素; (4)区域内水体硝态氮主要来源于铵态化肥、土壤有机氮、粪肥及污水, 硝化作用是主要的转化过程。研究结果将为进一步认识喀斯特地区氮循环过程及促进地区可持续发展提供理论基础。
西南喀斯特地区; 硝酸盐; 分布特征; 来源; 影响因素
0 引 言
硝态氮是溶解性无机氮在水体中最主要的存在形态, 是水体中重要的污染物之一, 尤其是高浓度硝酸盐对水生生态系统的危害已引发越来越多的关注(李思亮, 2005; 徐志伟等, 2014; Gutiérrez et al., 2018; 赵然等, 2019)。随着社会经济的高速发展, 城市及农田生态系统水体硝态氮污染日趋严重(张千千等, 2015)。硝态氮污染不仅会造成水质恶化, 浓度过高的硝酸盐进入人体后可被还原为亚硝酸, 还会引发婴儿高铁血红蛋白症和胃癌等疾病(Kohl et al., 1971; Fan and Steinberg, 1996; 王东升等, 1997)。因此, 控制并解决水体硝态氮污染是我国经济社会发展过程中亟待解决的重要环境问题。
与非喀斯特地区相比, 喀斯特地区水体硝态氮污染情况更为复杂和严重。喀斯特水文系统是一个发育于溶岩含水层中独特的水文系统, 它与其他水文系统相比具有高度的敏感性和脆弱性(袁道先, 2001)。喀斯特地区各种表层岩溶带、落水洞、竖井和塌陷十分发育, 这些通道把地下水和地表水直接联系在一起(Gunn and Bailey, 1993)。而且岩溶水在地下管道中流动多为紊流和管道流, 污染物一旦进入含水层, 便可迅速扩散, 造成大面积的污染。我国西南喀斯特地区是世界上面积最大、喀斯特发育最典型和人地矛盾尖锐的岩溶连续分布带(马芊红和张科利, 2018), 中心位于滇、贵、渝、桂为主体的岩溶高原和山地地区, 具有十分脆弱和高度敏感的生态系统。随着西部大开战略的实施, 西南喀斯特地区经济发展速度及城市化进程加快, 污水排放量以及农业面源输出量日益增加, 岩溶水体硝态氮污染日趋严重。因此, 西南岩溶地区水体硝态氮污染问题应该受到重视, 而明确区域内硝态氮的分布、厘清其来源及影响因素是治理的前提。
目前关于西南喀斯特地区硝态氮污染的研究较多, 但主要集中在某个单独的流域, 例如乌江流域(李思亮, 2005; Yue et al., 2015; Li and Ji, 2016; Wang et al., 2018)和赤水河流域(罗进等, 2014; 安艳玲等, 2015; 任奕蒙等, 2019; 秦立等, 2019)等, 缺乏硝态氮时空分布特征和来源的全域性视角分析, 而这是认识氮循环过程的关键所在, 也是区域生态治理的前提。基于此, 本研究系统地收集了近几十年来西南喀斯特地区硝态氮污染的相关研究, 对该区域内的乌江水系、西江水系、赤水河水系以及嘉陵江水系等主要水系内硝态氮的时空分布特征进行梳理, 并结合污染历史水平, 着重探讨西南喀斯特地区硝态氮的来源及影响因素。
1 西南喀斯特地区硝态氮的时空分布特征
1.1 空间分布特征
表1和图1中展示了硝态氮在西南喀斯特地区主要水系中的检出情况。在所列出的报道中,自2000年以来西南喀斯特地区的硝态氮质量浓度普遍较低, 平均为2.13 mg/L。整体而言, 西江水系(2.96 mg/L)、赤水河(2.95 mg/L)硝态氮的平均检出质量浓度最高, 嘉陵江水系(1.41 mg/L)最低, 乌江水系(BDL~11.4 mg/L, BDL表示低于检测线或未检出)及西江水系(BDL~ 19.04 mg/L)变幅较大。据《中国饮用水卫生标准》(GB5749-2006)规定, 硝态氮含量限值应小于10 mg/L。因此, 大部分西南喀斯特水系地表水在硝态氮指标分析上基本符合饮用卫生标准。但应引起注意的是, 西江水系南洞地区平均检出质量浓度高达11.92 mg/L, 最高检出质量浓度高达19.04 mg/L, 超出饮用水卫生标准规定限值。此外, 西江(梧州–肇庆段)、南盘江以及位于普定城关河的最高检出质量浓度均接近或大于10 mg/L, 硝态氮质量浓度超标, 存在饮用安全风险。

表1 西南喀斯特地区地表水NO− 3-N质量浓度分布
注: NO− 3-N表示硝态氮; BDL表示低于检测线或未检出; NA表示无相应数据。
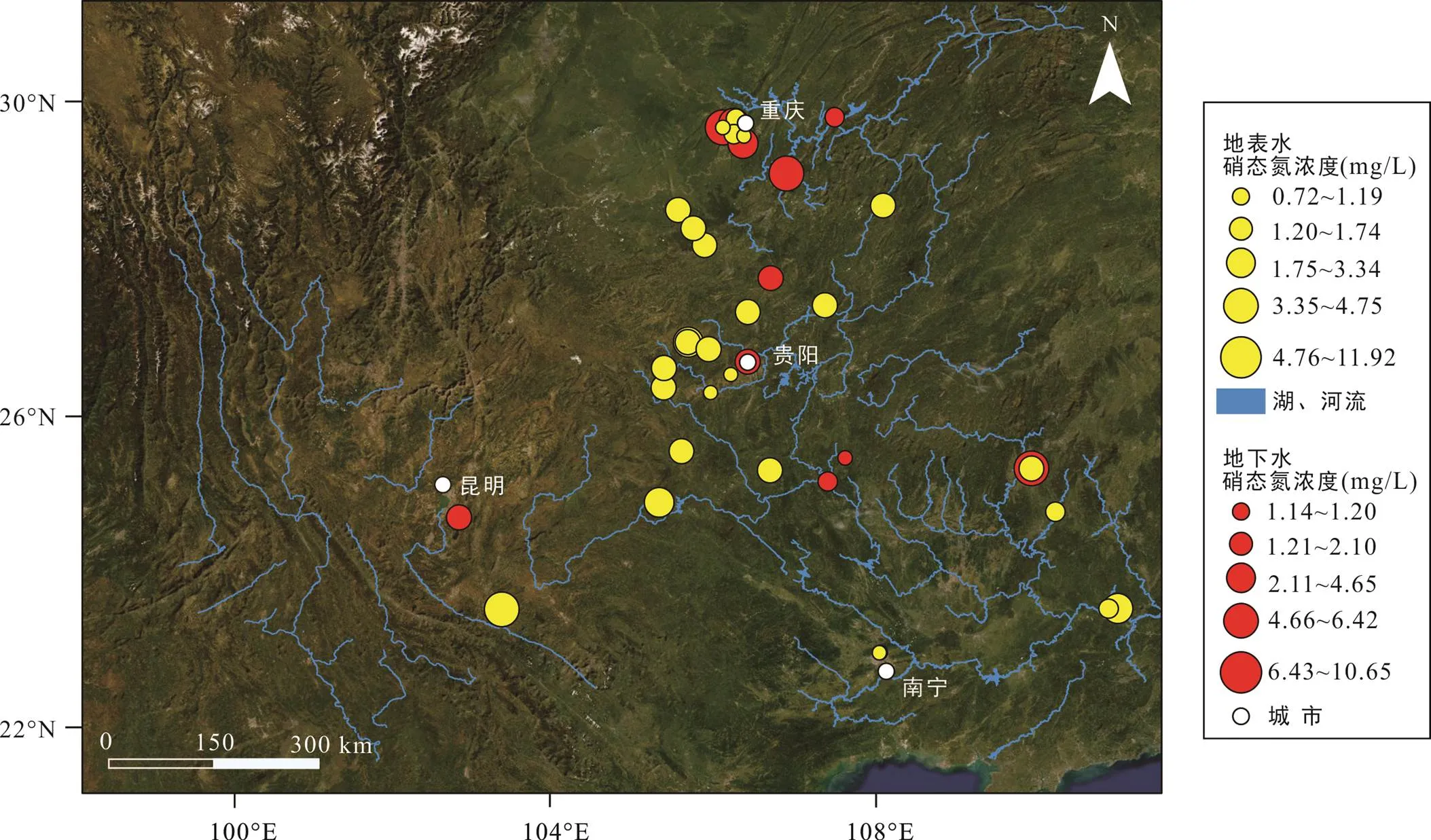
图1 西南喀斯特地区水体硝态氮质量浓度分布图
表2和图1为西南喀斯特地区地下水硝态氮质量浓度分布情况。近20年西南喀斯特地区地下水硝态氮平均检出质量浓度为6.36 mg/L, 其中以重庆金佛山地区的检出质量浓度最高, 其次是桂林东区和青木关地区。目前, 我国现行的地下水水质标准(GB/T 14848-2017)对五类水质的硝态氮限值做了规定: I类水≤2.0 mg/L, II类水≤5.0 mg/L, III类水≤20.0 mg/L, IV类水≤30.0 mg/L, V类水>30.0 mg/L, 而世界卫生组织及欧美各国关于饮用水硝态氮的限值分别为10 mg/L或11.3 mg/L。金佛山地区硝态氮平均检出质量浓度为25.25 mg/L, 最高检出质量浓度高达157.58 mg/L(2004年), 即使逐年下降趋势较显著, 但截至2009年平均检出质量浓度依旧较高(9.52 mg/L)。此外, 根据桂林东区(2012年)及青木关地下河(2017年)及南洞(2018年)地下水硝态氮平均检出质量浓度数据, 三地均高于10 mg/L, 且波动范围较大, 在国内地下水水质标准中位于II类至III类水之间; 若对标国际通行标准, 则接近水质标准的临界点。
1.2 时间分布特征
西南喀斯特地区地表水硝态氮检出质量浓度的空间差异性较为显著, 但总体仍呈现出逐年升高的趋势(表1)。其中, 桂林东区硝态氮质量浓度从上世纪八十年代的0.59 mg/L升高至2.00 mg/L左右, 显示出2~3倍的增量(Li et al., 2019), 西江从0.59 mg/L升高至3.99 m/L, 显示出6~7倍的增量; 嘉陵江水系自2005年至2017年间, 地表水硝态氮质量浓度存在小幅波动, 整体呈现小幅升高趋势; 乌江水系自上世纪90年代末至2015年间整体增幅虽较小, 但位于普定城管河的监测点于2015年却检测出异常高值(11.4 mg/L); 限于监测需求, 赤水河水系仅发表连续2~3年的硝态氮质量浓度数据, 但仍可在一定程度上反映出其质量浓度的年度增加趋势(表1)。
近20年来, 西南喀斯特区地下水硝态氮含量远超天然背景浓度值(2 mg/L)(蓝家程等, 2014)(表2)。整体来看, 贵州地下水硝态氮平均质量浓度呈现小幅升高, 表现较为平稳, 但需要引起注意的是仍有部分地区水样超标。重庆青木关地区地下水硝态氮质量浓度在监测期间翻倍增长, 2017年平均质量浓度高达10.47 mg/L。而在重庆金佛山地区, 地下水硝态氮质量浓度波动较大。来自1976的数据显示, 硝态氮平均检出质量浓度仅为1.82 mg/L, 地下水未受污染; 而至2004年, 平均检出质量浓度已高达25.25 mg/L,硝态氮污染严重; 从2005年起, 当地开展的测土配方施肥工作取得显著成效, 加上多年持续大面积退耕还林, 区内地下水硝态氮污染状况逐步改善(伍坤宇等, 2011), 并于2009年快速降至9.52 mg/L。与上述不同, 同属上游干流区(长江水系)的重庆老龙洞地下河则呈现逐年降低的趋势, 这主要归因于当地城市化加剧, 农业活动的减少。由于西江水系各监测点较为分散且无常年的连续监测, 统计学意义不明显, 此处不做阐述。

表2 西南喀斯特地区地下水NO− 3-N质量浓度分布
注: BDL表示低于检测线或未检出; NA表示无相应数据。
2 气候与土地利用方式变化对硝态氮分布的影响
2.1 降 水
大气降水入渗是地下水获得补充水量的主要方式, 也是可溶性氮向下迁移的主要载体(杨维等, 2008)。虽然有研究认为降水可能是局部地区地表水水体中硝态氮的主要来源(Burns and Kendall, 2002; Buda and DeWalle, 2009), 但其质量浓度普遍较低, 雨水降落后形成地表径流或下渗补给地下水, 一般表现为稀释效应, 可使水体硝酸盐污染得到一定程度的减轻(王开然, 2013)。如西江水系梧州段的监测数据表明, 旱季水体中的硝态氮质量浓度与污水排放量正相关, 而在雨水丰沛的8~9月呈现负相关关系(Li et al., 2019); 西江流经的南宁、贵港、梧州、百色和柳州等工业城市, 其水样监测结果同样发现水体中硝态氮质量浓度旱季高于雨季的现象(王开然, 2013; 马阔等, 2018; Li et al., 2019)。
降水对离子产生稀释效应的同时, 又能通过溶解土壤中的易溶盐(尤其是硝酸盐)造成部分区域硝态氮分布出现异常波动的情况, 特别是在季节性农业活动较强的流域内这种现象尤为显著(贾亚男, 2004; 戴启等, 2009; 郭芳等, 2011; 曾杰等, 2017; 盛婷等, 2018)。曾杰等(2017)研究了雨季降水对贵州后寨流域水体硝态氮输出的影响, 发现地表水和地下水硝态氮质量浓度对降水事件的响应相似, 降水发生时水体硝态氮质量浓度显著上升, 在持续多日降雨后, 氮素质量浓度则达到最高值。赤水河流域也发现同样现象(任奕蒙等, 2019), 均表现出与西江流域相反的特征。造成这种差异的原因之一就是后寨流域和赤水河流域相对强烈的农业活动, 每年6月份是大面积施肥活动的高发期, 大量的降水将含硝酸盐肥料、污水冲刷进入地表水系统。
相比于地表水系统干湿季硝态氮质量浓度差异所表现出的多样性, 在喀斯特分布区, 地下水系统中硝态氮在降水集中的丰水期质量浓度普遍高于枯水期, 这可能是由于降水的冲携作用对地下水硝态氮质量浓度影响更为强烈(贾亚男, 2004)。值得注意的是, 目前学界鲜少有关于喀斯特地区与非喀斯特地区水体硝态氮质量浓度对降水事件的响应差异的研究, 这一点应该引起重视。
2.2 土地利用方式
面源输入是流域氮的主要来源之一, 而土地利用方式是影响面源污染的关键因子(Bhaduri et al., 2002; 宋泽芬等, 2008)。流域内的面源污染主要来自于4个方面: 生活污染、农业面源污染、畜禽养殖污染以及城市降水径流污染。其中, 土地利用方式对面源污染的影响主要体现在农业面源污染以及城市降雨径流污染两方面。流域内主要的土地利用类型包括林地、草地、耕地、建设用地等, 土地利用类型不同造成植被、土壤及人为管理措施等方面的差异, 导致地表径流、泥沙迁移和地表污染物的拦截等因素的改变, 影响流域内硝态氮输入输出量。土地利用方式对地表水及地下水硝态氮质量浓度变化的影响基本一致。
林地的植被覆盖度较好, 可以通过入渗、植物根系的生物吸收作用滞留和吸附氮素, 因此林地面积与流域硝酸盐输出质量浓度常常表现为较显著的负相关关系(王夏晖等, 2005; Han et al., 2014)。秦立等(2019)通过对赤水河流域不同土地利用类型与氮素流失质量浓度进行Pearson相关分析发现, 研究区内林地面积与硝态氮输出质量浓度呈显著负相关关系(=−0.652), 林地对水体硝态氮输出起氮汇的作用。另外, 研究发现贵阳、荔波两地林区地下水硝态氮质量浓度(0.91 mg/L, 0.26 mg/L)远低于农区、居民区和工业区, 仅为居民区的1/6~1/4(赵杨, 2009), 凸显林地的调控作用。
根据2015年土地变更调查结果, 西南喀斯特地区四省市(贵州、云南、广西和重庆)总耕地面积达1800万公顷, 占区域总面积的20%, 是流域内主要的土地利用类型之一。区域内耕地化肥施用量较大, 但存在施用质量低及施用技术不合理等问题, 常导致化肥的大量浪费, 使得残留于土壤中未被植物吸收的化肥最后通过降雨冲刷和淋滤污染地表水及地下水系统。灌溉是农业的普遍行为, 无论是利用污水灌溉还是利用落水洞调节稻田水位, 都将直接把农田中高质量浓度的含氮物质带入流域水体中。因此, 耕地的水体硝态氮负荷一般较重, 特别是在丰水期, 受降水的影响硝态氮的输出显著增加(贾亚男, 2004; 赵杨, 2009; 秦立等, 2019)。此外, 水土流失是土壤氮流失的重要途经, 而坡耕地是水土流失的主要源地(贾亚男, 2004)。根据地方土地利用情况调查, 贵州省2002年25°以上的坡耕地高达84.58万公顷, 占总耕地面积26.68%; 云南省2015年坡耕地、梯田和望天田总计49.93万公顷, 占总耕地面积8.30%。西南岩溶区土壤层薄, 石漠化严重, 塌陷和漏斗分布密集, 加上大量坡耕地的开垦, 水土流失频发, 从而加重流域水体硝态氮污染。例如, 青木关地下河以及桂林东区地下水高硝态氮负荷就主要受农业活动持续加强的影响。具体体现为: 桂林东区地下水径流区内多分布有农田、水塘以及养殖场, 含氮污水及化肥经过灌溉、淋溶进入地下水水体中, 导致地下水上游至下游氮污染负荷逐渐加重(王开然, 2013); 而青木关地下河流经区内人口较少, 基本无工业生产, 人类活动以农业生产为主, 硝态氮质量浓度超标主要受到农业施肥的影响(盛婷等, 2018)。
随着西部大开发战略的实施, 中国西部城市化进程迅速, 建设用地中生活污水和工业废水等点源污染排放量日益增加。生活污水及含氨氮的工业废水直接排入河流、水塘和湖泊等地表水体, 加剧了地表水硝态氮污染。据统计, 过去20年间西南四省市污水排放量呈现波动式增长, 从2001年的86亿吨增长至2018年的105亿吨, 2009年的年排放总量高达117亿吨, 较2001年增长36%。这些大量排放的污水进入地表水系统后, 直接导致了流域水体硝态氮质量浓度的逐年升高。而岩溶含水层管道系统高度发达, 也极易受到人为污染的影响(Liu et al., 2006; Wang et al., 2017)。此外, 地下基础设施建设创造了大量的次生空隙, 如隧道、下水道、地铁、储水设施以及地下停车场等(Wu et al., 2018), 这些基础设施的建设采用的回填材料往往具有比土壤更高的透气性(苏跃, 2008), 从而使含氮的生活污水和工业废水极易通过土壤入渗以及次生空隙汇入地下径流中, 加大岩溶地下水硝态氮的负荷。总之, 城市活动的加强将刺激流域水体中硝态氮质量浓度的增加。如上个世纪80年代直到本世纪初, 桂林东区地下水硝态氮高值仍明显处于城市和工业区(贾亚男, 2004)。同样地, 王开然(2013)对桂林东区不同土地利用类型水体中硝态氮的含量进行调查后发现, 居民区地下水存在严重污染, 硝态氮质量浓度均值为20.81 mg/L, 达到了严重超标的程度。而金佛山地区地下水硝态氮质量浓度处于较高值可能归因于历史遗留的污染问题(伍坤宇等, 2011)。截止至2004年, 金佛山地区地下水处于严重污染程度, 采样点最高质量浓度达157.58 mg/L, 平均超标率高达451.64%; 2004年后, 由于当地产业结构调整和环保政策的施行, 区内地下水硝态氮污染得到逐步改善, 至2009年其质量浓度降为9.52 mg/L(伍坤宇等, 2011)。因此, 不难发现, 通过优化调整产业结构以及科学管控生产生活废水等系列性举措施的施行, 水体硝态氮污染的基本态势能够得到有效遏制。
2.3 其他影响因素
区域内硝态氮质量浓度影响因素除降水和土地利用方式外, 上覆土壤、地层构造以及地下水水位等都能在一定程度上影响其在水体中的质量浓度及分布。土壤厚度和质地决定了其透水性, 对硝化和反硝化作用有重要的影响(李正兆等, 2008; 苏跃, 2008)。岩溶流域内若土壤覆盖浅, 上覆土以粉砂、砾质粘土、沙砾土等透水性能良好的组分为主, 则隔污性能差(王开然, 2013)。不同的地层构造使地下水补给及径流排泄条件出现差异, 从而使地下水中污染物的空间分布表现出较大差异(梁秀娟等, 2007; 王开然, 2013)。如一些研究表明, 地下水中硝态氮的质量浓度常常沿着地下水径流路径呈现明显降低趋势(Simmons et al., 1992; Groffman et al., 1996)。此外, 也有研究证实, 地下水位的深度通过影响硝态氮的氧化还原条件而对其浓度产生影响(王开然, 2013)。
3 西南喀斯特地区硝态氮的来源及主要转化过程
已如上述, 水体中硝态氮的主要来源包括降雨、土壤有机氮、化肥、动物粪肥及污水等(Liu et al., 2006; Kendall et al., 2007; Li et al., 2013)。厘清硝态氮的来源不仅有助于加深对氮循环过程的理解, 同时可为硝态氮污染的治理提供有益的科学支撑。
不同来源的硝酸盐氮素具有不同的同位素组成, 运用15N(NO− 3)进行硝态氮的来源与转化分析研究已经有40多年的历史, 但15N(NO− 3)在运移、混合中受硝化、反硝化和同化等作用的影响, 造成同位素分馏和特征值改变, 无法清晰准确地划分来源(沈照理等, 1993; 王东升, 1997; 明晓星等, 2019)。随着同位素检测技术的发展,18O(NO− 3)也能被同时测定, 可有效识别水体氮转化过程对硝态氮同位素组成的影响。如经过硝化反应形成的18O(NO− 3)(−10‰~15‰)与大气沉降源(>45‰)存在明显区别。另外, 大量的研究表明, 反硝化过程会导致水体硝酸盐浓度降低, 同时会使未反应的NO− 3中富集15N和18O,15N/18O的比值趋近于1~2(Böttche et al., 1990; Aravena and Robertson, 1998; Mengis et al., 1999; Fukada et al., 2003)。因此,18O(NO− 3)等技术的发展可为有效厘清硝态氮来源提供方法学支持。
西南喀斯特地区水体中15N(NO− 3)值的分布范围大致为−4.3‰~25.0‰,18O(NO− 3)则在−10.8‰~23.5‰之间(表3)。其中, 地表水硝酸盐15N和18O空间分布的差异性并不明显, 这与地下水不同。从图2中可以看出, 水体硝酸盐15N(NO− 3)平均值集中分布在0~25‰之间,18O(NO− 3)平均值集中在0~15‰之间, 地下水水体中18O(NO− 3)平均值则较地表水偏重。可见西南喀斯特地区水体硝态氮来源比较复杂, 主要来源于铵态化肥、土壤有机氮、粪肥及污水, 而降水的贡献极小。
硝化作用是指铵态氮在微生物的作用下氧化为硝态氮的过程, 可以发生在土壤和水体中。理论上硝化作用形成的NO− 3有2/3的氧原子来源于水(或土壤水), 1/3的氧原子来源于溶解氧(dissolved oxygen, DO), 后者的同位素组成与大气中的O2相似。由此, NO− 3的18O的理论计算公式为:
18O(NO− 3) = 2/318O(H2O) + 1/318O(O2)(1)
式中, 大气18O一般为23.5‰,18O(H2O)通常在−25‰~ 4‰之间(Kendall et al., 2007), 则得到的18O(NO− 3)的理论值分布在−8.8‰~10.5‰之间。然而, 西南喀斯特地区属于亚热带季风气候, 较高温度驱动下的硝化细菌可能使18O(NO− 3)的变化难以确定, 变幅甚至更大(Fadhullah et al., 2020)。并且, 硝化作用对水、空气中的氧原子的利用可能不完全按照2∶1的比例进行分配, 因此可能会存在18O(NO− 3)高于理论值(Kendall and Aravena, 2000)。图2中可以看出流域内水体中的18O(NO− 3)均值大多分布在−5‰~10‰范围内, 说明流域内水体硝酸盐转化过程主要以硝化作用为主, 其他因素诸如温度等的影响较小。

表3 西南喀斯特地区水体硝酸盐同位素范围
注: NA表示无相应数据。
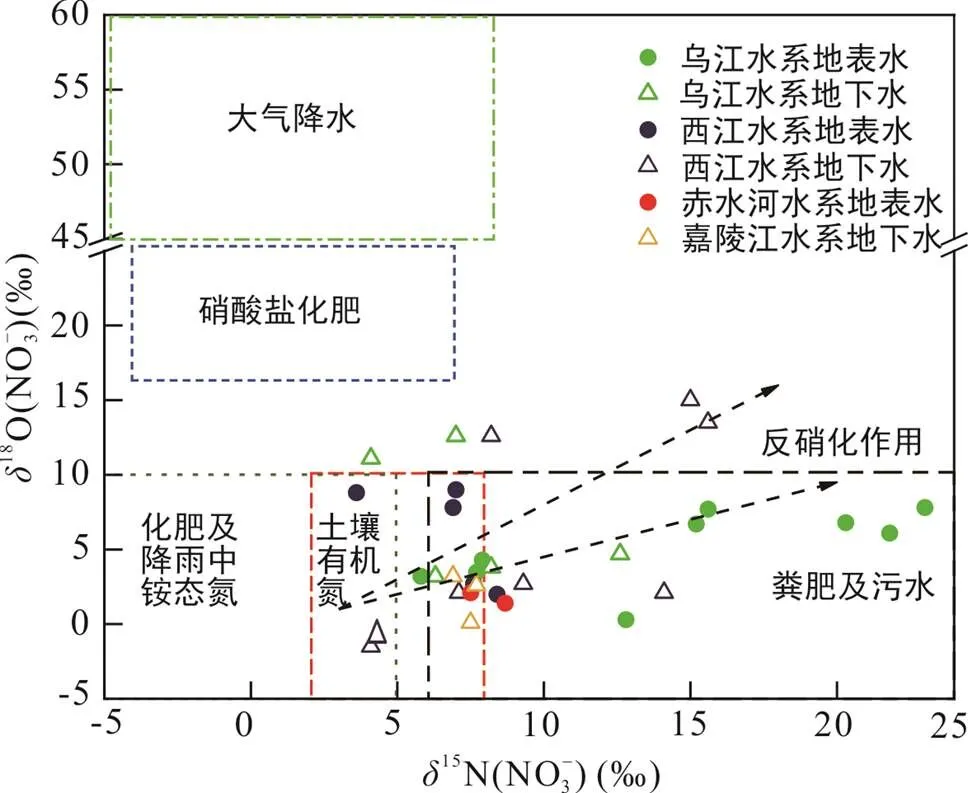
图2 西南喀斯特地区水体硝酸盐氮氧同位素平均值关系图(底图据李思亮, 2005; Li et al, 2019; 任奕蒙等, 2019)
反硝化作用是将NO− 3还原为N的气态产物(NO2、N2、N2O等), 气态产物释放到大气当中, 从而使得剩余部分的硝酸根富集18O和15N。Gillham and Cherry (1978)通过野外调查研究认为, 地下水环境中反硝化作用的DO上限为2.0 mg/L。DeSimone and Howes (1998)对地下水硝态氮污染监测时发现, 在2 大气沉降以及地表径流中各种无机氮和部分可溶性有机氮可以被水体中的生物同化吸收, 并且在同化吸收的过程中氮同位素分馏较大(−27‰~0‰) (Kendall and Aravena, 2000)。Granger et al. (2010)研究发现, 海洋浮游植物的生物同化作用可以降低地表水水体中硝酸盐浓度, 并且因为生物优先吸收偏轻的N、O同位素导致15N、18O在剩余部分富集, 使得水体中15N/18O富集比向1靠近。Wang et al. (2017)认为, 河下游硝酸盐浓度的降低以及15N的升高的主要原因是反硝化作用以及生物同化作用共同作用的结果。因此, 在图2中,15N/18O比值由2递减为1的过程中, 不仅发生了反硝化反应,而且由于地表水体中的生物量较大, 生物的同化吸收也起到了重要作用。这一因素应该引起我们的重视。 简而言之, 西南喀斯特地区水体中硝态氮主要来源于铵态化肥、土壤有机氮、粪肥及污水、硝态化肥, 硝化作用是主要的转化过程, 污染较为严重水体以及湖泊水位较深区域反硝化过程的影响不容忽视。进一步地, 为更精确解析硝态氮来源问题, 新技术新方法的运用成为必然之路, 如13C和11B与硝酸盐的氮氧双同位素联用等。总之, 随着社会生产力的极大发展, 诸如硝态氮污染在内的众多环境问题将更为深刻地影响着人们的生产生活, 如何在生态共同体视域下开展区域生态治理研究值得更多探索。 (1) 该区域地表水硝态氮平均检出质量浓度普遍不高, 但西江水系、乌江水系的检出质量浓度波动较大, 存在污染风险; 地下水硝态氮检出质量浓度波动范围较大, 尤其是重庆金佛山地区、青木关地区、桂林东区及南洞, 存在饮用安全风险。 (2) 近几十年来, 地表水硝态氮质量浓度总体呈现小幅增长的趋势, 而地下水检出质量浓度在不同地区的时间分布特征差异较大; 在控制因子上, 该地区无论地表水还是地下水均很大程度上受到来自人类活动的影响, 而降水对硝态氮的稀释和冲携作用也不容忽视; 同时, 通过运用硝酸盐氧氮同位素示踪方法, 发现西南喀斯特地区水体中硝态氮主要来源于铵态化肥、土壤有机氮、粪肥及污水, 硝化作用是主要的转化过程。 (3) 需要引起关注的是, 目前有关于喀斯特地区与非喀斯特地区水体硝态氮对降水事件的响应差异的研究较少, 相关工作的开展很有必要; 开发运用多指标示踪手段, 辨析污染物来源, 是未来的主攻方向, 可为硝态氮污染防治工作提供针对性方案; 在治理理念上, 坚持全域性视角探讨环境污染问题, 提出有针对性的生态安全调控对策建议, 为域内社会经济可持续发展提供科学支撑。 致谢:感谢两名匿名审稿人对本论文提供的建设性意见和建议, 这对本文的质量提升有很大的帮助, 作者在此表示最诚挚的感谢。 安艳玲, 吕婕梅, 吴起鑫, 罗进, 蒋浩, 彭文博, 于霞. 2015. 赤水河流域上游枯水期水化学特征及其影响因素分析. 环境科学与技术, 38(8): 117–122. 曹玉平, 袁热林, 焦树林, 张倩, 邓飞艳. 2018. 龙滩水库枯水期N、P元素空间分布特征. 水文, 38(2): 59–65. 戴启, 莫美仙, 陈海宁. 2009. 龙滩水库枯水期N、P元素空间分布特征. 云南地质, 28(4): 437–444. 段世辉, 蒋勇军, 张远瞩, 曾泽, 王正雄, 吴韦, 彭学义, 刘九缠. 2019. 岩溶槽谷区地下河硝酸盐来源及其环境效应: 以重庆龙凤槽谷地下河系统为例. 环境科学, 40(4): 1715–1725. 郭芳, 陈坤琨, 姜光辉. 2011. 岩溶地下河沉积物对氨氮的等温吸附特征. 环境科学, 32(2): 501–507. 贾亚男. 2004. 西南典型岩溶地区土地利用与土地覆被变化对岩溶水质的影响. 重庆: 西南师范大学博士学位论文: 99–103. 蓝家程, 杨平恒, 任坤, 陈雪彬, 徐昕, 胡宁. 2014. 重庆老龙洞地下河流域氮、磷及微生物污染调查研究. 环境科学, 35(4): 1297–1303. 李瑞. 2016. 里湖地下河N、S来源及其水–岩作用过程. 重庆: 西南大学硕士学位论文: 36–41. 李思亮. 2005. 喀斯特城市地下水C、N同位素地球化学——污染物迁移和转化研究. 贵阳: 中国科学院地球化学研究所博士学位论文: 62–85. 李正兆, 高海鹰, 张奇, 徐力刚. 2008. 抚仙湖流域典型农田区地下水硝态氮污染及其影响因素. 农业环境科学学报, 27(1): 0286–0290. 梁秀娟, 肖长来, 盛洪勋, 孟晓路, 李生海, 赵峰. 2007. 吉林市地下水中“三氮”迁移转化规律. 吉林大学学报(地球科学版), 37(2): 335–340. 刘婷婷. 2009. 嘉陵江水体中碳、氮、磷季节变化及其输出. 重庆: 西南大学硕士学位论文: 40–47. 罗进, 安艳玲, 吴起鑫, 杨瑞东, 蒋浩, 彭文博, 于霞, 吕婕梅. 2014. 赤水河中下游冬季河水化学空间分布特征分析. 地球与环境, 42(3): 297–305. 马阔, 吴起鑫, 韩贵琳, 董爱国. 2018. 南、北盘江流域枯水期水化学特征及离子来源分析. 中国岩溶, 37(2): 192–202. 马芊红, 张科利. 2018. 西南喀斯特地区土壤侵蚀研究进展与展望. 地球科学进展, 33(11): 1130–1141. 苗迎, 章程, 肖琼, 赵海娟, 李成习. 2018. 漓江段地表水体旱季硝酸盐动态变化特征及其来源. 环境科学, 39(4): 1589–1597. 明晓星, 杨平恒, 谢世友, 盛婷, 罗丹. 2019. 金佛山世界遗产地岩溶地下河系统硝酸盐来源与转化. 湖泊科学, 31(5): 1299–1309. 秦立, 付宇文, 吴起鑫, 安艳玲, 刘瑞禄, 吕婕梅, 吴振宇. 2019. 赤水河流域土地利用结构对氮素输出的影响. 长江流域资源与环境, 28(1): 19. 任奕蒙, 岳甫均, 徐森, 陈赛男, 王忠军, 李思亮. 2019. 利用氮氧同位素解析赤水河流域水体硝酸盐来源及其时空变化特征. 地球与环境, 47(6): 820–828. 申春华. 2019. 喀斯特地下暗河流域水体中硝酸盐的来源、运移过程及转化机制研究. 贵阳: 贵州大学硕士学位论文: 29–45. 沈照理, 朱宛华, 钟佐燊. 1993. 水文地球化学基础. 北京: 地质出版社: 60–68. 盛婷, 杨平恒, 谢国文, 洪爱花, 曹聪, 谢世友, 时伟宇. 2018. 基于15N和18O的农业区地下河硝酸盐污染来源. 环境科学, 39(10): 4547–4555. 宋泽芬, 王克勤, 杨云华, 李天兴. 2008. 澄江尖山河小流域不同土地利用类型面源污染输出特征. 水土保持学报, 22(2): 98–101. 苏跃. 2008. 喀斯特小流域土壤质量变化及其对水环境质量的影响. 重庆: 西南大学博士学位论文: 35–42. 汪智军. 2011. 青木关岩溶流域水——土系统碳氮同位素特征研究. 重庆: 西南大学硕士学位论文: 77–82. 王宝利, 刘丛强, 汪福顺, 刘小龙, 彭希, 赵颜创. 2015. 乌江梯级水库碳氮耦合的生物地球化学循环. 上海大学学报, 21(3): 294–300. 王东升. 1997. 氮同位素比 (15N/14N) 在地下水氮污染研究中的应用基础.地球学报, 18(2): 221–223. 王开然. 2013. 桂林东区峰林平原岩溶水系统氮的运移机理研究. 重庆: 西南大学硕士学位论文: 51–58. 王夏晖, 尹澄清, 单保庆. 2005. 农业流域“汇”型景观结构对径流调控及磷污染物截留作用的研究. 环境科学学报, 25(3): 293–299. 王中美, 谭正莲. 2013. 贵阳市岩溶地下水动态特征分析. 贵州大学学报(自然科学版), 30(1): 27–32. 吴起鑫, 韩贵琳, 李富山, 唐杨. 2015. 珠江源区南、北盘江丰水期水化学组成特征及来源分析. 环境化学, 34(7): 1289–1296. 伍坤宇, 王鹏, 沈立成, 肖琼. 2011. 金佛山地区地下水硝态氮污染时空变异性研究. 环境科学, 32(11): 3247– 3254. 肖欣, 陈淼, 吴永贵. 2015. 遵义市主城区地下水水化学特征及水质的时空变化. 桂林理工大学学报, 35(1): 142–146. 徐森, 李思亮, 钟君, 苏靖, 陈率. 2018. 赤水河流域水化学特征与岩石风化机制. 生态学杂志, 37(3): 667–678. 徐志伟, 张心昱, 于贵瑞, 孙晓敏, 温学发. 2014. 中国水体硝酸盐氮氧双稳定同位素溯源研究进展. 环境科学, 35(8): 3230–3238. 杨维, 郭毓, 王晓华, 王锋, 闫广宇. 2008. 氮素在包气带与饱水层迁移转化的实验研究. 环境科学研究, 21(3): 69–75. 袁道先. 2001. 全球岩溶生态系统对比: 科学目标和执行计划. 地球科学进展, 16(4): 461–466. 曾杰, 吴起鑫, 李思亮, 岳甫均. 2017. 雨季喀斯特小流域氮输出特征及其受降雨的影响. 水土保持学报, 31(3): 73–78. 张千千, 缪丽萍, 孙继朝, 刘景涛. 2015. 稳定同位素识别水体硝酸盐污染来源的研究进展. 长江流域资源与环境, 24(5): 742–749. 张兴波, 蒋勇军, 邱述兰, 曹敏, 胡毅军. 2012. 农业活动对岩溶作用碳汇的影响: 以重庆青木关地下河流域为例. 地球科学进展, 27(4): 466–476. 张远瞩, 贺秋芳, 蒋勇军, 李勇. 2016. 重庆南山表层岩溶泉与地下河三氮运移及氮通量估算. 环境科学, 37(4): 1379–1388. 张志远. 2018. 嘉陵江重庆主城段水环境状况及水中EOM/Fe3+/NO− 3对DBP光解的影响. 重庆: 重庆大学硕士学位论文: 28–33. 赵然, 韩志伟, 申春华, 张水, 涂汉, 郭永丽. 2019. 典型岩溶地下河流域水体中硝酸盐源解析. 环境科学. 41(6): 2664–2670. 赵彦龙, 董曼玲, 丁文慈, 李心清, 周会. 2014. 西江干流梧州–肇庆段水化学特征研究. 广东微量元素科学, 21(12): 1–6. 赵杨. 2009. 喀斯特地区城市化对浅层地下水质量的影响及评价. 贵阳: 贵州大学硕士学位论文: 41–43. 朱俊. 2005. 水坝拦截对乌江生源要素生物地球化学循环的影响. 贵阳: 中国科学院地球化学研究所博士学位论文: 34–41. Aravena R, Robertson W D. 1998. Use of multiple isotope tracers to evaluate denitrification in ground water: Study of nitrate from a large-flux septic system plume., 36(6): 975–982. Bhaduri B, Bright E, Coleman P, Dobson J. 2002. LandScan: Locating people is what matters., 5(2): 34–37. Böttcher J, Strebel O, Voerkelius S, Schrmidt H L. 1990. Using isotope fractionation of nitrate-nitrogen and nitrate- oxygen for evaluation of microbial denitrification in a sandy aquifer., 114(3–4): 413–424. Buda A R, DeWalle D R. 2009. Using atmospheric chemistry and storm track information to explain the variation of nitrate stable isotopes in precipitation at a site in central Pennsylvania, USA., 43(29): 4453–4464. Burns D A, Kendall C. 2002. Analysis of15N and18O to differentiate NO− 3 sources in runoff at two watersheds in the Catskill Mountains of New York., 38(5): 9–1. DeSimone L A, Howes B L. 1998. Nitrogen transport and transformations in a shallow aquifer receiving wastewater discharge: A mass balance approach., 34(2): 271–285. Fadhullah W, Yaccob N S, Syakir M, Muhammad S A, Li S L. 2020. Nitrate sources and processes in the surface water of a tropical reservoir by stable isotopes and mixing model., 700: 134517. Fan A M, Steinberg V E. 1996. Health implications of nitrate and nitrite in drinking water: An update on methemoglobinemia occurrence and reproductive and developmental toxicity., 23(1): 35–43. Fukada T, Hiscock K M, Dennis P F, Grischek T. 2003. A dual isotope approach to identify denitrification in groundwater at a river-bank infiltration site., 37(13): 3070–3078. Gillham R, Cherry J. 1978. Field evidence of denitrification in shallow groundwater flow systems., 13(1): 53–72. Granger J, Sigman D M, Rohde M M, Maldonado M T, Tortell P D. 2010. N and O isotope effects during nitrate assimilation by unicellular prokaryotic and eukaryotic plankton cultures., 74(3): 1030–1040. Groffman P M, Howard G, Gold A J, Gold A J, Nelson W M. 1996. Microbial nitrate processing in shallow groundwater in a riparian forest., 25(6): 1309–1316. Gunn J, Bailey D. 1993. Limestone quarrying and quarry reclamation in Britain., 21(3): 167–172. Guo F, Wang W K, Jiang G H, Huang S Y. 2016. Distribution and stable isotopic compositions of organic carbon in surface sediments in hyporheic zone of karst springs., 75(850). Gutiérrez M, Biagioni R N, Alarcón-Herrera M T, Rivas-Lucero B A. 2018. An overview of nitrate sources and operating processes in arid and semiarid aquifer systems., 624: 1513–1522. Han G L, Li F S, Tan Q. 2014. Effects of land use on water chemistry in a river draining karst terrain, southwest China., 59(5): 1063–1073. Jiang Y J, Wu Y X, Yuan D X. 2009. Human impacts on karst groundwater contamination deduced by coupled nitrogen with strontium isotopes in the Nandong underground river system in Yunan, China., 43(20): 7676–7683. Kendall C, Aravena R. 2000. Nitrate isotopes in groundwater systems. Boston: Springer: 283–284. Kendall C, Elliott E M, Wankel S D. 2007. Tracing anthropogenic inputs of nitrogen to ecosystems., 12: 375–449. Kohl D H, Shearer G B, Commoner B. 1971. Fertilizer nitrogen: Contribution to nitrate in surface water in a corn belt watershed., 174(4016): 1331–1334. Li C, Ji H B. 2016. Chemical weathering and the role of sulfuric and nitric acids in carbonate weathering: Isotopes (13C,15N,34S, and18O) and chemical constraints., 121(5): 1288–1305. Li C, Li S L, Yue F J, Liu J, Zhong J, Yan Z F, Zhang R C, Wang Z J, Xu S. 2019. Identification of sources and transformations of nitrate in the Xijiang River using nitrate isotopes and Bayesian model., 646: 801–810. Li S L, Liu C Q, Lang Y C, Zhao Z Q, Zhou Z H. 2010. Tracing the sources of nitrate in karstic groundwater in Zunyi, Southwest China: A combined nitrogen isotope and water chemistry approach., 60(7): 1415–1423. Li S L, Liu C Q, Li J, Xue Z C, Guan J, Lang Y C, Ding H, Li L B. 2013. Evaluation of nitrate source in surface water of southwestern China based on stable isotopes., 68(1): 219–228. Liu C, Wang Q X, Watanabe M. 2006. Nitrogen transported to three Gorges Dam from agro-ecosystems during 1980–2000., 81(3): 291–312. Mengis M, Schif S, Harris M, English M C, Elgood R, MacLean A. 1999. Multiple geochemical and isotopic approaches for assessing ground water NO− 3 elimination in a riparian zone., 37(3): 448–457. Simmons R C, Gold A J, Groffman P M. 1992. Nitrate dynamics in riparian forests: Groundwater studies., 21(4): 659–665. Wang Z J, Yue F J, Li S L, Li X D, Wang S L, Li C, Tao F X. 2018. Nitrate dynamics during impoundment and flood periods in a subtropical karst reservoir: Hongfeng Lake, Southwestern China.:, 20(12): 1736–1745. Wang Z J, Yue F J, Zeng J, Li S L. 2017. The influence of urbanization on karst rivers based on nutrient concentration and nitrate dual isotopes: An example from southwestern China., 36(3): 446–451. Wu Y, Luo Z, Luo W, Ma T, Wang Y X. 2018. Multiple isotope geochemistry and hydrochemical monitoring of karst water in a rapidly urbanized region., 218: 44–58. Yue F J, Li S L, Liu C Q, Lang Y C, Ding H. 2015. Sources and transport of nitrate constrained by the isotopic technique in a karst catchment: An example from southwest China., 29(8): 1883– 1893. Yue F J, Li S L, Liu C Q, Mostofa K M G, Yoshida N, Toyoda S, Wang S L, Hattori S, Liu X L. 2018. Spatial variation of nitrogen cycling in a subtropical stratified impoundment in southwest China, elucidated by nitrous oxide isotopomer and nitrate isotopes., 8(2): 186–195. Spatial-temporal distribution and sources of nitrate-nitrogen in karst water, Southwest China LI Dongli1, 2, HE Haibo1, 3* (1.State Key Laboratory of Environmental Geochemistry, Institute of Geochemistry, CAS, Guiyang 550081, Guizhou, China; 2. School of Earth System Science, Tianjin University, Tianjin 300072, China; 3. Yunnan Key Laboratory of Earth System Science, Yunnan University, Kunming 650500, Yunnan, China) Water nitrate contamination is a global environmental problem because of intensive human activities. Excessive nitrate can cause eutrophication, reduce water quality and even threaten human health. Controlling nitrate pollution is an urgent issue for social and economic development in China. The karst area of southwest China (KASC) is the largest karst landscape on the earth and has a fragile ecosystem; therefore, the nitrate pollution state in the KASC is serious and complicated. Thus, the premise of pollution control is to clarify the distribution, sources, and influencing factors of nitrate in the water of KASC. This review summarizes the recent monitoring results of nitrate to assess the spatial-temporal distribution characteristics and identify the sources of nitrate-nitrogen in the waterbodies of the KASC in recent years. The results indicate that the average detected concentration of nitrate in the surface water is not high, and the range of concentrations detected in groundwater in the KASC fluctuates greatly. The concentration of nitrate in surface water showns a slight upward trend overall, while the changes in groundwater concentrations over time have regional differences in recent decades. Human activities have a strong influence on the concentration and distribution of nitrate in the region, and the dilution and carryover effects of precipitation cannot be ignored. Nitrate dual isotopes suggest that nitrate in KASC mainly comes from NH+ 4 in fertilizers, soil organic nitrogen (SON), domestic waste, and manure, and that nitrification is the key transformation process. This study provides scientific support for further understanding the nitrogen cycling process in the karst areas and promotes the sustainable development of KASC. KASC; nitrate; distribution characteristic; sources; influencing factors X142 A 0379-1726(2022)01-0034-12 10.19700/j.0379-1726.2022.01.004 2020-04-30; 2020-07-05 国家自然科学基金(42007296)和中国博士后科学基金第14批特别资助(站中)(2021T140582)联合资助。 李冬丽(1994–), 女, 博士研究生, 环境专业。E-mail: lidongli2050@163.com 贺海波(1989–), 男, 助理研究员, 从事环境地球化学研究。E-mail: hehaibo@vip.gyig.ac.cn4 总 结
