微生态制剂的序贯性肠内营养对重型颅脑损伤患者营养状况的影响
2022-02-28徐建英饶美霞
徐建英 饶美霞
重型颅脑损伤患者病理生理改变复杂,代谢加快,对营养物质的需求增高,易出现营养不良,而营养不良会增加胃肠道出血、感染及死亡等不良预后的发生风险。因此在重型颅脑损伤患者的临床干预中,应当及时给予科学营养支持。研究指出,与肠外营养相比,肠内营养更符合人体消化生理,能更有效改善患者营养状况,可作为重症患者首选支持途径[1]。但常规肠内营养支持方案易出现喂养不耐受情况,近年来,序贯性营养支持在临床中得到运用,并受到广泛青睐。有学者认为,重型颅脑损伤患者肠道内环境改变及菌群紊乱,不利于机体康复,有必要添加微生态制剂[2]。本研究将微生态制剂的序贯性肠内营养应用,重型颅脑损伤患者营养支持方案,现报道如下。
1 资料与方法
1.1 临床资料 选取2018 年12 月至2020 年7 月本院收治的重型颅脑损伤患者98 例纳入研究。(1)纳入标准:①年龄18~60 岁;②符合重型颅脑损伤(闭合性)诊断标准[3];③经颅脑CT、MRI 明确;④格拉斯哥昏迷评分(GCS)为5~8 分,且持续至少12 h;⑤重症患者营养风险评分(NUTRIC)≥5 分;⑥胃潴留量≤150 mL;⑦血流动力学稳定;⑧预计存活时间≥7 d。(2)排除标准:①恶性肿瘤患者;②有消化道疾病、损伤或手术史;③合并免疫、血液、内分泌系统疾病;④合并其他高代谢性疾病;⑤存在早期肠内营养禁忌证;⑥处于哺乳期、妊娠期女性;⑦合并其他部位损伤;⑧肝、心、肾功能不全者。98 例患者以随机数字表法分组,对照组、观察组各49 例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。
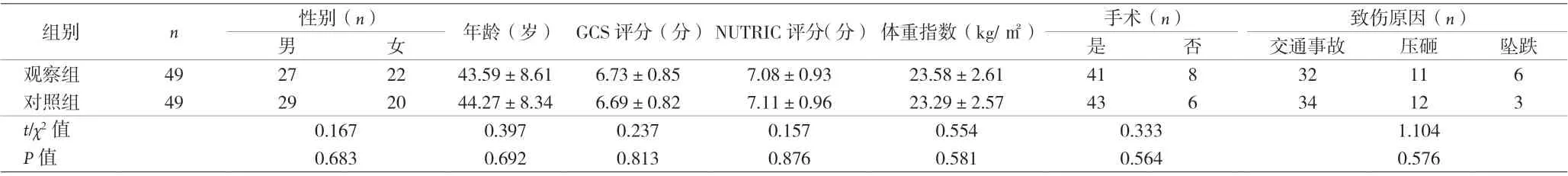
表1 两组患者一般资料比较
1.2 方法 两组均于患者入院后24~48 h 内实施肠内营养支持,目标喂养量25~30 kcal·(kg·d),喂养时床头抬高35~45°。对照组行序贯性肠内营养支持方案,第1 天通过14F 硅胶鼻胃管泵入500 mL 肠内营养混悬液(SP)[规格:500 mL/瓶(1 kcal/mL);批准文号:H20010285],之后每日泵入总量增加500 mL,起始泵入速度25 mL/h,根据患者具体情况逐渐将泵入速度提升至75 mL/h,第3 天开始替换为肠内营养混悬液(TPF)[规格:500 mL/瓶(1kcal/mL);批准文号:H20030012],泵入速度75 mL/h,每日泵入目标喂养量。观察组序贯性肠内营养支持与对照组一致,同时于肠内营养第1 天开始,给予双歧三联活菌肠溶胶囊(规格:210 mg/粒;批准文号:S19993065),630 mg/次,以20 mL 温水稀释后,自鼻胃管缓慢注入,每8 h 注入1次,每日3 次。
1.3 观察指标 (1)营养状况:分别于营养支持前1 d、营养支持第7 天,采集两组患者肘静脉血3 mL(空腹),离心处理,离心半径、速率、时间分别为10 cm、2,500 r/min、15 min,血清分离后,采用全自动生化分析仪测定总蛋白(TP)、白蛋白(ALB)、血红蛋白(Hb)水平。(2)肠黏膜屏障指标:分别于营养支持前1 d、营养支持第7 d,采集两组患者肘静脉血3 mL(空腹),离心处理,离心半径、速率、时间分别为8 cm、3,000 r/min、10 min,血清分离后,采用酶学分光光度法测定D-乳酸(D-LA)、内毒素(BT)、二胺氧化酶(DAO)水平。(3)营养支持相关不良反应:记录营养支持7 d 内两组患者相关不良反应(如腹泻、呕吐等)。
1.4 统计学方法 采用SPSS 24.0 统计软件。计量资料符合正态分布以(±s)表示,组内比较采用配对t检验,组间比较采用两独立样本t检验。计数资料以[n(%)]表示,采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者营养状况比较 见表2。
表2 两组患者营养支持前1 d、第7天血清TP、ALB、Hb水平比较(±s)

表2 两组患者营养支持前1 d、第7天血清TP、ALB、Hb水平比较(±s)
注:与本组营养支持前1 d 比较,*P<0.05
组别 n TP(g/L) ALB(g/L) Hb(g/L)营养支持前1 d 肠内营养第7 天 营养支持前1 d 肠内营养第7 天 营养支持前1 d 肠内营养第7 天观察组 49 68.48±9.62 66.74±8.83 38.49±5.18 37.65±7.23 125.81±14.93 124.34±12.02对照组 49 69.02±9.51 62.38±8.25* 39.26±5.07 32.19±7.74* 127.25±15.16 117.61±11.58*t 值 0.279 2.526 0.744 3.609 0.474 2.823 P 值 0.781 0.013 0.459 0.001 0.637 0.006
2.2 两组患者肠黏膜屏障指标比较 见表3。
表3 两组患者营养支持前1 d、第7天血清D-LA、BT、DAO水平比较(±s)
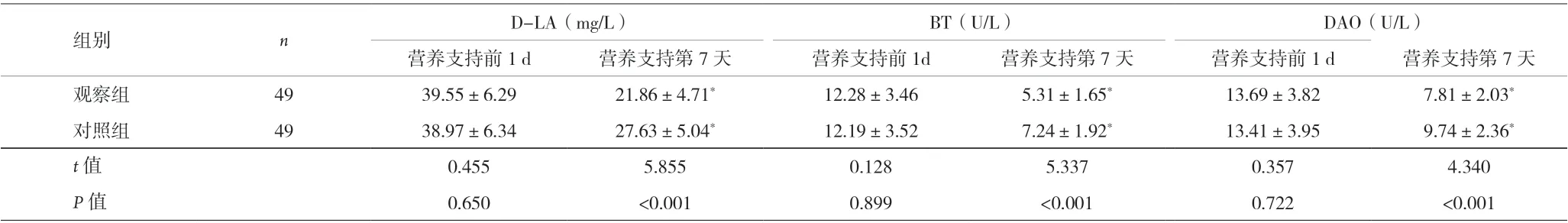
表3 两组患者营养支持前1 d、第7天血清D-LA、BT、DAO水平比较(±s)
注:与本组营养支持前1 d 比较,*P<0.05
组别 n D-LA(mg/L) BT(U/L) DAO(U/L)营养支持前1 d 营养支持第7 天 营养支持前1d 营养支持第7 天 营养支持前1 d 营养支持第7 天观察组 49 39.55±6.29 21.86±4.71* 12.28±3.46 5.31±1.65* 13.69±3.82 7.81±2.03*对照组 49 38.97±6.34 27.63±5.04* 12.19±3.52 7.24±1.92* 13.41±3.95 9.74±2.36*t 值 0.455 5.855 0.128 5.337 0.357 4.340 P 值 0.650 <0.001 0.899 <0.001 0.722 <0.001
2.3 两组患者营养支持相关不良反应 见表4。
3 讨论
营养支持途径分为肠内与肠外两种,其中肠内营养更符合生理,对肠黏膜结构与屏障功能的完整性有维持作用[4]。研究认为,在胃肠道解剖、功能允许,且血流动力学及内环境稳定情况下,对于无法自主进食的危重患者而言,应尽早实施经鼻胃管肠内营养支持[5]。由于重型颅脑损伤可引起脑-肠轴紊乱,导致消化道功能减弱,胃肠对于整蛋白制剂的耐受较差,若接受常规肠内营养支持,易出现腹泻、腹胀等不良反应,同时难以保障营养成分的吸收[6]。有学者指出,在重症脑血管病患者早期肠内营养支持中,首选以短肽为基础的营养制剂,待患者胃肠功能有所恢复后,再过渡至以整蛋白为基础的营养制剂,不仅能提高营养质量,同时能减少相关不适[7]。
有报道指出,重型颅脑损伤患者普遍存在肠道菌群失调,有必要予以微生态制剂进行调整[8]。另有研究指出,益生菌在促进营养物质吸收、抑制局部炎症、保护肠黏膜方面均有积极作用[9-12]。双歧三联活菌肠溶胶囊是由粪肠球菌、双歧杆菌、嗜酸乳酸杆菌经适当配制而成的微生态制剂,给药方便,三种益生菌进入肠道后作用迅速且持久。
本研究将添加微生态制剂的序贯性肠内营养支持方案应用于临床,结果显示,观察组患者营养支持第7天血清TP、ALB、Hb 水平明显高于同期对照组,且与营养支持前比较,无明显下降,提示该方案在保障患者良好营养状况方面有确切效果。考虑原因为在肠内营养支持同时添加微生态制剂,可直接增加肠内益生菌数量,竞争性抑制致病菌在肠内的增殖,减少肠源性毒素生成,促进营养物质吸收;同时能加快糖类分解,促进分泌型免疫球蛋白A 生成,增强机体免疫力。有报道指出,重型颅脑损伤患者由于胃肠道灌注水平降低,消化、吸收功能出现障碍,加之炎症反应、菌群失调等因素影响,可损害肠黏膜屏障功能[13-14]。D-LA 是肠道细菌发酵产生的代谢物质,BT 为革兰氏阴性菌细胞壁最外层成分,DAO 是肠黏膜上层绒毛内存在的具有高活性的代谢酶,当肠道功能出现损伤,肠黏膜通透性改变时,上述物质可透过黏膜进入血液,呈现异常高表达,是反映肠黏膜屏障功能的重要指标。本研究中,与对照组比较,观察组营养支持第7 天上述指标水平下降更明显,考虑原因为序贯性肠内营养支持能在早期减弱消化酶过度分泌引起的肠道刺激,同时添加微生态制剂后,可有效改善肠道内环境,调节菌群失调,减轻炎症,减少毒素产生。本研究还显示,观察组高水平胃残余量、腹泻、腹胀等营养支持相关不良反应发生率相较于对照组,明显较低,提示添加微生态制剂的序贯性肠内营养支持方案具有更高安全性。
综上所述,微生态制剂的序贯性肠内营养能有效改善重型颅脑损伤营养状况和肠黏膜屏障功能,减少不良反应的发生。
