沉香中倍半萜类化合物与生物活性研究进展及其质量标志物预测分析
2022-02-24王云云侯文成魏建和刘洋洋
王云云,侯文成,魏建和,刘洋洋*
沉香中倍半萜类化合物与生物活性研究进展及其质量标志物预测分析
王云云1, 2,侯文成2,魏建和1, 2,刘洋洋1, 2*
1. 中国医学科学院 北京协和医学院药用植物研究所,中草药物质基础与资源利用教育部重点实验室,濒危药材繁育国家工程实验室,北京 100193 2. 中国医学科学院 北京协和医学院药用植物研究所海南分所,海南省南药资源保护与开发重点实验室,国家中医药管理局沉香可持续利用重点研究室,海南 海口 570311
沉香为名贵药材和香料,倍半萜类化合物是沉香的特征成分和主要活性成分,根据其分子骨架可将沉香倍半萜类化合物分为8类。系统地总结了从沉香中分离出的倍半萜类化合物,并对其调节中枢神经系统、抗炎、抗肿瘤细胞毒、抑菌等活性的研究现状进行综述,并在此基础上结合质量标志物(quality marker,Q-Marker)的核心概念,从生源途径、传统药效、传统药性和化学成分等方面对沉香的Q-Marker进行预测分析,α-沉香呋喃、β-沉香呋喃、沉香螺旋醇可作为沉香的Q-Marker,为建立和完善沉香质量标准提供依据,以期为沉香质量的深入研究提供参考。
沉香;质量标志物;倍半萜;β-沉香呋喃;α-沉香呋喃;沉香螺旋醇
沉香为瑞香科沉香属spp. Lam.和拟沉香属spp. Gaertn.植物含树脂的木材,沉香属25个物种和拟沉香属8个物种均可产沉香[1]。沉香作为名贵香料,位居“沉檀龙麝”4大名香之首[2],作为药材最早记载于《名医别录》,列为上品[3],其性辛、苦,微温,具有行气止痛、温中止呕和纳气平喘等功效,主治胸腹胀满疼痛、胃寒呕吐呃逆和肾虚气逆喘急等症[4]。倍半萜为C-15萜烯[5],是高沸点芳香精油的主要组成成分,在沉香中常以烯烃或氧化烯烃形式存在。1959年Jain等[6]首次从马来沉香Lamk.所产沉香中分离鉴定出桉烷型倍半萜agarol,此后越来越多的倍半萜类化合物从沉香中分离获得,并发现其具有调节中枢神经系统和抗炎等活性。中药的有效性是中医临床用药的基础,2016年,刘昌孝院士[7]首次提出中药质量标志物(quality marker,Q-Marker)的概念,以新的观点系统地阐明中药质量与疗效间的关系,为完善我国中药质量标准,提高标准的科学合理性及可操作性,并强化标准的权威性和严肃性,指明了方向[8]。如决明子[9]、三七[10]、红芪[11]、山楂[12]等药材均基于此概念进行了Q-Marker预测。本文对从沉香中分离鉴定的倍半萜类化合物及其生物活性的研究进展进行总结,并结合Q-Marker的定义,从生源途径、传统药效、传统药性和化学成分等方面对沉香Q-Marker进行预测分析,以期为沉香的临床应用和进一步研究提供参考。
1 倍半萜类化合物
截至2021年3月,国内外学者已从沉香中分离并鉴定出210个倍半萜类化合物。主要分为呋喃型、螺旋烷型、杜松烷型、艾里莫酚烷型、桉烷型、前香草烷型、愈创木烷型和蛇麻烷型[13-15],化学结构见图1。呋喃型和桉烷型倍半萜类化合物具有相同的基本结构,属于桉烷型骨架类型,因特征的呋喃环结构,大多数学者将含有呋喃环的倍半萜另分为一类[16],也有研究将呋喃型归入桉烷型[15]。
1.1 呋喃型倍半萜
呋喃型倍半萜具有十氢化萘骨架,骨架外有1个甲氧基连接而成的呋喃环。1986年杨峻山等[17]从白木香(Lour.) Gilg.所结沉香中分离鉴定出呋喃型倍半萜去氢白木香醇(A11),经结构改造后得到的布格呋喃,已按1.1类抗广泛焦虑症新药进行开发并完成了IIa期临床试验[18-20]。至今,国内外已从沉香中分离鉴定出12个呋喃型倍半萜类化合物,见图1、表1。
1.2 螺旋烷型倍半萜
螺旋烷型倍半萜结构中具有特征的螺环结构。沉香螺旋醇(B5)是沉香中的特征化合物和香气成分[31],首次由印度学者Varma等[32]从马来沉香精油中分离而来,此后杨峻山等[33]又于白木香中分离获得。现代药理研究表明沉香螺旋醇可通过ip和脑室内注射给药对中枢神经系统产生有效影响,是潜在的抗精神病药[34]。国内外已从沉香中分离鉴定出13个螺旋烷型倍半萜类化合物,见图2、表2。
1.3 桉烷型倍半萜
桉烷型倍半萜是一类具有十氢化萘骨架的双环倍半萜,是沉香中分离的单体化合物中结构最丰富的一类,多数具有重要的生物活性,国内外已从沉香中分离鉴定出54个桉烷型倍半萜类化合物,见图3、表3。其中6个桉烷型倍半萜以内酯的形式存在[52,55],(+)-methyl selina-4,11-dien-14-oate(C28)、(+)-methyl-9-hydroxyselina-4,11-dien-14-oate(C29)、(−)-methyl selina-3,11-dien-14oate(C44)、5β,7β--elema-1,3-dien-11,13-dihydroxy-11-methyl ester(C52)、5β,7β--4α-hydroxy-eudesma-11,13-dihydroxy-11-methyl ester(C53)和5α,7α--4(14)-ene-eudesma-11,13-dihydroy-11-methyl ester(C54)的生物活性尚不明确。然而,倍半萜内酯类化合物抗肿瘤活性研究的报道很多[56],部分化合物已应用于临床治疗癌症,可克服普通化学药的不良反应和低药效。因此,沉香中的桉烷型倍半萜内酯可能是潜在的抗癌药物天然来源,有待进一步研究。

图1 沉香中呋喃型倍半萜类化合物的化学结构
表1 沉香中的呋喃型倍半萜类化合物
Table 1 Agarofuran-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 A1二氢沉香呋喃马来沉香21 A2去甲沉香呋喃酮马来沉香22-24 A3β-沉香呋喃马来沉香21,25 A4α-沉香呋喃马来沉香21,24,26 A54-羟基二氢沉香呋喃马来沉香22 A63,4-二羟基二氢沉香呋喃马来沉香22 A7环氧-β-沉香呋喃马来沉香23 A8白木香醇白木香17,24,27-28 A9baimuxifuranic acid白木香29 A10异白木香醇白木香29 A11去氢白木香醇白木香17 A124-羟基白木香醇白木香30
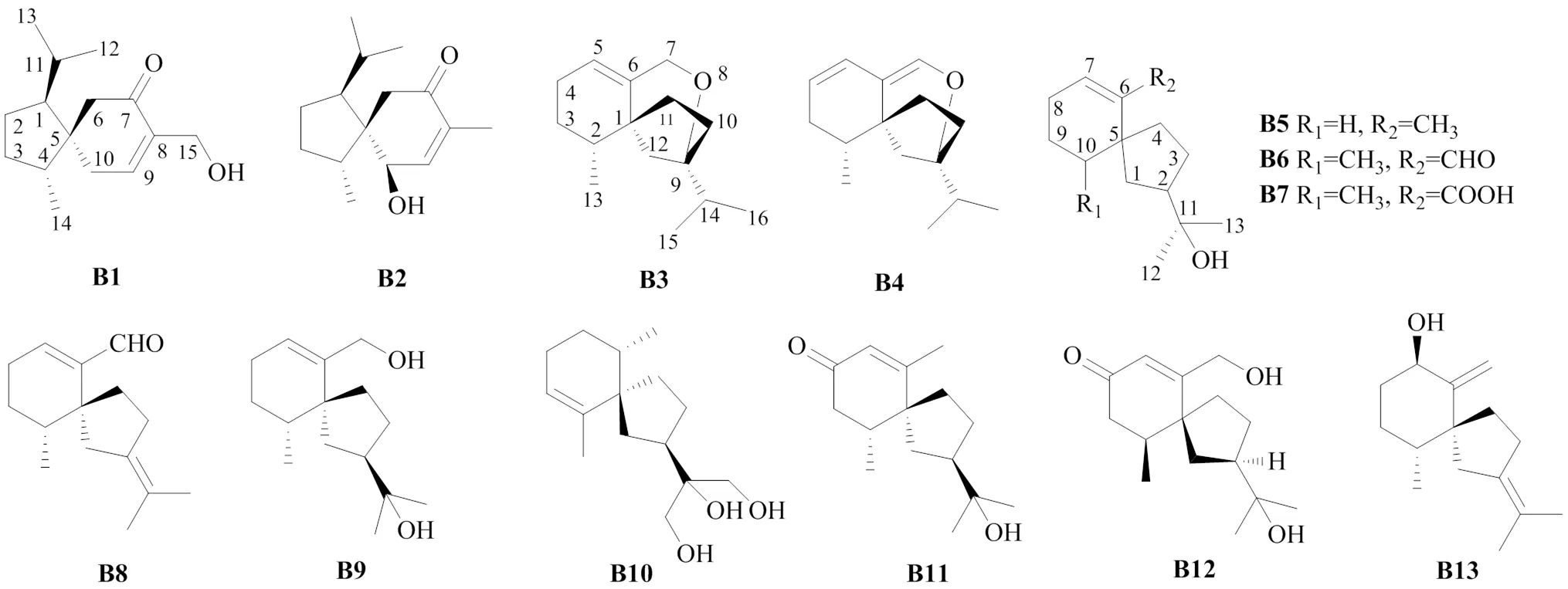
图2 沉香中螺旋烷型倍半萜类化合物的化学结构
表2 沉香中的螺旋烷型倍半萜类化合物
Table 2 Agarospirane-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 B14-epi-15-hydroxyacorenone白木香35-38 B24-epi-10-hydroxyacoronene 白木香36 B3rel-(1R,2R)-9-isopropyl-2-methyl-8-oxatricyclo[7.2.1.01,6]dodec-5-ene马来沉香39 B4rel-(1R,2R)-9-isopropyl-2-methyl-8-oxatricyclo[7.2.1.01,6]dodeca-4,6-diene马来沉香39 B5沉香螺旋醇马来沉香32,40 B6白木香醛白木香24-26,28,33,41 B7白木香酸白木香24,25,28,33 B8rel-(5R,10R)-2-isopropylidene-10-methyl-spiro[4,5]dec-6-ene-6-carbaldehyde马来沉香24,28,39 B9baimuxinol白木香27 B10rel-(2R,5R,10S)-6(7)-spirovetiven-11,12,13-triol沉香属42 B11(4R,5R,7R)-1(10)-spirovetiven-11-ol-2-one白木香43 B122-oxo-12-hydroxy-hinesol白木香44 B13rel-(5R,7R,10R)-2-isopropylidene-10-methyl-6-methylene-spiro[4.5]decan-7-ol马来沉香39
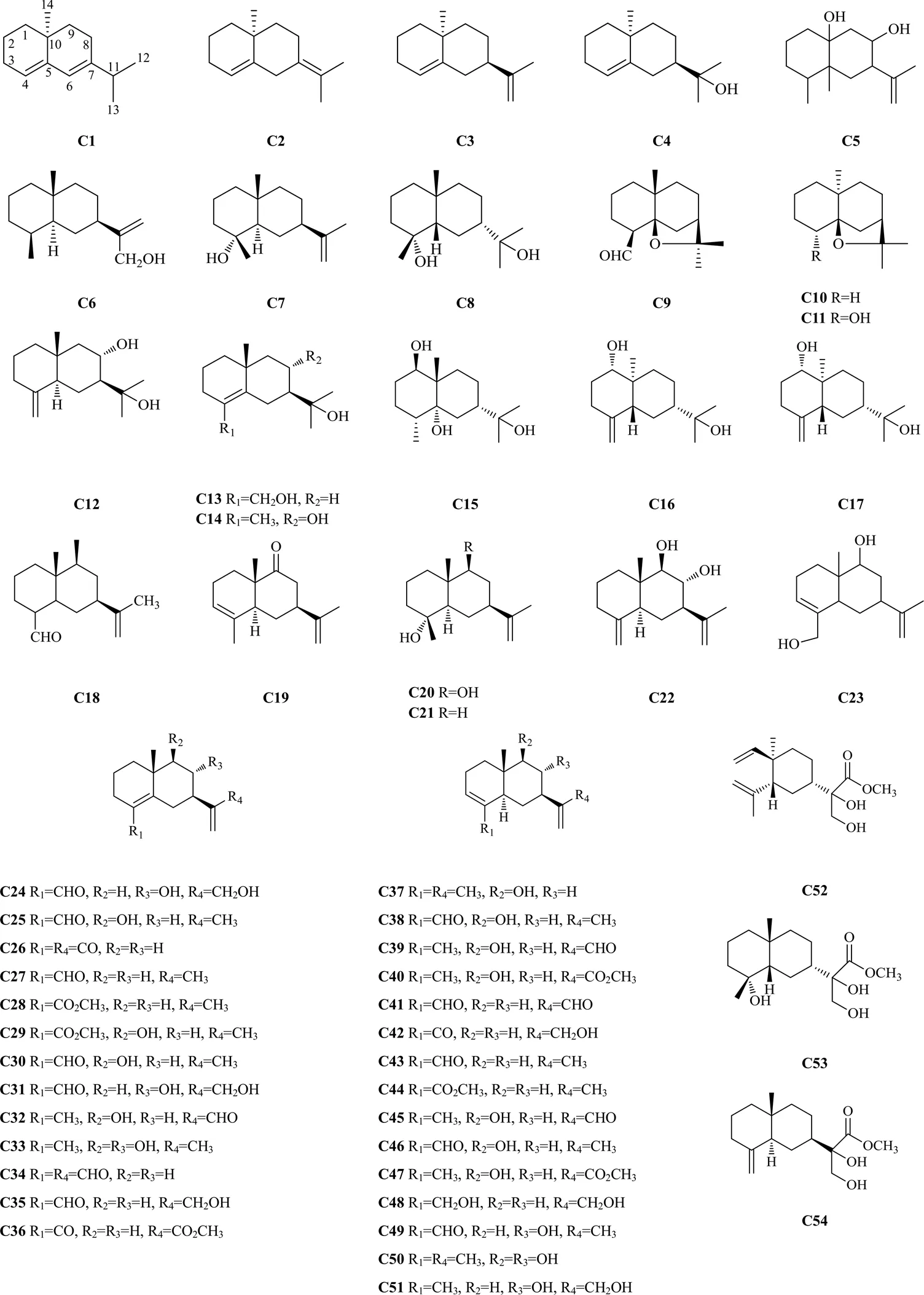
图3 沉香中桉烷型倍半萜类化合物的化学结构
表3 沉香中的螺旋烷型倍半萜类化合物
Table 3 Eudesmane-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 C1(S)-4a-rnethyl-2(1-methylethyl)-3,4,4a,5,6,7-hexahydronaphthalene马来沉香45 C2(S)-4a-methyl-2-(1-methylethylidene)-1,2,3,4,4a,5,6,7-octahydronaphthalene马来沉香45 C3(2R,4aS)-4a-methyl-2-(1-methylethenyl)-1,2,3,4,4a,5,6,7-octahydronaphthalene马来沉香45 C4(2R,4aS)-2-(4a-methyl-1,2,3,4,4a,5,6,7-octahydro-2-naphthyl)-propan-2-ol 马来沉香45 C53-isopropenyl-4a,5-dimethyl-octahydro-naphthalene-2,8a-diol白木香24 C6agarol马来沉香6 C75α,7α(H)-eudesm-11(13)-en-4α-ol白木香27 C8(−)-7βH-eudesmane-4α,11-diol白木香35,46 C9(1S,2S,6S,9R)-6,10,10-trimethyl-11-oxatricyclo[7.2.1.01.6]dodecane-2-carbaldehyde 马来沉香23 C10(1R,6S,9R)-6,10,10-trimethyI-11-oxatricyclo[7.2.1.01,6]dodecane马来沉香45 C11(1R,2R,6S,9R)-6,10,10-trimethyl-11-oxatricyclo[7.2.1.01,6]dodecan-2-ol马来沉香45 C125-desoxylongilobol柯拉斯那沉香A. crassna Pierre38,47 C13eudesm-4-ene-11,15-diol马来沉香38,48-49 C14eudesma-4-en-8,11-diol白木香48 C15eudesmane-1β,5α,11-triol白木香35 C16ent-4(15)-eudesmen-1α,11-diol白木香46 C17ent-4(15)-eudesmen-11-ol-1-one白木香35 C18(7S,9S,10S)-(+)-9-hydroxyselina-4,11-dien-14-al白木香38 C19(−)-selina-3,11-dien-9-one马来沉香50 C20(4R,5R,7S,9S,10S)-(–)-eudesma-11(13)-en-4,9-diol 白木香27,38 C21selin-11-en-4α-ol白木香38 C22(+)-eudesma-4(14),11(13)-dien-8α,9β-diol 白木香38 C23selina-3,11-dien-9,15-diol白木香51 C248α,12-dihydroxy-selina-4,11-dien-14-al白木香35 C259β-hydroxy-selina-4,11-dien-14-al白木香35 C26selina-4,11-diene-12,15-dial马来沉香49 C27(+)-selina4,11-dien-14-al马来沉香24,52 C28(+)-methyl selina-4,11-dien-14-oate马来沉香52 C29(+)-methyl-9-hydroxyselina-4,11-dien-14-oate马来沉香52 C30(7S,9S,10S)-(+)-9-hydroxy-selina-4,11-dien-14-al白木香38,46 C31(7S,9S,10S)-(+)-8,12-dihydroxy-selina-4,11-dien-14-al白木香46 C32(+)-9β-hydroxyeudesma-4,11(13)-dien-12-al白木香38 C33(+)-eudesma-4,11(13)-dien-8α,9β-diol白木香38 C3412,15-dioxo-selina-4,11-dine白木香38 C3512-hydroxy-4(5),11(13)-eudesmadien-15-al 白木香27,38 C36methyl-15-oxo-eudesmane-4,11(13)-dien-12-oate柯拉斯那沉香48 C37(+)-selina-3,11-dien-9-ol马来沉香50 C389β-hydroxy-selina-3,11-dien-14-al白木香35 C399β-hydroxy-selina-3,11-dien-12-al白木香35

续表3
1.4 杜松烷型倍半萜
杜松烷型倍半萜与桉烷型结构类似,区别在于异丙基取代基和2个甲基取代基的位置不同。1980年Pant等[57]从马来沉香中分离到2个杜松烷型倍半萜石梓呋喃(D4)和agarol(D5),石梓呋喃为agarol的C-8脱氢氧化而来。另外需要注意的是,agarol(D5)与1959年Jain等[6]从真菌感染的马来沉香中分离鉴定出的桉烷型倍半萜agarol(C6),命名相同,实为2个不同结构的化合物。国内外已从沉香中分离鉴定出7个杜松烷型倍半萜类化合物,见图4、表4。
1.5 艾里莫酚烷型倍半萜
艾里莫酚烷型倍半萜的结构类似于桉烷型和杜松烷型,三者结构上的相同点为均具有十氢化萘骨架,不同点在于异丙基取代基和2个甲基取代基的位置不同。国内外已从沉香中分离鉴定出39个艾里莫酚烷型倍半萜类化合物,见图5、表5。

图4 沉香中杜松烷型倍半萜类化合物的化学结构
表4 沉香中的杜松烷型倍半萜类化合物
Table 4 Cadinane-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 D1cis-7-hydroxycalamenene白木香58 D2(7β,8β,9β)-8,9-epoxycalamenen-10-one柯拉斯那沉香47 D38βH-dihydrogmelofuran马来沉香57 D4石梓呋喃马来沉香57 D5agarol马来沉香57 D6malacinones A 马来沉香59 D7malacinones B马来沉香59
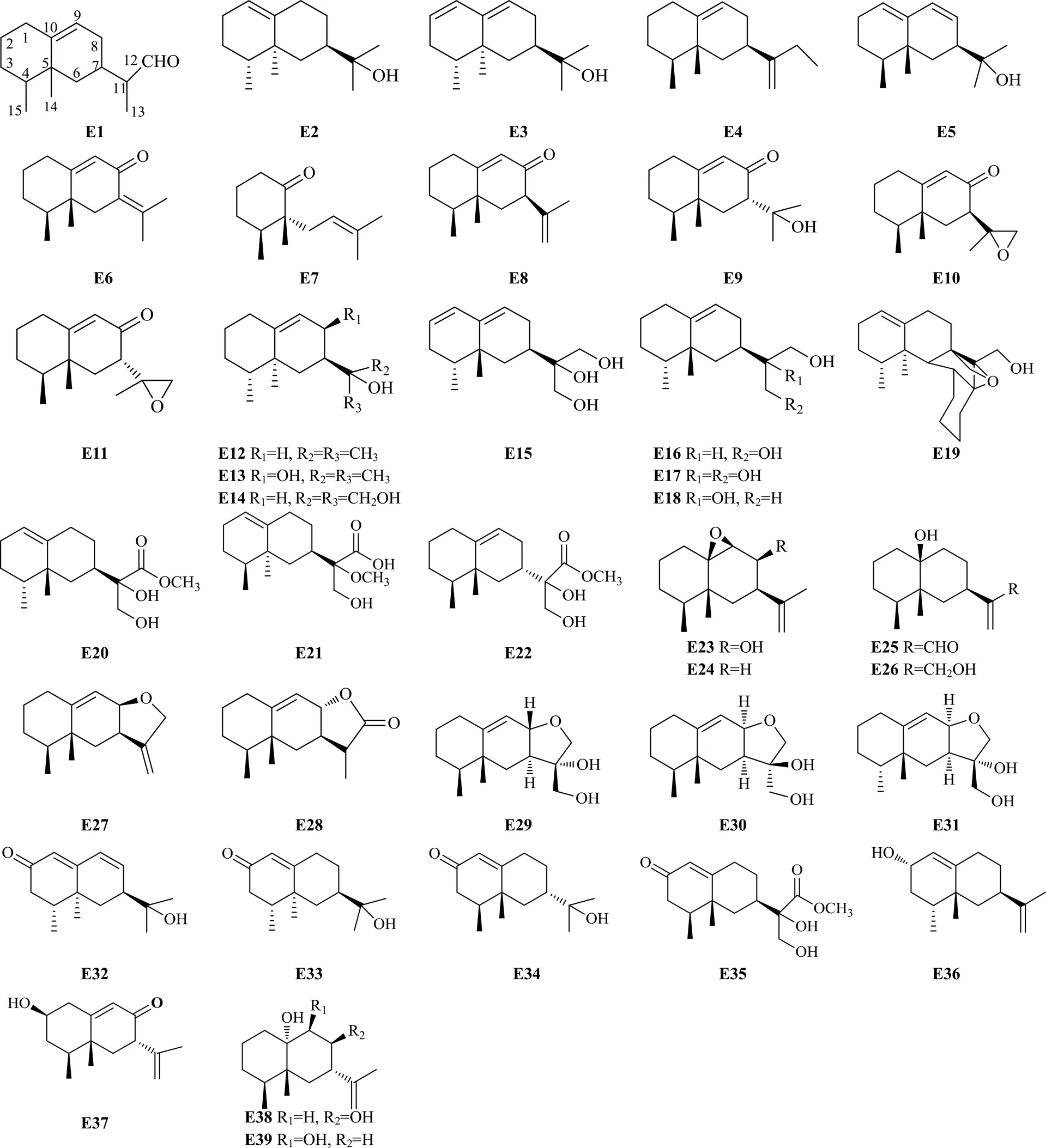
图5 沉香中艾里莫酚烷型倍半萜类化合物的化学结构
表5 沉香中的艾里莫酚烷型倍半萜类化合物
Table 5 Eremophilane-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 E12-(1,2,3,5,6,7,8,8a-octahydro-8,8a-dimethyl-2-naphthyl)-propanal 马来沉香39 E2缬草萜烯醇马来沉香37,40 E3(−)-dehydrojinkoh-eremol马来沉香52 E4rel-(2R,8S,8aR)-2-(1,2,3,5,6,7,8,8a-octahydro-8,8a-dimethyl-2-naphthyl)-prop-2-en-1-ol马来沉香39 E5rel-(2R,8S,8aR)-2-(1,2,6,7,8,8a-hexahydro-8,8a-dimethyl-2-naphthyl)-propan-2-ol马来沉香39 E6二氢卡拉酮白木香25,60 E72,t-3-dimethyl-r-2-(3-methyl-2-butenyl)-1-cyclohexanone马来沉香23 E8neopetasane白木香27,30,35,37,52 E9ligudicin C白木香60 E107α-H-9(10)-ene-11,12-epoxy-8-oxoeremophilane白木香30,35,47 E117β-H-9(10)-ene-11,12-epoxy-8-oxoeremophilane白木香30 E12jinkoh-eremol马来沉香40 E13(–)-eremophila-9-en-8β,11-diol 白木香38,48 E14eremophil-9-ene-11,12,13-triol沉香属42 E154β,7α-H-eremophil-1(2),9(10)-dien-11,12,13-triol柳叶拟沉香Gyrinops salicifolia Ridl53 E164β,7α-H-eremophil-9(10)-ene-12,13-diol柳叶拟沉香53 E174β,7α-H-eremophil-9(10)-ene-11,12,13-triol柳叶拟沉香53 E18eremophil-9(10)-ene-11,12-diol柳叶拟沉香53 E192-[(2β,8α,8aα)-8,8a-dimethyl-1,2,3,4,6,7,8,8a-octahydronaphthalen-2-yl] propane-1,2-diol柯拉斯那沉香48 E204β,7α-H-11,13-dihydroxy-eremophil-1(10)-ene-11-methyl ester柳叶拟沉香53 E21crasscid A柯拉斯那沉香48 E227β-H-9(10)-ene-eremophil-11,13-dihydroxy-11-methyl ester沉香属55 E23(1αβ,2β,3β,4αβ,5β,8αβ)-octahydro-4α,5-dimethyl-3-(1-methylethenyl)-3H-naphth[1,8a-b]oxiren-2-ol马来沉香49 E24(+)-9β,10β-epoxyeremophila-11(13)-en白木香38 E252-[(2β,4αβ,8β,8αβ)-decahydro-4α-hydroxy-8,8α-dimethylnaphthalen-2-yl] prop-2-enal 马来沉香35,38,49 E26(1β,4αβ,7β,8αβ)-octahydro-7-[1-(hydroxymethyl)ethenyl]-1,8α-dimethylnaphthalen- 4α(2H)-ol 马来沉香37,38,49 E27rel-(3R,7R,9R,10S)-9,1O-dimethyl-6-methylene-4-oxatricyclo[7.4.0.03,7] tridec-1-ene马来沉香30,39 E28(rel)-4β,5β,7β-eremophil-9-en-12, 8α-olide柳叶拟沉香61 E297α-H-11α,13-dihydroxy-9(10)-ene-8α,12-epoxyemophane沉香属55 E3011,13-dihydroxy-9(10)-ene-8β,12-epoxyemophilane柯拉斯那沉香42,47 E314β,7α,8α-H-eremophil-9(10)-ene-8,12-epoxy-11α,13-diol柳叶拟沉香53 E32(+)-11-hydroxyvalenc-1(10),8-dien-2-one白木香38 E3311-hydroxy-valenc-1(10)-en-2-one白木香35,37,38 E3411-hydroxy-valenc-1(10)-en-2-one白木香27 E35(4S,5R,7R)-11,12-dihydroxy-eremophila-1(10)-ene-2-oxo-11-methyl ester柯拉斯那沉香47 E36(+)-trans-nootkatol柳叶拟沉香53 E37petafolia B白木香27 E38(+)-4a,5-dimethyl-3-(prop-1-en-2yl)-octahydronaphthalene-2β,8a-diol白木香28 E39(1β,3α,4aβ,5β,8aα)-4a,5-dimethyl-3-(prop-1-en-2-yl) octahydronaphthalene-1,8a(1H)-diol柯拉斯那沉香48
1.6 前香草烷型倍半萜
前香草烷型倍半萜是自然界中罕见的三环型倍半萜。沉香中重要的香味成分jinkohol(F6)和jinkohol II(F7)[15,40-41]属于该类结构的典型化合物。国内外已从沉香中分离鉴定出23个前香草烷型倍半萜类化合物,见图6和表6。

图6 沉香中前香草烷型倍半萜类化合物的化学结构
表6 沉香中的艾里莫酚烷型倍半萜类化合物
Table 6 Prezizaane-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物来源文献 F1agarozizanol B沉香属62 F2aquilarene F沉香属63 F3daphnauranol D马来沉香64 F4daphnauranol B马来沉香64 F5daphnauranol C马来沉香64 F6jinkohol马来沉香41,62 F7jinkohol Ⅱ马来沉香40,62 F8agarozizanol D沉香属62 F9agarozizanol C沉香属62 F10jinkohol acid沉香属62 F11aquilarene A沉香属63 F12aquilarene B沉香属63 F13aquilarene C沉香属63 F14aquilarene D沉香属63 F15aquilarene E沉香属63 F16agarozizanol A沉香属62 F17aquilarene G沉香属63 F18aquilarene H沉香属63 F19aquilarene I沉香属63 F20agarozizanol E沉香属62 F21agarozizanol F沉香属62 F22iso-khusenol沉香属62 F23aquilarene J沉香属63
1.7 愈创木烷型倍半萜
愈创木烷型倍半萜是一类具有五元和七元环偶联结构的倍半萜烯化合物,其中大部分包含4,10-二甲基-7-异丙烯基。该类化合物在沉香中也较为丰富,单体的细胞活性测试结果表明,该类型的化合物多数具有乙酰胆碱酯酶抑制活性。国内外已从沉香中分离鉴定出46个愈创木烷型倍半萜类化合物,见图7、表7。

图7 沉香中愈创木烷型倍半萜类化合物的化学结构
表7 沉香中的艾里莫酚烷型倍半萜类化合物
Table 7 Guaiane-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 G1(–)-guaia-1(10),11-dien-15-al马来沉香50,65 G2(–)-guaia-1(10),11-dien-15-ol马来沉香65 G3(–)-guaia-1(10),11-diene-15-carboxylic acid马来沉香65 G4methyl guaia-1(10),11-diene-15-carboxylate马来沉香65 G5(+)-12,13-dihydroxyguaiol沉香属42 G6(+)-1,5-epoxy-nor-ketoguaiene马来沉香52 G7(–)-1(10)-epoxyguai-11-ene马来沉香65 G8(+)-guaia-1(10),11-dien-9-one马来沉香65 G9(–)-rotundone马来沉香65 G101α-hydroxy-4α,10α-dimethyl-5βH-octahydro-azulen-8-one白木香54 G11呋喃白木香醛白木香25 G12呋喃白木香醇白木香25,29,66 G13qinanol E白木香66 G14qinanol A白木香66 G15qinanol B白木香66 G16qinanol C白木香66 G17qinanol D白木香66 G187β,10β-epoxy-4αH-guaia-1(5),11(13)-dien-12-ol马来沉香67 G19α-kessyl alchol白木香36 G20chamaejasmone D马来沉香64 G21auranticanol A马来沉香64 G22chamaejasmone E马来沉香64 G23(–)-guaia-1(10),11-dien-15,2-olide马来沉香65 G2411β-hydroxy-13-isopropyl-dihydrodehydrocostus lactone白木香68 G251α,7α-dihydroxy-8oxo-4αH,5αH-guaia-9(10),11(13)-dien-12-oate马来沉香67 G261α-hydroxy-4βH-5βH-7βH-11αH-8,9-secoguaia-9(10)-en-8,12-olide白木香54 G271β-hydroxy-4βH-5βH-7βH-11αH-8,9-secoguaia-9(10)-en-8,12-olide白木香54 G281,10-dioxo-4αH-5αH-7βH-11αH-1,10-secoguaia-2(3)-en-12,8β-olide白木香54 G291,5;8,12-diepoxy-guaia-12-one白木香37 G301(5)-ene-7,10-epoxy-guaia-12-one丝沉香A. filaria (Oken) Merr.69 G311,8-epoxy-5H-guaia-9-en-12,8-olide丝沉香69 G322-oxo-5β,10β-peroxyl-1αH,4αH,7αH,8βH-guaian-8α,12-olide马来沉香67 G334αH,7αH-14-nor-guaia-1(5)-en-8α,12-olide马来沉香67 G3410α-hydroxy-4αH,5αH,7αH,8βH-guaia-1(2)-en-8α,12-olide 马来沉香67 G35(4R)-3-oxo-gweicurculactone丝沉香69 G36(4R,5S)-3-oxo-5,6-dihydro-gweicurculactone丝沉香69 G377βH-guaia-1(10)-en-12,8β-olide白木香54 G38奇楠内酯白木香36 G39(–)-gweicurculactone柳叶拟沉香53 G402-oxoguaia-1(10),3,5,7(11),8-pentaen-12,8-olide柳叶拟沉香53,69 G41愈创木内酯柳叶拟沉香53 G424β,5α,7α,8α-H-3β-hydroxy-1(10)-ene-8,12-epoxy-guaia-12-one柳叶拟沉香53 G433-oxo-7-hydroxylholosericin A白木香37 G443,3,7-trimethyltricycloundecan-8-one 白木香70 G45长叶烯白木香70 G46qinan-guaiane-one白木香36
1.8 蛇麻烷型倍半萜
蛇麻烷型倍半萜的结构中具有7/10双环环系。Ma等[64]研究表明化合物aquilanol A(H2)和aquilanol B(H3)可能是由前体12-hydroxyhumula-2,6,9-triene(H1)转化而来。目前已从沉香中分离鉴定出8个蛇麻烷型倍半萜类化合物,见图8、表8。
1.9 其他
此外,还有8个倍半萜类单体化合物因结构特异,不在前文总结的8类结构之列,大部分均从白木香中分离得到,见图9、表9。化合物1,5,9-trimethyl-1,5,9-cyclododecatriene(O6)[37]为单环倍半萜。化合物humulene diepoxide A(O2)[70]和kobusone(O3)[70]结构中含有活性部位三元氧环,化合物8,8a-dimethyl-1,7,8,8a-tetrahydro-naphthalene- 2,6-dione(O7)[24]结构中则含有2个羰基活性基团。同时,化合物caryophyllenol-II(O1)[70]、kobusone(O3)[70]和β-石竹烯(O5)[71]结构中具有罕见的4/9环系。
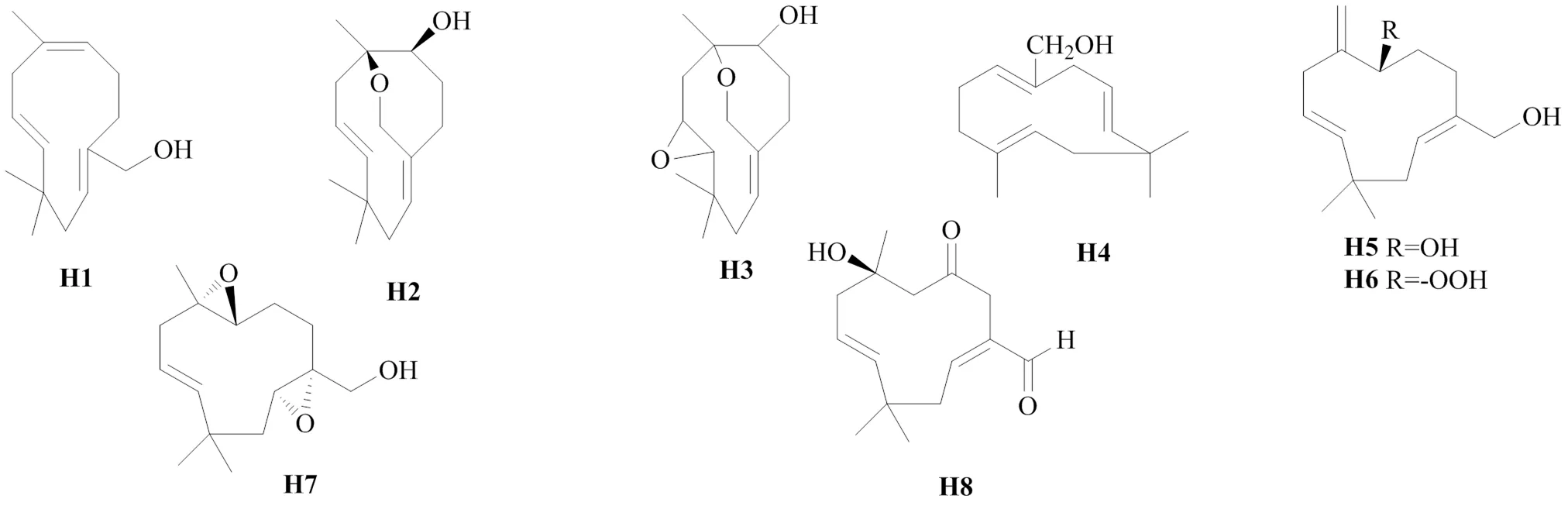
图8 沉香中蛇麻烷型倍半萜类化合物的化学结构
表8 沉香中的蛇麻烷型倍半萜类化合物
Table 8 Humulane-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 H112-hydroxyhumula-2Z,6E,9E-triene 马来沉香64 H2aquilanol A马来沉香64 H3aquilanol B马来沉香64 H414-hydroxy-α-humulene白木香38 H5(6R)-6-hydroxy-humula-2E,9E,7(13)-trien-12-ol马来沉香67 H6(6R)-6-hydroperoxyl-humula-2E,9E,7(13)-trien-12-ol马来沉香67 H72,3,6,7-diepoxy-9E-humulen-12-ol马来沉香67 H8(7R)-12-formyl-7β-hydroxy-humula-2Z,9E-dien-5-one马来沉香67
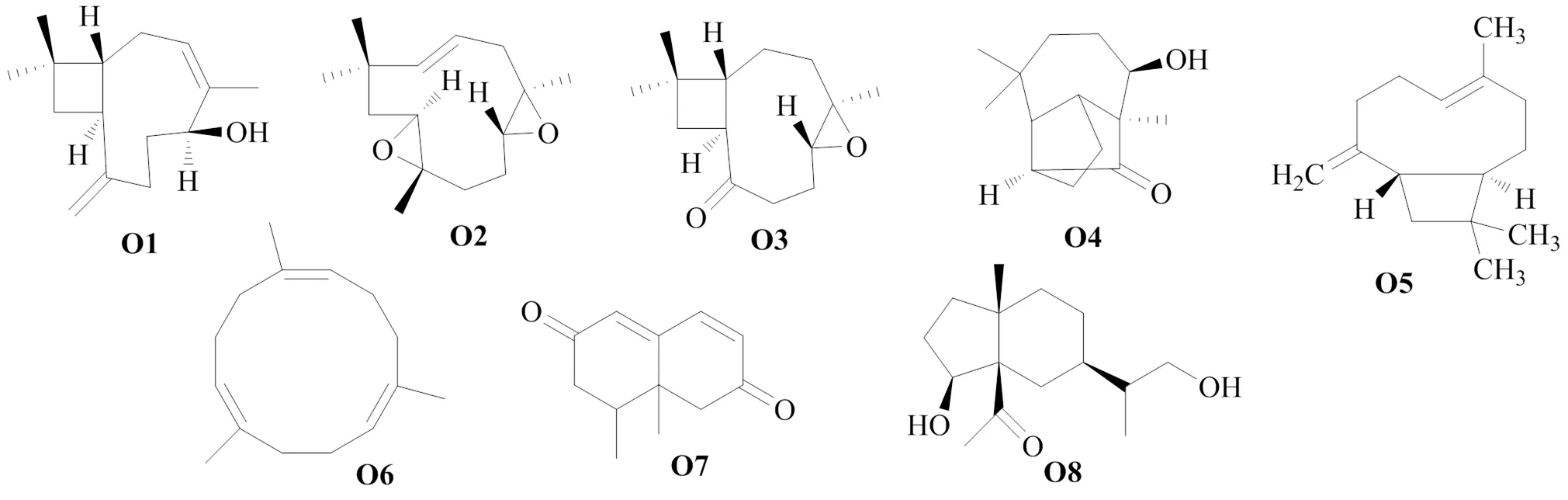
图9 沉香中其他倍半萜类化合物的化学结构
表9 沉香中的其他倍半萜类化合物
Table 9 Other-type sesquiterpenes in Aquilariae Lignum Resinatum
编号化合物名称来源文献 O1caryophyllenol-Ⅱ白木香70 O2humulene diepoxide A 白木香70 O3kobusone 白木香70 O4(+)-8β-hydroxy-longicamphenylone白木香68 O5β-石竹烯柯拉斯那沉香71 O61,5,9-trimethyl-1,5,9-cyclododecatriene白木香35 O78,8a-dimethyl-1,7,8,8a-tetrahydro-naphthalene-2,6-dione白木香24 O812-hydroxy-dihydrocyperolone 柳叶拟沉香61
2 生物活性
2.1 调节中枢神经系统
历代本草记载沉香有清人神、益气和神等功效。现代药理研究发现,沉香挥发油吸入给药[72-73]或ip给药[74-75]均有一定的镇静安神作用。Wang等[76]通过对小鼠脑内神经递质水平的检测,表明了沉香精油发挥镇静安神作用是通过增强A型γ-氨基丁酸受体实现的。接着,其使用一系列动物行为测试对束缚应激诱导的小鼠模型进行进一步研究,发现沉香精油发挥抗焦虑和抗抑郁作用与抑制促肾上腺皮质激素释放因子基因表达和下丘脑-垂体-肾上腺轴的过度活跃有关[77]。沉香精油是多种化学成分的复杂混合物,其有效的中枢神经系统活性成分值得进一步研究和寻找。
中国医学科学院药物研究所药理室[75]研究发现sc α-沉香呋喃(A4)50 mg/kg有显著延长戊巴比妥钠睡眠时间的作用,ip α-沉香呋喃40 mg/kg有加强士的宁惊厥效应的作用,ip α-沉香呋喃25 mg/kg有较轻度抑制小鼠自主活动的效应。Ueda等[43]从越南沉香的醇提取物中分离到的螺旋烷型倍半萜(4,5,7)-1(10)-spirovetiven-11-ol-2-one(B11)对大鼠培养的神经元细胞中脑源性神经营养因子mRNA表达具有显著诱导作用。jinkoh-eremol(E12)和沉香螺旋醇(B5)也具有一定的镇静作用[34,78],可抑制小鼠自主活动、协同戊巴比妥钠延长小鼠睡眠时间和抑制乙酸诱发的小鼠扭体反应,另外,其通过抑制多巴胺D2与[3]-raclopride结合和5-羟色胺受体与[3]-ketanserin结合而发挥中枢神经系统抑制作用的活性与氯丙嗪作用相似[79]。(+)-8β-hydroxy-longicamphenylone(O3)和11β-hydroxy-13-isopropyl-dihydrodehydrocostus lactone(G24)则可通过抑制大鼠脑突触体中的[3]-5-羟色胺再摄取,在体外表现出有效的抗抑郁活性[68]。此外,因乙酰胆碱酯酶抑制剂被认为是对抗阿尔茨海默病的潜在治疗剂,近年来许多研究筛选了沉香中的倍半萜类单体化合物对乙酰胆碱酯酶的抑制活性[35,37,44,46-48,53,55,58,66]。
2.2 抗炎
沉香传统上可用于治疗炎症性疾病,包括关节痛、风湿病、关节炎和哮喘等症[80]。一氧化氮(nitric oxide,NO)是炎症的介体,在炎症过程中起着至关重要的作用,NO释放抑制剂被认为是各种炎症相关疾病的治疗剂。采用小鼠单核巨噬细胞RAW264.7建立的体外抗炎活性筛选模型,发现白木香醇(A8)、petafolia A(C51)、1α,7α-dihydroxy-8oxo-4α,5α-guaia-9(10),11(13)-dien-12-oate(G25)等一些倍半萜类单体化合物对RAW264.7巨噬细胞中脂多糖诱导的NO释放有抑制作用[27,54,67,81]。Wang等[60]研究表明二氢卡拉酮(E6)在RAW264.7/Luc-P1细胞系中可抑制核因子-κB活化,但在RAW264.7巨噬细胞中对脂多糖诱导的NO释放没有抑制作用。
2.3 抗肿瘤
Dahham等[71]从柯拉斯那沉香中分离得到的β-石竹烯(O11)对人结肠癌细胞HCT116的增殖、迁移、侵袭和球状体形成具有有效的抑制作用。另外,通过对胰腺癌PANC-1细胞、结肠癌HT-29细胞、浸润性鳞状癌ME-180细胞、前列腺癌PC3细胞、白血病癌K562细胞、浸润性乳腺癌MCF-7细胞、人慢性髓原白血病K562细胞株和人肝癌BEL-7402细胞系等测试,发现(4,5)-3-oxo-5,6-dihydro-gweicurculactone(G36)[69]、1(5)-ene-7,10-epoxy-guaia-12-one(G30)[69]、1,8-epoxy-5-guaia-9-en-12,8-olide(G31)[69]和(rel)-4β,5β,7β-eremophil-9-en-12,8α-olide(E28)[61]也具有较弱的细胞毒活性。
2.4 抑菌
采用滤纸片琼脂法评估了来自白木香和柯拉斯那沉香的多个倍半萜类单体化合物对金黄色葡萄球菌和青枯雷尔氏菌的抑制活性,发现其抑菌效果均优于硫酸卡那霉素[35,37,46,47]。Dahham等[71]研究表明,β-石竹烯(O5)可显著抑制蜡状芽孢杆菌MTCC1307、枯草芽孢杆菌MTCC6910、大肠杆菌MTCC732、肺炎克雷伯菌MTCC7028、金黄色葡萄球菌MTCC7405和铜绿假单胞菌MTCC4302等6种致病菌的生长繁殖。而(+)-4a,5-dimethyl-3-(prop-1-en-2yl)-octahydronaphthalene-2β,8a-diol(E38)[28]和3-isopropenyl-4a,5-dimethyl-octahydro-naphthalene-2,8a- diol(C5)[24]则对耐药金黄色葡萄球菌具有一定的抑制作用。
2.5 抗葡萄糖苷酶
α-葡萄糖苷酶是治疗2型糖尿病的靶标,沉香中分离到的倍半萜类单体化合物jinkohol(F6)、jinkohol II(F7)、agarozizanol E(F20)、-khusenol(F22)、aquilarene D(F14)、aquilarene E(F15)、eudesma-4-en-8,11-diol(C14)、2-oxoguaia-1(10),3,5,7(11),8-pentaen-12,8-olide(G40)被证明具有显著的抗葡糖苷酶活性,分析这些化合物的结构类型发现,多数为具有三环结构的前香草烷型倍半萜。
2.6 其他
Dahham等[71]通过2,2-联苯基-1-苦基肼基和铁还原抗氧化能力清除测定法评估柯拉斯那沉香沉香精油中的β-石竹烯(O5)和白木香人工打洞沉香中的2-oxo-12-hydroxy-hinesol(B12)[44],发现两者均有较强的抗氧化活性。艾里莫酚烷型倍半萜(+)--nootkatol(E36)[82]则具有一定的抗胃溃疡活性。
3 Q-Marker预测分析
为更好地评价沉香质量,依据刘昌孝院士提出的Q-Marker[7]的概念及基本条件,对沉香Q-Marker进行预测分析。
3.1 基于植物亲缘学及化学成分特有性的Q-Marker预测分析
当前对沉香化学成分的研究主要集中在白木香马来沉香柯拉斯那沉香丝沉香和柳叶拟沉香,其主要分布于中国、伊朗、孟加拉国、不丹、东南亚等地[1]。而Lee等[83]考证认为和为同一物种,本文亦将中分离到的倍半萜类化合物纳入马来沉香。Ishihara等[84]发现马来沉香富含氧化愈创木烷型和桉烷型倍半萜,而白木香则富含氧化螺旋烷型倍半萜,并对倍半萜的生物合成途径进行了推测。本文对不同类型倍半萜生物合成途径进行归纳,见图10,倍半萜类化合物生源途径为甲戊二羟酸途径,先由乙酰辅酶A反应生成焦磷酸异戊烯酯,后进一步合成焦磷酸香叶酯、焦磷酸金合欢酯,焦磷酸金合欢酯在倍半萜环化酶催化作用下合成倍半萜,先经双键断裂缩合形成germacryl阳离子和humulyl阳离子[64,85],再经过不同程度的氧化、双键转位形成呋喃型、螺旋烷型、艾里莫酚烷型、桉烷型、愈创木烷型和蛇麻烷型的倍半萜。
3.2 基于传统药效的Q-Marker预测分析
传统功效是对中药有效性的概括,也是临床用药的主要依据。《本草纲目》记载沉香:“治上热下寒,气逆喘急,大肠虚闭,心神不足,胃寒久呃”。《本草原始》记载:“沉香补右肾命门,补脾胃,益气和神”。《海药本草》记载沉香:“主心腹痛,霍乱、驱恶邪、清人神”。现代药理研究表明沉香中倍半萜类单体化合物具有广泛的药效活性,“治心神不足”“益气和神”“清人神”即体现在沉香中的倍半萜类化合物对中枢神经系统的调节作用。据此推测,沉香中倍半萜类化合物是沉香传统功效的主要药效物质基础,可以作为沉香Q-Marker筛选的重要依据。
3.3 基于传统药性的Q-Marker预测分析
中药药性理论为中医药理论体系中的重要组成部分,中药的性味和归经影响病症治法和遣药组方,因此也应作为Q-Marker确定的依据之一。沉香性辛、苦,微温,归脾、胃、肾经。对辛味中药化学成分进行分析发现[86-87],辛味药的化学成分多以挥发油和萜类为主。张静雅等[88]认为苦味中药的化学成分大多包括生物碱、挥发油及苦味素等,苦温药以挥发油为主要成分。另外杨文国等[89]对辛味中药挥发油的“四气”药性和化学成分关联性的考察表明挥发油中倍半萜类成分是和“四气”药性相关性最大的化学成分。据此可认为沉香挥发油中倍半萜类化合物是其性味“辛、苦,微温”的主要物质基础,在药性方面起决定作用,应将其作为沉香Q-Marker选择的重要参考依据。
3.4 基于化学成分可测性的Q-Marker预测分析
沉香化学成分受其基原、结香方式和结香时间等影响[90],且不同品质沉香的主要倍半萜类化合物存在差异[91-92]。因此,分析沉香化学成分可用于沉香基原和产地鉴别以及品质评价。β-沉香呋喃(A3)、α-沉香呋喃(A4)、10--γ-eudesmol和γ-桉叶醇为沉香精油的特征成分[93-95]。Jia等[96]研究则结合Fisher和Bayes判别分析得到26个挥发性成分可区分惠安系沉香和星洲系沉香。Jalil等[97]研究发现柯拉斯那沉香、白木香和近全缘沉香所产沉香中的β-沉香呋喃(A3)、α-桉叶醇和沉香螺旋醇(B5)含量存在差异。可见,倍半萜类化合物与沉香的来源及品质密切相关。
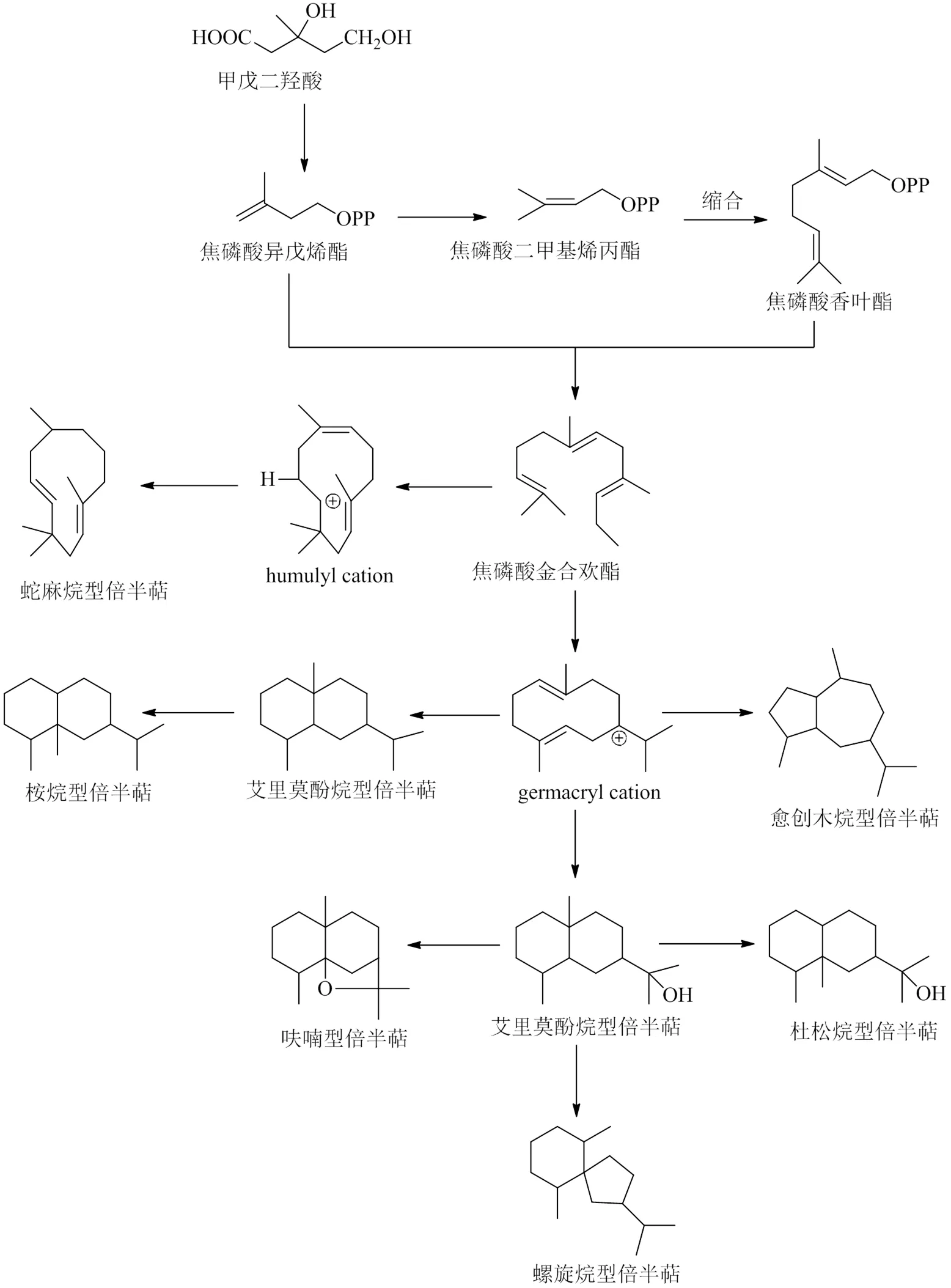
图10 沉香中倍半萜类化合物的生物合成途径
此外,化学成分可测性也是Q-Marker选择的重要依据,沉香挥发性成分的测定通常结合气相色谱-质谱联用(GC-MS)分析技术,传统的一维色谱在分辨率、灵敏度、峰容量等方面都受到限制,全二维气相色谱-飞行时间质谱(GC×GC-TOFMS)技术则可实现对复杂物质体系更准确的分离、检测及结构鉴定[98]。Tajuddin等[99]应用GC×GC-TOFMS技术从马来沉香精油中共鉴定出300多种化合物。Wong等[100]则应用该技术研究马来沉香精油的质量分级。
沉香倍半萜类化合物是沉香Q-Marker的重要选择,但是具有特异性及活性的化学成分通常含量低、难分离,因此,仍需进一步深入研究。
4 结语及展望
沉香药用历史悠久,倍半萜类化合物丰富多样,具有中枢神经系统、抗炎、抑菌、抗肿瘤等活性,对糖尿病、阿尔茨海默病等疾病有潜在的治疗作用。本文在对沉香中倍半萜类化合物及其生物活性系统总结的基础上,以中药Q-Marker的理论为指导,根据沉香化学成分、传统药效、传统药性相关证据,并结合倍半萜类成分的生源途径进行分析,详细的阐明了沉香药效可能的物质基础。并依据存在于中药材中,并与功效相关的化学物质;具有明确化学结构的物质;可以进行定性鉴别和定量测定的物质;遵循组方配伍,以君药为主,臣、佐、使药兼顾的原则的代表性物质等几个原则[7,101],预测沉香中呋喃型倍半萜β-沉香呋喃(A3)、α-沉香呋喃(A4)和螺旋烷型倍半萜沉香螺旋醇(B5)均可考虑作为沉香药材潜在的中药Q-Marker。
本文对沉香药材Q-Marker进行预测分析,可为沉香临床应用的安全性和有效性提供科学借鉴,为沉香的深入研究提供合理依据。随着研究的推进和分析技术的进步,可能会有更多的化学成分被选中为Q-Marker。
利益冲突 所有作者均声明不存在利益冲突
[1] 中华人民共和国濒危物种进出口管理办公室中华人民共和国濒危物种科学委员会. 濒危野生动植物种国际贸易公约附录Ⅱ [S]. 2017: 43.
[2] 刘凡. 丁谓《天香传》与海南沉香论述 [J]. 南海学刊, 2019, 5(2): 109-114.
[3] 梁·陶弘景. 名医别录 [M]. 北京: 人民卫生出版社, 1986: 64.
[4] 中国药典 [S]. 一部. 2020: 193.
[5] Petronilho S, Coimbra M A, Rocha S M. A critical review on extraction techniques and gas chromatography based determination of grapevine derived sesquiterpenes [J]., 2014, 846: 8-35.
[6] Jain T C, Bhattacharyya S C. Structure, stereochemistry and absolute configuration of agarol, a new sesquiterpene alcohol from agarwood oil [J]., 1959, 1(9): 13-17.
[7] 刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker): 中药产品质量控制的新概念 [J]. 中草药, 2016, 47(9): 1443-1457.
[8] 肖治均, 刘传鑫, 杨欣欣, 等. 雷公藤研究进展及其质量标志物的预测分析 [J]. 中草药, 2019, 50(19): 4752-4768.
[9] 董玉洁, 蒋沅岐, 刘毅, 等. 决明子的化学成分、药理作用及质量标志物预测分析[J]. 中草药, 2021, 52(9): 2719-2732.
[10] 刘耀晨, 张铁军, 郭海彪, 等. 三七的研究进展及其质量标志物预测分析[J]. 中草药, 2021, 52(9): 2733-2745.
[11] 冯慧敏, 李成义, 何军刚, 等. 红芪化学成分和药理作用研究进展及质量标志物(Q-Marker)的预测分析[J]. 中草药, 2021, 52(9): 2831-2842.
[12] 董嘉琪, 陈金鹏, 龚苏晓, 等. 山楂的化学成分、药理作用及质量标志物(Q-Marker)预测[J]. 中草药, 2021, 52(9): 2801-2818.
[13] Gao M, Han X M, Sun Y,. Overview of sesquiterpenes and chromones of agarwood originating from four main species of the genus[J]., 2019, 9(8): 4113-4130.
[14] Chen H Q, Wei J H, Yang J S,. Chemical constituents of agarwood originating from the endemic genusplants [J]., 2012, 9(2): 236-250.
[15] Li W, Chen H Q, Wang H,. Natural products in agarwood andplants: Chemistry, biological activities and biosynthesis [J]., 2021, 38(3): 528-565.
[16] Kalra R, Kaushik N. A review of chemistry, quality and analysis of infected agarwood tree (sp.) [J]., 2017, 16(5): 1045-1079.
[17] 杨峻山, 陈玉武. 国产沉香化学成分的研究II.白木香醇和去氢白木香醇的分离和结构 [J]. 药学学报, 1986, 21(7): 516-520.
[18] Guo J Y, Wang W J, Fang H J,. Novel agarofuan derivatives, their preparation, pharmaceutical composition containing them and their use as medicine: China, EP1132383 B1 [P]. 2010-05-26.
[19] Guo J Y, Wang W J, Fang H J,. Agarofuan derivatives, their preparation, pharmaceutical composition containing them and their use as medicine: China, US6486201 [P]. 2002-11-26.
[20] Guo J Y, Wang W, Zhang W,. New agarofuran derivatives, their preparations, pharmaceutical compositions containing them and their uses as medicaments: China, AU8748901 [P]. 2002-02-18.
[21] Maheshwari M L, Jain T C, Bates R B, et al. Terpenoids-XLI: Structure and absolute configuration of α-agarofuran, β-agarofuran and dihydroagarofuran [J]., 1963, 19(6): 1079-1090.
[22] Maheshwari M L, Varma K R, Bhattacharyya S C. Terpenoids-XLVII: Structure and absolute configuration of norketoagarofuran, 4-hydroxydihydroagarofuran, 3,4-dihydroxydihydroagarofuran and conversion of β-agarofuran to α-agarofuran [J]., 1963, 19(10): 1519-1525.
[23] Nät R, Velluz A, Thommen W, et al. New compounds identified in agarwood (Roxb.) [J]., 1993, 8(6): 307-313.
[24] 雷智东. 沉香抗菌活性成分的研究 [D]. 广州: 广东药学院, 2015.
[25] 徐金富, 朱亮峰, 陆碧瑶, 等. 中国沉香精油化学成分研究 [J]. 植物学报, 1988, 30(6): 635-638.
[26] Nakanishi T, Yamagata E, Yoneda K,. Three fragrant sesquiterpenes of agarwood [J]., 1984, 23(9): 2066-2067.
[27] 余章昕, 王灿红, 陈德力, 等. 通体结香技术产沉香的倍半萜及其抗炎活性研究 [J]. 中国中药杂志, 2019, 44(19): 4196-4202.
[28] 吕开原, 雷智冬, 刘元瑞, 等. 沉香的倍半萜类化学成分研究 [J]. 中草药, 2020, 51(9): 2390-2394.
[29] Yang J S. Baimuxifuranic acid, a new sesquiterpene from the volatile oil of(Lour.) Gilg. [J]., 1992, 3(12): 983-984.
[30] Yang D L, Wang H, Guo Z K,. Fragrant agarofuran and eremophilane sesquiterpenes in agarwood ‘Qi-Nan’ from[J]., 2014, 8: 121-125.
[31] Pripdeevech P, Khummueng W, Park S K. Identification of odor-active components of agarwood essential oils from Thailand by solid phase microextraction-GC/MS and GC-O [J]., 2011, 23(4): 46-53.
[32] Varma K R, Maheshwari M L, Bhatta-Charyya S C. Terpenoids-LXII: The constitution of agarospirol, a sesquiterpenoid with a new skeleton [J]., 1965, 21(1): 115-138.
[33] 杨峻山, 陈玉武. 国产沉香化学成分的研究-Ⅰ. 白木香酸和白木香醛的分离和结构测定[J]. 药学学报, 1983, 18(3): 191-198.
[34] Okugawa H, Ueda R, Matsumoto K,. Effect of jinkoh-eremol and agarospirol from agarwood on the central nervous system in mice [J]., 1996, 62(1): 2-6.
[35] 李薇. 白木香与人工打洞沉香的化学成分与生物活性研究 [D]. 海口: 海南大学, 2014.
[36] Yang D L, Wang J, Li W,. New guaiane and acorane sesquiterpenes in high quality agarwood “Qi-Nan” from[J]., 2016, 17: 94-99.
[37] Li W, Liao G, Dong W H,. Sesquiterpenoids from Chinese agarwood induced by artificial holing [J]., 2016, 21(3): 274.
[38] Huo H X, Zhu Z X, Pang D R,. Anti-neuroinflammatory sesquiterpenes from Chinese eaglewood [J]., 2015, 106: 115-121.
[39] Niif R, Velluz A, Brauchli R,. Agarwood oil (Roxb.). Its composition and eight new valencane-, eremophilane- and vetispirane- derivatives [J]., 1995, 10(3): 147-152.
[40] Nakanishi T, Yamagata E, Yoneda K,. Jinkohol, a prezizane sesquiterpene alcohol from agarwood [J]., 1981, 20(7): 1597-1599.
[41] Nakanishi T, Yamagata E, Yoneda K,. Jinkoh-eremol and jinkohol II, two new sesquiterpene alcohols from agarwood [J]., 1983, 1(3): 601.
[42] Tian H, Wang H, Yang L,. Two new sesquiterpenoids from agarwood originated fromsp. [J]., 2020, 22(7): 626-631.
[43] Ueda J Y, Imamura L, Tezuka Y,. New sesquiterpene from Vietnamese agarwood and its induction effect on brain-derived neurotrophic factor mRNA expression[J]., 2006, 14(10): 3571-3574.
[44] 向盼, 曾艳波, 梅文莉, 等. 人工打洞沉香的化学成分及生物活性研究 [J]. 中药材, 2017, 40(10): 2339-2343.
[45] Näf R, Velluz A, Busset N,. New Nor-sesquiterpenoids with 10--eudesmane skeleton from agarwood (Roxb.) [J]., 1992, 7(6): 295-298.
[46] Li W, Cai C H, Guo Z K,. Five new eudesmane-type sesquiterpenoids from Chinese agarwood induced by artificial holing [J]., 2015, 100: 44-49.
[47] Wang H N, Dong W H, Huang S Z,. Three new sesquiterpenoids from agarwood of[J]., 2016, 114: 7-11.
[48] 康科星, 戴好富, 王佩, 等. 柯拉斯那沉香的倍半萜类化学成分研究 [J]. 中草药, 2017, 48(22): 4601-4607.
[49] Wu B, Lee J G, Lim C J,. Sesquiterpenoids and 2-(2-phenylethyl)-4-chromen-4-one (=2-(2-phenylethyl)-4H-1-benzopyran-4-one) derivatives fromagarwood [J]., 2012, 95(4): 636-642.
[50] Ishihara M, Tsuneya T, Shiga M,. Three sesquiterpenes from agarwood [J]., 1991, 30(2): 563-566.
[51] 邝彤东, 陈惠琴, 李薇, 等. 人工打洞沉香中1个新的倍半萜 [J]. 中国中药杂志, 2017, 42(23): 4618-4623.
[52] Ishihara M, Tsuneya T, Uneyama K. Fragrant sesquiterpenes from agarwood [J]., 1993, 33(5): 1147-1155.
[53] Shao H, Mei W L, Kong F D,. Sesquiterpenes of agarwood from[J]., 2016, 113: 182-187.
[54] Zhao H, Peng Q, Han Z,. Three new sesquiterpenoids and one new sesquiterpenoid derivative from Chinese eaglewood [J]., 2016, 21(3): 281.
[55] Li W, Yang Y L, Yang L,. New sesquiterpenoids bearing 11-methyl ester group of agarwood [J]., 2020, 143: 104557.
[56] Babaei G, Aliarab A, Abroon S,. Application of sesquiterpene lactone: A new promising way for cancer therapy based on anticancer activity [J]., 2018, 106: 239-246.
[57] Pant P, Rastogi R P. Agarol, a new sesquiterpene from[J]., 1980, 19(8): 1869-1870.
[58] 李薇, 梅文莉, 董文化, 等. 国产绿奇楠沉香的化学成分研究 [J]. 热带亚热带植物学报, 2019, 27(2): 196-202.
[59] Ma C T, Cho E, Nguyen H T,. Malacinones A and B, two novel sesquiterpenoids with 6/6/5 tricyclic ring system from the agarwood of[J]., 2020, 61(1): 151355.
[60] Wang S L, Tsai Y C, Fu S L,. 2-(2-phenylethyl)-4-chromen-4-one derivatives from the resinous wood ofwith anti-inflammatory effects in LPS-induced macrophages [J]., 2018, 23(2): 289.
[61] 陈惠琴, 郭丰娟, 蔡彩虹, 等. 柳叶拟沉香中倍半萜类化合物的研究 [J]. 中国中药杂志, 2019, 44(11): 2274-2277.
[62] Yang L, Yang Y L, Dong W H,. Sesquiterpenoids and 2-(2-phenylethyl)chromones respectively acting as α-glucosidase and tyrosinase inhibitors from agarwood of anplant [J]., 2019, 34(1): 853-862.
[63] Yang Y L, Li W, Wang H,. New tricyclic prezizaane sesquiterpenoids from agarwood [J]., 2019, 138: 104301.
[64] Ma C T, Eom T, Cho E,. Aquilanols A and B, macrocyclic humulene-type sesquiterpenoids from the agarwood of[J]., 2017, 80(11): 3043-3048.
[65] Ishihara M, Tsuneya T, Uneyama K. Guaiane sesquiterpenes from agarwood [J]., 1991, 30(10): 3343-3347.
[66] Yang D L, Li W, Dong W H,. Five new 5, 11-epoxyguaiane sesquiterpenes in agarwood “Qi-Nan” from[J]., 2016, 112: 191-196.
[67] Ma C T, Ly T L, Le T H V,. Sesquiterpene derivatives from the agarwood ofand their anti-inflammatory effects on NO production of macrophage RAW 264.7 cells [J]., 2021, 183: 112630.
[68] Yang L, Qiao L R, Zhang J J,. Two new sesquiterpene derivatives from Chinese eaglewood [J]., 2012, 14(11): 1054-1058.
[69] Mi C N, Mei W L, Wang H,. Four new guaiane sesquiterpenoids from agarwood of[J]., 2019, 135: 79-84.
[70] 杨林, 乔立瑞, 谢丹, 等. 国产沉香中的倍半萜类和单萜类化学成分 [J]. 中国中药杂志, 2012, 37(13): 1973-1976.
[71] Dahham S S, Tabana Y M, Iqbal M A,. The anticancer, antioxidant and antimicrobial properties of the sesquiterpene β-caryophyllene from the essential oil of[J]., 2015, 20(7): 11808-11829.
[72] Takemoto H, Ito M, Shiraki T,. Sedative effects of vapor inhalation of agarwood oil and spikenard extract and identification of their active components [J]., 2008, 62(1): 41-46.
[73] Rahman H, Eswaraiah M C, Ramesh S,. Study of anxiolytic activity of some essential oils used by inhalational exposure in mice [J]., 2013, 1(1): 1-4.
[74] 王帅, 周岳, 马富超, 等. 通体沉香对小鼠催眠和自主活动抑制作用 [J]. 国际药学研究杂志, 2016, 43(6): 1082-1087.
[75] 中国医学科学院药物研究所. 中草药现代研究(五卷) [M]. 北京: 中国协和医科大学出版社, 2010: 3-5.
[76] Wang S, Wang C H, Peng D Q,. Agarwood essential oil displays sedative-hypnotic effects through the GABAergic system [J]., 2017, 22(12): 2190.
[77] Wang S, Wang C H, Yu Z X,. Agarwood essential oil ameliorates restrain stress-induced anxiety and depression by inhibiting HPA axis hyperactivity [J]., 2018, 19(11): 3468.
[78] Ueda J Y, Imamura L, Tezuka Y,. New sesquiterpene from Vietnamese agarwood and its induction effect on brain-derived neurotrophic factor mRNA expression[J]., 2006, 14(10): 3571-3574.
[79] Okugawa H, Ueda R, Matsumoto K,. Effects of agarwood extracts on the central nervous system in mice [J]., 1993, 59(1): 32-36.
[80] Hashim Y Z H Y, Kerr P G, Abbas P,.spp. (agarwood) as source of health beneficial compounds: A review of traditional use, phytochemistry and pharmacology [J]., 2016, 189: 331-360.
[81] 霍会霞. 沉香的化学成分研究 [D]. 北京: 北京中医药大学, 2016.
[82] Yamahara J, Li Y H, Tamai Y. Anti-ulcer effect in rats of bitter cardamon constituents [J]., 1990, 38(11): 3053-3054.
[83] Lee S Y, Mohamed R.[M]. Singapore: Springer Singapore, 2016: 1-20.
[84] Ishihara M, Tsuneya T, Uneyama K. Components of the volatile concentrate of agarwood [J]., 1993, 5(3): 283-289.
[85] Ito M, Okimoto K I, Yagura T,. Induction of sesquiterpenoid production by methyl jasmonate incell suspension culture [J]., 2005, 17(2): 175-180.
[86] 孙玉平, 张铁军, 曹煌, 等. 中药辛味药性表达及在临证配伍中的应用 [J]. 中草药, 2015, 46(6): 785-790.
[87] 周复辉, 易增兴, 罗亨凡. 辛味中药化学成分的分析 [J]. 安徽农业科学, 2006, 34(12): 2760,2782.
[88] 张静雅, 曹煌, 许浚, 等. 中药苦味药性表达及在临证配伍中的应用 [J]. 中草药, 2016, 47(2): 187-193.
[89] 杨文国, 朱学敏, 吴凤烨, 等. 基于逐步判别法分析辛味中药挥发油“四气”药性、透皮促渗能力和化学成分的关联因素 [J]. 中草药, 2019, 50(17): 4219-4224.
[90] 李远彬. 基于色谱联用技术的沉香标志性差异成分分析研究 [D]. 广州: 广州中医药大学, 2017.
[91] Ishihara M, Tsuneya T, Uneyama K. Components of the agarwood smoke on heating [J]., 1993, 5(4): 419-423.
[92] Ismail N, Ibrahim M, Zareen S,. Analysis of aroma profile of agarwood incense smoke by SPME and GC-FID combined with GC-MS [J]., 2016, 15(3/4): 101-108.
[93] Ismail N, Rahiman M H F, Taib M N,. Analysis of chemical compounds of agarwood oil based on headspace-solid phase microextraction combined with gas chromatography mass-spectrometry [A] // 2013 IEEE 9th International Colloquium on Signal Processing and its Applications [C]. Kuala Lumpur: IEEE, 2013: 215-218.
[94] Ismail N, Ali N A M, Jamil M,. Major volatile chemical compounds of agarwood oils from Malaysia based on Z-score technique [J]., 2015, 51(4): 776-779.
[95] Ismail N, Jamil M. Analysis of high quality agarwood oil chemical compounds by means of SPME/GC-MS and Z-score technique [J]., 2013, 17(3): 403-413.
[96] Jia D Y, Yi S L. Classification of hoi-an and sin-chew agarwood by components analysis of VOCs released in heat-treated agarwood using TD-GCMS and chemometric methods [J]., 2018, 13(2): 2916-2931.
[97] Jalil M, Hamid H A, Tahir P M,. Determination of Agarwood volatile compounds from selectedspecies plantation extracted by Headspace-Solid Phase Microextraction (HS-SPME) method [J]., 2018, 368: 012023.
[98] Chin S T, Marriott P J. Multidimensional gas chromatography beyond simple volatiles separation [J]., 2014, 50(64): 8819.
[99] Tajuddin S N, Muhamad N S, Yarmo M A,. Characterization of the chemical constituents of agarwood oils from Malaysia by comprehensive two-dimensional gas chromatography-time-of-flight mass spectrometry [J]., 2013, 23(1): 51-52.
[100] Wong Y F, Chin S T, Perlmutter P,. Evaluation of comprehensive two-dimensional gas chromatography with accurate mass time-of-flight mass spectrometry for the metabolic profiling of plant-fungus interaction in[J]., 2015, 1387: 104-115.
[101] 管鑫, 李若诗, 段宝忠, 等. 重楼属植物化学成分、药理作用研究进展及质量标志物预测分析 [J]. 中草药, 2019, 50(19): 4838-4852.
Research progress on sesquiterpenoids inand their biological activities and predictive analysis on quality marker
WANG Yun-yun1, 2, HOU Wen-cheng2, WEI Jian-he1, 2, LIU Yang-yang1, 2
1. Key Laboratory of Bioactive Substances and Resources Utilization of Chinese Herbal Medicine, Ministry of Education & National Engineering Laboratory for Breeding of Endangered Medicinal Materials, Institute of Medicinal Plant Development, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100193, China 2. Hainan Provincial Key Laboratory of Resources Conservation and Development of Southern Medicine & Key Laboratory of State Administration of Traditional Chinese Medicine for Agarwood Sustainable Utilization, Hainan Branch of the Institute of Medicinal Plant Development, Chinese Academy of Medical Sciences and Peking Union Medical College, Haikou 570311, China
Chenxiang () is a precious medicinal material and spice. Sesquiterpenoids are the characteristic components and main active ingredients of it. According to their molecular skeleton, the sesquiterpenoids contained incould be divided into eight categories. Sesquiterpenoids isolated fromand research status of central nervous system activity, anti-tumor cytotoxic activity, antibacterial activity, anti-inflammatory activity and other biological activities were reviewed in this paper. And on the basis of the above, combined with the core concept of quality marker (Q-Marker), Q-Markers ofwerepredicted and analyzed and analyzed from the aspects of biogenic pathway, traditional medicine, traditional properties, and chemical composition. α-Agarofuran, β-agarofuran, and agarospirol can be used as the main Q-Markers of, which provide a basis for establishing and improving the quality standards ofand for further research and development of.
; Q-Marker; sesquiterpenoid; β-agarofuran; α-agarofuran; agarospirol
R282.710.5
A
0253 - 2670(2022)04 - 1191 - 19
10.7501/j.issn.0253-2670.2022.04.028
2021-05-19
国家重点研发计划项目(2018YFC1706403);海南省重点研发计划项目(ZDYF2020111)
王云云(1996—),女,硕士研究生,研究方向为中药质量分析。E-mail: cloud22wang@163.com
刘洋洋(1985—),男,副研究员,硕士生导师,研究方向为中药质量控制技术及其应用。E-mail: eadchris@163.com
[责任编辑 崔艳丽]
