咳嗽变异性哮喘患者疗效与布地奈德福莫特罗疗程的相关性研究
2022-02-22刘威威苏玉峰王欢李敏吴旭兰陈晓香
刘威威,苏玉峰,王欢,李敏,吴旭兰,陈晓香
咳嗽变异性哮喘(cough variant asthma,CVA)是一种特殊类型的哮喘,初期以咳嗽症状为主,随着病情持续进展,出现了一系列与哮喘类似的病理变化,若未给予有效干预,则可进展为典型哮喘[1],临床常采用吸入性激素、β2-受体激动剂、白三烯受体拮抗剂等药物来抑制炎症反应及过敏递质释放,从而缓解患者的临床症状[2]。布地奈德福莫特罗是吸入性激素与支气管舒张剂的复合制剂,吸入用药使用便捷,且安全、有效[3]。有研究认为,CVA的治疗疗程不应短于8周[4]。现有研究表明,布地奈德福莫特罗疗程是影响CVA疗效及预后的独立影响因素[5]。基于此,本研究旨在探讨布地奈德福莫特罗疗程与CVA疗效的关系,以期为临床用药提供参考,现报道如下。
1 资料与方法
1.1 一般资料 选取廊坊市人民医院门诊2018年8月至2020年3月收治的CVA患者200例,均符合中华医学会制定的《咳嗽的诊断与治疗指南(2015)》[6]中的CVA诊断标准,并经临床症状及体征、实验室及肺功能检查确诊,且年龄≥18岁。排除标准:(1)急性肺炎、肺结核、肺脓肿、气胸及其他肺部疾病者;(2)合并其他脏器危重症,或昏迷、休克、意识障碍致无法交流者;(3)入组前4周口服糖皮质激素、抗胆碱类药物、β2-肾上腺素能受体激动剂治疗者;(4)对本研究药物有成瘾史或戒断史者。按照随机数字表法将所有患者分为A组56例、B组69例和C组75例。A组中男26例,女30例;年龄22~75岁,平均(38.9±7.8)岁;病程9~59周,平均(15.8±4.6)周。B组中男34例,女35例;年龄21~78岁,平均(41.3±6.5)岁;病程9~68周,平均(17.8±4.0)周。C组中男38例,女37例;年龄23~71岁,平均(41.8±8.7)岁;病程9~72周,平均(16.8±5.4)周。三组患者性别(χ2=0.784,P=0.215)、年龄(F=1.256,P=0.087)、病程(F=1.089,P=0.096)比较,差异无统计学意义。本研究经廊坊市人民医院医学伦理委员会审核批准,患者及家属对本研究知情并签署知情同意书。
1.2 治疗方法 所有患者予以常规治疗,如予以茶碱缓释片、西替利嗪片、丙卡特罗片等进行对症治疗,待病情缓解后采用布地奈德福莫特罗粉吸入剂(AstraZeneca AB公司生产,批准文号:注册证号H20140458,规格:160 μg/4.5 μg/吸)吸入治疗,1吸/次,2次/d,其中A组疗程为8周、B组疗程为16周、C组疗程为24周。
1.3 观察指标 (1)应用森迪斯肺功能仪检测三组患者治疗前后肺通气功能指标,包括用力肺活量(forced vital capacity,FVC)、第1秒用力呼气容积(forced expiratory volume in one second,FEVl)、呼气流量峰值(peak expiratory flow,PEF)。(2)比较三组患者治疗前后气道炎症指标,包括白介素(interleukin,IL)-10、IL-5,具体操作为:将负压吸痰管插入至患者气道深部,而后将痰液吸入无菌试管中,按照操作规范制备痰标本,取痰液黏稠的部分置入小试管中,加入二硫苏糖醇充分混匀,3 000 r/min离心10 min(离心半径10 cm),取上层痰液。应用酶标仪采用酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)检测IL-10、IL-5水平。人IL-10试剂盒是由美国阿迪公司生产,人IL-5试剂盒由上海晶抗生物工程有限公司生产,具体操作严格按照试剂盒说明书进行。(3)比较三组患者治疗前后血嗜酸粒细胞计数(eosinophil,EOS)及血清免疫球蛋白E(immunoglobulin E,IgE)水平,具体操作为:抽取患者血液标本10 ml并置于抗凝管中,其中5 ml血样,应用日本希森美康XT-4000i全自动五分类血细胞分析仪检测血EOS;另外5 ml血样,采用ELISA检测血清IgE水平。(4)比较三组患者治疗前后哮喘控制测试(asthma control test,ACT)评分,该测试包含5个问题,每个问题评分范围为1~5分,评分≥25分为完全控制、20~24分为控制良好、<20分为未控制。
1.4 统计学方法 应用SPSS 17.0统计学软件进行数据处理。计量资料以(±s)表示,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验;计数资料以相对数表示,组间比较采用χ2检验;指标间的相关性分析采用Spearman秩相关分析。以P<0.05为差异有统计学意义。
2 结果
2.1 肺通气功能指标 三组患者治疗前FVC、FEV1、PEF比较,差异无统计学意义(P>0.05)。三组患者治疗后FVC、FEV1、PEF比较,差异有统计学意义(P<0.05);其中B、C组患者治疗后FVC、FEV1、PEF高于A组,C组患者治疗后FVC、FEV1、PEF高于B组,差异有统计学意义(P<0.05),见表1。
表1 三组患者治疗前后FVC、FEV1、PEF比较(±s)Table 1 Comparison of FVC,FEV1,PEF before after treatment among the three groups
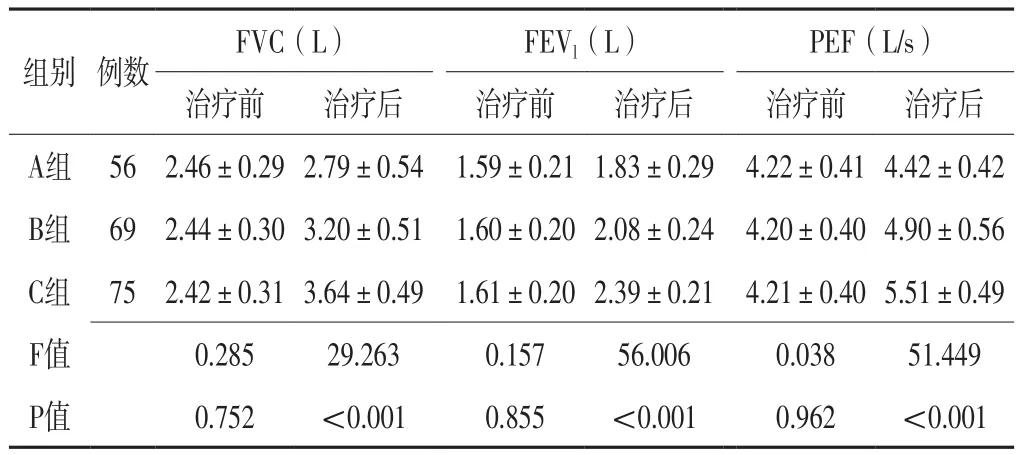
表1 三组患者治疗前后FVC、FEV1、PEF比较(±s)Table 1 Comparison of FVC,FEV1,PEF before after treatment among the three groups
注:A组患者疗程为8周,B组患者疗程为16周,C组患者疗程为24周;a表示与A组比较,P<0.05;b表示与B组比较,P<0.05;FVC=用力肺活量,FEV1=第1秒用力呼气容积,PEF=呼气流量峰值
组别 例数FVC(L) FEVl(L) PEF(L/s)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后A组 56 2.46±0.29 2.79±0.54 1.59±0.21 1.83±0.29 4.22±0.41 4.42±0.42 B组 69 2.44±0.30 3.20±0.51 1.60±0.20 2.08±0.24 4.20±0.40 4.90±0.56 C组 75 2.42±0.31 3.64±0.49 1.61±0.20 2.39±0.21 4.21±0.40 5.51±0.49 F值 0.285 29.263 0.157 56.006 0.038 51.449 P值 0.752 <0.001 0.855 <0.001 0.962 <0.001
2.2 气道炎症指标 三组患者治疗前痰IL-10、IL-5水平比较,差异无统计学意义(P>0.05)。三组患者治疗后痰IL-10、IL-5水平比较,差异有统计学意义(P<0.05);其中B、C组患者治疗后痰IL-10水平高于A组,IL-5水平低于A组,差异有统计学意义(P<0.05);C组患者治疗后痰IL-10水平高于B组,IL-5水平低于B组,差异有统计学意义(P<0.05),见表2。
表2 三组患者治疗前后痰IL-10、IL-5水平比较(±s,ng/L)Table 2 Comparison of levels of IL-10 and IL-5 in sputum before and after treatment among the three groups
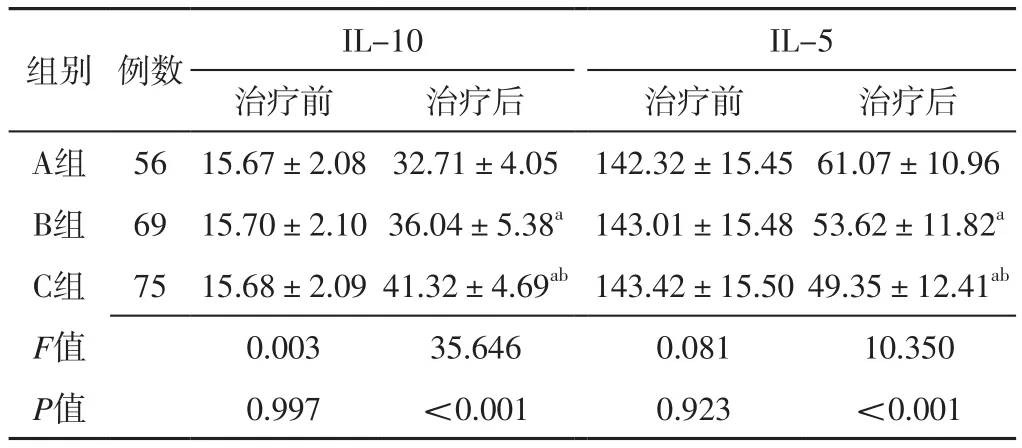
表2 三组患者治疗前后痰IL-10、IL-5水平比较(±s,ng/L)Table 2 Comparison of levels of IL-10 and IL-5 in sputum before and after treatment among the three groups
注:IL=白介素;a表示与A组比较,P<0.05;b表示与B组比较,P<0.05
组别 例数 IL-10 IL-5治疗前 治疗后 治疗前 治疗后A组 56 15.67±2.08 32.71±4.05 142.32±15.45 61.07±10.96 B组 69 15.70±2.10 36.04±5.38a143.01±15.48 53.62±11.82a C组 75 15.68±2.09 41.32±4.69ab143.42±15.50 49.35±12.41ab F值 0.003 35.646 0.081 10.350 P值 0.997 <0.001 0.923 <0.001
2.3 血EOS、血清IgE水平 三组患者治疗前血EOS及血清IgE水平比较,差异无统计学意义(P>0.05)。三组患者治疗后血EOS及血清IgE水平比较,差异有统计学意义(P<0.05);其中B、C组患者治疗后血EOS及血清IgE水平低于A组,C组患者治疗后血EOS及血清IgE水平低于B组,差异有统计学意义(P<0.05),见表3。
表3 三组患者治疗前后血EOS、血清IgE水平比较(±s)Table 3 Comparison of blood EOS and serum IgE level before and treatment among the three groups
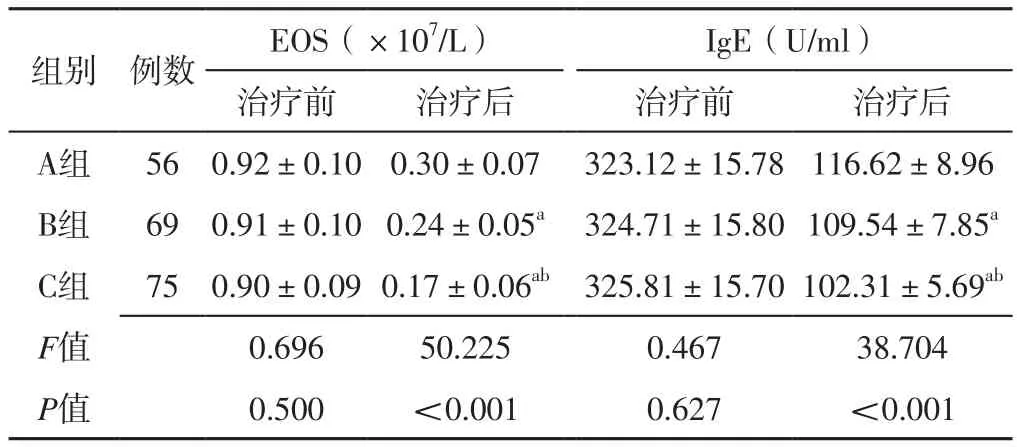
表3 三组患者治疗前后血EOS、血清IgE水平比较(±s)Table 3 Comparison of blood EOS and serum IgE level before and treatment among the three groups
注:EOS=嗜酸粒细胞计数,IgE=免疫球蛋白E;a表示与A组比较,P<0.05;b表示与B组比较,P<0.05
组别 例数 EOS(×107/L) IgE(U/ml)治疗前 治疗后 治疗前 治疗后A组 56 0.92±0.10 0.30±0.07 323.12±15.78 116.62±8.96 B组 69 0.91±0.10 0.24±0.05a 324.71±15.80 109.54±7.85a C组 75 0.90±0.09 0.17±0.06ab 325.81±15.70 102.31±5.69ab F值 0.696 50.225 0.467 38.704 P值 0.500 <0.001 0.627 <0.001
2.4 哮喘控制情况 三组患者治疗前ACT评分比较,差异无统计学意义(P>0.05);三组患者治疗后ACT评分比较,差异有统计学意义(P<0.05)。B组、C组患者治疗后ACT评分高于A组,C组患者治疗后ACT评分高于B组,差异有统计学意义(P<0.05),见表4。
表4 三组患者治疗前后ACT评分比较(±s,分)Table 4 Comparison of ACT score before and after treatment among the three groups
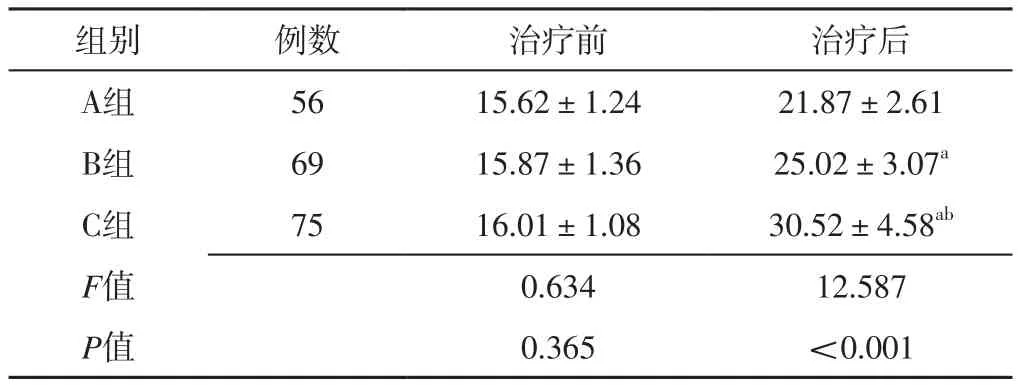
表4 三组患者治疗前后ACT评分比较(±s,分)Table 4 Comparison of ACT score before and after treatment among the three groups
注:a表示与A组比较,P<0.05;b表示与B组比较,P<0.05
组别 例数 治疗前 治疗后A组 56 15.62±1.24 21.87±2.61 B组 69 15.87±1.36 25.02±3.07a C组 75 16.01±1.08 30.52±4.58ab F值 0.634 12.587 P值 0.365 <0.001
2.5 CVA患者观察指标与布地奈德福莫特罗疗程的相关性 Spearman秩相关分析结果显示,CVA患者治疗后FVC(rs=0.265)、FEV1(rs=0.326)、PEF(rs=0.417)、痰IL-10水平(rs=0.412)、ACT评分(rs=0.358)与布地奈德福莫特罗疗程呈正相关(P<0.001),痰IL-5水平(rs=-0.386)、血EOS(rs=-0.315)及血清IgE水平(rs=-0.391)与布地奈德福莫特罗疗程呈负相关(P<0.001)。
3 讨论
CVA是哮喘的前期阶段,多认为与气道炎症、气道高反应性、变应原致敏等有关,进而影响肺通气功能。多数CVA患者需要长期维持治疗,避免病情进一步恶化,尤其是CVA急性期患者,更需应用有效的药物来抑制炎症及过敏反应发生,进而改善肺通气功能。
近年吸入制剂在肺部疾病的治疗中体现出一定优势,但传统的吸入装置较易受场地、操作人员及治疗时间等影响而受限[7]。随着雾化吸入逐渐向便携化、综合化发展,布地奈德福莫特罗将吸入性激素与长效β2-受体激动剂的靶点效应联合起来,通过不同的作用机制来抑制炎症及气道重构,疗效明显优于单一用药[8]。目前不同疗程的布地奈德福莫特罗对CVA疗效的影响尚未可知。《咳嗽的诊断与治疗指南(2015)》[6]指出,CVA患者的用药疗程不短于8周,但未明确指出最佳疗程。目前,布地奈德福莫特罗疗程与经济因素、患者依从性、不良反应有关。但在实际工作中,用药疗程一般根据医疗工作者的临床经验及患者的具体情况而定,基层医院不规范用药情况较严重,一方面为追求更可靠的疗效,随意延长疗程,但药物累积和不良反应增多一定程度上加重了患者的经济负担;另外,医疗工作者易受患者主观想法的影响,缩短了用药疗程而导致疗效欠佳[9]。
吸入制剂的优势在于可减少临床起效剂量,但仍能保证局部暴露剂量,即可最大可能地发挥生物学效应。布地奈德是目前局部抗炎作用较强及不良反应较少的一种激素,其具有的酯化作用可延长药物在气道内的保留时间,便于药效发挥[10]。药代动力学研究发现,吸入1 mg布地奈德10 min后即可达到最大血药浓度,雾化吸入生物利用度约为26%[11]。此外,偶尔过量用药不会产生任何症状,但长期使用布地奈德的急性及亚急性毒性会随之升高[12]。研究表明,布地奈德引起的体质量降低、淋巴及肾上腺皮质萎缩等全身症状较其他皮质激素弱或大体一致,主要与布地奈德的分子构型有关[13]。福莫特罗属于一类长效β2-受体激动剂,其亲水性和亲脂性较高,用药后3~5 min即可起效,且药效可维持8~12 h[14]。研究表明,采用β2-受体激动剂治疗者较易出现心悸、震颤等不良反应,长期高剂量使用会影响胰岛素、脂肪酸、甘油和酮体的代谢,进而出现高血糖、低钾血症和代谢性酸中毒[15]。布地奈德福莫特罗的药品说明书中已提及布地奈德与福莫特罗合并使用并不会增加不良反应,且与口服制剂相比,吸入制剂的不良反应较少。
理论上,CVA需要长期维持治疗,但采用固定剂量的布地奈德福莫特罗长期治疗的局部和全身作用尚不完全清楚,一旦哮喘被控制,建议调整为最小剂量[14]。巨噬细胞、淋巴细胞及中性粒细胞可分泌多种炎性细胞及炎性递质,从而参与CVA的病理生理过程;此外,致敏性物质也是CVA的重要诱因,EOS、IgE可有效预测CVA的治疗效果[16-17]。本研究结果显示,B、C组患者治疗后FVC、FEV1、PEF、痰IL-10水平高于A组,痰IL-5水平、血EOS及血清IgE水平低于A组;C组患者治疗后FVC、FEV1、PEF、痰IL-10水平高于B组,痰IL-5水平、血EOS及血清IgE水平低于B组,此外B、C组患者治疗后ACT评分高于A组,C组患者治疗后ACT评分高于B组,表明与采用布地奈德福莫特罗治疗8周、16周相比,布地奈德福莫特罗治疗24周可更有效地改善CVA患者的肺通气功能、过敏情况,减轻气道炎症,进而有效控制哮喘。本研究进一步行相关性分析结果显示,CVA患者治疗后FVC、FEV1、PEF、痰IL-10水平、ACT评分与布地奈德福莫特罗疗程呈正相关,痰IL-5水平、血EOS及血清IgE水平与布地奈德福莫特罗疗程呈负相关,表明随着布地奈德福莫特罗疗程增加,CVA患者肺通气功能及过敏情况逐渐改善,气道炎症逐渐减轻,哮喘控制效果更佳,分析原因可能与长疗程布地奈德福莫特罗治疗更有利于彻底清除患者的气道炎症及过敏递质有关。
综上所述,随着布地奈德福莫特罗疗程增加,CVA患者肺通气功能、过敏情况及哮喘控制效果逐渐改善,气道炎症逐渐减轻,故本研究建议布地奈德福莫特罗疗程为24周。但本研究为单中心研究,样本量较小,随访时间较短,未能排除患者治疗依从性、基础疾病、生活方式等其他因素对研究结果的影响,导致结论可能存在一定偏倚,有待今后扩大样本量、延长随访时间深入分析不同布地奈德福莫特罗吸入疗程对CVA患者远期预后的影响,以为选择布地奈德福莫特罗吸入的最佳疗程提供高级别的证据支持。
作者贡献:刘威威进行文章的构思与设计,撰写、修订论文,负责文章的质量控制及审校,并对文章整体负责、监督管理;苏玉峰进行研究的实施与可行性分析;王欢、吴旭兰、陈晓香进行数据收集、整理、分析;李敏进行结果分析与解释。
本文无利益冲突。
