重庆市临床研究协调员/临床监查员的工作流动性现状和对策
2022-02-20曹丽亚陈勇川郭薇谢林利
曹丽亚 陈勇川 郭薇 谢林利

中圖分类号 R95 文献标志码 A 文章编号 1001-0408(2022)03-0275-05
DOI 10.6039/j.issn.1001-0408.2022.03.04
摘 要 目的 了解重庆市临床研究协调员(CRC)、临床监查员(CRA)的工作流动性现状,探讨提高CRC、CRA工作稳定性的可行方法。方法 以问卷形式对重庆市22家药物临床试验机构的200名CRC和 CRA进行工作流动性情况调查,内容涉及人员基本情况、工作流动性情况、流动原因等方面。结果与结论 回收有效问卷178份,有效回收率89.00%,其中CRC问卷回收110份,CRA问卷回收68份。被调查的CRC和CRA中,主要为20~30岁的年轻人,分别占各职业人群的87.27%、82.35%;CRA学历水平整体略高于CRC;所学专业和既往工作经历主要以医药相关为主,其他非医药相关职业转行从事CRC的比例高于CRA。CRC工作年限在3年以内的占88.18%,其中具有1~<3年的工作经验后,既往工作单位数量在2个及以上的占50.00%;CRA工作年限在3年以内的占64.70%,其中具有1~<3年的工作经验后,既往工作单位数量在2个及以上的占70.37%。CRC平均每人经手临床试验项目5.38项,完成1.22项;CRA平均每人经手7.47项,完成2.04项。CRC和CRA跳槽或离职的主要原因包括薪资低于期望、晋升机会少、工作量太大,分别占各职业人群的83.64%/80.88%、45.45%/39.71%、31.82%/26.47%。作为临床试验中的重要组成部分,CRC、CRA工作流动性较大。建议建立统一的行业标准,规范CRC、CRA的管理权责,同时优化CRC、CRA的工作模式,提高职业认同感和归属感,从而提高相关从业人员的工作稳定性。
关键词 临床研究协调员;临床监查员;工作流动性;临床试验
Status quo and countermeasures of job mobility among clinical research coordinator/clinical research associate in Chongqing
CAO Liya1,CHEN Yongchuan1,GUO Wei2,XIE Linli1(1. Dept. of Pharmacy, the First Affiliated Hospital of Army Medical University, Chongqing 400038, China; 2. Clinical Research Center, the Affiliated Stomatological Hospital of Chongqing Medical University, Chongqing 400038, China)
ABSTRACT OBJECTIVE To investigate the job mobility of clinical research coordinators (CRCs) and clinical research associates (CRAs) in Chongqing, and to explore the feasible methods to improve the job stability of CRCs and CRAs. METHODS Questionnaire survey was conducted to investigate the job mobility of 200 CRCs and CRAs working in 22 drug clinical trial institutions of Chongqing. The contents included basic information, job mobility, and reasons for mobility. RESULTS & CONCLUSIONS Totally 178 valid questionnaires were recovered, with an efficient recovery rate of 89.00%, of which 110 were recovered from CRCs and 68 were recovered from CRAs. Among the surveyed CRCs and CRAs, the age distribution was mainly 20-30 years old, accounting for 87.27% and 82.35% of the respective population respectively. The overall educational degree of CRAs were slightly higher than those of CRCs. The majors and previous work experience were mainly related to medicine; the proportion of other non-medicine-related professions who switched to CRCs was higher than that of CRAs. Totally 88.18% had CRC working experience within 3 years; after having 1-<3 years of work experience, 50.00% had worked in 2 or more work units. Totally 64.70% had CRA working experience within 3 years; after having 1-<3 years of work experience, 70.37% had worked in 2 or more work units. CRCs handled 5.38 items of clinical trials and completed 1.22 items on average; CRAs handled 7.47 items and completes 2.04 items on average. Main reasons of CRCs and CRAs for job-hopping included low salary below expectations, few promotion opportunities, and too much workload, accounting for 83.64%/80.88%, 45.45%/39.71%, 31.82%/26.47%, respectively. As an important part of clinical trials, CRCs and CRAs had high job mobility. It is suggested to establish a unified industry standard, standardize the management rights and responsibilities of CRCs and CRAs, optimize the working mode of CRCs and CRAs, and improve professional identity and sense of belonging, so as to improve the job stability of relevant employees.
KEYWORDS clinical research coordinator; clinical research associate; job mobility; clinical trial
我国医药研发审评审批制度的改革、国家食品药品监督管理总局加入人用药品注册技术要求国际协调会(International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use,ICH)和一系列相关法律法规及指导原则的相继发布,对我国临床试验的质量提出了更高要求,临床试验参与各方需紧密配合、高效合作,才能高质量和高效率地完成试验项目,投入国际环境中参与竞争[1-3]。临床研究协调员(clinical research coordinator,CRC)、临床监查员(clinical research associate,CRA)在临床试验中起到至关重要的作用。CRC是研究者、申办者和受试者之间的纽带,在研究中心协助研究者进行非医学性判断的事务工作[4];而CRA则对各研究中心进行监查,管理试验数据,对临床试验过程进行质量控制[1]。药物臨床试验登记与信息公示平台显示,2016-2020年,我国开展药物临床试验的数量逐年递增。作为临床试验带来的新兴职业,CRC和CRA显示出较大的市场空缺。目前,该领域暂无统一的行业准入标准和行业规范,《药物临床试验质量管理规范》(Good Clinical Practice,GCP)要求CRA应当受过相应培训,具备医学、药学等临床试验监查所需知识,能够有效履行监查职责,而对CRC则没有具体规定[1];一般行业内仅要求CRC和CRA应具有护理学、药学、临床医学等生命科学领域教育背景,通过所在公司GCP相关法规和临床试验专业技术培训,获得GCP证书等,即可从事相关工作[5-6]。CRC、CRA行业的蓬勃发展给临床试验开展带来利处,但也凸显出一些问题,较为突出的如CRC、CRA工作流动性较大,临床试验项目实施过程中频繁更换CRC、CRA给临床试验开展带来阻力等。本文通过对重庆市22家药物临床试验机构的CRC、CRA进行问卷调查,了解相关从业人员的工作流动情况,为更好地开展临床试验工作提供参考依据。
1 资料与方法
采用问卷调查的方式,在2019年以重庆市22家临床试验机构在研临床试验项目中的CRC和CRA作为调查对象发放调查问卷。将回收的问卷进行流水编号,录入问卷数据库保存后进行下一步统计分析。问卷设置单选、多选和填空题,内容包括被调查对象的年龄、学历、专业、既往工作经历、工作单位性质等基本信息;针对工作流动性的调查包括从业年限、既往工作单位数量、经手临床试验项目数量、完成临床试验项目数量等;对CRC、CRA工作流动原因的调查包括职业满意度、工作流动的主要原因、在研临床试验项目数量、工作分布的研究中心数量、管理情况等方面。采用Excel软件进行统计分析,计数资料采用人数(个数)和百分比进行描述,计量资料采用平均数表示。
2 结果
2.1 CRC和CRA的基本情况
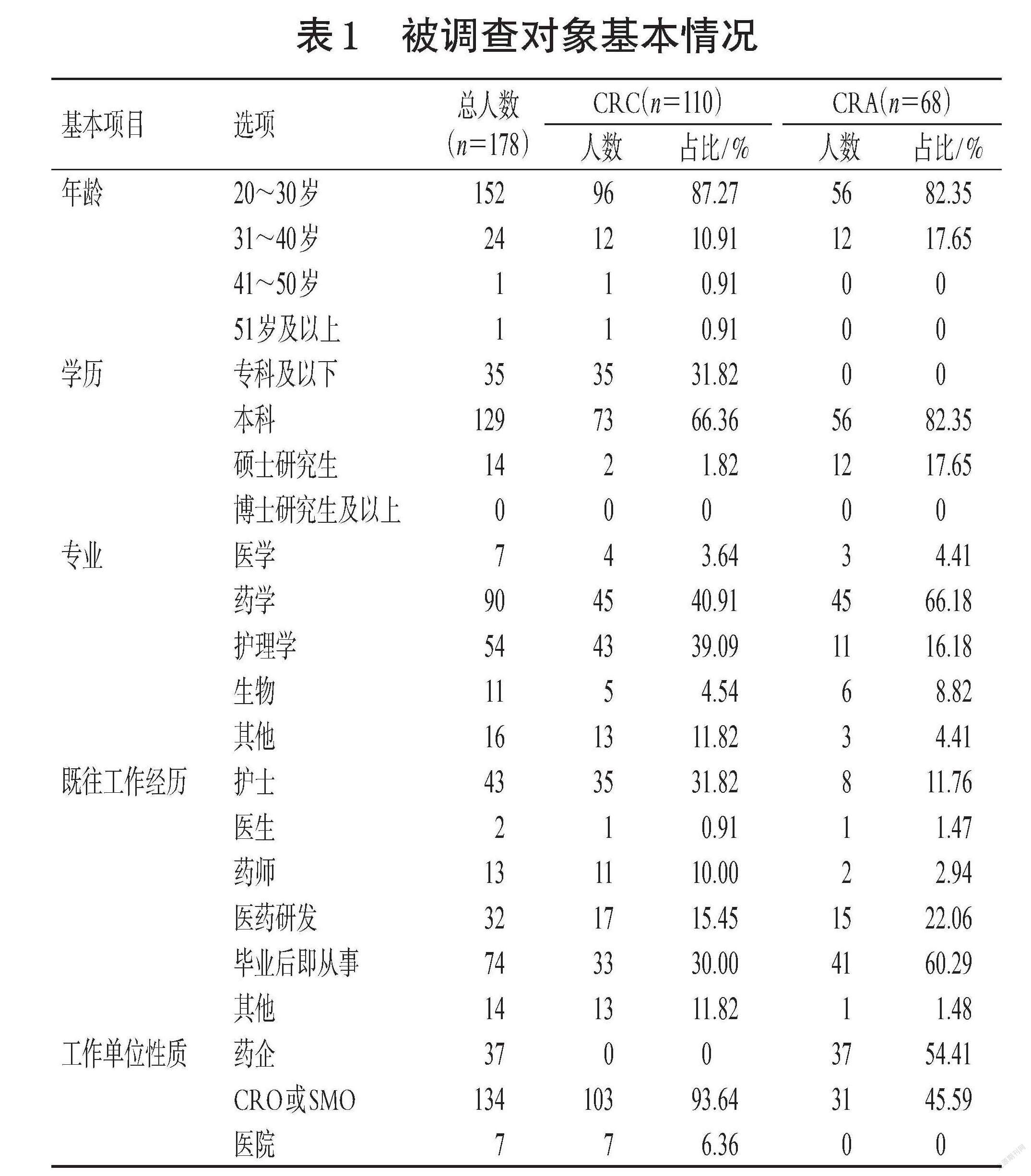
本次调查共计发放问卷200份,收回有效问卷178份(有效回收率89.00%),其中CRC问卷回收110份、CRA问卷回收68份。被调查CRC的年龄主要为20~30岁,占总人数的87.27%;学历主要为本科(占66.36%),其次是专科及以下(占31.82%);专业背景方面,40.91%是药学,39.09%是护理学;既往工作经历方面,31.82%是护士转行,30.00%是毕业后即从事CRC工作,由其他非医药相关专业(销售、教师、文员、质量检验等职业)转行做CRC的占11.82%;工作单位性质方面,93.64%来源于第三方公司合同研究组织(contract research organization,CRO)或临床机构管理组织(site management organization,SMO),6.36%来源于医院。被调查的CRA年龄主要为20~30岁,占总人数的82.35%;本科学历占82.35%,硕士研究生学历占17.65%;专业背景主要为药学(占66.18%),其次是护理学(占16.18%);既往工作经历方面,毕业后即从事CRA的比例达到60.29%,其次是医药研发转行(占22.06%);工作单位性质方面,54.41%来源于药企(申办方),45.59%来源于第三方CRO公司。综合上述结果可以看出,总体上临床试验行业对CRA的学历、专业背景和既往工作经历方面的要求高于CRC,CRC的行业准入标准稍低于CRA。被调查对象基本情况见表1。
2.2 CRC和CRA工作流动性调查结果
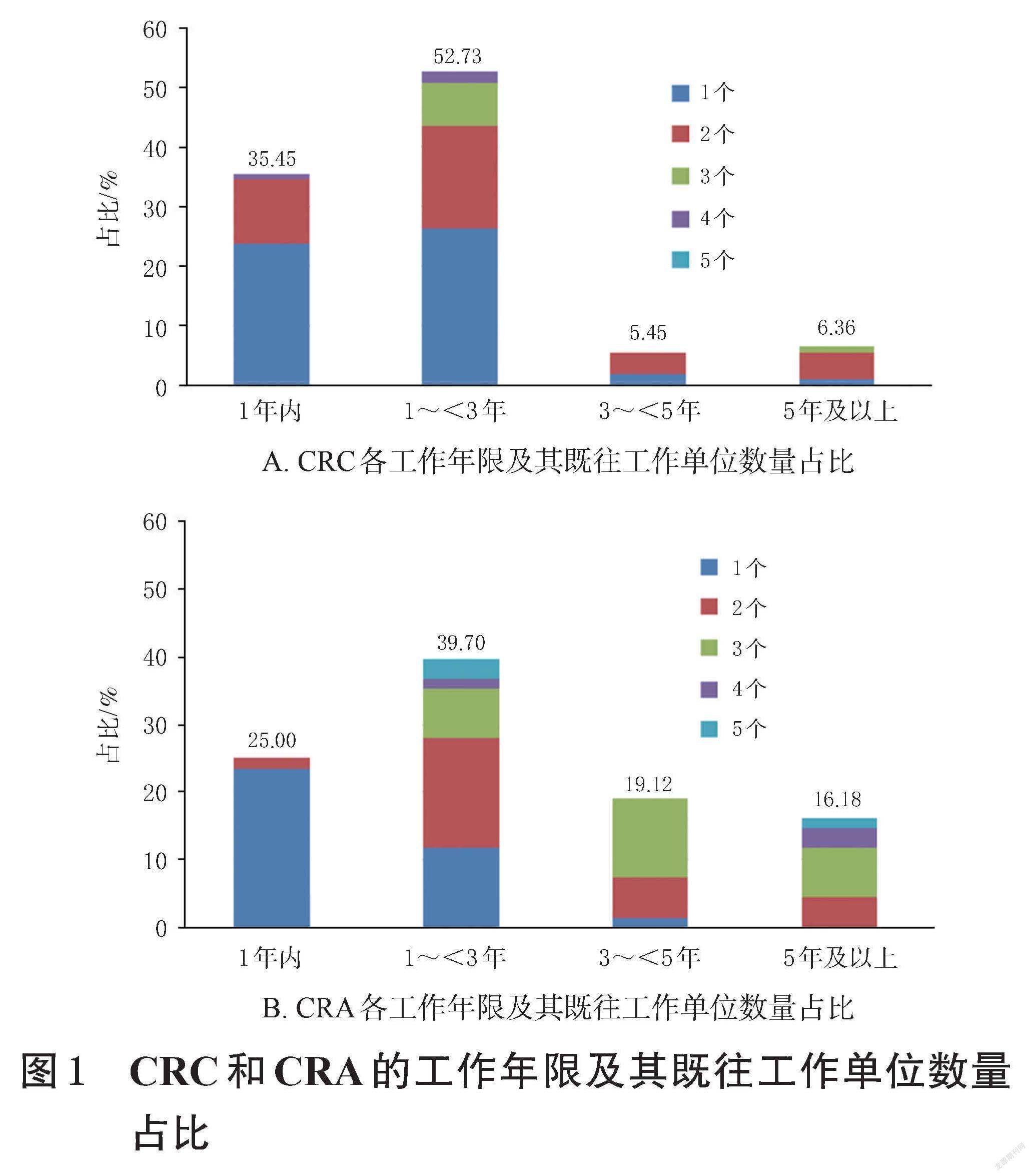
在178份问卷中,CRC工作年限在1年以内的有39人,占被调查CRC的35.45%,其中既往工作单位数量在2个及以上的占33.33%;工作年限为1~<3年的有58人,占被调查CRC的52.73%,其中既往工作单位数量在2个及以上的占50.00%;工作年限为3~<5年的有6人,占被调查CRC的5.45%,其中既往工作单位数量在2个及以上的占66.67%;工作年限为5年及以上的有7人,占被调查CRC的6.36%,其中既往工作单位数量在2个及以上的占85.71%。CRA工作年限在1年以内的有17人,占被调查CRA的25.00%,其中既往工作单位数量在2个及以上的占5.88%;工作年限为1~<3年的有27人,占被调查CRA的39.70%,其中既往工作单位数量在2个及以上的占70.37%;工作年限为3~<5年的有13人,占被调查CRA的19.12%,其中既往工作单位数量在2个及以上的占92.31%;工作年限在5年及以上的有11人,占被调查CRA的16.18%,既往工作单位数量均在2个及以上。CRC和CRA的工作年限及其既往工作单位数量占比见图1。
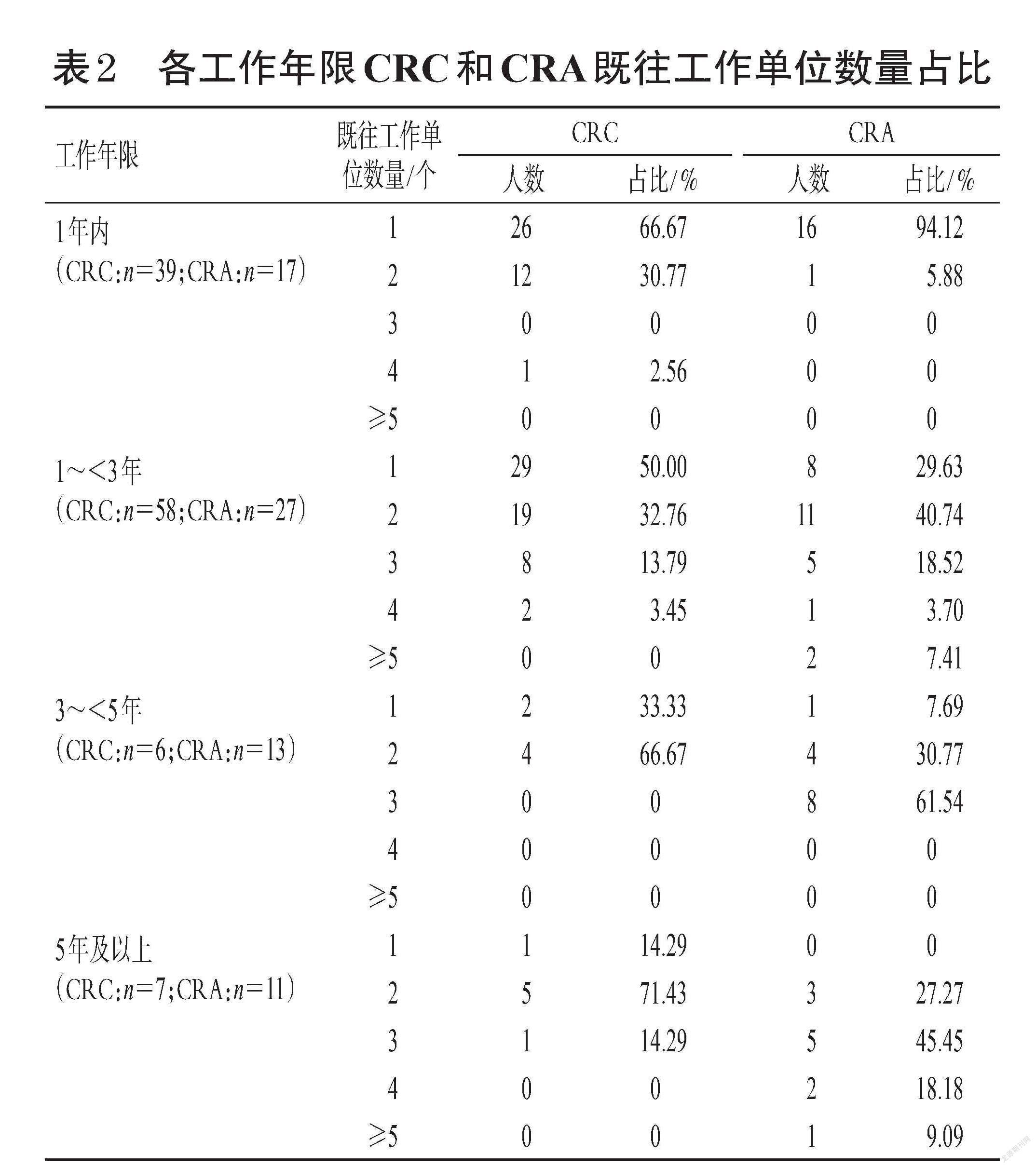
由图1可以看出,工作年限1年内的CRC既往工作单位数量在2个及以上的比例明显高于CRA,考虑与CRC准入门槛较低和市场需求量大相关。而1年及以上工作年限的CRA既往工作单位数量明显多于CRC,考虑原因是经验足的CRA市场竞争力较大。总体来说,有一定工作经验后,CRC和CRA跳槽或离职的比例较高。各工作年限CRC和CRA既往工作单位数量占比见表2。
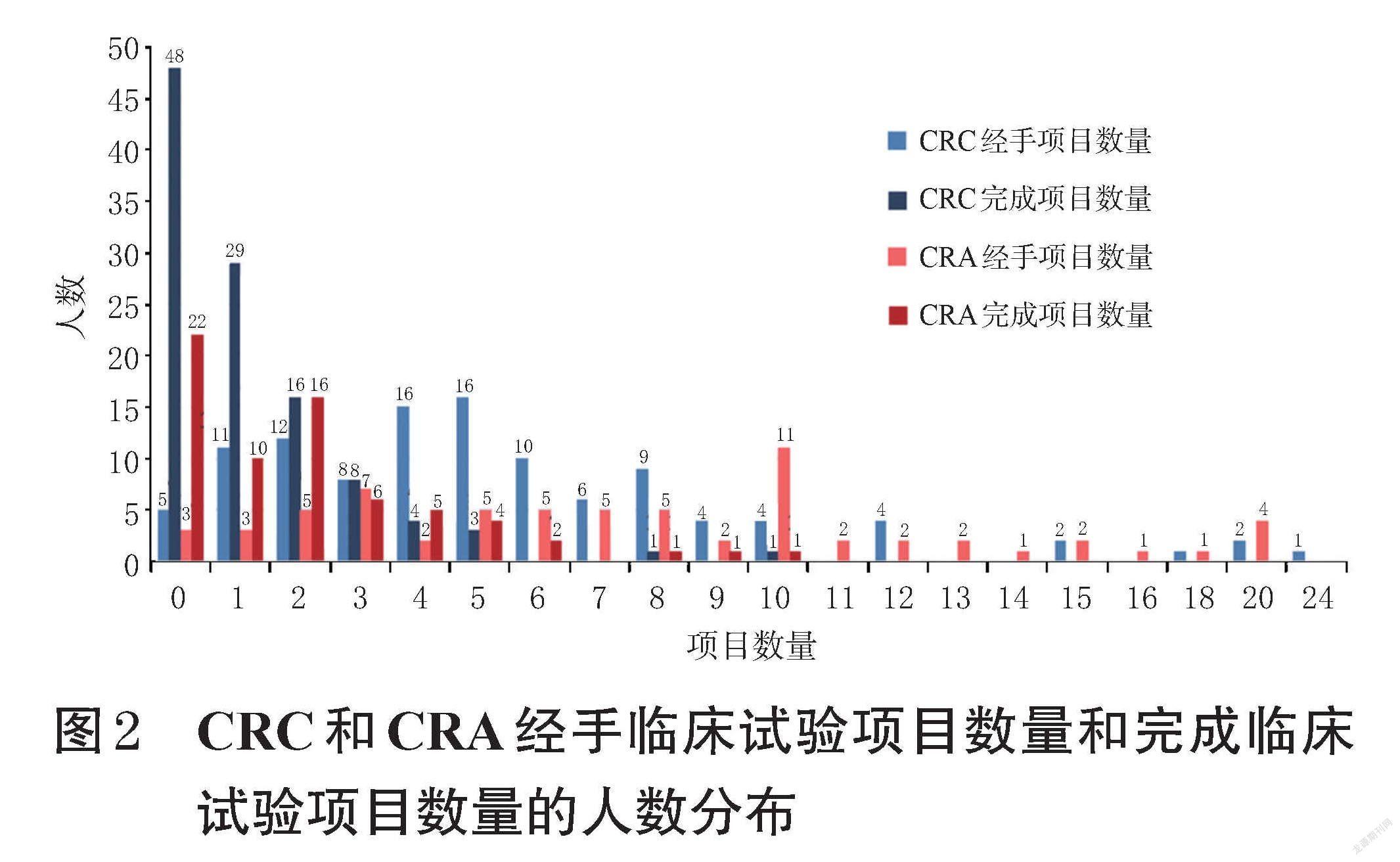
在经手临床试验项目数量和完成数量方面,CRC平均每人经手临床试验项目5.38项,而平均仅完成1.22项,其中48人完成的数量为0(占43.64%);CRA平均每人经手临床试验项目7.47项,而平均仅完成2.04项,其中22人完成的数量为0(占32.35%)。CRC和CRA经手临床试验项目数量和完成临床试验项目数量的人数分布见图2。
2.3 CRC和CRA流动原因调查结果
在对CRC和CRA的职业满意度调查中,满意和非常满意的占96.64%,表明他们对于自身行业是很看好的。针对CRC/CRA自身或周围同事跳槽或离职的主要原因调查结果显示,薪资低于期望、晋升机会和空间较少、工作量太大分别占各职业人群的83.64%/80.88%、45.45%/39.71%、31.82%/26.47%;略有差别的是,针对CRC的调查结果中,医生、医技科室不配合占比较高,达到19.09%,CRA则为0。CRA跳槽或離职的其他原因主要是出差频率太高,CRC跳槽或离职的其他主要原因主要包括转行做CRA,这也从侧面反映出CRA的职业认同感略高。CRC和CRA工作流动原因调查结果见表3。
2.4 CRC和CRA承担在研临床试验项目情况的调查结果
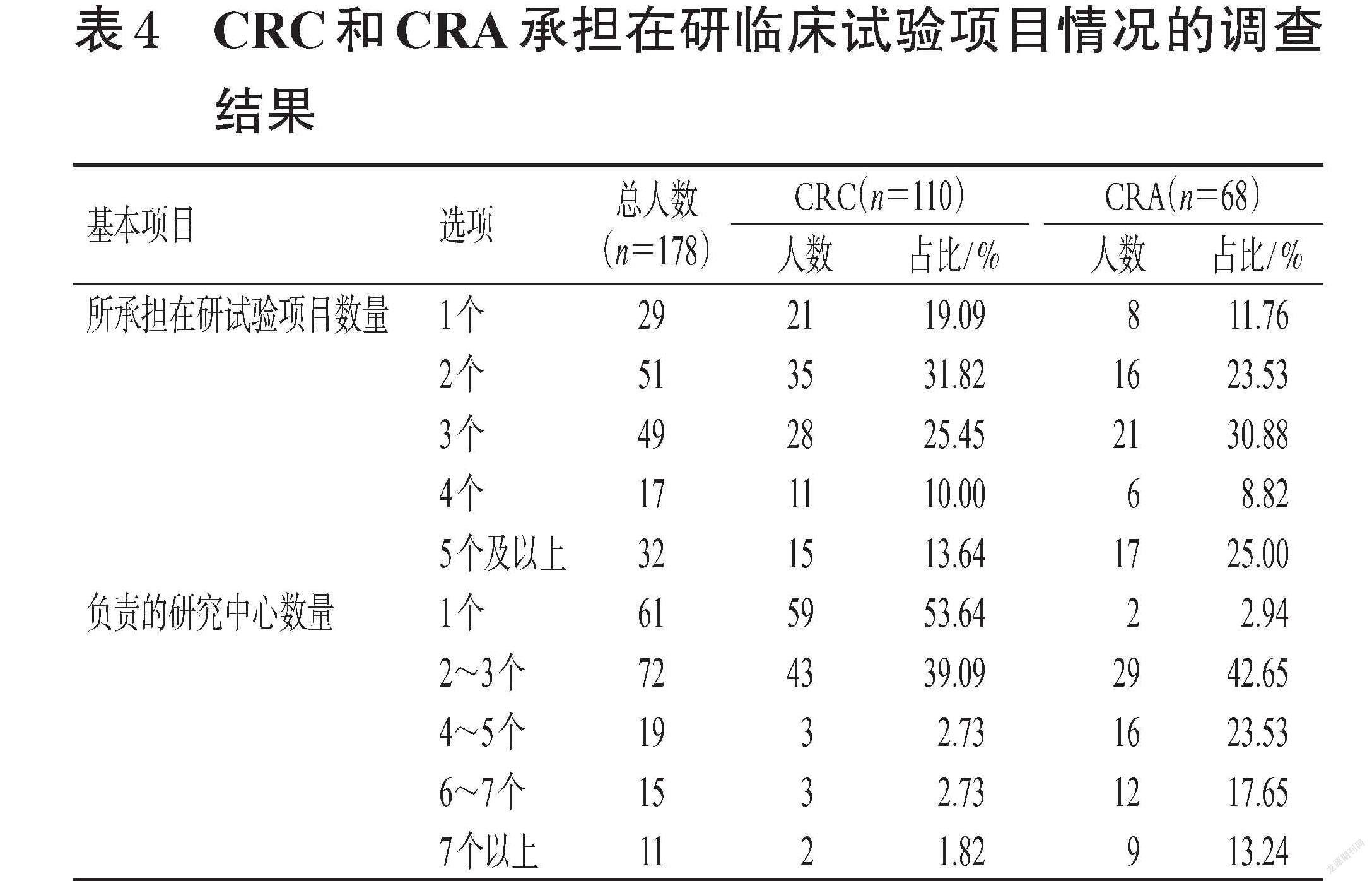
对CRC和CRA承担在研临床试验项目情况的调查结果显示,CRC中有80.91%承担2个及以上的试验项目,所承担试验项目分布在2个及以上研究中心的占46.36%;CRA中有88.24%承担2个及以上的试验项目,所承担试验项目分布在2个及以上研究中心的占97.06%。总体而言,CRA承担的临床试验项目数量和其负责的研究中心数多于CRC。CRC和CRA承担在研临床试验项目情况的调查结果见表4。
2.5 CRC和CRA主要管理方的调查结果
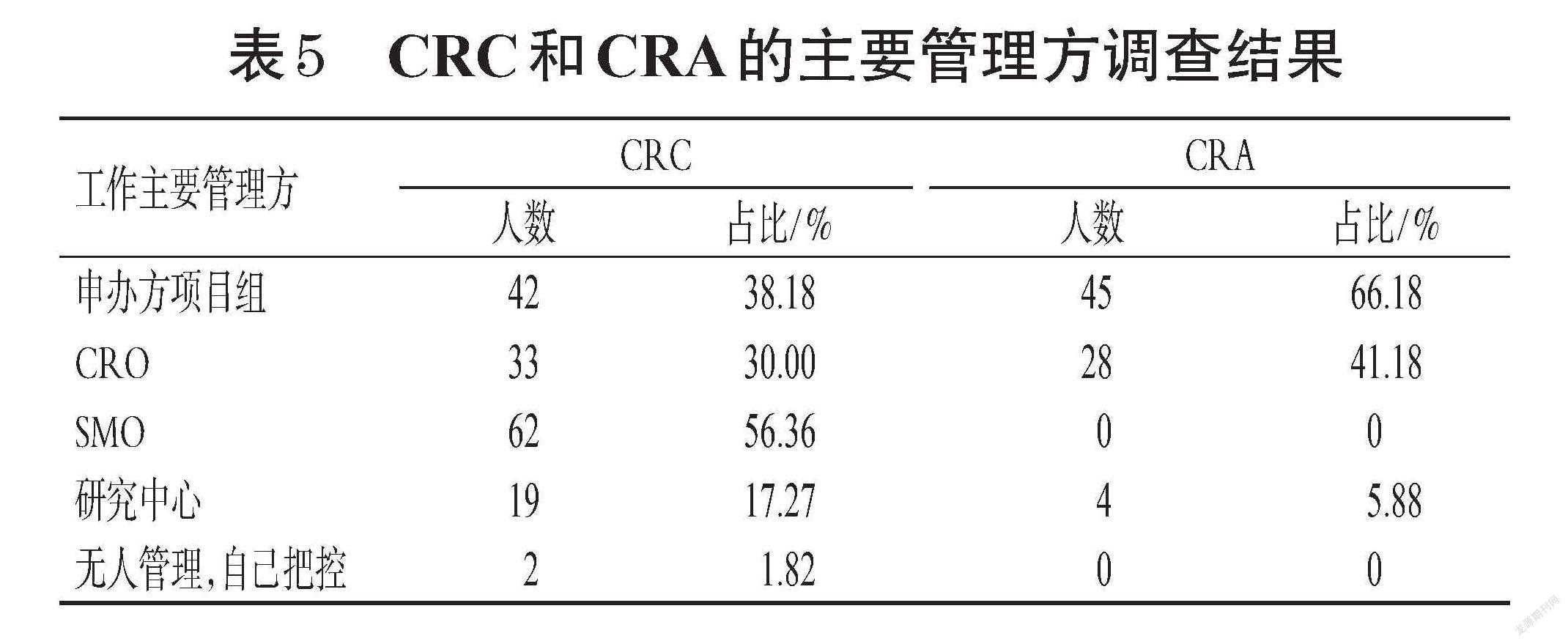
对CRC和CRA主要管理方的调查发现,CRC主要受所在SMO、申办方项目组和第三方CRO公司管理,CRA主要受申办方项目组和第三方CRO公司管理。相比之下,研究机构对CRC和CRA管理较少:仅有17.27%的CRC和5.88%的CRA表示自己的工作受研究机构管理,而有1.82%的CRC表示自己的工作不受各方管理、工作缺乏归属感。CRC和CRA主要管理方的调查结果见表5。对CRC和CRA接受研究机构管理的意愿进行调查发现,88.20%的被调查者认为临床试验机构有必要对他们进行管理。
3 分析与建议
3.1 CRC和CRA行业缺口较大且无统一行业标准
根据本文调查结果发现,重庆市CRC、CRA从业人员多为年轻人群,学历、专业和既往工作背景要求并不是十分严格,行业准入门槛并不高,其中以CRC更为明显。此外,其他行业转行做CRC、CRA的比例较高,说明该职业属于新兴且热门的行业。自国家药品监督管理局(National Medical Products Administration,NMPA) 2018年7月27日发布《关于调整药物临床试验审评审批程序的公告》以来,我国临床试验的开展由审批制改为默示许可制[7]。随着该公告的出台,一方面,临床试验项目数量快速增加,质量要求也逐步向国际标准看齐,CRC和CRA的市场仍存在较大缺口;另一方面,行业发展时间不长,CRC和CRA在经历过相关培训后即可上岗,目前并无统一行业标准[8-9],且在有一定实际经验后CRC、CRA具有相当的竞争力,工作流动可以给他们带来更高的收入和更好的发展[10-11]。
我国医药研发事业不断发展的过程中,临床试验对CRA、CRC等相关人才的要求势必越来越高。故笔者建议我国应建立专业且具有公信力的组织或机构,制定从业人员的行业规范和资质认定标准,以此规范CRC、CRA的行业准入条件和职业细则要求,提高CRC、CRA的整体专业水平和工作稳定性。
3.2 优化工作模式,提高CRC和CRA的工作稳定性
本调查结果显示,CRC和CRA经手的临床试验项目数量多,而实际完成的数量很少。客观上,部分临床试验开展周期较长,更换CRC或CRA不可避免:一方面CRC和CRA本身流动性较大,离职、跳槽是较为普遍的现象;另一方面,公司整体的协调安排往往从加快受试者入组或数据清理速度方面考虑,在临床试验开展过程中,常出现协调CRC和CRA至其他研究项目或其他研究中心的情况。而由此带来的后果是CRC和CRA对试验项目和研究中心办事流程不熟悉,导致临床试验项目进展缓慢、质量下降。
CRC绝大部分来源于SMO/CRO,同时承担多项临床试验的协助工作,大多需要奔波于各家研究中心。此外,除协助研究者安排访视、数据录入等工作外,CRC还承担了大量职责界限模糊的“协助”“协调”的事务性工作,这增加了CRC的工作负荷和心理压力[12-13]。但目前,CRC的薪资和晋升空间普遍低于CRA,除了跳槽去其他公司,还有相当部分获得临床试验经验后转行做CRA。目前,尚无相关法规规范CRC的权责要求,故笔者建议在相关法规及指导原则中,明确CRC分工权责和职业要求:一方面,可降低因权责界限模糊给临床试验带来的风险;另一方面,也可提高CRC的职业认同感和价值感。
CRA多来源于申办方或第三方CRO公司。相比于CRC,CRA具有管理研究中心数量多、需要多地出差等特点,其监查频率的高低和对研究中心的熟悉程度直接影响临床试验项目质量。不同申办方或第三方CRO公司的人员稳定性不一致,尤其是来源于第三方CRO公司的CRA流动性较大,不少第三方CRO公司的CRA在有工作经验后,选择跳槽至申办方。CRA的另一个离职原因主要是出差频率太高,这和临床试验的多中心特点和中心地点的选择以及公司安排有关。近年来,笔者在工作中发现驻地CRA开始出现,其在对研究中心熟悉程度、与研究者和机构的沟通流畅度、对资料完整性和试验项目整体质量把控上都显示出一定优势。笔者建议申办方或第三方CRO公司视试验项目和研究中心分散情况,派遣驻地CRA或集中研究中心办公。
3.3 规范CRC和CRA管理权责,提高行业的职业认同感和归属感
CRC和CRA都是我国临床试验发展带来的新兴行业,随着我国医药研发事业的发展,这一人群的队伍势必还将壮大。CRC的工作特点在于,其主要来源于第三方公司,被派遣到医院参与临床试验工作;在与各方协调沟通时,CRC处于相对弱势的地位,心理上易出现孤立无援的感觉。此外,不少临床试验机构并没有建立相应的管理和保障制度,甚至不能提供基本的工作场所和设施,这使得他们的工作归属感和职业认同感缺乏[13]。而CRA具有出差频率高、研究中心分散等特点,且大多数同样面临工作场所和设施缺乏、医生配合度不高、机构和伦理沟通困难等问题。
目前,因临床试验周期较长、行业本身不成熟和职业特点等因素,CRC和CRA的人员流动不可避免,他们所在公司和研究中心需要建立互助共赢的管理体系,来减少由CRC、CRA人员流动带来的不利影响[14]。申办方和第三方公司需要规范人员管理和提供相应的晋升通道和制度保障,来提高从业人员的职业归属感和认同感;研究机构应该承担CRC和CRA的管理职责,建立相应的管理制度和给予硬件条件支撑。而在监管层面上,尚未在GCP和相关法律法规上明确规定相关从业人员的行业标准和制度,形成相关政策或共识对CRC、CRA行业进行规范和制度保障,故监管部门可建立注册登记制度、出台相关法规政策或行业规范和共识,来提高相关从业人员的工作稳定性。
本研究尚存在一些不足,例如调查人数较少、调查区域较为单一等,结论有一定的局限性;部分调查项目设置还不够深入,例如薪资是CRC、CRA工作流动的主要原因,但本问卷未设置其具体薪资范围等问题,因此无法了解整体行业薪资水平;此外CRC和CRA行业的工作流动性也受国家医药行业重大政策的影响,本研究尚未将宏观政策因素的影响进行调研。后续将考虑以上不足,继续进一步深入研究。
参考文献
[ 1 ] 国家药品监督管理局,国家卫生健康委.关于发布药物临床试验质量管理规范的公告 [EB/OL].(2020-04-23)[2021- 05-20]. https://www.nmpa.gov.cn/zhuanti/ypzhcglbf/ypzhcglbfzhcwj/20200426162401243.html.
[ 2 ] 郭薇,谢林利,曹丽亚,等.加入ICH对我国药物临床试验机构工作的影响和思考[J].中国药房,2019,30(11):1445-1448.
[ 3 ] 国家市场监督管理总局.药品注册管理办法:国家市场监督管理总局令第 27 号[EB/OL].(2020-03-30)[2020-06-01]. http://gkml.samr.gov.cn/nsjg/fgs/202003/t20200330_313670. html.
[ 4 ] 刘晓红,李丹,江旻.临床研究协调员的工作范畴及现状分析[J].中国临床药理学杂志,2020,36(6):706-708.
[ 5 ] 广东省药学会.药物临床试验 CRC管理·广东共识:2020年版[J].今日药学,2020,30(12):799-801.
[ 6 ] 王廷春,譚波,吴炜毅,等.药物临床试验 监查稽查·广东共识:2020年版[J].今日药学,2020,30(11):741-746.
[ 7 ] 国家市场监督管理总局.关于调整药物临床试验审评审批程序的公告 [EB/OL].(2018-07-27)[2020-09-20]. https://www.nmpa.gov.cn/directory/web/nmpa/xxgk/ggtg/ywlchshyjgrdgg/20180727172901286.html.
[ 8 ] 石佳嘉,董凌云,武志昂.我国临床试验监查员离职意愿影响因素分析[J].中国药事,2019,33(8):887-895.
[ 9 ] 赵海娟,张可欣,刘伟,等.临床研究协调员在临床试验工作中重要性的调查研究[J].中国临床药理学杂志,2018,34(15):1923-1925.
[10] 张智慧,武志昂,潘岩.药物临床试验监查员工作满意度影响因素分析[J].中国药业,2020,29(16):15-18.
[11] 张邦禹,张鹏,徐瑛,等. 5家SMO公司临床研究助理工作满意度、职业倦怠与离职意愿现状调查及分析[J].中国新药杂志,2019,28(10):1237-1242.
[12] 黄倩,刘健,吴丽花.基于医疗机构视角的临床研究协调员现状分析及管理优化探讨[J].中国新药与临床杂志,2021,40(4):270-272.
[13] 刘璐,周吉银.临床研究协调员管理模式存在的问题与对策[J].中国临床药学杂志,2019,28(5):379-381.
[14] 李树婷,刘洋,高志刚,等.中国临床研究助理的生态环境及现场管理组织发展报告[J].中国新药杂志,2018,27(11):1266-1272.
(收稿日期:2021-06-22 修回日期:2021-12-23)
(编辑:刘明伟)
主管药师,硕士。研究方向:药理学、药物临床试验机构管理。电话:023-68766776。E-mail:caoliya008@163.com
通信作者:主管药师。研究方向:药物临床试验机构管理。电话:023-68766775。E-mail:24310479@qq.com
