移动应用对癌症患者居家口服抗癌药物依从性及不良反应影响的系统评价
2022-02-17李晓莉孟爱凤徐桂华邾萍智晓旭
李晓莉 孟爱凤 徐桂华 邾萍 智晓旭
(1.南京中医药大学护理学院,江苏 南京 210023; 2.江苏省肿瘤医院 江苏省肿瘤防治研究所 南京医科大学附属肿瘤医院护理部,江苏 南京 210093)
手术、化疗、放疗是癌症治疗的三大传统手段,口服抗癌药物的使用正在改变癌症治疗的管理方式[1]。传统的院内医护监管转变为患者居家自我管理,随之一些问题逐渐显现。良好的依从性是保证药物疗效的基础,但癌症患者居家口服抗癌药物的服药依从性情况往往不容乐观。口服抗癌药物的不良反应与药物依从性息息相关,患者常常在识别、应对不良反应方面存在困难。基于移动应用的干预措施在提供高质量家庭监管方面弥补了院内与院外之间的差距[2],近年来被广泛运用到癌症患者的居家监测当中。鉴此,本研究拟通过循证方法,形成移动应用在干预癌症患者居家口服抗癌药依从性和不良反应方面影响的结论,旨在将来为患者制定有效干预措施时提供依据。
1 资料与方法
1.1文献纳入与排除标准 纳入标准:(1)研究对象确诊为癌症患者,正在居家口服抗癌药物。(2)干预措施为常规药物宣教的基础上使用移动应用进行依从性和不良反应的干预。(3)主要结局指标为药物依从性和症状负担相关指标。(4)文献类型为随机对照试验。排除标准:(1)非中英文文献。(2)会议论文和学位论文。(3)数据不完整、无法获取全文或重复发表的文献。
1.2检索策略 本研究检索的英文数据库包括Pubmed、Embase、Cochrane Library、Web of science、CINAHL。中文数据库包括知网、维普、万方和中国生物医学文献数据库,检索时限为建库至2020年2月1日。此外,采用滚雪球方法对纳入文献的参考文献进行筛选,作为补充。英文检索词包括“oral anticancer agent*、oral endocrine/hormonal agent*、oral targeted agent*、oral chemotherap*、mobile applications、website、internet、e-health、mobile phone、obedience*、concordance*、persistence*、compliance*、adherence*、symptom*、side effect*、effect*, side、adverse reaction*、randomized controlled trial、rct”等,中文检索词包括“口服抗癌药、口服内分泌药、口服靶向药、口服化疗、移动应用、网页、移动健康、智能电话、依从、症状、副作用、不良反应、随机”等,采用主题词和自由词相结合进行检索。具体检索策略(以PUBMED为例)。见图1。

图1 以Pubmed数据库为例的检索策略二维码
1.3文献筛查和质量评价 2名研究者根据循证问题(P、I、C、O)独立检索,采用endnote文献管理工具进行文献查重,后阅读文献标题和摘要进行筛选。如2位研究者产生分歧,由第3位研究者做出最终的判断决定。经过筛选后,最终纳入文献由2名研究者分别提取文章信息,内容包括研究时间、研究地点、样本量、干预组和对照组的干预措施、结局指标和结果、研究结论。质量评价由2名研究者按照Cochrane系统评价手册中的随机对照试验质量评价标准独立评价,包括随机顺序的产生、随机方案分配隐藏、盲法、结局指标数据的完整性、选择性报告研究结果、其他方面的偏倚来源等7个方面;分别对每个方面做出“偏倚风险低”“偏倚风险高”“不清楚”的判断。如研究完全满足评价标准,则发生各种偏倚的可能性小,质量等级评为A;部分满足,发生偏倚的可能性为中度,质量等级评为B;完全不满足,发生偏倚的可能性高,质量等级评为C。如产生意见分歧,由第3名研究者仲裁决定。
1.4统计学方法 采用RevMan 5.3软件对资料进行Meta分析。首先对文献进行异质性检验,若P>0.1,I2<50%,选用固定效应模型;若P<0.1,I2≥50%,但临床异质性小且需要合并时,选择随机效应模型或者亚组分析及敏感性分析。若异质性过大,且无法判断异质性的来源,则不纳入Meta分析,采用描述性分析。
2 结果
2.1检索结果及纳入文献的一般情况 初步检索相关文献共1 739篇,剔除重复文献406篇,经阅读文题和摘要后剔除文献1 256篇,经阅读全文后剔除文献70篇(干预人群不符8篇,干预措施不符8篇,结局指标不符1篇,文献类型不符14篇,数据不完整3篇,未获取全文36篇),最终纳入7篇随机对照研究。其中中文文献1篇,英文文献6篇,共795例患者,纳入文献的详细资料,见表1。
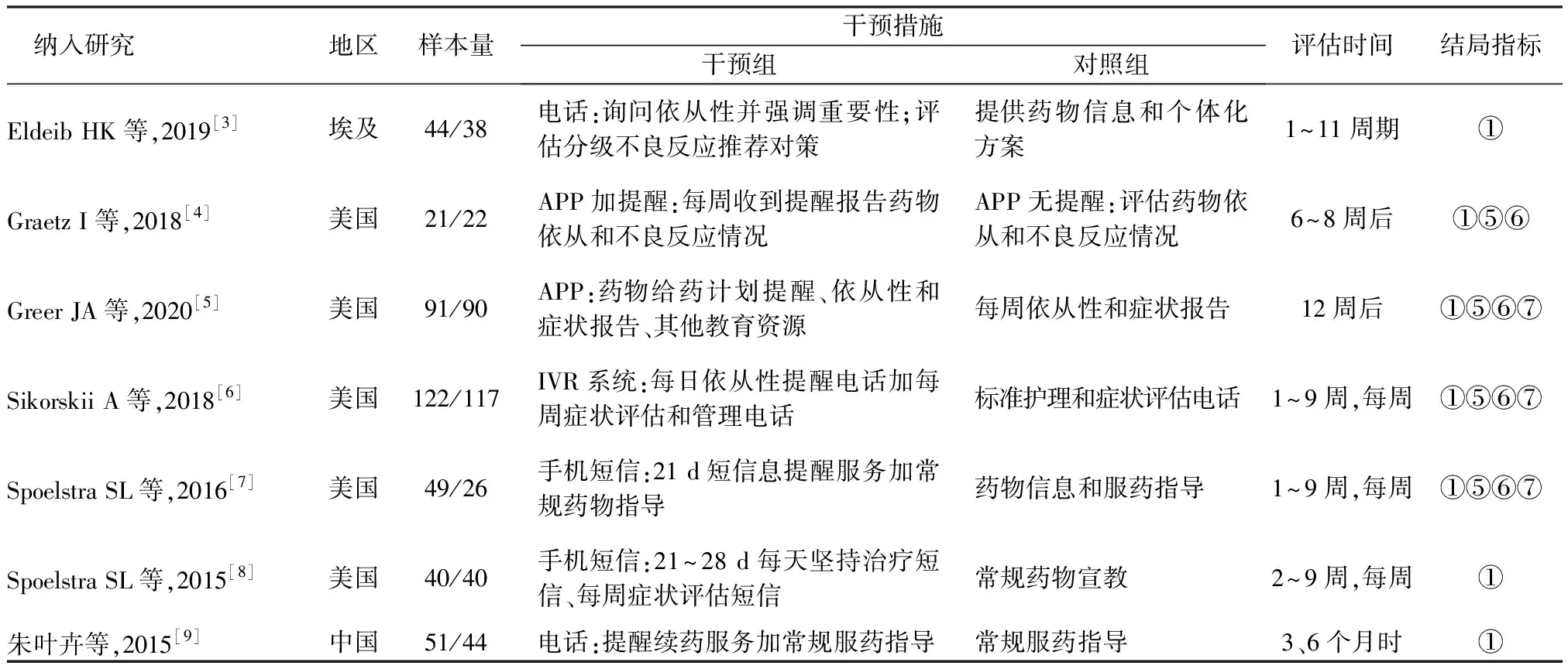
表1 纳入文献的详细资料
2.2纳入文献的质量 纳入的7篇文献方法学质量评价均为B级,见表2。
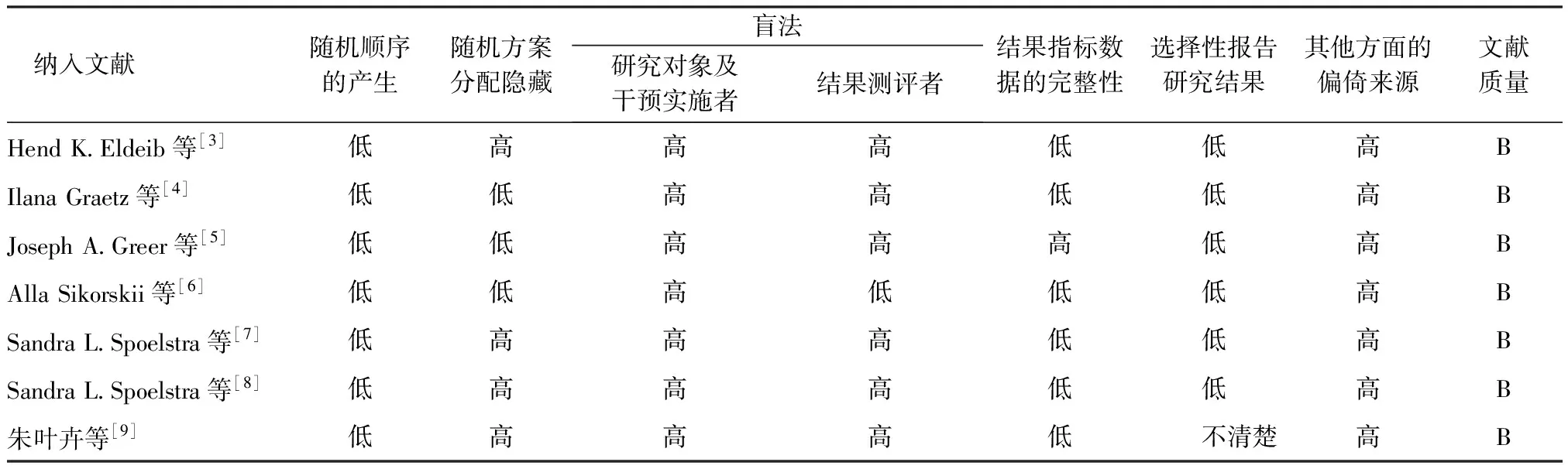
表2 纳入文献的方法学质量
2.3研究结果
2.3.1对药物依从性的影响 本次研究纳入的7篇文献中,采用了4种不同的方式测量药物依从性,但每种结局指标的呈现方式不同或数据不完整,只可进行描述性分析。药片计数法即要求患者在评估时间计算药盒中的剩余药量,根据推算来评价是否有漏服等依从性不良的情况。在此次系统评价中,有2项研究[3,7]采用药片计数法衡量依从性的情况,但因统计方法不同,无法进行合并分析。一项研究[3]存在选择性报告,仅通过文字描述可得患者总体依从性无显著差异(P=0.354),干预组的依从性在第11周期显著高于对照组(P=0.046)。在另外一项研究[7]中,作者采用依从人数/总人数×100%来计算依从率,研究结果显示,干预组仅在第7周和退出时依从率高于对照组。但变化趋势显示,随着时间的推移,对照组的依从性下降,而干预组随着时间的推移依从性上升。药物依从性量表是最早被广泛使用测量服药依从性的量表,主要通过患者回忆在过去一段时间内的服药情况来确定患者的依从性。有2项研究[4-5]采用量表的形式测量患者的服药依从性,因2项研究对结局的表现形式不同,故无法进行同质性分析。其中一项研究[4]显示,与APP组相比,APP+提醒组有更好的依从性,呈现显著性差异(P<0.05),即在研究结束时,100%的APP+提醒组参与者报告有良好的依从性,而相比之下,APP组参与者只有72.7%的患者报告依从性良好。在另外一项研究中[5],总体上2组依从性无显著差异,但针对基线测量时存在药物依从性问题的亚组患者来说,分配到移动应用程序组比分配到标准治疗组的患者平均依从性更好(分别为86.23%和63.94%;P=0.034)。
另3项研究[6-8]采用多学科协作的测量方式,考虑到服药过程中医生根据病情进行的剂量调整,结合药剂科的处方剂量,计算相对剂量强度(RDI)值,即服用剂量与处方剂量的比率×100%,RDI<0.8则通常被作为不依从的标准。在这几项研究中,一项研究[7]因未获得患者完整的自我报告和医疗记录文件的剂量变化,未对此指标的结果给予描述。另外2项研究结局指标的呈现方式不同,不强行进行同质性分析。在Sikorskii A[6]的研究中,只有1例患者在第4周出现依从不足(RDI<0.8);8例患者(对照组和干预组各4例)在第8周不依从;在第12周,没有患者不依从,2组之间无显著性差异,且2组长期维持高RDI的状态。在Spoelstra S L[8]的研究中,作者仅用依从率展示干预结果,显示2组之间无统计学意义(P>0.05)。药物占有比(MPR),即治疗期间所获药物治疗的天数/治疗的总天数×100%。MPR的范围为0~100%,此值越高说明服药依从性越好。在本次纳入的中文文献中[9],作者采用MPR值呈现患者的服药依从性情况。借助电话随访的干预形式,干预组和对照组患者的依从性在3个月和6个月时都存在显著差异(P=0.022,P=0.040)。且随着干预时间的增加,干预组患者的MPR呈稳定略升的趋势,而对照组略呈下降趋势。
2.3.2对药物不良反应的影响 3项研究以不良反应数量为结局指标,研究间有统计学异质性(P<0.000 01,I2=100%),采用随机效应模型进行。见图2。3项研究以不良反应的严重程度为结局指标,研究间有统计学异质性(P<0.000 01,I2=95%),采用随机效应模型进行。见图3。2项研究以不良反应的干扰程度为结局指标,研究间有统计学异质性(P<0.000 01,I2=78%),采用随机效应模型进行。见图4。

图2 移动应用实施与否对患者不良反应发生数量的Meta分析结果图
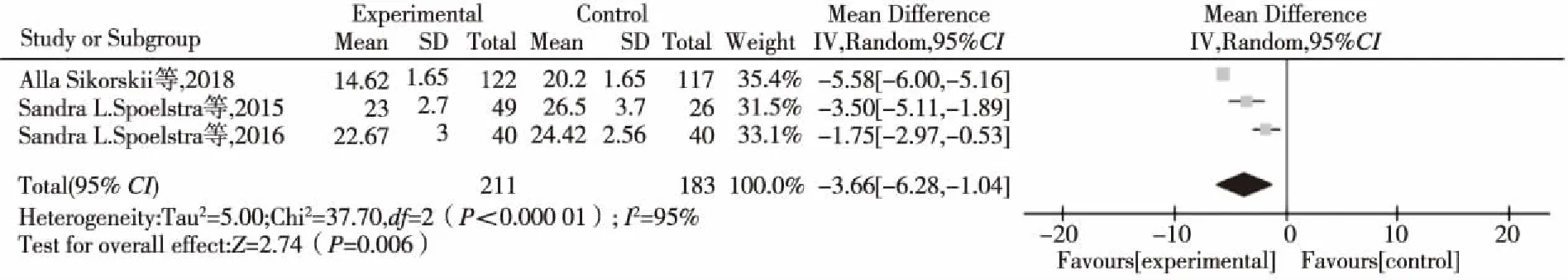
图3 移动应用实施与否对患者不良反应发生的严重程度的Meta分析结果图
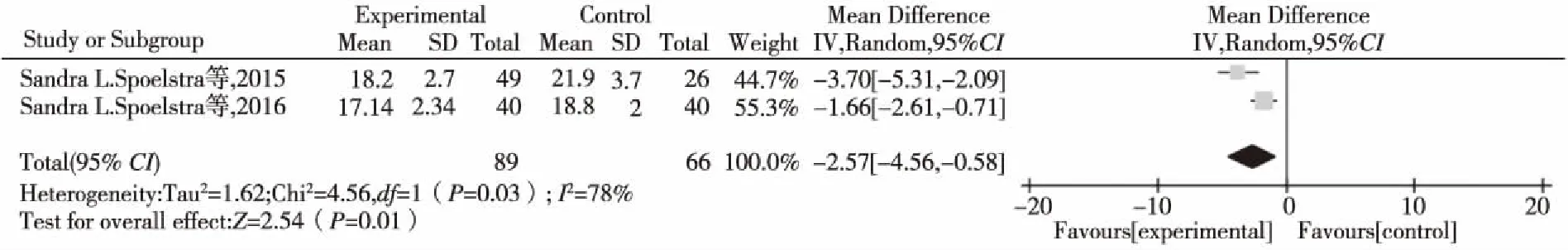
图4 移动应用实施与否对患者不良反应的干扰程度的Meta分析结果图
3 讨论
3.1对药物依从性的影响效果 相对于常规护理组,移动应用干预下仅有2项研究[4,9]显示在干预结束时,干预组的依从性高于对照组,存在显著性差异。其余5项均显示,2组患者的总体依从性无显著差异。分析原因如下:目前只有2项研究显示总体依从性有显著差异,但该种情况可能与患者在一开始就具备良好的服药依从性有关。在Greer J A[5]的研究中,针对基线测量时存在药物依从性问题的亚组患者来说,分配到移动应用程序组的患者比分配到标准治疗组的患者平均依从性更好(分别为86.23%和63.94%;P=0.034)。随着时间的推移,2项研究[7,9]均显示对照组的依从性下降,而干预组随着时间的推移依从性上升。该情况可能是由于后续药物毒性症状和治疗效果的影响,不加以干预的对照组患者依从性会随即下降。因此,若移动干预重点针对已存在或即将出现依从性问题的患者,这将在一定程度上提高移动应用干预的有效性,保证资源的有效利用率。但目前几乎没有证据表明:哪些患者、癌症类型和治疗特征与依从性的早期下降有关;此外,从成本效益上考虑,什么程度的干预即可让居家癌症患者恢复或维持较好的依从性,也无明确证据支持。未来还需深入探讨癌症患者居家口服抗癌药物依从性变化的特征。
药物依从性的测量方法众多,不同的测量方法各有侧重点。Eldeib H K[3]阐述药片计数较MEMS(medication event monitoring system,服药监控系统,例如电子药瓶)可能高估依从性,同时也有学者[7]解释自我报告药片计数由于记忆偏差、社会期望偏差和自我观察错误,存在高估依从性的问题,导致结果统计不准确。但另一项研究[4]则表示,通过依从性量表自我报告来衡量依从性,不如电子监控系统或药片计数可靠。因此,何种测量方式能够最准确反映患者依从性的真实情况有待进一步探究。RDI(相对剂量强度)的测定,结合处方中药物剂量的变化,动态评估患者的依从性,更具有灵活性,但在评估相对剂量强度时,我们很难从药房配药记录中获得客观数据,以确定肿瘤学家是否增加、减少或停止了口服抗癌药物的剂量。因此,充分发挥多学科协作模式的优越性,与医师、药房合作,准确获悉患者药物剂量的变化,将在最大程度上发挥RDI测量的优越性。
在纳入的7项研究中,仅一项研究[7]样本量超过了200例,其余研究样本量较小,3项研究[4,7-8]为大规模随机对照试验前期的试点或可行性研究,在此条件下则可能出现2组患者依从性差异不显著的情况。纳入的国外研究中,干预时间至多12周,以上研究结果可能与干预时长不够有关。患者初接受治疗时,对药物疗效充满信心,依从性可能较好,但受到疗效不佳的影响,患者的依从性可能下降。因此延长干预时间,探索移动应用在较长一段时间内对依从性的干预效果,将在一定程度上补充现有的证据。
3.2对药物不良反应的影响效果 不良反应的测量,通常从不良反应的数量、严重程度、干扰程度3方面综合考量。分析结果显示,干预组和对照组的不良反应数量间不存在差异。抗癌药物由于其毒性,不良反应的发生率因人而异,而移动应用无法从根本上减少发生不良反应的种类。在严重程度和干扰程度上,移动应用显示出了其有效性,打破了时间和空间距离,定时电话或APP进行症状评估,并根据症状严重程度给予合适的症状管理工具包,可以及时遏制不良反应的发展,及时的医护反馈在心理上和身体上都能减少症状对患者的持续影响。但由图3和图4可知,I2均>50%,研究之间有较大的异质性,可能是因为其中2项研究[7-8]仅为小样本试验,与另外一项大样本干预研究之间样本量差距较大。因此,将来还需进一步开展多中心、大样本随机对照试验来验证移动应用在居家口服抗癌药物不良反应方面的有效性。
综上所述,本研究未得出移动应用对癌症患者居家口服抗癌药物依从性影响的一致结论。未来可不断获取最新结果来更新此次的不一致结论。本次纳入的研究多来自于国外,国内学者在开展此类研究时,需考虑尽可能纳入更多样本,观察干预措施在较长周期内的干预效果;合理选择结局指标,正确分析药物依从性变化的趋势和规律,旨在及时、有效、经济地采用移动应用方式,对居家口服抗癌药的患者实施精准干预。
