成人型卵巢颗粒细胞瘤腹膜后复发一例并文献复习
2022-02-17徐朝辉任延英曲慧张帆陈鑫
徐朝辉,任延英,曲慧,张帆,陈鑫
1.大连医科大学附属第二医院疝与结直肠外科,辽宁 大连 116023;2.大连医科大学,辽宁 大连 116044
卵巢颗粒细胞瘤(granulosa cell tumor of ovary,GCT)是相对罕见的卵巢低度恶性肿瘤,占所有卵巢肿瘤的2%~8%[1-2],整体复发率为6%~50%[3]。根据其病理组织形态,可分为成人型颗粒细胞瘤(adult type granulosa cell tumor,AGCT)及幼年型颗粒细胞瘤(juvenile type granulosa cell tumor,JGCT)两种。GCT是病因不明的惰性肿瘤,预后较好,5年总生存率为80%~97%[4],但临床有晚期复发的特点。2020年大连医科大学附属第二医院手术治疗GCT腹膜后复发1例,现报道如下并复习相关文献。
病 例 资 料
病人:女性,56岁,因“右上腹部不适7 d,发现腹腔内肿物1 d”于2020年6月13日收治我科。病人2006年曾于大连市妇产医院行卵巢肿瘤切除手术,术后病理证实:右侧GCT、子宫平滑肌瘤伴红色变性。术后未行其他治疗。本次入院后体检:一般状态可,全身体表淋巴结未见肿大,心、肺阴性。右上腹可触及一约拳头大小包块,边界欠清,活动度差,局部压痛。影像学检查:(1)肝胆脾胰彩超:右上腹紧邻肝脏及右肾见一混合回声,范围约11.5 cm×6.7 cm,边界尚清,形态规则,以实性为主,内部及周边可见血流信号。(2)腹盆腔增强CT:胰腺头部后方见囊实性不均匀性混杂密度影,最大层面约为10 cm×8 cm,增强扫描其实性区显示明显不均匀强化,周围结构受推压、移位改变(图1)。为明确腹腔内占位病变性质,行CT引导下腹腔内肿物穿刺活检术,病理提示性索间质细胞瘤,考虑颗粒细胞瘤(成人型)。
病人于2020年6月29日全身麻醉下行腹膜后巨大肿物切除术+输尿管镜下右侧输尿管D-J管置入术。考虑腹膜后巨大肿瘤与右侧输尿管关系密切,为避免术中损伤右侧输尿管,故麻醉后先经输尿管镜右输尿管内置入D-J管。探查见肿物位于后腹膜,大小约12 cm×11 cm×7 cm,肿物底部深达下腔静脉表面,内侧为肠系膜上静脉外侧,肿瘤无腹盆腔内种植及转移。打开升结肠外侧腹膜及十二指肠外侧腹膜至肿瘤表面,可见肿瘤表面存在包膜,分别沿着肾脂肪囊表面、横结肠系膜无血管区及肿物包膜处行钝性及锐性分离结扎并离断肿瘤内侧及根部数支供血血管,止血可靠,肿物完整切除后送病理检测(大体标本见图2)。本例标本经4%中性甲醛液固定后常规HE染色,光镜下观察。免疫组织化学采用Envision法于全自动免疫组织化学仪进行检测,主要试剂选用兔抗人雌激素受体(estrogen receptor,ER)单克隆抗体(工作液,克隆号:SP1),兔抗人孕激素受体(progesterone receptor,PR)单克隆抗体(工作液,克隆号:1E2),兔抗人增殖细胞相关核抗原(Ki67)单克隆抗体(工作液,克隆号:30-9),由上海罗氏制药有限公司提供;鼠抗人上皮膜抗原(epithelial membrane antigen,EMA)单克隆抗体(工作液,克隆号:GP1.4),鼠抗人抑制素(Inhibin-α)单克隆抗体(工作液,克隆号: AMY82),由北京中杉金桥生物技术有限公司提供。HE染色镜检:纤维组织内见肿瘤细胞呈巢状排列,细胞核卵圆形至多角形,细胞形态尚温和,核膜清晰,核仁明显,可见核沟,细胞胞质透亮或嗜酸性,伴出血、坏死及囊性变。免疫表型: ER(+),PR(+),Inhibin-α(+),EMA(-),Ki67(10%~20% +)。特殊染色结果:网织纤维染色(团巢周围+)(图3)。诊断:腹腔复发型颗粒细胞瘤(成人型)。手术过程顺利,恢复良好,术后第5天痊愈出院。术后2个月拔除右输尿管D-J管。术后3个月、6个月、12个月腹部CT见图4,随访至今,未见复发转移,未诉不适。
讨 论
根据中英文数据库的检索结果显示,GCT大部分原发病灶常常局限于卵巢,手术切除后预后较好,5年总生存率可达90%[3-6]。
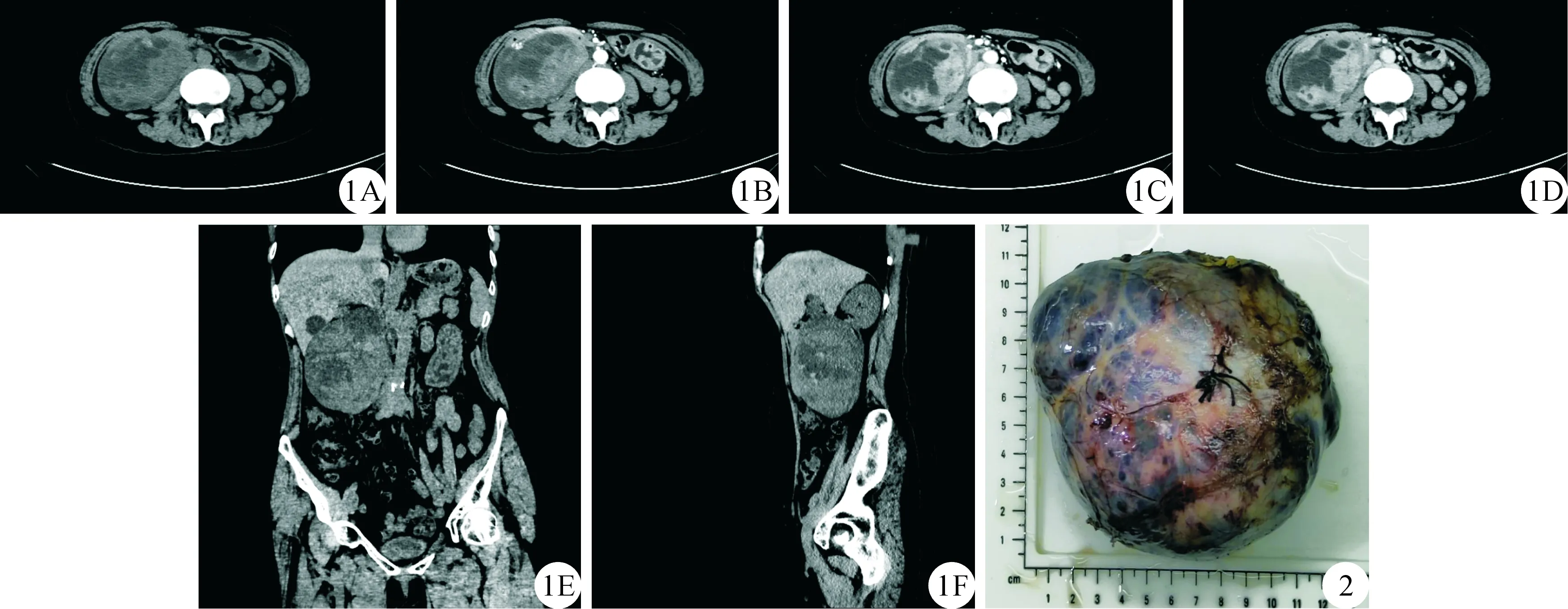
图1 术前增强CT A.平扫;B.动脉期;C.静脉期;D.延迟期;E.冠状位;F.矢状位 图2 术中大体标本 肿物位于后腹膜,大小约12 cm×11 cm×7 cm
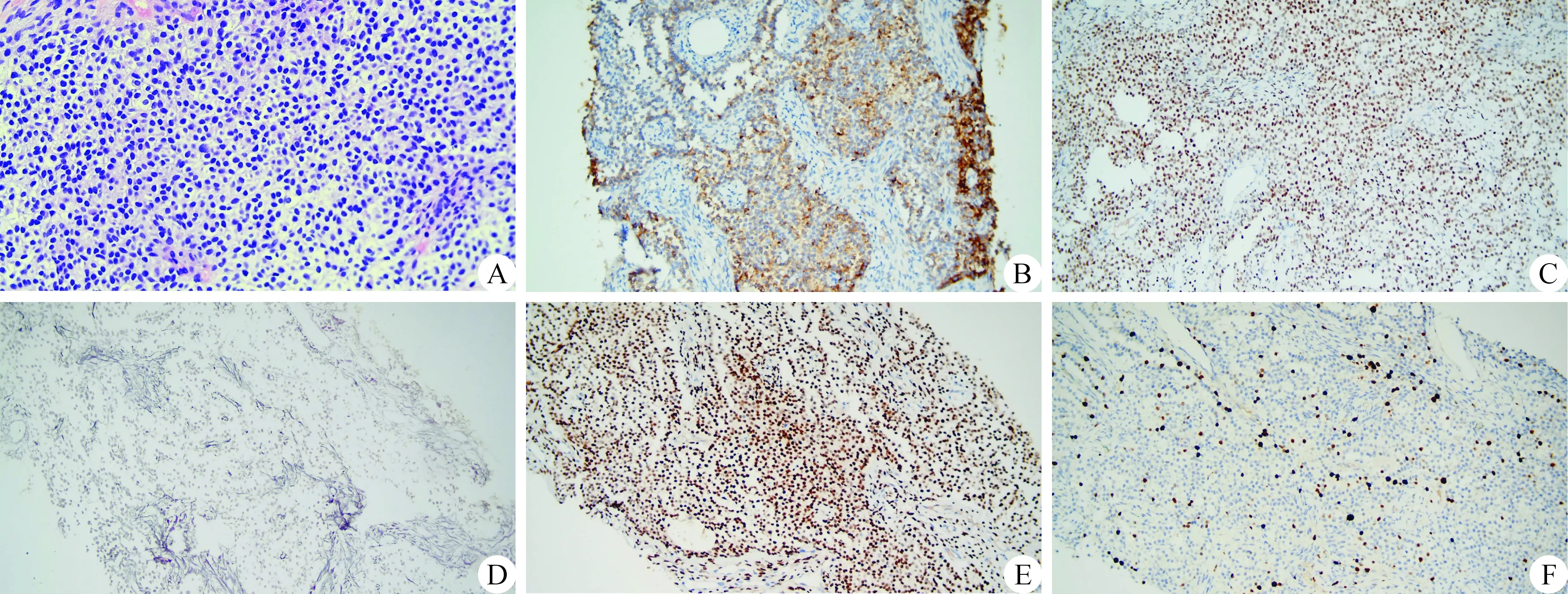
图3 术后HE染色(×400)及免疫组织化学(×200)结果 图A~F分别为HE染色、Inhibin-α(+)、雌激素受体(ER)(+)、网织纤维染色(团巢周围+)、孕激素受体(PR)(+)、Ki67(10%~20% +)
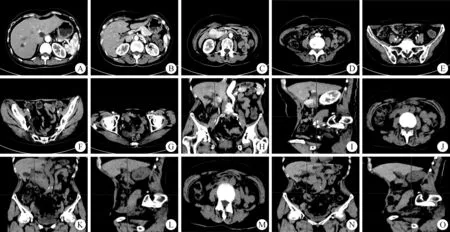
图4 术后CT检查未见复发转移 术后3个月(A~G.横轴位;H.冠状位;I.矢状位);术后6个月(J.横轴位;K.冠状位;L.矢状位);术后12个月(M.横轴位;N.冠状位;O.矢状位)
复发已成为本病治疗失败的最主要原因。据统计,20%的Ⅰ期病人在20年后复发,甚至出现多次复发或多个部位同时受累的情况,复发后预后较前明显下降[7]。Nathalie等[8]报道了1例原发肿瘤切除术后40年盆腔内复发的病例,这是目前已知最长时间的复发病例。目前国内外相关报道较为局限,对其临床特点等认知相对有所欠缺,故本文通过少见的AGCT切除术后腹膜后复发的报道,结合既往文献归纳相关知识,以期为规范诊疗提供借鉴。
复发后病人常以因肿瘤增大而引起的腹痛、腹胀、腹部不适等非特异性症状及CT意外发现而就诊,本例病人即偶因腹部症状于体检时发现,严重者甚至可出现自发性的囊性肿瘤破裂出血[9]。AGCT的复发路径与上皮性卵巢癌相似,多局限于盆腔,但也可随着血行转移到肝脏、心脏、肺、骨、脾,腹膜后转移,腹膜种植到肝周、膈肌、大网膜、小肠系膜等部位[4,10]。综上所述,AGCT具有晚期复发、复发时无特异表现、可多次或多部位复发及复发后预后差的临床特点,这种不可预测的行为,使病人的管理趋于复杂化,也表明了对AGCT病人密切监测、延长随访甚至终生随访的必要性。对有此病史者应定期复查,以利于早期发现和早期手术,减少病人的损伤。
国内学者[11]根据肿瘤成分将GCT分为囊性、囊实性和实性为主性肿块,其分型主要受肿瘤大小和血供的影响。一般认为,早期肿瘤较小且富含血供,不容易坏死囊变故多以实性为主。而本例病人即属囊实性类圆形肿块,增强CT显示实性区明显不均匀强化,大体标本可见完整包膜,表面及边缘光整,质韧,内可见多处出血、坏死和囊性变,符合颗粒细胞瘤的特点。复发性颗粒细胞瘤的鉴别应包括类癌、小细胞癌、未分化癌、卵巢上皮样癌和间质瘤等,ER、PR、Inhibin-α、EMA、CD99等相互结合有助于鉴别此病[12]。典型的成人型颗粒细胞呈卵圆形,具有特征性的纵行核沟,含菊形团状结构(Call-Exner小体),周围可见网状纤维分布[13]。相比于其他免疫标记,抗苗勒激素(anti-Müllerian hormone,AMH)和Inhibin-α在AGCT的评估、随访及复发中具有重要价值,且发现其水平与复发疾病的严重程度呈正相关[14-16],其有望成为本病有价值的肿瘤标志物。
由于其发病率较低,且多以小型报道为主,治疗方法上目前并无特殊进展。Zhao等[17]学者认为无进展生存期(PFS)>61个月和复发后治疗方式是二次复发的独立危险因素。具体来讲,PFS长或完整切除复发灶联合辅助化疗的病人,复发后预后好。另有研究指出,年龄、肿瘤分期、核分裂象与异型性等可能是有效的复发预测因子,定期随访中应重视此类高危人群。肖会廷等[18]报道了13例复发型AGCT病人,9例行手术治疗,中位生存时间为27个月(其中3例死于二次复发,2例复发后仍无瘤生存,4例死于其他原因),明显优于保守治疗病人(中位生存时间仅为10.5个月)。同样,Chua等[19]报道了5例复发病人再次手术治疗后的无瘤生存时间为10~95个月。由此,最大程度的减瘤手术仍是AGCT病人复发乃至多次复发最重要的治疗手段,积极手术有助于改善症状和延长生命[13,20]。而手术范围根据生育情况、年龄及临床期别的不同亦有区别。多项研究表明[6,21-23],常规放化疗及激素治疗或许不能减少局部复发和转移率,但能限制疾病进展和延长远期生存率,具有一定的价值,但缺乏高级别的证据支持,故临床应用仍需慎重。
综上所述,AGCT具有“晚期复发、多部位复发”的特征,应坚持长期随访,CT有助于诊断,必要时可行穿刺确诊。发生腹膜后转移时仍应采取积极的手术治疗,使病人再次达到长期的无病生存,改善预后。未来仍需要更多的实验和流行病学数据,使该病呈现全貌。
利益冲突所有作者均声明不存在利益冲突
