典型腐蚀介质中阴离子对镁合金腐蚀行为影响的研究进展
2022-02-16王保杰
许 凯, 王保杰, 孙 杰
(沈阳理工大学环境与化学工程学院, 辽宁 沈阳 110159)
0 前 言
镁是一种银白色的金属,原子序数为12,其密度为1.738 g/cm3。 镁元素在地壳中分布较为广泛,金属镁以其密度低、比强度高、比刚度高[1]、阻尼性好、导热性好以及减振性好等特性[2-4],逐渐在现代化工、机械生产中占据重要地位。 金属镁的生产方法主要有氯化熔盐电解法[5]、热还原法[6]。 镁在标准大气压下是密排六方结构,其标准电极电位为-2.37 V,是电负性很强的金属。 为了提高镁的物理、化学及工艺性能,通常在纯镁中添加合金化元素与镁形成固溶体[7,8]。 比如Mg-Li合金中金属锂的加入使其具有了较低的密度和较强的塑性变形能力。 但也会引发工程强度低的问题,这可以通过合金化、热处理和机械大变形等解决[9,10]。 镁合金通常根据合金化组元的不同划分为二元、三元及多元合金体系,主要包括Mg-Al、Mg-Li、Mg-Zn、Mg-RE 等合金系,其被誉为“二十一世纪绿色工程材料[11-13],在汽车、电子[14]、电器、航空航天、国防军工[15]、交通等领域有着广泛的应用需求与价值[16-18]。从国际上看,我国是世界上镁资源最为丰富的国家之一,作为镁主要来源的白云石、菱镁矿等矿石[19],其探明储量高达50 亿吨,略低于俄罗斯,位居世界第二[20]。
镁是不可再生资源,为了减少由于自然环境或是人为因素而导致金属镁的损耗,对镁合金材料腐蚀行为的研究也就变得十分迫切。 镁合金的腐蚀类型可以概括为全面腐蚀和局部腐蚀[21]。 全面腐蚀是指镁合金在水溶液以及典型腐蚀介质中出现全表面或大部分表面被腐蚀的现象。 局部腐蚀就是镁合金表面只有一部分被腐蚀,主要类型有点蚀、丝状腐蚀、缝隙腐蚀等[22]。局部腐蚀主要发生在镁合金表面氧化膜的脆弱处,是膜层连续性遭到破坏处,主要为杂质、非金属夹杂物或者膜层本身的物理缺陷。 镁合金具有活泼的化学性质,即使在空气中也会发生腐蚀。 而在溶液中镁合金的腐蚀机制是一种电化学过程,会在其表面生成一种氧化膜,这种膜层对镁合金具有一定的防护作用[23],发生腐蚀的阳极及阴极反应如下[24,25]:
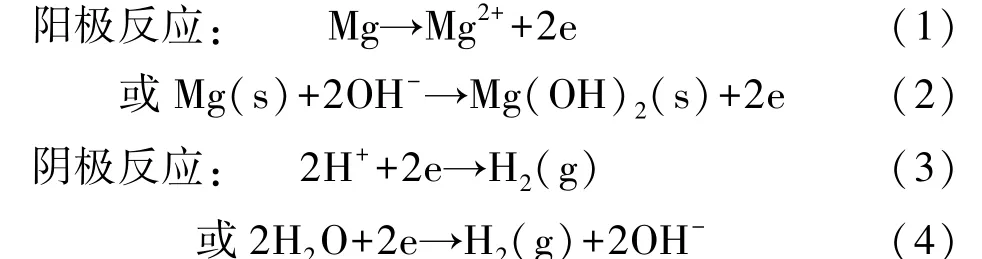
为了更好地防止镁合金因腐蚀造成的金属材料浪费,必须先了解其在典型腐蚀介质中的腐蚀行为。 本文主要介绍镁合金在含有氯离子、磷酸根离子、碳酸根离子、硫酸根离子溶液中的腐蚀行为。
1 镁合金在氯离子溶液中的腐蚀行为
在自然界中,氯元素主要是以化合态广泛分布在海水、盐湖等环境中,Cl-具有半径小、吸附能力强的特点,可以轻易地穿过膜层缝隙或者吸附在金属表面,并将氧化膜中氧排掉,使得表面膜层被破坏,加速腐蚀。由于Mg 较为活泼及电极电位较低的化学性质,其在空气中表面会生成具有一定防护作用的氧化膜。 将镁合金置于含有Cl-溶液中,其表面所形成的氧化膜会被破坏掉,从而使得镁合金的耐蚀性下降。 对于镁合金的腐蚀行为来说,在含有Cl-的腐蚀介质中Cl-的浓度、溶液的pH 值及阳离子的不同均存在一定的影响。 腐蚀介质中Cl-浓度增大,致使合金的腐蚀电位降低,腐蚀电流密度提高,Cl-对膜层的破坏就愈发严重,使本应该随时间延长而降低的腐蚀速率提高了,甚至由于其腐蚀产物在晶界处堆积产生应力,出现腐蚀开裂现象。汪利娜等[26]通过研究AZ61 镁合金在NaCl 溶液中的腐蚀行为,发现NaCl 浓度增加会使本应该随时间延长而降低的腐蚀速率提高了,使其腐蚀程度加深。 景霞[27]通过电化学测试对不同Cl-浓度下AZ40 镁合金的腐蚀行为进行了研究,发现腐蚀介质中Cl-浓度增加会降低AZ40 镁合金的开路电位(开路电位从相对于SCE 的-1.50 V 降低到-1.59 V),增大其腐蚀电流密度(如图1 所示),但是会形成具有一定防护作用的腐蚀产物阻挡层。

图1 AZ40 镁合金在不同浓度NaCl 介质中的自腐蚀电位变化曲线和极化曲线[27]Fig. 1 Corrosion potential curves and polarization curves of AZ40 magnesium alloy in NaCl solution with different concentrations[27]
张汉茹等[28]研究了不同浓度的NaCl 溶液对AZ91D 镁合金腐蚀形貌的影响,发现AZ91D 镁合金在相同的盐浴时间下随NaCl 浓度改变其腐蚀程度存在差异,在4 d 时合金表面均已经形成全面腐蚀,3.5%和10.0%NaCl 浓度下均出现了腐蚀开裂,且后者较为严重。 Liu 等[29]研究了AM60 镁合金在NaCl 溶液中的腐蚀行为,电化学试验结果表明AM60 镁合金的耐腐蚀性随腐蚀介质中Cl-浓度增加逐渐降低,腐蚀局部化程度更严重,提出了一个腐蚀模型来解释Cl-浓度的影响(如图2 所示)。 根据模型得出,镁合金浸入溶液中,会使得表面薄而致密的MgO 膜转化成Mg(OH)2,同时空气中CO2溶解于溶液,与镁合金表面的Mg(OH)2形成MgCO3[30],溶液中Cl-也会吸附在镁合金表面发生反应生成可溶性的MgCl2,破坏了表面Mg(OH)2膜层[31]。当Cl-浓度为0.01 mol/L 时,由于吸附Cl-较少,被破坏膜层处会迅速生成MgCO3,阻止了腐蚀的进一步发展。当Cl-浓度升高,使得表面膜层的破坏不能得到MgCO3的及时补偿,导致腐蚀加速进行。
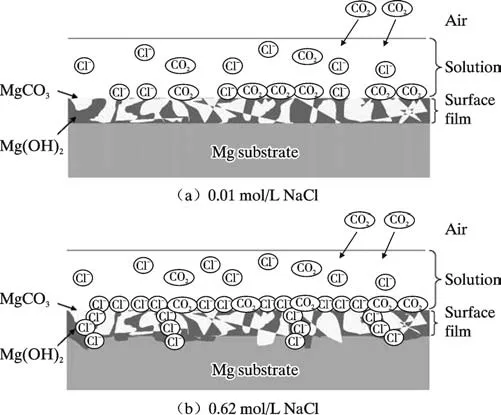
图2 AM60 镁合金的腐蚀模型[29]Fig. 2 Corrosion model of AM60[29]
镁合金在含有Cl-的腐蚀介质中时,阳离子的种类不同也会引起Cl-对镁合金腐蚀行为的变化。 Ca2+会在其表面腐蚀产物中形成Ca(OH)2沉淀,从而减小阳极的合金面积,形成小阳极大阴极的电化学反应机制,导致阳极电流密度集中,加速镁合金的腐蚀。 尹少荣等[32]使用电化学极化曲线和阻抗谱等方法研究了在含有不同阳离子的氯盐中AZ91D 镁合金的腐蚀速率的变化,发现在腐蚀发生的初期,腐蚀速率大小顺序是NH4Cl>NaCl>CaCl2。
在含有Cl-的腐蚀介质中酸碱度对镁合金的腐蚀行为也会造成一定的影响。 在碱性环境中,镁合金的腐蚀速率逐渐降低,其表面会形成一层保护性膜层,提高其耐腐蚀能力,随着pH 值的增加,镁合金的腐蚀电位增大,镁合金表面在弱碱性NaCl 介质中形成腐蚀产物膜,在强碱性NaCl 介质中形成钝化膜,防护性逐渐提高;而在酸性环境中,随着pH 值的降低,镁合金的腐蚀速率增大,腐蚀程度加深,最终出现腐蚀开裂现象。黄晓梅等[33]用电化学方法对镁与Mg-15Li 合金在碱性NaCl 溶液中的腐蚀行为进行了比较,发现在弱碱性环境中镁合金表面生成腐蚀产物膜,相比于纯镁的腐蚀坑大而深,Mg-15Li合金的腐蚀特点表现为全面点腐蚀。 在Cl-浓度低于0.4 mol/L 的强碱性环境中,Mg-15Li合金表面会形成稳定的钝化膜,提高Cl-浓度将导致镁锂合金的点蚀电位降低[34]。
马全友等[35]采用电化学方法对AZ91D 镁合金在碱性含Cl-环境下的腐蚀行为进行了研究,发现在碱性环境中镁合金的开路电位提高,且随溶液的pH 值增大,开路电位升高,镁合金的耐蚀性增强。 在pH 值为9 的情况下镁合金生成的腐蚀产物膜层的防护性较弱,而在pH 值为12 的溶液中,镁合金表面生成稳定的钝化膜,其防护性较强。 随吸附在膜层表面Cl-浓度的增加其稳定性逐渐降低,进而破坏钝化膜。 AZ91D 镁合金在碱性环境中主要发生式(2)、(4)及如下反应:

同样,对于酸性环境,随着Cl-浓度的增加,镁合金的开路电位降低,阻抗减小,腐蚀电流密度增大。 H+的浓度越大,镁合金的腐蚀就越严重,在pH =2 时出现了腐蚀开裂的迹象,腐蚀产物为MgO 和Mg(OH)2。AZ91D 镁合金在酸性环境中主要发生为式(1)、(3)以及如下反应[36]:

不同成分的镁合金在含有Cl-的腐蚀介质中,耐蚀性均有所不同,其差异主要与每一种合金的成分种类、含量、成分分布是否均匀及金属间化合物的分布情况、晶粒尺寸等有关。 Cheng 等[37]研究了AZ31、AZ91、AM60 和ZK60 4 种轧制镁合金在1 mol/L NaCl 溶液中的腐蚀行为,发现ZK60 镁合金最耐蚀,其次是AM60、AZ31,最差的是AZ91。 ZK60 镁合金的耐蚀性最佳主要是由于Zn 的标准电极电位较低,而且合金中的锆元素能细化晶粒并且可与合金中的Fe、Si 元素形成金属间化合物。 Nguyen[38]研究了Mg-5Al、Mg-5Al-1Sn、Mg-5Al-1Mn、Mg-5Al-1Zn 4 种镁合金在3.5%NaCl 溶液中的腐蚀行为,发现合金元素的添加使得合金晶粒尺寸减小,增加了表面活性原子数量,加速了保护层的形成,并抑制了阴极析氢反应,使腐蚀电流密度降低,减缓了合金的腐蚀速率。
近些年,为了更广泛地应用镁合金,研究人员将对其进行合金化处理作为主要探索方向。 主要是通过向镁合金中添加合金化元素以改变合金的微观结构,一般是生成新的金属间化合物,细化金属晶粒,均匀化耐蚀相,减少金属中的位错孪晶等,以阻止局部点状腐蚀的生长,提高表面腐蚀产物膜的稳定性,减少合金表面的电偶腐蚀,从而提高合金在Cl-介质中的耐蚀性。 Hu等[39]研究了添加Sm 元素对AZ91 镁合金在含有0.1 mol/L NaCl 溶液中腐蚀行为的影响,发现添加的Sm 元素会与合金中的Al 元素结合生成金属间化合物Al2Sm,使得合金中β 相面积分数降低,镁合金在0.1 mol/L NaCl 中浸泡3 h 的局部腐蚀点尺寸减小。 Srinivasan 等[40]通过向添加了Si 元素的AZ91 镁合金中再次添加Sb 元素,发现改变了金属间化合物Mg2Si 的结构,呈现出沿晶界均匀分布的细小多边形,提高了其在3.5%NaCl 溶液中的耐蚀性。 Li 等[41]在热挤压AZ31镁合金中添加Sm 元素使合金结构中位错、孪晶均有所减少,并通过失重法发现其在3.5%NaCl 溶液中的腐蚀速率降低,腐蚀电位升高,局部点蚀面积减小且点蚀坑较浅。 Li 等[42]研究了添加Y 元素的AZ63 镁合金在3.5%NaCl 中的腐蚀行为,发现Y 的添加提高了氧化层中Al2O3的含量,并且使金属间相变得离散化,减轻了微电偶腐蚀,Y 合金化有效降低了AZ63 镁合金的腐蚀速率。 Jia 等[43]研究了准晶相的添加对Mg-50Zn-5Y合金的腐蚀性能的影响,发现添加6%的准晶相使合金拥有最小的晶粒尺寸及析出相颗粒,使得微耦合腐蚀更加分散,提高了耐蚀性。 Liao 等[44]研究了不同晶粒大小的AZ31B 镁合金,发现晶粒越小,在0.1 mol/L NaCl 溶液中表面形成的膜层的击穿电位越大,膜层越稳定,耐蚀性越好。
除了在镁合金中添加合金元素,还可以通过如轧制、电子束处理、喷丸处理、均匀化处理、搅拌摩擦加工等技术改变合金的晶粒大小,或使合金微观结构均质化等,主要使合金快速在腐蚀环境中形成稳定膜层或是减少合金中的偏析、晶界共晶及缺陷,以提高其耐蚀性,目前的研究表明晶粒细化对金属耐蚀性的影响小于合金本身成分对耐蚀性的影响。 Pei 等[45]通过累积叠轧焊(ARB)技术使得AZ63 镁合金晶粒尺寸减小,Mg17Al12相体积分数降低,增强了在3.5%NaCl 环境中表面形成的氧化层的耐蚀性,减小了微电池腐蚀的效果。 Iranshahi 等[46]对铸态AZ91 镁合金进行电子束处理,合金组织出现晶粒减小且均匀分布的特征,在3.5%NaCl 溶液中由铸态合金的局部腐蚀转变为电子束处理之后合金的均匀腐蚀形式,并且形成的腐蚀产物膜层更具有保护性。 Liu 等[47]对经过剧烈喷丸处理的AZ31和AZ91 镁合金在3.5%NaCl 溶液中的腐蚀行为进行了研究,发现经过剧烈喷丸处理后表面的晶粒大小达到纳米级,AZ31 镁合金由于表面形成了致密膜层,耐蚀性有所提高,而AZ91 镁合金的耐蚀性变化不大,主要是由于其中的β 相对其腐蚀性能起到关键作用,而该研究的处理方式并未改变β 相的属性。 Naik 等[48]利用热处理的方式对AZ80 镁合金进行均匀化处理,使得合金中的三元相消失,而第二相以细颗粒的形式均匀分散,降低了其在NaCl 溶液中的腐蚀速率。 Hassani等[49]对AZ91C 镁合金进行搅拌摩擦处理,发现合金晶粒尺寸减小,微观结构均质化,能够更快地形成稳定膜层从而提高了其耐蚀性。 目前这些研究都主要集中在腐蚀性能的表征上,而对于其腐蚀原理的描述以及模型建立上仍需要更多研究。
2 镁合金在硫酸根离子溶液中的腐蚀行为


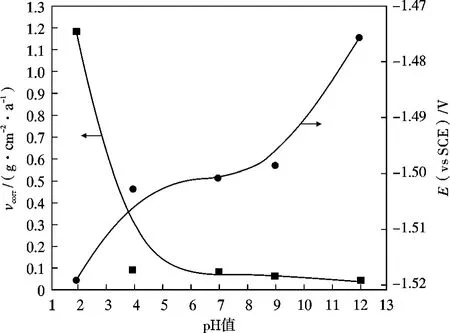
图3 在Na2SO4溶液中AZ91D 镁合金的电极电位和腐蚀速率与pH 值的关系[50]Fig. 3 The relationship between electrode potential/corrosion rate and pH value of AZ91D magnesium alloy in Na2SO4 solution [50]

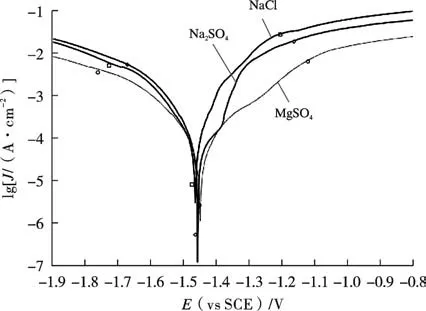
图4 压铸AZ91D 镁合金分别在0.6 mol/L NaCl、Na2SO4和MgSO4溶液中的极化曲线[56]Fig. 4 Polarization curves of die-cast AZ91D alloy in 0.6 mol/L NaCl, Na2SO4 and MgSO4 solutions[56]
向斌等[60]通过模拟不同pH 值酸雨的腐蚀介质的方法研究了AM60B 合金的腐蚀行为,发现AM60B 镁合金的腐蚀电位随pH 值的降低向负方向移动,阻抗谱容抗弧减小,合金的表面膜层的破坏程度增大,腐蚀电流密度升高,合金的腐蚀加速,腐蚀程度逐渐增大,其产物主要是MgO 和MgAl2(SO4)4·2H2O。 镁合金在酸雨环境中除了可发生式(1)和(3)反应,还可以在其表面发生式(10)~(13)反应[61]:
表面膜溶解过程:

3 镁合金在磷酸根离子溶液中的腐蚀行为
镁合金可与含有磷酸盐的溶液发生反应,在金属表面生成化学转化膜,这本质上是一种受控制的金属腐蚀过程[62]。 镁合金与P发生反应在其表面生成磷酸盐转化膜,能够阻止溶液继续腐蚀镁合金,具有良好的保护作用。 用不同成分的磷化液制得的磷酸盐转化膜差别很大,主要分为锰系磷化膜、锌系磷化膜、钡系磷化膜、钙系磷化膜[63]。


图5 AZ31 镁合金在含磷酸根离子的腐蚀介质中的开路电位-时间曲线[71]Fig. 5 Open circuit potential-time curve of AZ31 magnesium alloy in phosphate-containing corrosive medium[71]
镁合金的表面成膜原理是在浸入磷化溶液之后发生Mg 的溶解[72],作为微阴极区合金中β 相上析出氢气[73]如反应式(1)、(3),还有少许的Al 也会发生如下溶解反应:

析氢反应使得β 相附近溶液的pH 值升高,加快了磷化溶液的电离使得含磷的离子浓度升高,促进了磷化晶核的形成[74]、生长,最终形成膜层,其中主要的反应如下所示:

4 镁合金在碳酸根离子溶液中的腐蚀行为
Na2CO3可减缓镁合金的腐蚀过程,属于无机缓蚀剂。 目前,关于镁合金的相关研究较少。 镁合金在含CO23-的腐蚀介质中,随着CO23-浓度的增加,腐蚀速率减小,主要是由于腐蚀介质中含有CO23-,腐蚀产生的游离Mg2+与CO23-相结合,在金属表面形成了较为致密的碳酸镁膜层,抑制了点蚀的形成,有效地保护了镁合金,具有缓蚀的作用。 合金结构越均匀,晶粒尺寸越小,合金的耐蚀性也越好。 关景鑫等[75]研究了AZ91D镁合金在含Na2CO3的NaCl 溶液中的腐蚀行为,阻抗谱显示高频区的容抗弧随Na2CO3浓度的增加明显增大,说明电荷传递电阻增加从而抑制了镁合金的腐蚀,导致其腐蚀面积及腐蚀点逐渐减少,腐蚀速率越低,其缓蚀效果越好。 究其原因是生成了碳酸镁难溶沉淀物并在金属表面形成了一层薄膜。 沈长斌等[76]研究了Na2CO3对搅拌摩擦加工AZ31 镁合金的腐蚀行为的影响,发现搅拌摩擦加工使得合金晶粒尺寸减小、均匀化,在腐蚀介质中,随着Na2CO3浓度的增大,腐蚀电流密度逐渐减小且经过搅拌摩擦加工的合金耐蚀性更佳。 Prince 等[77]研究得出AZ31 镁合金在Na2CO3中的腐蚀受到了抑制作用,主要是由于在合金表面形成的碳酸镁膜层有效保护了合金基体。 主要发生式(5)及如下反应:
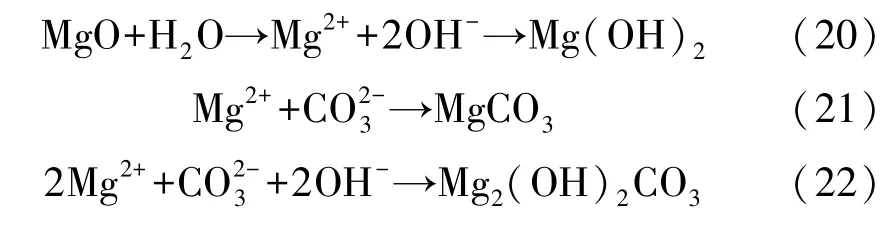
5 结束语
腐蚀行为的研究主要分为2 个方面:(1)由于合金的组织结构不同,在相同环境中的腐蚀行为存在差异;(2)腐蚀介质的不同造成合金的腐蚀行为存在一定差异。 针对镁合金腐蚀行为的研究也不例外,在合金结构方面,可以通过添加一些合金成分改变原来合金的晶粒大小、合金中的多元相含量及分布、稳定相的含量及分布;还可以通过轧制、挤压、搅拌摩擦处理、喷丸、电子束处理等技术手段改变合金或者合金表面的微观结构,以减小腐蚀介质中的微电偶腐蚀或者减慢腐蚀的发生,亦或是使腐蚀产物膜层更加致密稳定。 不同腐蚀介质中的离子也会导致镁合金的腐蚀行为不同,Cl-一般会使镁合金腐蚀加速,并破坏表面形成的膜层。S、P、C通常在镁合金表面形成具有保护性的膜层,降低合金的腐蚀速率。 溶液中的pH 值越大,腐蚀电位就会越大,腐蚀电流密度也会减小,腐蚀速率减慢,甚至会生成具有一定防护作用的膜层,提高合金的耐蚀性。 随着腐蚀介质温度的升高,腐蚀速率加快。腐蚀离子不同也会导致腐蚀行为存在差异。
目前对镁合金的腐蚀行为研究主要集中于合金在腐蚀介质环境中的腐蚀速率、腐蚀形貌、腐蚀产物、电化学腐蚀过程等腐蚀性能的表征,而对合金化工艺研究不足,多是进行单一元素合金化,缺少复合合金化对腐蚀行为影响的研究,并且在腐蚀机理上的研究不够系统、深入,有关不同合金化元素共存时对镁合金腐蚀行为的影响也缺乏认识,很少建立腐蚀模型对腐蚀机理进行解释,无法对以后镁合金的应用或者表面处理方法的改进提供指导。 近些年的研究也缺乏使用一些先进技术去认识镁合金的腐蚀机理,比如使用扫描振动参比电极技术、扫描开尔文探针测量技术、微区电化学阻抗技术、扫描电化学显微镜技术,这些技术可用于镁合金中局部腐蚀的机理和相组织腐蚀电化学的研究。
在不同的阴离子环境中,镁合金的腐蚀行为与其形成的腐蚀产物膜层有着密切联系,大力研究合金表面产物膜层结构及膜层生长过程十分重要。 腐蚀行为的研究可最终指明其腐蚀机理,进而提高镁合金材料的适用性,有利于镁合金的应用与开发,将来可以注重以下2 个方面的研究:(1)通过腐蚀膜层有效组分研究设计一种耐蚀性较强的镁合金;(2)根据腐蚀机理改进镁合金的表面处理工艺。
