在体单向肠灌流法研究胡黄连总苷中4个成分的大鼠肠吸收特性*
2022-02-07张琬靖曹宁宁李晓璇裴帅蔡楠肖学凤
张琬靖 ,曹宁宁 ,李晓璇 ,裴帅 ,蔡楠 ,肖学凤
(1.天津中医药大学中药学院,天津 301617;2.成都先导药物开发股份有限公司研发化学中心,四川 610200;3.天士力控股集团有限公司研究院现代中药开发中心,天津 300410)
胡黄连总苷是从玄参科植物胡黄连Picrorhiza scrophulariiflora Pennll的干燥根茎,经水提、大孔树脂分离后得到的有效部位。胡黄连总苷主要含胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ、草夹竹桃苷等成分[1],是天士力控股集团研究院在研的中药创新药,于2012年6月取得临床批件,临床定位于治疗非酒精性脂肪性肝炎。药理研究表明,胡黄连总苷具有降血脂、抗脂质过氧化、增强免疫、保肝抗炎等药理作用[2-4]。目前,胡黄连总苷的肠吸收相关研究尚未见报道,故本文对胡黄连总苷中4个成分在大鼠的不同肠段吸收特性进行探讨,可为胡黄连总苷的临床合理用药提供实验依据。
口服给药是常用的给药途径,肠道为其主要吸收部位,药物经胃肠道吸收进入血液而发挥药效作用。考察药物在肠道中的吸收特性,在一定程度上可反映药物经口服后整体的吸收情况[5-6]。因此,本研究采用大鼠在体单向肠灌流法,运用高效液相色谱(HPLC)技术同时测定胡黄连总苷肠灌流液中胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ、草夹竹桃苷共4个成分的浓度,以吸收速率常数(Ka)和有效渗透系数(Peff)为评价指标,考察4个成分分别在十二指肠、空肠、回肠、结肠的吸收情况,阐明4个成分的肠吸收特性,旨在为胡黄连总苷的临床合理用药提供参考。
1 仪器与材料
1.1 仪器 岛津LC-2030C高效液相色谱仪(包括LC-20AD二元泵,CTO-20AC柱温箱,SIL-20AC自动进样器,UV检测器,LabSolutions工作站,日本岛津公司);EX-H3052百万分之一电子分析天平(上海赞维衡器有限公司);TG16-WS高速离心机(湘仪CENCE公司);KQ5200DE超声波清洗器(昆山市超声仪器有限公司);HH-4数显恒温水浴锅(常州朗越仪器制造有限公司);恒流蠕动泵(保定兰格恒流泵有限公司);VORTEX 2涡旋混合器(德国IKA公司);FE28 pH计(瑞士Mettler Toledo公司);Milli-Q型超纯水器(美国Millipore公司)。
1.2 试剂与试药 胡黄连总苷粉末由天士力控股集团研究院提供(批号:20190101,胡黄连总苷中主要成分胡黄连苷Ⅰ和胡黄连苷Ⅱ质量分数之和为38.32%);胡黄连苷Ⅰ对照品(批号:111727-201702,纯度95.6%,中国食品药品检定研究院);胡黄连苷Ⅱ对照品(批号:111596-201604,纯度96.2%,中国食品药品检定研究院);胡黄连苷Ⅲ对照品(批号:MUST-20090408,纯度99.7%,成都曼斯特生物科技有限公司);草夹竹桃苷对照品(批号:AF20100207,纯度98.0%,成都埃法生物科技有限公司);乙腈(色谱级,美国Fisher公司);冰醋酸(色谱级,天津市科密欧化学试剂有限公司);其余试剂均为分析纯;实验用水为Milli-Q超纯水。
1.3 实验动物 SPF级雄性SD大鼠,购自斯贝福(北京)生物技术有限公司,许可证号:SCXK(京)2019-0010,体质量 180~200 g,饲养于天津中医药大学实验动物中心。饲养条件:(22±2)℃,湿度(50±10)%,自由摄食和饮水。实验动物的饲养和操作规程均遵守天津中医药大学实验动物饲养和使用的相关规定(伦理审查编号:TCM-LAEC2022193)。
2 方法与结果
2.1 胡黄连总苷制备工艺 称取适量胡黄连粗粉,加适量纯水浸泡,以纯水渗漉,收集渗漉液,浓缩至相当于1 g/mL原药材的浓缩液。经大孔吸附树脂,以纯水、乙醇洗脱,收集洗脱液、浓缩、冷冻干燥,经乙酸乙酯-乙醇回流提取,过滤,滤液浓缩、真空干燥,得胡黄连总苷。
2.2 Kreb-Ringer’s(K-R)缓冲液的配制 精密称取氯化钙0.37 g,氯化钠7.80 g,氯化钾0.35 g,碳酸氢钠1.37 g,磷酸二氢钠0.32 g,加适量纯水使其溶解,再加入氯化镁0.02 g,葡萄糖1.40 g,充分混匀,加纯水定容至1 000 mL,用1 mol/L磷酸调pH至6.8,即得K-R缓冲液。
2.3 空白灌流液的制备 取健康SD大鼠6只,实验前禁食24 h,自由饮水,腹腔注射10%水合氯醛溶液,麻醉后将其固定在手术台上,沿腹腔中线打开腹腔,于十二指肠上部和结肠下部两端切口,用预热至37℃的生理盐水将肠内容物冲洗干净后插管,结扎固定。伤口处用浸有生理盐水的纱布覆盖保湿,红外灯照射大鼠腹部保温。
用预热至37℃的K-R缓冲液以1 mL/min的流速灌流,待肠段内充满K-R缓冲液时,将流速降低至0.2 mL/min,灌流平衡30 min后开始计时。进口瓶装有K-R缓冲液,出口瓶用于收集流出灌流液,收集120 min的灌流液,流出灌流液离心半径10 cm,12 000 r/min 离心 10 min,取上清液,合并,即得空白灌流液。
2.4 胡黄连总苷灌流液的配制 精密称取胡黄连总苷粉末0.10 g,置于200 mL容量瓶,用K-R缓冲液溶解并定容,配制成浓度为0.5 mg/mL的胡黄连总苷灌流液。
2.5 混合对照品溶液的配制 精密称取胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ、草夹竹桃苷对照品适量,分别用50%乙腈溶解,配制成浓度为1.0 mg/mL的各对照品储备液。
精密移取上述对照品储备液适量,加空白灌流液稀释,配制成胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ、草夹竹桃苷浓度分别为 200、200、50、50 μg/mL的混合对照品溶液。
2.6 色谱条件 WondaSilC18色谱柱(4.6mm×250mm,5 μm);流动相:乙腈-0.5%冰醋酸水溶液(15.5∶84.5);流速:1.0 mL/min;检测波长:280 nm;柱温:30 ℃;进样量:10 μL。
2.7 方法学考察
2.7.1 专属性 分别取空白灌流液、混合对照品溶液和胡黄连总苷灌流液适量,按“2.6”项下色谱条件进样分析,记录其色谱图,如图1所示。结果显示,空白灌流液对胡黄连总苷中4个成分的测定无干扰,表明该方法专属性良好。
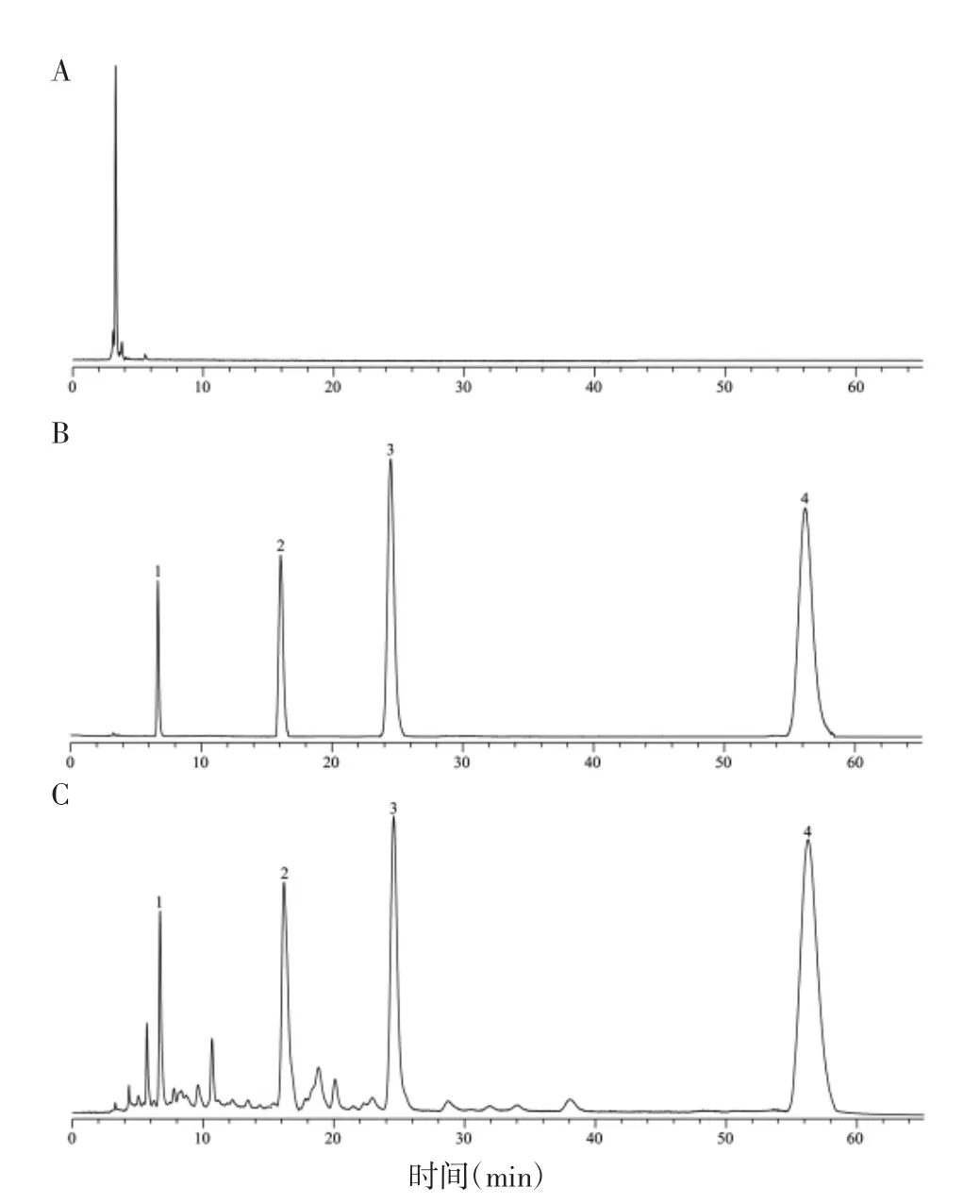
图1 胡黄连总苷中4个成分的专属性Fig.1 Specificity of 4 components of TGPS
2.7.2 线性关系、检测限及定量限 精密移取“2.5”项下混合对照品溶液适量,用空白灌流液稀释,分别配制成胡黄连苷Ⅰ和胡黄连苷Ⅱ浓度均为200、160、80、40、20、10 μg/mL,胡黄连苷Ⅳ和草夹竹桃苷浓度均为 50、40、20、10、5、2.5 μg/mL 的对照品溶液。按“2.6”项下色谱条件进样分析,记录峰面积。以各对照品浓度为横坐标(X),对照品峰面积为纵坐标(Y),绘制标准曲线。此外,以信噪比(S/N)为3时的浓度作为各成分的检测限,S/N为10时的浓度为各成分的定量限。胡黄连总苷中4个成分的线性关系、检测限及定量限结果见表1。

表1 4个成分的线性关系、检测限及定量限Tab.1 Investigation results of linear relationship of 4 components
结果表明,胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ、草夹竹桃苷在各自浓度范围内线性关系良好。2.7.3 精密度 精密称取6份胡黄连总苷粉末,按“2.4”项下方法配制供试品溶液,并按“2.6”项下色谱条件进样分析,计算胡黄连总苷中4个成分峰面积RSD,以考察其精密度。结果显示,胡黄连总苷中4个成分峰面积的RSD分别为:胡黄连苷Ⅰ0.87%、胡黄连苷Ⅱ0.52%、胡黄连苷Ⅳ0.92%、草夹竹桃苷0.98%,表明该仪器精密度良好。
2.7.4 加样回收率 精密称取6份胡黄连总苷粉末,每份约0.1 g,精密加入胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ和草夹竹桃苷对照品,按“2.4”项下配制方法,配制供试品溶液,并按“2.6”项下色谱条件进样分析,计算加样回收率、平均加样回收率及RSD,结果见表2。
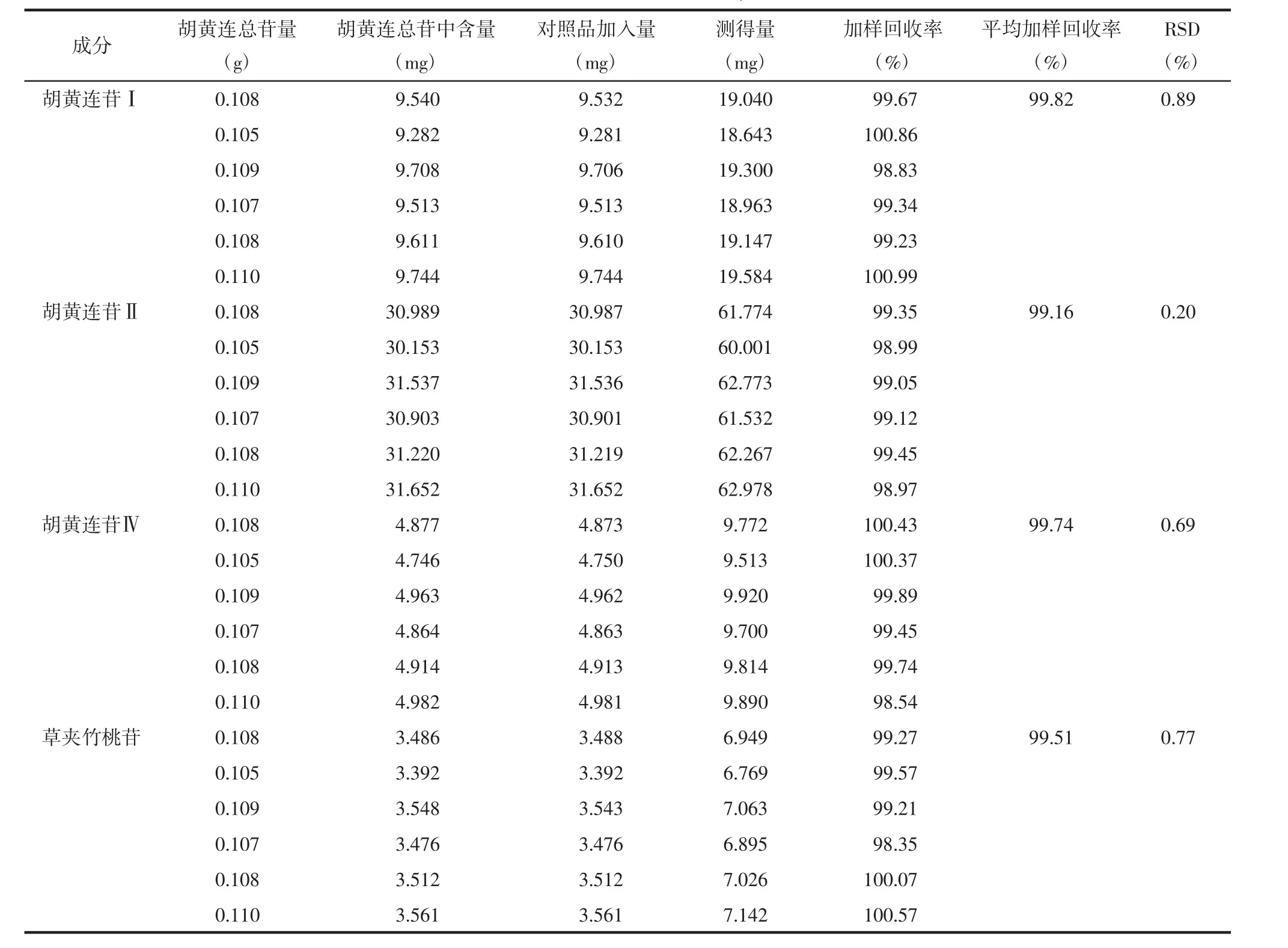
表2 4个成分的加样回收率Tab.2 Recovery test of 4 components
结果显示,胡黄连总苷中胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ和草夹竹桃苷的平均加样回收率分别为99.82%、99.16%、99.74%、99.51%,加样回收率RSD均小于0.89%,表明该方法加样回收率良好。
2.7.5 稳定性 精密称取胡黄连总苷粉末适量,按“2.4”项下方法配制供试品溶液,置37℃水浴中,分别于第 0、2、4、8、12、24 h 取样,按“2.6”项下色谱条件进样分析,计算各成分峰面积的RSD。结果显示,胡黄连总苷中4个成分的峰面积RSD分别为:胡黄连苷Ⅰ0.89%、胡黄连苷Ⅱ0.74%、胡黄连苷Ⅳ0.90%、草夹竹桃苷0.83%,表明各成分在24 h内稳定性良好。
2.7.6 耐用性 精密称取胡黄连总苷粉末适量,按“2.4”项下方法配制供试品溶液。在“2.6”色谱条件基础上,改变色谱柱、柱温、流速及流动相比例,测定供试品溶液中各成分含量,并计算RSD,以考察该方法的耐用性。结果见表3。

表3 4个成分的耐用性Tab.3 Durability test of 4 components
结果显示,胡黄连总苷中胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ和草夹竹桃苷含量RSD均小于0.93%,表明测定条件小的变动能满足系统适用性试验要求,该方法具有较好的耐用性。
2.8 大鼠在体肠吸收实验
2.8.1 在体单向肠灌流法 为保证大鼠肠道良好的吸收状态,每只大鼠仅使用单一肠段进行单次试验。取健康SD大鼠24只,随机分为4组,分别为十二指肠组、空肠组、回肠组和结肠组,每组6只。实验前大鼠禁食24 h,自由饮水,腹腔注射10%水合氯醛溶液,麻醉后将其固定在手术台上,沿腹腔中线打开腹腔,选取需要考察的肠段约10 cm(不同肠段区间:十二指肠为距幽门1 cm处开始,空肠为距幽门15 cm处开始,回肠为距盲肠上行20 cm处开始,结肠为距盲肠后端开始)。于所选肠段两端切口,用预热至37℃的生理盐水将肠内容物冲洗干净后插管,结扎固定。伤口处用浸有生理盐水的纱布覆盖保湿,红外灯照射大鼠腹部保温。
用预热至37℃的胡黄连总苷灌流液以1mL/min的流速灌流,待肠段内充满胡黄连总苷灌流液时,将流速降低至0.2 mL/min,灌流平衡30 min后开始计时。进口瓶装有胡黄连总苷灌流液,为流入灌流液;出口瓶用于收集流出灌流液,进口瓶和出口瓶均提前称重,每隔15 min更换进口瓶和出口瓶,同时记录进口瓶和出口瓶的质量,共收集8个时间段的流出灌流液,实验持续时长120 min,流出灌流液离心半径10 cm,12 000 r/min离心10 min,取上清液,用0.45 μm 微孔滤膜过滤,按“2.6”项下色谱条件进样分析。
实验结束后处死大鼠,剪下所考察肠段,测量不同肠段长度(L)和周长,由3次周长测量值求得平均半径(R)。
2.8.2 肠吸收参数计算 采用重量法对流入灌流液和流出灌流液体积和密度进行校正,消除灌流液体积和密度变化对实验结果产生的影响[7]。精密吸取1.0 mL流入灌流液,置于已知质量的玻璃瓶中,称量液体质量,计算流入灌流液密度ρin;精密吸取1.0 mL流出灌流液,置于已知质量的玻璃瓶中,称量液体质量,计算流出灌流液密度ρout。按下列公式计算肠吸收参数吸收速率常数(Ka)和有效渗透系数(Peff),以此分析胡黄连总苷中4个成分在大鼠十二指肠、空肠、回肠、结肠的肠吸收特性。
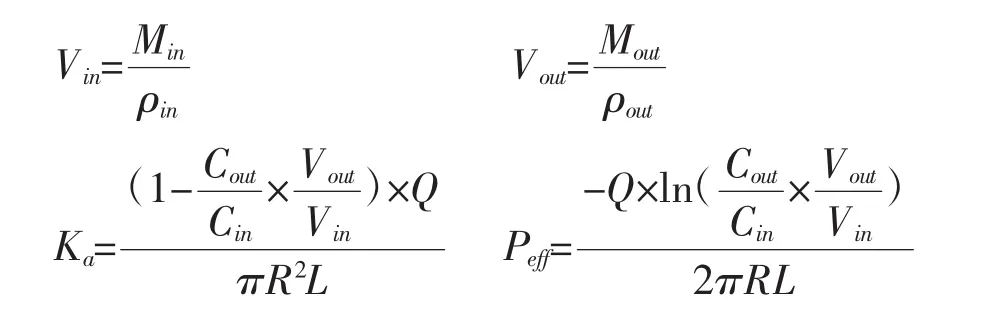
其中Vin、Vout分别为流入灌流液体积、流出灌流液体积(mL);Min、Mout分别为流入灌流液质量、流出灌流液质量(g);Cin、Cout分别为流入灌流液中各成分浓度、流出灌流液中各成分浓度(μg/mL);R、L为被考察肠段的半径、长度(cm);Q为灌流速度(0.2 mL/min)。
2.8.3 统计学分析 采用SPSS 25.0软件进行数据分析,实验数据以均数±标准差(±s)表示。多组间比较采用单因素方差分析(One-Way ANOVA),组间两两比较采用LSD检验。P<0.05为差异有统计学意义。
2.8.4 胡黄连总苷中4个成分在大鼠不同肠段的吸收特性 取浓度为0.5 mg/mL的胡黄连总苷灌流液,采用在体单向肠灌流法进行灌流,以肠吸收参数Ka和Peff为评价指标,考察胡黄连总苷中胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ、草夹竹桃苷共4个成分分别在大鼠十二指肠、空肠、回肠、结肠的吸收特性。其中Ka代表成分从吸收部位进入体循环的速度,反映成分在不同肠段中的吸收快慢,Ka越大,表明成分在该肠段中的吸收越快;Peff代表成分透过生物膜的渗透能力,反映成分在不同肠段中的吸收能力的强弱[8]。一般当Peff>2.0×10-5cm/min 时,表明成分在该肠段中吸收良好[9]。胡黄连总苷中4个成分在大鼠不同肠段的吸收速率常数和有效渗透系数见表4和表5,4个成分在不同肠段的吸收速率常数和有效渗透系数见图2。
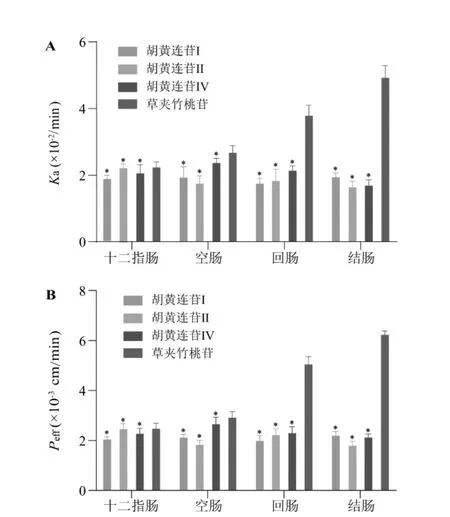
图2 胡黄连总苷中4个成分在不同肠段的吸收速率常数和有效渗透系数比较Fig.2 Compare with Kaand Peffof 4 components of TGPS in different intestinal segments
表4 胡黄连总苷中4个成分在不同肠段的吸收速率常数(±s,n=6)Tab.4 Kaof 4 components of TGPS in different intestinal segments(±s,n=6)

表4 胡黄连总苷中4个成分在不同肠段的吸收速率常数(±s,n=6)Tab.4 Kaof 4 components of TGPS in different intestinal segments(±s,n=6)
注:与十二指肠比较,*P<0.05;与空肠比较,#P<0.05;与回肠比较,△P<0.05。
成分Ka(×10-2/min)十二指肠 空肠 回肠 结肠胡黄连苷Ⅰ 1.91±0.11 1.97±0.33 1.79±0.16 1.98±0.13胡黄连苷Ⅱ 2.24±0.16 1.76±0.26* 1.84±0.38* 1.65±0.21*△胡黄连苷Ⅳ 2.10±0.26 2.41±0.14* 2.17±0.15# 1.73±0.17*#△草夹竹桃苷 2.28±0.16 2.72±0.21* 3.83±0.31*#4.97±0.36*#△
表5 胡黄连总苷4个成分在不同肠段的有效渗透系数(±s,n=6)Tab.5 Peffof 4 components of TGPS in different intestinal segments(±s,n=6)

表5 胡黄连总苷4个成分在不同肠段的有效渗透系数(±s,n=6)Tab.5 Peffof 4 components of TGPS in different intestinal segments(±s,n=6)
注:与十二指肠比较,*P<0.05;与空肠比较,#P<0.05;与回肠比较,△P<0.05。
成分Peff(×10-3cm/min)十二指肠 空肠 回肠 结肠胡黄连苷Ⅰ 2.04±0.11 2.11±0.13 1.99±0.20 2.19±0.17△胡黄连苷Ⅱ 2.46±0.22 1.83±0.17* 2.22±0.25*#1.79±0.18*△胡黄连苷Ⅳ 2.27±0.22 2.65±0.28* 2.29±0.26# 2.12±0.14#草夹竹桃苷 2.47±0.31 2.91±0.24* 5.05±0.43*#6.23±0.27*#△
由表可知,胡黄连总苷中4个成分在不同肠段均 Ka>1.65×10-2/min,Peff>2.0×10-5cm/min,表明各成分在不同肠段的吸收速度和吸收能力均良好,即各成分在不同肠段均易吸收,但各成分在不同肠段的吸收速度和吸收能力存在一定差异。通过比较不同肠段的Ka、Peff值,结果显示:1)胡黄连总苷中胡黄连苷Ⅰ在不同肠段的Ka、Peff值大小顺序为:结肠>空肠>十二指肠>回肠,其中,除结肠与回肠的Peff值有显著性差异(P<0.05),其余参数均无显著性差异(P>0.05),因此,胡黄连苷Ⅰ无主要吸收部位。2)胡黄连总苷中胡黄连苷Ⅱ在不同肠段的Ka、Peff值大小顺序为:十二指肠>回肠>空肠>结肠,其中,十二指肠和回肠、结肠、空肠的Ka、Peff值差异均有统计学意义(P<0.05),因此,十二指肠为胡黄连苷Ⅱ的主要吸收部位。3)胡黄连总苷中胡黄连苷Ⅳ在不同肠段的Ka、Peff值大小顺序为:空肠>回肠>十二指肠>结肠,其中,空肠和回肠、十二指肠、结肠的Ka、Peff值差异均有统计学意义(P<0.05),因此,空肠为胡黄连苷Ⅳ的主要吸收部位。4)胡黄连总苷中草夹竹桃苷在不同肠段的Ka、Peff值大小顺序为:结肠>回肠>空肠>十二指肠,其中,结肠和回肠、空肠、十二指肠的 Ka、Peff值差异均有统计学意义(P<0.05),因此,结肠为草夹竹桃苷的主要吸收部位。
比较胡黄连总苷中4个成分在不同肠段的Ka、Peff值,结果显示,各成分的 Ka、Peff值大小顺序为:在十二指肠中,草夹竹桃苷>胡黄连苷Ⅱ>胡黄连苷Ⅳ>胡黄连苷Ⅰ;在空肠中,草夹竹桃苷>胡黄连苷Ⅳ>胡黄连苷Ⅰ>胡黄连苷Ⅱ;在回肠中,草夹竹桃苷>胡黄连苷Ⅳ>胡黄连苷Ⅱ>胡黄连苷Ⅰ;在结肠中,草夹竹桃苷>胡黄连苷Ⅰ>胡黄连苷Ⅳ>胡黄连苷Ⅱ。值得注意的是,在不同肠段中,草夹竹桃苷与其他3个成分比较,Ka、Peff值差异均有统计学意义(P<0.05),且其在不同肠段的吸收均最佳。
3 讨论
3.1 肠吸收研究方法的选择 影响口服药物的药效因素众多,除药物的化学成分复杂外,其在体内的吸收过程也是重要影响因素[10]。肠吸收作为口服药物的主要吸收途径,目前对其的研究方法主要有3种,分别为体外法、体内法和在体法[11]。体外法主要有2种研究方法,分别为外翻肠囊法和Caco-2细胞模型法,其操作简单、实验周期短,可用于药物早期高通量筛选,但体外环境无法保证血液的正常供应和神经系统的完整性,生物活性较差,不能反映药物在肠道环境中的真实吸收情况[12-13];体内法主要研究方法为血药浓度法,采用整体动物进行实验,能真实地反映药物经口服后在体内的吸收情况,但实验周期较长,影响因素较多,无法特异性地反映药物在肠道的吸收特性[14];在体法主要研究方法为循环肠灌流法和单向肠灌流法,前者灌流时间长、流速快,易损伤肠黏膜,而单向肠灌流法由于具有灌流时间短、流速低等特点,对肠黏膜的影响较小,可模拟真实的肠道环境,且此方法已被美国FDA认可,应用广泛[15-16],因此,本课题采用在体单向肠灌流法研究胡黄连总苷中4个成分的肠吸收特性,整体反映药物在肠道的吸收情况。
3.2 灌流液体积校正方法的选择 在体单向肠灌流过程中,肠道不仅吸收药物,同时也会吸收或分泌水分,导致直接测得的药物浓度与实际药物浓度之间有偏差。此外,由于在肠灌流过程中,可能会引起肠壁细胞溶蚀破裂、肠黏膜脱落等现象,进而导致流出灌流液密度发生变化,故需通过校正流出灌流液的体积和密度,以校正药物浓度,保证实验数据的准确性[17]。灌流液体积和密度的校正方法主要有2种,分别为标示物法和重量法[18]。标示物法是指在灌流液中加入不易被肠道吸收的物质作为标示物,以标示物为参照量对药物浓度进行校正,常用的标示物为酚红和14C-PEG[19],但研究显示,肠道对酚红存在一定程度的吸收,且酚红可能干扰某些成分的转运和分析测定,不适于对所有成分的肠吸收研究[20];14C-PEG具有放射性,安全性和检测方法的复杂性制约其在普通实验室应用[21]。重量法通过计算流入和流出肠道的灌流液质量比对药物浓度进行校正,可节省检测标示物浓度的过程,操作相对简单,同时可真实地反映药物在肠道的吸收情况[22]。因此,本课题采用重量法对灌流液体积和密度进行校正,消除灌流液体积和密度的变化对实验结果的影响,以增加实验结果准确性。
3.3 胡黄连总苷中4个成分的肠吸收特性 本研究以Ka和Peff为评价指标,考察胡黄连总苷中4个成分分别在十二指肠、空肠、回肠、结肠的吸收情况,以阐明胡黄连总苷中4个成分的肠吸收特性。实验结果显示,胡黄连总苷中4个成分在不同肠段的吸收速度和吸收能力均良好,即4个成分在不同肠段均易吸收。但在不同肠段的吸收速度和吸收能力存在一定差异,推测可能与各成分的化学结构有关,胡黄连总苷中4个成分的化学结构式见图3。
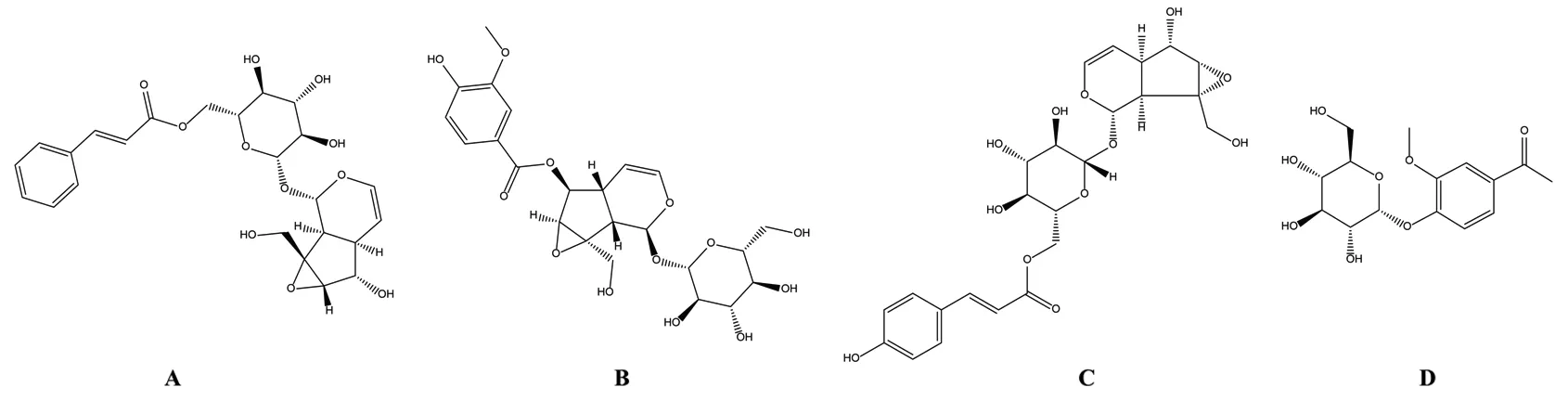
图3 胡黄连总苷中4个成分的化学结构式Fig.3 Chemical structures of 4 components of TGPS
胡黄连苷Ⅰ、胡黄连苷1、胡黄连苷3均为环烯醚萜苷类成分,其中,胡黄连苷I为肉桂酸与糖酯化生成的一种环烯醚萜苷,其苯环上无酚羟基等酸性基团和甲氧基等供电子基团,故胡黄连苷Ⅰ显中性,推测此可能为胡黄连苷Ⅰ无主要吸收部位的原因。胡黄连苷Ⅱ和胡黄连苷Ⅳ均在胡黄连苷Ⅰ的结构基础上引入酚羟基,酚羟基显酸性,但由于其它基团的存在导致各成分的酸性程度有所差异。其中,胡黄连苷Ⅱ酸性最强,主要吸收部位在十二指肠;胡黄连苷Ⅱ中酚羟基对位为碳氧双键,而胡黄连苷Ⅳ中酚羟基对位为碳碳双键,碳碳双键的吸电子能力弱于碳氧双键,导致胡黄连苷Ⅳ酸性减弱,其吸收部位向后移动,故胡黄连苷Ⅳ主要吸收部位在空肠;草夹竹桃苷为苯乙酮苷类成分,苯乙酮母核呈中性,但由于其酚羟基邻位为甲氧基,甲氧基作为供电子基团可减弱草夹竹桃苷的酸性[23],导致其吸收部位后移,主要在结肠被吸收。此外,与胡黄连苷Ⅰ、胡黄连苷Ⅱ、胡黄连苷Ⅳ相比,草夹竹桃苷在不同肠段中吸收最好,可能与其分子量较小,较易透过生物膜有关。因此,初步推断,胡黄连总苷中4个成分在不同肠段的吸收程度不同与各成分中酚羟基、碳碳双键、甲氧基等基团位置和分子量大小有关。
综上,本研究考察了胡黄连总苷中4个成分在大鼠不同肠段的吸收特性,结果表明,胡黄连总苷中4个成分在大鼠不同肠段的吸收速度和吸收能力均良好,但各成分在不同肠段的吸收速度和吸收能力存在一定差异。其中,胡黄连苷Ⅰ无主要吸收部位;胡黄连苷Ⅱ、胡黄连苷Ⅳ和草夹竹桃苷的主要吸收部位分别为十二指肠、空肠和结肠;草夹竹桃苷与其他3个成分比较,在不同肠段中吸收均最佳,为胡黄连总苷的临床合理用药提供明确参考。
