大环内酯类药物对合并铜绿假单胞菌感染的慢性气道炎症性疾病的疗效观察
2022-02-02林鸿斌
林鸿斌
(揭阳市慈云医院,广东 揭阳 522000)
PA(铜绿假单胞菌)为常见非发酵菌,在自然界中分布广泛,属革兰阴性杆菌[1]。慢性气道炎症性疾病是感染PA的高危人群,包括肺囊性纤维化、支气管扩张症和慢性阻塞性肺病等。大环内酯类药物近年来逐渐被应用于临床中,其能够通过抑制生物被膜形成,并通过调节机体免疫功能等,对PA生物被膜相关感染起到较好的治疗作用[2]。本文将大环内酯类药物应用于合并PA感染的慢性气道炎症性疾病80例患者中,对其临床疗效进行了探究,现报道如下。
1 资料与方法
1.1 一般资料
选取2020年3月-2021年9月广东省揭阳市慈云医院内科收治的80例合并PA感染的慢性阻塞性肺疾病、支气管扩张、肺囊性纤维化患者为研究对象,依据入院时间将所选对象随机分为对照组(n=40例)和观察组(n=40例)纳入标准:(1)对于研究的开展,医院伦理委员会均知情同意;(2)伴有慢性气道炎症性疾病者;(3)经MRI等影像学检查提示存在结构性肺病者;(4)伴有慢性咳嗽、咳痰、喘息等不适且症状间断加重表现者;(5)经实验室检查检出PA者。排除标准:(1)肝功能不全者;(2)对大环内酯类药物过敏者[3];(3)对大环内酯类药物不良反应耐受性差者;(4)伴有致死性心律失常风险较高的心血管病者。经对两组的一般资料情况展开比较,资料数据有可比性(P>0.05)。见表1。
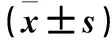
表1 一般资料比较[n(%)]或
1.2 研究方法
对照组在发生呼吸系统症状急性加重后给予选用敏感型抗菌药物抗感染,出院后继续予对症治疗8w。对于观察组者,则是于急性加重期予以敏感性抗菌药物与大环内酯类抗菌药物进行抗感染治疗,并在出院后持续进行14元大环内酯类抗菌药物(口服用药)进行治疗。其中,若患者伴慢性阻塞性肺疾病,可于急性期予以250mg剂量的大环内酯类抗菌药物,2次/日;待到稳定期时,持续予以250mg剂量的大环内酯类抗菌药物,2次/日,共治疗6个月。若患者伴支气管扩张,可于急性期予以250mg剂量大环内酯类抗菌药物,2次/日;待到稳定期时,持续予以250mg剂量大环内酯类抗菌药物,2次/日,共治疗2个月。若患者伴肺囊性纤维化,于急性期予以250mg剂量大环内酯类抗菌药物,1次/日;待到稳定期时,持续予以250mg剂量大环内酯类抗菌药物250mg,1次/日,共治疗6个月。
1.3 观察指标
依据PA及临床症状改善情况评估两组治疗后的成功率情况,其中①痊愈:临床症状恢复至PA感染前的健康水平且身体机能恢复到正常状态,痰病原学培养结果为阴性;②显效:临床症状明显好转且体征基本恢复至正常,痰培养结果依然为阴性;③有效:临床症状有所改善,但部分指标无明显改善;④无效:相比治疗前,临床症状改善不明显,病情呈现加重趋势。总有效率=(①+②)/(①+②+③+④)*100%。同时,还对两组的第1秒用力呼吸容积(FEV1)及其与用力肺活量的比(FEV1/FVC)和最大呼气流速(PEF)等肺功能指标,以及心率(HR)、呼吸频率(RR)、血氧饱和度(SpO2)等呼吸功能指标和降钙素原(PCT)进行了对比。
1.4 统计学方法
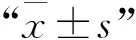
2 结果
2.1 治疗成功率对比
在对比两组患者治疗成功率时,与对照组(75.00%)相比观察组(97.50%)更高(P<0.05)。见表2。

表2 比较两组的治疗成功率[n(%)]
2.2 肺功能指标对比
在对比两组的肺功能指标时,治疗前FEV1、FEV1/FVC、PEF无统计学差异(P>0.05)。与治疗前相比,治疗后各指标升高,且观察组较对照组更高(P<0.05)。见表3。
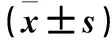
表3 比较两组的肺功能指标
2.3 呼吸功能及PCT指标对比
在对比两组的呼吸功能及PCT指标时,治疗前各指标无统计学差异(P>0.05)。治疗后的HR、RR、PCT均低于治疗前,SpO2高于治疗前(P<0.05)。相较于对照组,观察组的HR、RR、PCT更低且SpO2更高(P<0.05)。见表4。
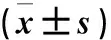
表4 比较两组的呼吸功能及PCT指标
3 讨论
近年来PA感染率、耐药率以及病死率居高不下,而这些与PA的易定植、易变异和存在多种耐药机制的特点息息相关[4]。生物被膜的形成是PA重要耐药机制之一。PA能够通过生物被膜的形式生存,对抗菌药物与机体免疫的杀伤作用逃避[5]。大环内酯类药物尽管无抗PA作用,但却能够对生物被膜产生抑制作用,并增强对细胞吞噬作用。在大环内酯类药物中,克拉霉素、红霉素、阿奇霉素以及罗红霉素等都能够抑制PA重要耐药机制[6]。除此之外,大环内酯类药物还具有较强的抗菌活性,免疫调节和抗炎作用。在此次研究中,将大环内酯类抗菌药物应用于合并PA感染的慢性气道炎症性疾病中,其有效率可达97.50%,FEV1、FEV1/FVC、PEF肺功能指标能够得到改善,HR、RR、SpO2以及PCT指标也均能够改善。这可能是由于大环内酯类药物是一类治疗感染性疾病的药物,14元环大环内酯类抗菌药物,经对50s核糖体中的肽酰转移酶活性的阻断,以起到快速抑菌的作用。同时,还能够通过调控炎症细胞,如白介素-6等,以起到抗炎作用。
细菌在自然条件下的存在形式包括浮游与生物膜,不同生存状态下的同一细菌,其抗菌药物敏感性之间差异显著。伴随着临床对抗菌药物使用,使得细菌感染被有效控制,但也会衍生出一些严重性问题,如致病菌感染、细菌耐药等。细菌生物膜形成与细菌耐药不但易增加细菌复发感染的机率,而且清除难度大,比如,铜绿假单胞菌引起的肺部慢性感染。就现下而言,临床对治疗铜绿假单胞菌慢性感染开展了广泛研究,如大环内酯类药物的治疗机制。
生物膜形成是一个动态过程,其过程包括三个,即细菌黏附、形成微菌落和包裹细胞外多聚基质。就生物膜来说,细胞外多聚糖是必不可少的组成,这也是支持细菌出现耐药性的重要因素。而在黏液性铜绿假单胞菌生物膜多糖、非黏液型铜绿假单胞菌生物膜中,藻酸盐、表多糖分别是其主要成分。针对铜绿假单胞菌藻酸盐,14、15元环大环内酯类可起到良好抑制效果,克拉霉素、大环内酯类及琥乙红霉素则能对生物膜中藻酸盐、蛋白质和多糖产生作用,能使其有效降低,在琥乙红霉素与克拉霉素药物浓度中,若藻酸盐、蛋白质和多糖每毫升未超过10mg时则会呈现明显降低趋势,同时,二者之间没有明显的互相抑制作用。与非黏液株相比,在作用于黏液株生物膜方面,罗红霉素、克拉霉素和琥乙红霉素更强,对于铜绿假单胞菌生物膜,阿奇霉素的作用效果则最强,当阿奇霉素的最低抑菌浓度大于或等于1/156时,则能有效抑制黏液型铜绿假单胞菌藻酸盐,或者当最低抑菌浓度大于或等于1/16时,能更好地抑制非黏液型铜绿假单胞菌生物膜。14、15元环大环内酯类对于藻酸盐的抑制,主要是对藻酸盐合成限速酶鸟苷二磷酸-D-甘露脱氢酶酶活性的抑制而实现,但此种则不具备对16元环大环内酯类作用,有效作用位点需5位以上的糖链结构。
通过开展光化学反应检测可知,在分析多形核白细胞数量方面,与游离型铜绿假单胞菌比较,在生物膜中,非黏液株和黏液株减少明显。且有报道指出,藻酸盐为黏液株生物膜核心组成成分,而吞噬细菌和多形核白细胞趋化作用易受其阻碍,当酶分解藻酸盐后,可进一步提高多形核白细胞对黏液株吞噬作用,减少多形核白细胞在非黏液株生物膜中的数量,生物膜数量增加,而调查巨噬细胞核中心粒细胞情况是受自身信号经对分子3-oxo-C12-HIS浓度水平一定程度诱导所致,导致机体清除细菌能力下降。
对于表多糖与藻酸盐的生成,应用大环内酯类药物能有效抑制其产生,对铜绿假单胞菌生物膜(经黏液株、非黏液株)的产生予以阻碍,同时,对于QS系统以及其自身信号诱导分子3-oxo-C12-HIS,特定大环内酯类药物的实施还能起到良好抑制作用,从而阻断3-oxo-C12-HIS诱导,加快中性粒细胞、巨噬细胞凋亡,增强细胞灭杀和吞噬细菌的能力。有研究表明,大环内酯类药物能一定程度影响互吞噬细胞功能,且能对被转运至多形核白细胞处产生影响,相比细胞外浓度,在细胞内的浓度能高达数倍。相比细胞外环境浓度,在肺泡巨噬细胞合成纤维细胞、多形核白细胞中,阿奇霉素浓度能高至100多倍,然而,经比较实施大环内酯类药物对多形核白细胞预处理,对铜绿假单胞菌作用,以及对多形核白细胞未处理作用方面发现,无明显差异性。通过利用大环内酯类药物起到作用的周围细菌与生物膜对非黏液型铜绿假单胞细菌与多形核白细胞吞噬黏液型的能力进行加强,取得的治疗疗效明显优于对多形核白细胞本身直接应用的效果。同时,大环内酯类药物对痰液的产生也有良好的抑制作用,可以减轻痰液的黏稠度并将其清除。以罗红霉素、阿奇霉素的应用最为常见。由此可知,在对感染铜绿假单胞菌的慢性气道炎症性病症患者实施大环内之类药物具有一定有效性。
综上所述,通过破坏生物被膜辅助抗感染、通过抗炎及调节免疫减少炎症对支气管肺组织的破坏及延缓肺功能的恶化,改善患者预后,不仅能够增强治疗有效率,而且能够改善肺功能、呼吸功能指标。
