基于石灰石粉钙源的微生物固化砂土试验研究
2022-01-13程瑶佳唐朝生泮晓华王殿龙
程瑶佳,唐朝生,刘 博,泮晓华,王殿龙,吕 超,李 昊
南京大学 地球科学与工程学院,南京 210023
微生物诱导碳酸钙沉积(Microbial Induced Calcite Precipitation,简称MICP)技术是近年来发展起来的一种新型土体改良技术。微生物分泌的脲酶水解尿素产生碳酸根离子,与土体中的钙离子结合,生成具有胶结作用的碳酸钙,从而粘结土颗粒,填充土体孔隙,达到改善土体物理力学性质的目的(Haouzi et al., 2018; Liu et al., 2019; Jiang et al., 2020)。相比于传统的土体改良技术,该技术具有生态环保、经济高效、对土体扰动小的优势(钱春香等,2015; 李明东等,2016;Choi et al., 2017)。因此,近年来引起了国内外学者的广泛关注,并围绕改性土体的工程性质进行了广泛研究。
微生物固化土体的影响因素众多,菌液浓度、营养液成分、反应温度和pH等对固化效果的影响不容忽视。梁仕华等(2018)分别选用氯化钙和硝酸钙作为营养液中的钙源,发现硝酸钙的微生物固化效果较氯化钙更好。彭劼等(2018)通过MICP水溶液试验和一维砂柱加固试验发现,在10~30℃范围内,相对低温条件下,钙离子消耗量大,砂柱固化效果更好。李成杰等(2018)探究了氯化钙、醋酸钙、乳酸钙、葡萄糖酸钙四种不同钙源及Ca2+浓度对MICP的影响,结果表明,氯化钙作为钙源生成的碳酸钙晶体最稳定,其浓度为0.25 M时,碳酸钙沉积效率最高。Jiang等(2019)研究发现0.2 M和1.0 M胶结液浓度条件下,微生物固化砂土边坡提高其抗侵蚀性的效果最好,而2.0 M的胶结液改性效果较差。Cheng等(2014)研究不同因素对微生物固化砂土效果的影响,结果表明,较高的土体初始干密度,室温和中性条件下,胶结的砂柱强度较好。Zhang等(2014)通过单轴抗压强度试验和微观形态分析,研究表明,以醋酸钙作为钙源比以氯化钙和硝酸钙作为钙源处理的砂柱强度更高,用醋酸钙处理生成的碳酸钙晶体类型主要为文石,用其他两种钙源处理生成的主要为方解石。在微生物诱导碳酸钙沉积过程中,微生物作为成核位点,吸引大量钙离子积聚在细胞表面,使得碳酸钙沉淀得以产生(Whiffin et al., 2007)。因此,钙源的种类对微生物诱导碳酸钙沉积的效果有十分重要的影响。
目前,MICP技术多用钙盐(如CaCl2、Ca(NO3)2、Ca(CHCOO)2)等作为钙源,其中应用最广泛的为CaCl2,其价格昂贵,具有腐蚀性,且对环境有污染(Dejong et al., 2006; Cheng et al., 2014)。因此,寻找一种成本低、污染小的钙源具有十分重要的意义。石灰石粉是一种廉价而丰富的材料,可以从废弃建筑材料和采石场中大量获得,如能将其成功应用于MICP中,将大大节约成本和提高环保性(杨华山等,2006;马烨红等,2007;刘数华和阎培渝,2008)。
为此,本文提出利用石灰石粉成为钙源,用于微生物诱导碳酸钙沉积作用来固化土体。通过加入乙酸溶解石灰粉释放钙离子,作为微生物固化土体过程的钙源。通过开展无侧限抗压强度试验,微观结构的扫描电镜观察、碳酸钙含量测定等测试分析,对将石灰石作为取钙源用于微生物固化土体的可行性进行验证。同时,与氯化钙和醋酸钙进行对比,探讨不同钙源对改性土体力学特性和微观结构的影响,分析其固化机制和固化效果。
1 试验材料与方法
1.1 试验材料
1.1.1 石灰石粉
本文所用石灰石粉为重质碳酸钙,由天然石灰石磨碎而成。表1为所用石灰石粉成分表,其中碳酸钙含量达到98.5%以上。

表1 石灰石粉成分表Table 1 Table of limestone powder composition
1.1.2 砂
本文所用砂为石英质河砂,砂的比重为2.65,内摩擦角为43°。试验前将砂过0.25 mm和2 mm筛,经过颗分试验得到砂的不均匀系数Cu为1.78,曲率系数Cc为1.05,为级配不良砂。
1.2 样品制备与处理
1.2.1 钙源的提取与制备
钙离子通过石灰石粉和乙酸溶液反应获得,其化学原理见式(1)。为了确定石灰石粉和乙酸溶液反应的最优配比(w:v),试验共设置五组1:1、1:2、1:4、1:6和1:8不同配比的反应溶液。将20 g石灰石粉分别与不同体积的20%浓度醋酸溶液混合,在室温(30℃)下反应3 d后,对生成物进行过滤,取上清液,用钙离子计测定其钙离子浓度。取钙离子浓度最大时的配比作为最优配比,进行后续钙离子的提取。之后,参照最优配比,将足量的石灰石粉和对应体积的20%浓度醋酸溶液混合。充分反应后,取上清液测定反应后的pH,并用250 g/L NaOH溶液调节溶液的pH至6.96,再次测定溶液的钙离子浓度。之后,将溶液稀释至钙离子浓度为0.5 M,作为最终石灰石粉提取钙源,以待后续试验。
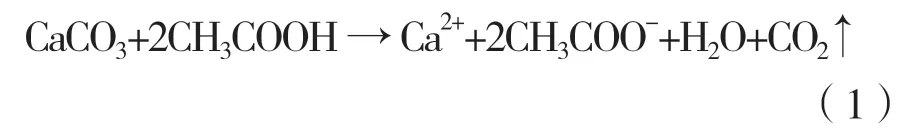
1.2.2 细菌与培养基
试验所用菌株为巴氏芽孢八叠球菌(Sporosarcina pasteurii, ATCC 11859),购自美国菌种保藏中心。该菌为为化能异养型革兰氏阳性菌,产生的脲酶具有较高的活性,其在岩土工程领域应用广泛,具有代表性。试验采用NH4-YE液体培养基,每升(L)含酵母提取物20 g,硫酸铵10 g和三羟甲基氨基甲烷(Tris-base,pH=9.0)15.75 g。培养基配置完成后,在高压灭菌锅内120 ℃高温灭菌30 min。待培养基冷却,将菌液以3:100的比例接种至培养基。之后,在30℃恒温震荡培养箱中以150转/分的速度震荡培养24 h。用分光光度计测得菌液的OD600值为1.68,同时用电导率仪测得其脲酶活性为3.85 mM urea hydrolysed/min。
1.2.3 胶结液配制
胶结液包括尿素(0.5 M),钙源(0.5 M)和营养肉汤(3 g/L),主要用于为MICP过程提供Ca2+和CO32-,以及为细菌的新陈代谢和生长繁殖提供充足的营养物质。为探究不同钙源的影响,同时由于乙酸根离子可以很容易地被自然微生物降解,对环境的负面影响较小。本文采用了醋酸钙、氯化钙和石灰石提取钙源作为钙源,分别进行了试验。
1.2.4 土样制备
试验所用制备砂柱的模具为高72 mm,直径36 mm,厚度1 mm的多孔塑料软管,孔直径和孔间距均为5 mm,软管外围包裹一层纱布以防漏砂。制样时,称取一定质量的砂装入模具中,控制砂柱干密度为1.52 g/cm3。在模具底部和顶部分别放置一块透水石,透水石用纱布包裹,以保证后续浸泡过程菌液和胶结液能够顺利入渗,同时防止砂颗粒流失,试验砂柱模型如图1所示。本次试验共制备3组砂柱试样,每组试样包含3个平行样。
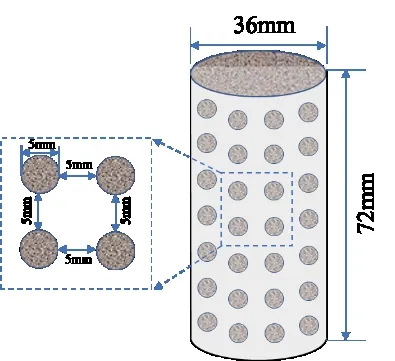
图1 试验砂柱模型Fig. 1 Sand pillar model of test
1.2.5 MICP处理
将制备好的试样在菌液中浸没30 min,以保证试样饱和和细菌充分定植。之后将三组试样分别转移入石灰石粉提取钙源、氯化钙和醋酸钙三种不同钙源的胶结液中,并确保试样被完全浸没,浸泡过程如图2所示。在30℃恒温条件下养护7 d之后,将试样取出置于室内风干15 d直至试样质量不再变化,室内温度控制在30±1℃,相对湿度控制在50±5%。完成第一轮胶结后,更换模具外围和透水石四周的纱布,防止纱布上沉积的碳酸钙影响后续溶液的入渗,之后重复上述步骤,共进行3轮胶结。

图2 试样浸泡过程Fig. 2 Process of sample soaking
1.3 试验方法
1.3.1 无侧限抗压强度试验
为评价MICP处理后固化砂柱的力学特性,对试样开展无侧限抗压强度试验。试样养护完成后进行拆模,并用去离子水清洗试样以去除残余盐分。将试样放入烘箱烘干后,进行无侧限抗压强度试验。将试样放在试验机平台上,调整平台位置,使试样和上部加载板刚好接触后,开始试验,轴向应变加载速率为1 mm/min,并记录量力环变形和位移值,直到试样破坏。
1.3.2 碳酸钙含量测定试验
用酸洗法测定试样碳酸钙含量,其化学原理见式(2)。取破坏后未压碎的砂块,称其质量为m1,用研钵研磨粉碎后,加入烧杯中,为保证试验结果的准确性,每组选取的砂块质量均为20 g左右。再用5 M的盐酸溶液浸泡,直至没有气泡产生,视为碳酸钙完全溶解。将反应后的砂样用去离子水清洗,烘干后,称砂样质量为m2(g)。碳酸钙含量λ(%)可用式(3)计算得到。
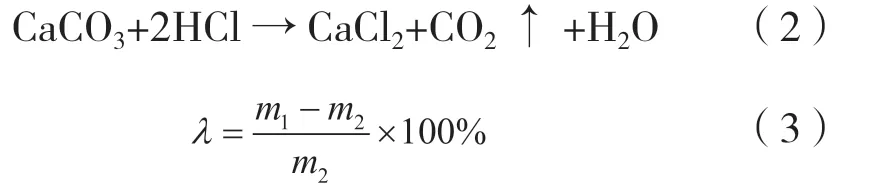
1.3.3 扫描电镜试验
为分析试样的微观结构特征,对试样进行扫描电子显微镜(SEM)试验。在对试样开展无侧限抗压强度试验后,选取一些典型块状样品用于SEM观测。本文选用的扫描电镜型号是ZEISS Sigma 500。
2 结果与讨论
2.1 钙源提取
图3为在不同石灰石粉和乙酸溶液配比(W:V)下,反应后溶液中的钙离子浓度。从图中可以看出,在1:1,1:2,1:4和1:6配比下,钙离子浓度随着配比的减小而略有减小,但相差不大,基本维持在1.99左右。而在1:8配比下,钙离子浓度显著减小,仅为1.41 M,这主要是因为乙酸溶液过量,溶液体积增大。为获得较高的钙离子浓度,并避免石灰石粉的浪费,试验确定1:6的石灰石粉和乙酸溶液配比为最优配比,在此配比下进行后续钙源的提取。
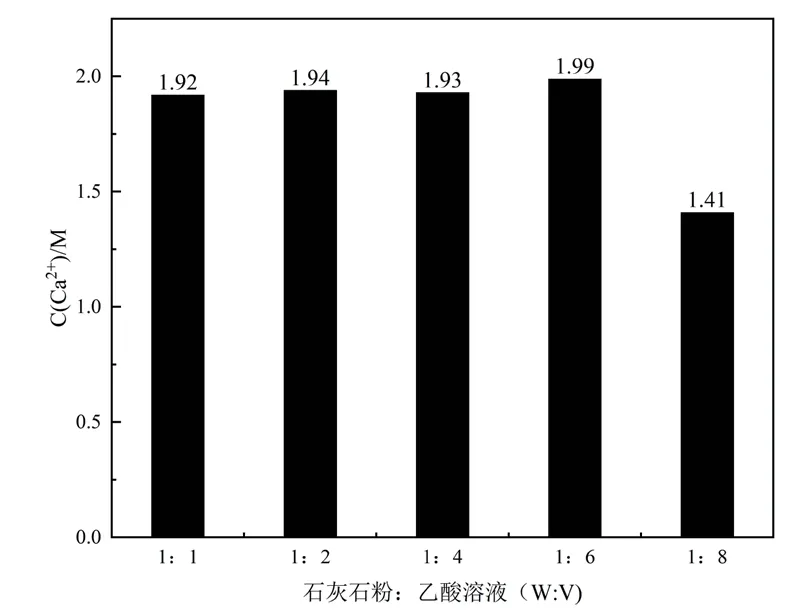
图3 不同配比(W:V)下反应溶液中钙离子浓度Fig. 3 Concentration of calcium ion in reaction solution under different proportioning (W:V)
2.2 无侧限抗压强度
无侧限抗压情况下不同钙源固化砂柱的应力—应变曲线见图4。从图中可以看出:不同钙源固化的砂柱表现出了相似的曲线特征,在加载前期,砂柱内的孔隙逐渐被压密,曲线呈现缓慢增长。随后,应力随应变线性快速增加,达到峰值后,应变继续增加,应力急剧减小到零,呈现典型的脆性破坏模式。
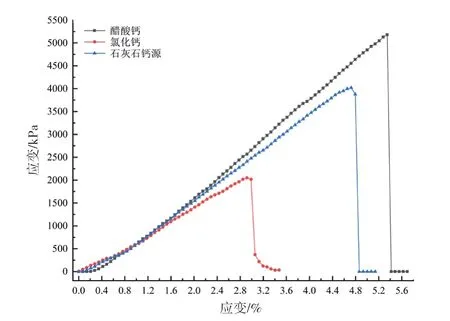
图4 三组试样的应力-应变曲线Fig. 4 Stress-strain curves of three soil samples
图5展示了不同钙源固化砂柱的平均无侧限抗压强度。醋酸钙固化砂柱的无侧限抗压强度略高于石灰石粉提取钙源固化砂柱。而氯化钙固化砂柱的无侧限抗压强度远低于前两者,仅为2.49 MPa,是醋酸钙固化砂柱的一半。这一研究结果与Zhang等(2014)的研究结果一致,即醋酸钙和石灰石粉提取钙源试样的强度高于氯化钙试样的强度。
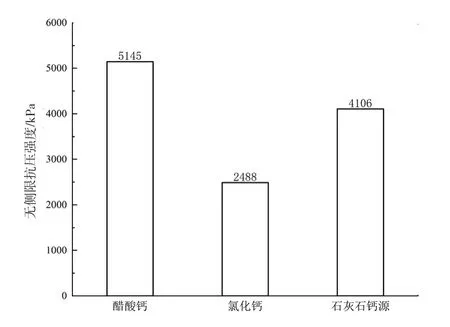
图5 三组试样无侧限抗压强度Fig. 5 Unconfined compression strengths of three soil samples
图6为不同钙源固化砂柱的表观图和破坏形态。观察图6a、c和e固化砂柱的表观图可以看出,醋酸钙和石灰石钙源固化砂柱的表面较光滑,孔隙少,而氯化钙固化砂柱的表面较粗糙,可见明显砂颗粒,孔隙较多。其原因是醋酸钙和石灰石钙源条件下产生的碳酸钙较多,填充了砂柱与模具接触的孔隙以及表面砂颗粒间的孔隙,因而其强度也更高。从图6b、f中可以看出,醋酸钙和石灰石钙源固化砂柱的破坏主要发生在薄弱区,而其他部分仍然保持完整,试样的整体性较高。观察图6e,氯化钙固化砂柱破坏后的残余砂块较小,试样整体发生破坏。这主要是由于氯化钙条件下,碳酸钙产量更小,试样的强度低,松散度高,完整性差。

图6 砂柱表观图和破坏形态Fig. 6 Sand column view and damage morphology
2.3 碳酸钙产量
学界普遍认为,评价微生物固化土体效果的重要指标之一是微生物诱导生成的碳酸钙含量。图7为三组试样中各个平行样的平均碳酸钙含量。如图所示,同一组试样的碳酸钙相差不大。醋酸钙和石灰石粉提取钙源固化砂柱的平均碳酸钙含量分别为16.6%和17.1%,二者相差不大,氯化钙固化砂柱中碳酸钙含量最少,仅为13.4%。醋酸钙和石灰石粉提取钙源的产量更高,说明二者作为钙源与巴氏芽孢八叠球菌的生物化学反应更加充分。
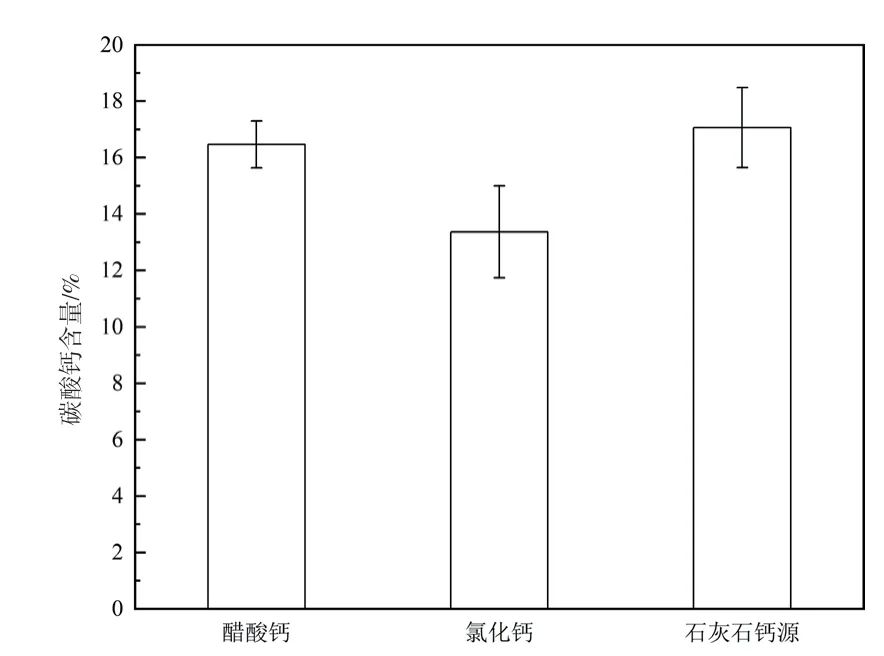
图7 三组试样的碳酸钙含量Fig. 7 Calcium carbonate content of three soil samples
图8给出了各组试样的平均碳酸钙含量以及无侧限抗压强度。从图中可以看出,不同钙源固化砂柱的碳酸钙含量和无侧限抗压强度基本呈正相关关系,这与以往的研究结果相似(Cheng et al., 2014; 梁仕华等,2018)。
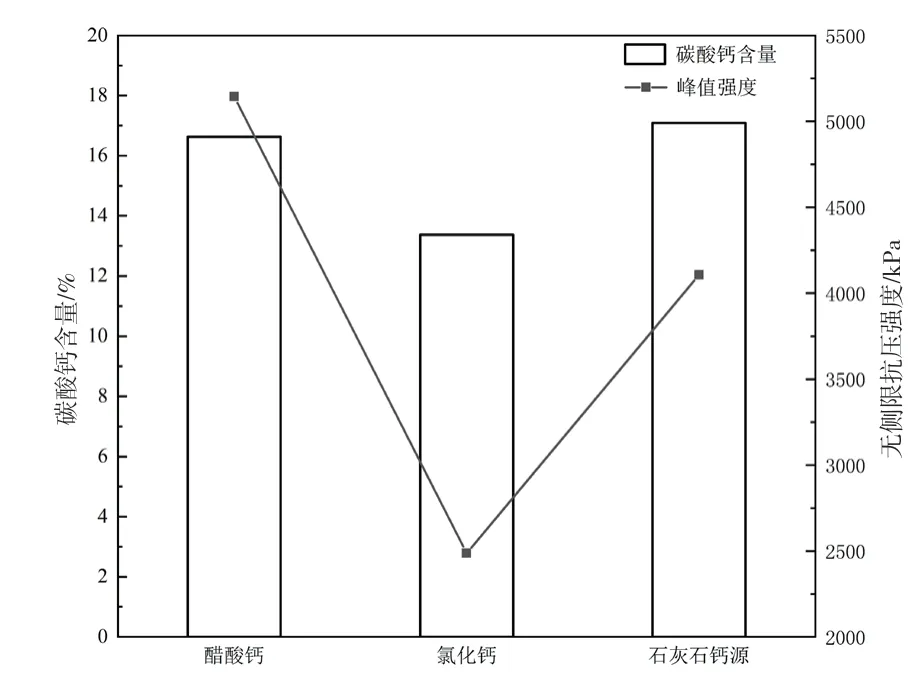
图8 不同钙源对碳酸钙含量和无侧限抗压强度的影响Fig. 8 Influence of different calcium on calcium carbonate content and unconfined compression strengths
2.4 微观结构
为探究不同钙源对微生物固化砂柱微观结构的影响,选取试样的SEM图像进行分析,如图9所示。观察30倍放大条件下的SEM图像可以看出,醋酸钙固化砂柱中砂土颗粒的表面和接触点间均沉积大量碳酸钙,土体结构较致密。碳酸钙主要通过沉积在砂土颗粒接触点之间,联结相邻的土颗粒,从而促进土颗粒的胶结,土体完整性上升,强度提高(Van Paassen et al., 2009; Soon et al., 2013, 2014; Cheng et al., 2016; 季斌等, 2017)。而氯化钙作为钙源固化的砂柱中,砂土颗粒表面和孔隙间沉积的碳酸钙较醋酸钙少,存在更多的土颗粒接触处以及土颗粒表面未被碳酸钙覆盖。石灰石钙源固化砂柱中,砂土颗粒表面和颗粒之间亦形成了大量的碳酸钙沉积。

图9 不同钙源在不同放大倍数下的SEM图像Fig. 9 SEM photos of of different calcium sources at different magnification
从200~1000倍放大条件下的SEM图像中可以看出,以醋酸钙作为钙源,利用巴氏芽孢杆菌诱导生成的碳酸钙晶体主要为薄片状堆叠的方解石。氯化钙诱导生成的碳酸钙晶体主要为六面体状的方解石。利用石灰石钙源诱导生成的晶体亦为薄片状堆叠的方解石型碳酸钙,但其尺寸和致密性略小于醋酸钙诱导生成的碳酸钙晶体。
对石灰石钙源固化砂柱试样的位置1和位置2(图9)进行EDS元素分析,试验结果如图10所示。位置1的主要元素为O、Si和C(图10a),这主要是由于该处位置为砂土颗粒以及少量CH3COO-。位置2的主要元素为O、C和Ca,验证了该位置处大量碳酸钙沉淀的存在。
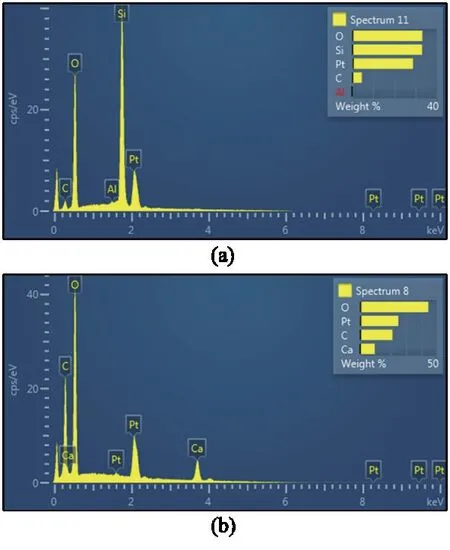
图10 石灰石钙源固化砂柱试样的EDS图Fig. 10 EDS photos of sand column sample treated by calcium source from limestone
从以上结果可以看出,醋酸钙和石灰石钙源固化砂柱的性质类似。这是由于利用石灰石粉提取钙源过程中使用的是醋酸提取石灰石粉中的钙离子,生成的钙源主要为醋酸钙,故二者性质类似。而醋酸钙和氯化钙诱导生成不同的形状的方解石型碳酸钙,这是因为微生物诱导碳酸钙沉积过程中,钙源作为重要的反应物,对于生成的碳酸钙晶体形貌有一定的影响(李沛豪等,2010; Liu et al., 2017)。由此可见,不同的钙源主要通过影响微生物成矿过程的晶型晶貌、晶体含量、晶体分布及胶结特征来改变固化效果。
3 结论
本文将石灰石粉提取钙源用于微生物固化土体反应,通过开展无侧限抗压强度试验,对石灰石钙源固化砂柱的力学特性进行研究,并与醋酸钙和氯化钙钙源进行对比,结合不同钙源固化砂柱的碳酸钙产量和微观结构的分析,得到以下主要结论:
(1)将石灰石粉提取钙源用于微生物诱导碳酸钙固化土体是可行的,甚至优于传统的钙源,固化砂柱的强度和碳酸钙含量较高,结构致密,完整性高。
(2)不同钙源固化砂柱的力学特性不同。三者均呈典型的脆性破坏模式,但醋酸钙固化砂柱的无侧限抗压强度略高于石灰石钙源固化砂柱,而氯化钙固化砂柱的无侧限抗压强度远低于前两者。氯化钙固化砂柱破坏后的完整性低于其他两者。
(3)不同钙源固化砂柱的碳酸钙含量不同。醋酸钙和石灰石钙源固化砂柱的碳酸钙含量相差不大,氯化钙固化砂柱中碳酸钙含量更少。不同钙源固化砂柱的碳酸钙含量和无侧限抗压强度基本呈正相关关系。
(4)醋酸钙和石灰石钙源固化砂柱中砂土颗粒的表面和接触点间均沉积大量碳酸钙,碳酸钙晶体主要为薄片状堆叠的方解石。氯化钙固化砂柱中碳酸钙沉积量低于前两者,碳酸钙晶体主要为六面体状的方解石。
(5)不同的钙源主要通过影响微生物成矿过程的晶型晶貌、晶体含量、晶体分布及胶结特征来改变固化效果。
