洞庭湖不同湖区水体DOM的荧光特征及来源
2022-01-07马飞扬樊团团孙小平明峻德王世同张英豪姚昕
马飞扬,樊团团,孙小平,明峻德,王世同,张英豪,姚昕*
1. 聊城大学环境与规划学院,山东 聊城 252059;2. 山东省聊城生态环境监测中心,山东 聊城 252000
溶解性有机质(dissolved organic matter,DOM)是一类由多种活性有机物(如多糖、蛋白质和木质素)组成的复杂的多相混合物,包括氨基、羧基、酯、酮、酚等多种官能团(Zhang et al.,2021)。主要集中在富营养化湖泊、海洋及河口等水体中,其复杂的化学结构和光学特性对水生生态系统中有机污染物迁移转化和水生生态系统具有重要影响(Graeber et al.,2015;Butturini et al.,2020)。内陆湖泊中的 DOM 主要受陆源输入和生物内源降解释放的影响,外源以人为污染物、土壤等输入为主,而内源DOM的主要源于浮游植物、藻类、水生植物等腐蚀降解(Kothawala et al.,2012;吕伟伟等,2018;Lao et al.,2019)。DOM是陆地和水生环境之间进行密切联系的“关系纽带”,对其含量、来源、荧光特征及环境行为的分析以准确地了解水体污染物的来源及受污染程度,这对于水环境污染防治工作具有十分重要的指导性意义,且洞庭湖作为长江流域内重要的调蓄型湖泊,良好的水质状况是人类用水安全的重要保障(Wang et al.,2017;Bertolet et al.,2018;Shan et al.,2019;Butturini et al.,2020)。
紫外-可见光谱(ultraviolet-visible absorption spectrum,UV-Vis)、平行因子分析法(parallel factoranalysis,PARAFAC)和同步荧光光谱(synchronous fluorescence spectroscopy,SFS)等技术手段已普遍用于湖泊及河流等水体DOM的研究当中,利用DOM的光谱特性解析湖泊水体的水质状况及污染物来源成为水质环境监测中必不可少的监测技术手段之一(Cheng et al.,2015;吕伟伟等,2018)。洞庭湖作为长江流域重要的渔业和淡水资源库,对中国长江流域沿岸的发展具有重要经济价值和生态价值,由于其湖面广阔,夏季雨量丰沛,入湖河流众多,沿岸城市密集加之工业排污和水产养殖,在多种自然和人为因素影响下,不同湖区的水质状况不尽相同。鉴于此,本文利用紫外-可见光谱(UV-Vis)、平行因子分析法(PARAFAC)、同步荧光光谱(SFS)技术分析夏季洞庭湖的水体中DOM的来源、特性及不同湖区DOM来源的差异性,为保障长江流域调水安全和水质监管提供一定参考。
1 材料与方法
1.1 研究区概况
洞庭湖(111°40′—113°10′E、28°30′—29°31′N)位于长江中游的荆江河段南部,涉及湘、鄂、黔等六省,南有四水汇入,北有三口分泄长江之水。研究地处亚热带季风湿润气候区,年均气温 16.4—17.0 ℃,年降雨量为1307.6—1505.2 mm。洞庭湖是中国淡水湖泊中水量最大的通江湖泊,受自然因素和人为因素的影响,分流入湖的洪水夹带大量泥沙于湖盆,导致洞庭湖面积不断缩小,并逐渐被分割为东、南、西三部分(Dai et al.,2017;胡光伟等,2019)。
1.2 样品的采集与预处理
2020年6月在洞庭湖共采集19个样品,DT(1—9)源于东洞庭湖,DT(10—15)位于南洞庭湖,DT(16—19)设于西洞庭湖(图1)。采集水体表层0.5 m深处的水样500 mL,低温保存,采样结束后2—3 d内完成DOM的三维荧光光谱及紫外吸收光谱分析(Zhou et al.,2013)。
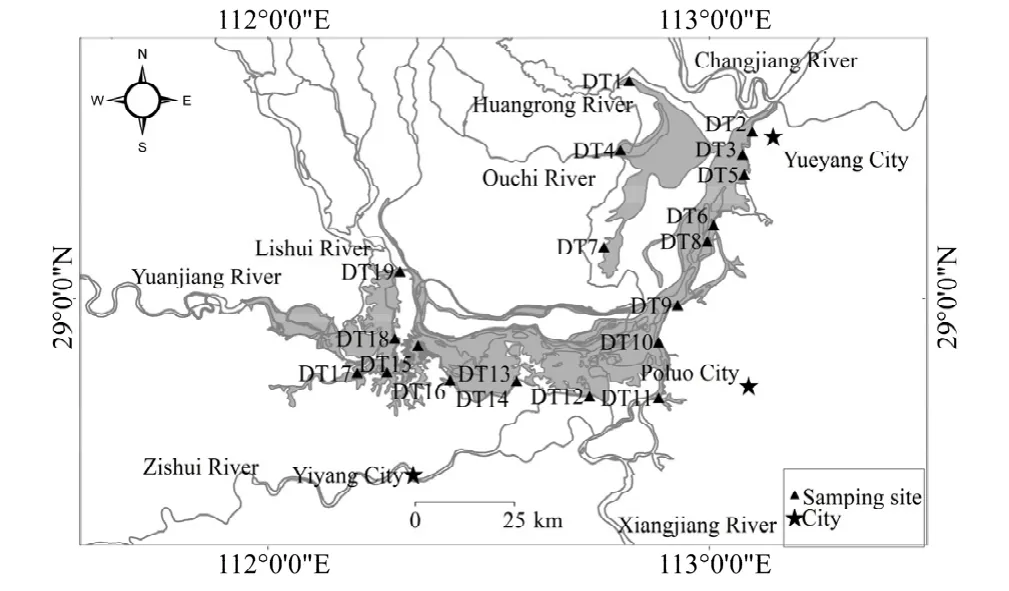
图1 洞庭湖采样点位置Fig. 1 Location of sampling sites in Dongting Lake
1.3 样品的测定
1.3.1 DOM荧光测定
样品经0.70 µm的GF/F滤膜(预先于450 ℃灼烧)过滤,过滤后的水用于其他指标及三维荧光光谱、同步荧光光谱测定。DOM 的三维荧光光谱(EEM)及同步荧光光谱(SFS)采用荧光光谱仪(F-7000,日立)测定。三维荧光光谱扫描范围为发射波长250—550 nm,间隔为1 nm,激发波长200—450 nm,间隔为5 nm,扫描速度为2400 nm/min,激发和发射狭缝带宽为5 nm,Milli-Q水作为空白参比。同步荧光光谱扫描范围为200—450 nm,间隔为0.2 nm,扫描速度均为240 nm/min。
1.3.2 PARAFAC
在 MATLAB中利用 DOM Fluor工具箱运行PARAFAC模型对样点的三维荧光数据进行分析。PARAFAC法计算过程可以称为交替最小二乘(ALS)算法(Gou et al.,2017):
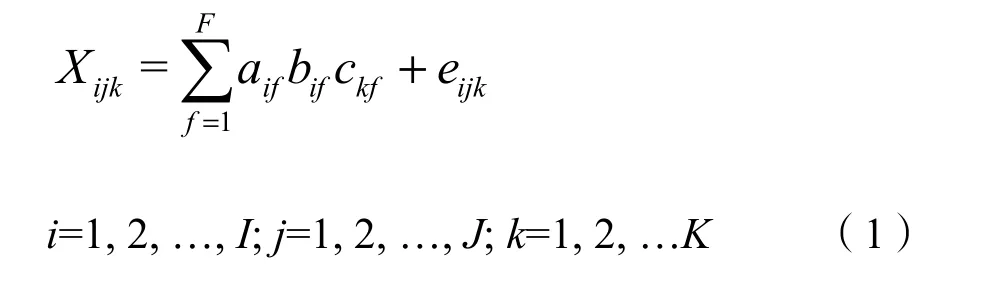
式中:
Xij——第i个样点再激发波长为k、发射波长为j处的荧光强度;
aif——第i个样点的第f次分析的含量;
bjf和ckf——与第f次分析后激发波长为j、发射波长为k光谱的线性相关;
eijk——系统残差,是不受模型控制的变量;
F——模型中选择的组分因子数量。
1.3.3 光谱吸收系数的测定
采用UV-Vis光谱仪(UV-T6,屹谱)得到DOM的吸收光谱,使用10 mm的石英比色皿,波长范围200—800 nm,间隔1 nm,狭缝宽度1 nm,波长扫描速度为210 nm/min。Milli-Q水作为空白参比,以700 nm处的吸收值作为基线进行光谱校正,而后根据公式(2)计算对应波长的吸收系数(Li et al.,2014;Qiao et al.,2021):

a(λ)——经过散射校正后的波长 λ处的吸收系数(m−1);
λ——波长(nm);
D(λ)——波长λ处的吸光度;
r——光程路径(m)。
A250/A365指250 nm和365 nm处吸光度的比值,腐殖酸所占比例越高则A250/A365值越小,相对分子量越大(Olefeldt et al.,2013;Elena et al.,2019);吸收系数a254常用来表征DOM的相对浓度;ASUV、ASUV-260指吸收系数a254、a260与DOC的比值,表征DOM腐殖化程度和疏水性(Li et al.,2014;Kim et al.,2017;Jian et al.,2021)。
1.3.4 半变异函数
半变异函数γ(h)可以用于分析洞庭湖水质参数空间变异特征,以用来区分结构因素(湖泊水文环境、底泥、水生生物活动等)与随机因素(径流注入、人类活动等)的影响程度,公式如下(陈昭等,2019;李庚飞等,2020):
正如有的学者所言,“刑事政策的终极目的是维护社会秩序,也即强调构成社会的个人和集团之间的调和、安定并促进社会的发展。”[5]刑事立法政策作为一项公共政策,其反映的是政府机构与其周围环境之间的关系,公民意志作为众多关系中的重要一环,对于一项刑事立法政策是“良策”还是“恶策”具有决定性的影响。刑事立法政策要做到调和社会关系、维持社会秩序就必须适度接纳民意。
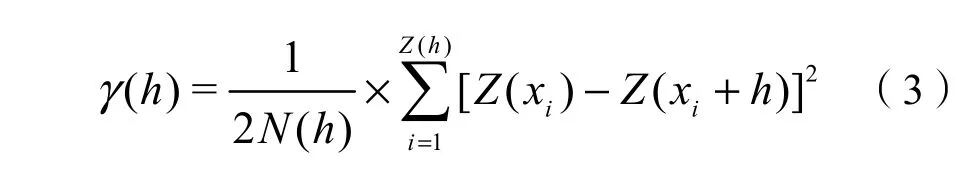
式中:
h——步长,是分隔两个采样点的矢量;
N(h)——相隔h的点对数;
Z(xi)和Z(xi+h)——营养盐在位置xi和xi+h处的实际测量值。
通过半变异函数和半方差图得到的块金值(C0)、基台值(C0+C)和变程值(a)一定程度上可用于揭示空间变异和相关性,C0和(C0+C)的比值块金系数可用于表征某参数的空间相关程度。
1.3.5 主要水质参数测定
溶解性有机碳(DOC)的质量浓度使用Elementar vario TOC分析仪测定;COD、TN、TP、Chla等质量浓度参照相关文献方法进行测定(吕伟伟等,2018)。
1.4 数据处理
采样点的分布及各参数的空间分布特征图使用ArcGIS 10.6软件进行绘制,使用R 4.0.2进行相关性图的绘制,样本相关参数(均值、标准差等)及显著性检验等采用 IBM SPSS Statistics 23.0软件分析,相关性分析用于检测变量间的相关程度;P>0.05表示未达到显著检验水平,0.01<P<0.05为显著水平,P<0.01为极显著水平。

图 2 洞庭湖夏季A250/A365(a)、a254(b)、ASUV(c)、ASUV-260(d)、FI(e)、BIX(f)、HIX(g)、Fmax(h)组分 C1(i)、C2(j)、C3(k)、C4(l)的空间分布Fig. 2 Spatial distribution of A250/A365 (a), a254 (b), ASUV (c), ASUV-260 (d), FI (e), BIX (f), HIX (g), Fmax (h) and C1 (i),C2 (j), C3 (k), C4 (l) in Dongting Lake in summer
2 结果与分析
2.1 洞庭湖相关水质指标
洞庭湖水体中 ρ(DOC)为 5.02 mg·L−1,变化范围在 3.70—9.45 mg·L−1之间,ρ(COD)取值为 3.43 mg·L−1,变化范围为 2.37—6.60 mg·L−1;ρ(TN)为 2.02 mg·L−1,变化范围为 1.47—2.72 mg·L−1;ρ(TP)取值为0.14 mg·L−1,取值范围为 0.08—0.24 mg·L−1;ρ(Chla)为 10.41 mg·L−1,范围在 3.66—34.39 mg·L−1;水质硬度为 171.11 mg·L−1,范围在 109.37—215.36 mg·L−1之间。ρ(COD)符合《地表水环境质量标准》(GB 3838—2002)Ⅰ类标准;ρ(TN)超过《地表水环境质量标准》(GB 3838—2002)Ⅴ类标准;ρ(TP)符合《地表水环境质量标准》(GB 3838—2002)Ⅲ类标准。与以往的研究相比,洞庭湖的水体中的ρ(COD)、ρ(TN)、ρ(TP)、ρ(Chla)均有很大程度的增加(熊剑等,2016)。
2.2 紫外光谱特征
A250/A365、a254、ASUV、ASUV-260等吸收参数的空间分布如图2所示。洞庭湖A250/A365变化范围为3.34—6.86(均值为 5.41±0.80)(P>0.05),说明洞庭湖DOM以类富里酸物质为主(Elena et al.,2019;翟天恩等,2017)。a254变化范围为 9.52—28.88 m−1,均值为 (13.59±6.04) m−1(P>0.05);ASUV值为(2.68±0.22) L·mg−1·m−1, 范 围 在 2.35 — 3.24 L·mg−1·m−1之间;ASUV-260值范围为 2.18—2.99 L·mg−1·m−1,均值为 (2.48±0.21) L·mg−1·m−1。洞庭湖各吸收参数空间上呈现一定的分布规律,即a254、ASUV、ASUV-260最大值均出现在洞庭湖东部,南洞庭湖的 ASUV、ASUV-260显著高于西洞庭湖(t=2.894,P=0.020;t=2.355,P=0.013)(图 2a—d)(表1),与东洞庭湖并无显著差异,这可能与洞庭湖复杂的水文环境及水向东过程中受太阳光辐射导致水体中物质性质发生变化有关(Ma et al.,2009;Jian et al.,2021)。
利用地统计分析中的半变异函数 γ(h)分析来区分结构因素与随机因素对DOM空间变异特征的影响(陈昭等,2019;李庚飞等,2020)。结果如表1所示,整体上,洞庭湖 A250/A365、a254、ASUV和 ASUV-260块金系数均小于0.25,为强烈的空间自相关性,主要受结构性因素的影响。变异系数表明,洞庭湖东、南、西3个湖区A250/A365、a254、ASUV和ASUV-260均呈弱变异,主要受结构性因素的影响。
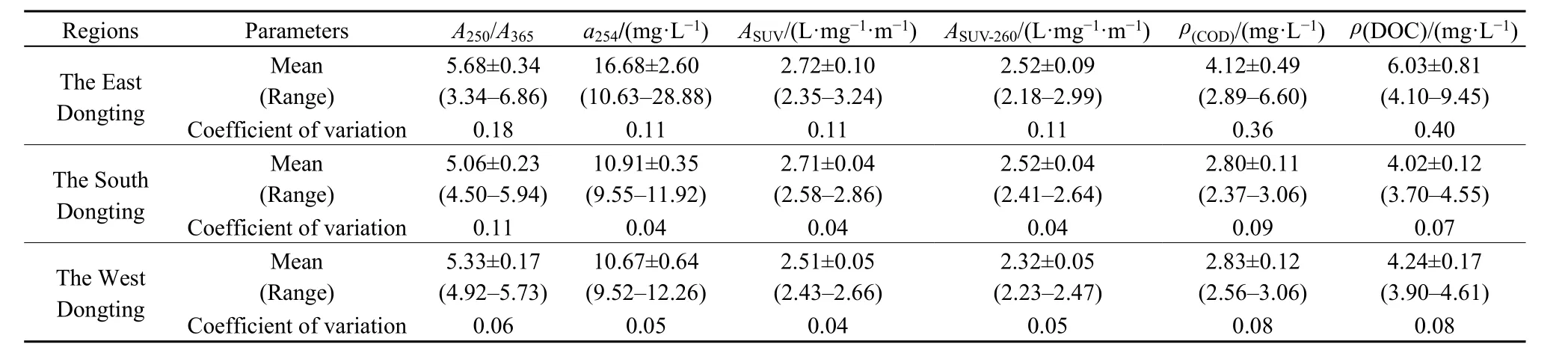
表1 洞庭湖东、南、西3个湖区的A250/A365、a254、ASUV、ASUV-260、ρ(COD)、ρ(DOC)吸收参数比较Table 1 Comparison of absorption parameters for A250/A365, a254, ASUV, ASUV-260, ρ(COD), ρ(DOC) in three lakes of Dongting
2.3 荧光光谱分析
2.3.1 同步荧光光谱特征
如图3a—c,剔除部分异常值(DT7)后,洞庭湖东、南、西3个湖区的SFS均存在明显且相似的荧光峰。同步荧光谱图显示洞庭湖DOM中存在类蛋白(PLF)、类富里酸(FLF)和类腐殖质(HLF)3类物质(Wu et al.,2019;栗婷婷等,2018)。东洞庭湖多数样点的最高峰为FLF荧光峰,DT5最高峰为PLF峰,FLF最高峰出现在DT1,其次DT4,最小值出现在DT2。南洞庭湖各样点FLF区域内的峰值高低顺序为 DT11>DT10>DT13>DT14> DT15,样点(除DT11)的最高峰均处于FLF区域,而FLF和 PLF区域内的最高峰均在 DT11,FLF区域内DT14峰值最低。西洞庭DT17、DT19位于PLF区域的峰最高,其余样点的高值均分布在 FLF范围内,高低顺序为 DT17>DT19>DT16>DT18。

图3 洞庭湖东、南、西3个湖区DOM的同步荧光光谱Fig. 3 Synchronous fluorescence spectra of DOM from East Dongting Lake (a), South Dongting Lake (b), and West Dongting Lake (c)
SFS测定PLF、FLF、HLF的区域面积可以用来解释相应荧光物质的含量变化(图4a)(刘文等,2016)。东洞庭湖PLF区域面积显著高于南洞庭湖(t=2.195,P=0.035)、西洞庭湖(t=1.872,P=0.031),各湖区 PLF区域面积大小顺序为东洞庭湖(408.11±152.02 a.u.)>南洞庭湖 (265.18±50.35 a.u.)>西洞庭湖 (259.83±43.27 a.u.);东洞庭湖FLF区域面积显著高于西洞庭湖(t=1.796,P=0.035),整体表现为东洞庭湖 (777.10±303.89 a.u.)>南洞庭湖(553.37±75.27 a.u.)>西洞庭湖 (495.10±60.07 a.u.);HLF在各湖区含量大小为东洞庭湖 (21.67±8.59 a.u.)> 南 洞 庭 湖 (16.34±1.69 a.u.)> 西 洞 庭 湖(14.89±2.02 a.u.),3个湖区 HLF含量无显著差异(P>0.05)。3类物质各荧光峰面积之和占总面积的百分比如图4b所示,PLF变化范围为 30.18%—37.65%,FLF变化范围为 60.92%—67.74%,HLF变化范围为1.44%—2.10%,东洞庭湖水体中的类蛋白和类富里酸物质均高于其他湖区,类富里酸物质是洞庭湖水体DOM的主要组成部分。
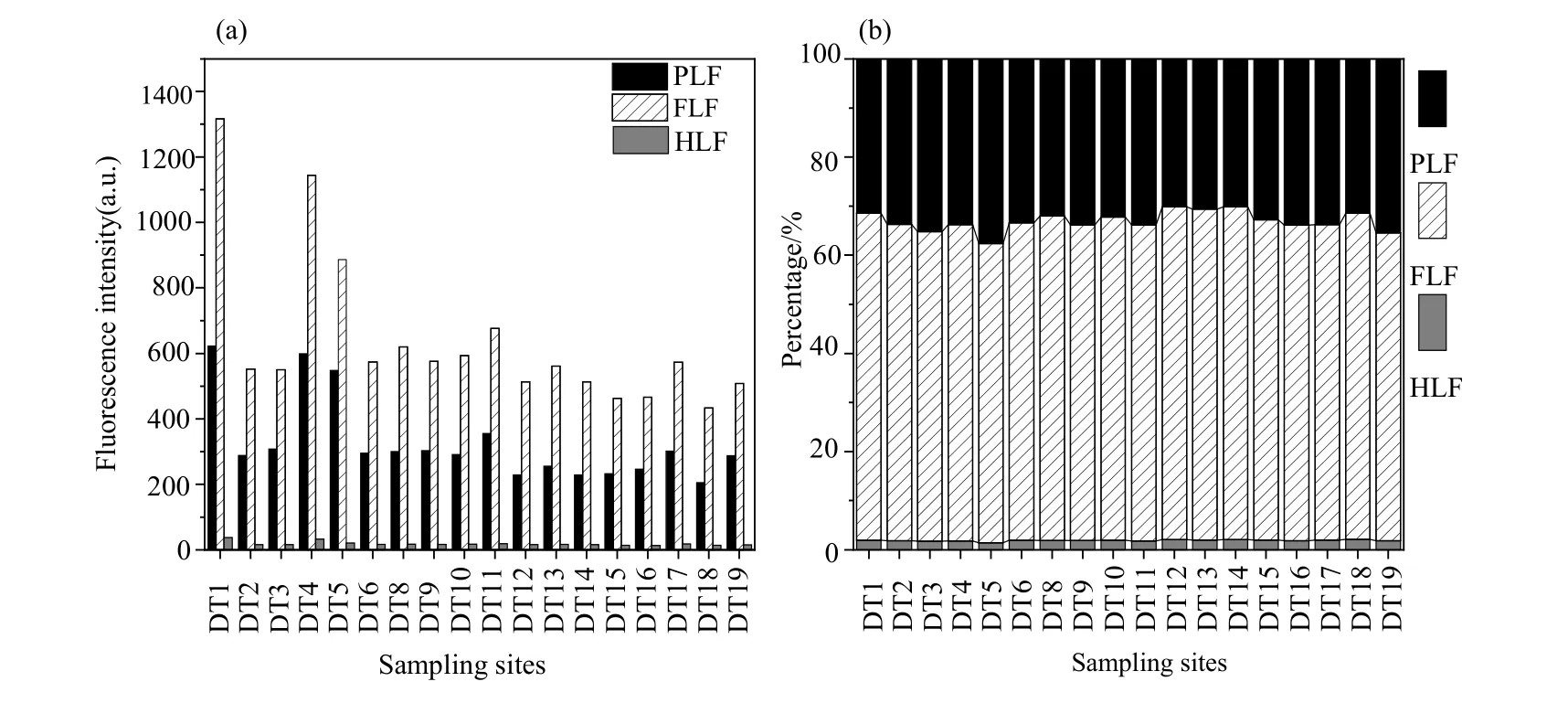
图4 东洞庭湖(DT1—DT9)、南洞庭湖(DT10—DT15)、西洞庭湖(DT16—DT19)DOM物质含量(a)和百分比(b)的分布Fig. 4 Distributions of the contents (a) and percentages (b) of DOM fractions in East Dongting Lake (DT1-DT9),South Dongting Lake (DT10-DT15) and West Dongting Lake (DT16-DT19)
2.3.2 三维荧光光谱特征分析
三维荧光测定共检测出5个荧光峰,峰A和峰C为类富里酸荧光峰值(Cheng et al.,2015)、D峰为生物降解来源的类酪氨酸(Chen et al.,2015)、峰T为生物降解来源的类色氨酸(Bu et al.,2019)、M峰属于海源类腐殖质荧光物质降解产物(Cheng et al.,2015)。与太湖等典型富营养化湖泊呈现强烈的类蛋白荧光信号不同,洞庭湖东、南、西3个湖区均呈现较强的类腐殖质荧光特征(吕伟伟等,2018)。
平行因子分析(PARAFAC)得出了 4个荧光组分(图5):C1(Ex/Em:240,340/430 nm)主要反映了长波类腐殖质的荧光性质,对应A峰和C峰;C2(Ex/Em:250,310/400 nm)属于典型的短波类腐殖质的荧光性质,对应传统的A峰和M峰;C3(Ex/Em:230,280/375 nm)为类蛋白荧光基团,对应传统的T峰和D峰;C4(Ex/Em:250/480 nm)为类胡敏酸荧光组分,与A峰相对应。

图5 三维荧光结合平行因子分析模型识别的4种荧光组分Fig. 5 Four different fluorescence component identified by 3D EEM-PARAFAC model
洞庭湖总荧光强度Fmax取值范围为0.52—1.53 R.U,均值为 (0.75±0.27) R.U,变异系数为0.52,为中等程度的空间变异,受结构性因素和随机因素影响,空间上呈现“东>南>西”的分布趋势(图2h)。东、南、西3个湖区间的总荧光强度(取值范围)分别为:(0.92±0.343) R.U(范围为 0.70—1.53 R.U)、(0.66±0.10) R.U(范围为 0.53—0.79 R.U)、(0.59±0.09) R.U(范围为0.52—0.72 R.U)。3个湖区总荧光强度的空间变异结果显示,东洞庭湖为强变异(变异系数为 0.70),含量变幅较大,最高值出现在东洞庭湖西北部湖域,说明东洞庭湖 DOM受结构性因素和随机因素的共同影响;南洞庭湖(变异系数为0.15)、西洞庭湖(变异系数为0.16)均为弱变异,主要受结构性因素影响。为进一步了解洞庭湖3个湖区DOM的来源,对洞庭湖4类组分在3个湖区荧光强度及贡献率进行分析。其中,类富里酸组分在 3个湖区的荧光强度(组分 C1、C2 荧光强度之和)分别为(0.53±0.21)、(0.39±0.06)、(0.33±0.05) R.U,贡献率分别为(57.25%±1.43%)、(58.59%±1.06%)、(56.86%±1.14%),东洞庭湖的类富里酸组分荧光强度显著高于西洞庭湖(t=1.848,P=0.046);类蛋白组分C3在3个湖区的荧光强度分别为(0.24±0.08)、(0.16±0.03)、(0.15±0.03) R.U,贡献率分别为(25.84%±2.08%)、(23.65%±1.63%)、(25.66%±1.56%),东洞庭湖显著高于南洞庭湖(t=2.355,P=0.037);类胡敏酸组分C4在3个湖区的 荧 光 强 度 分 别 为 (0.16±0.06)、 (0.12±0.01)、(0.10±0.01) R.U,贡献率分别为(16.91%±0.81%)、(17.76%±0.65%)、(17.48%±0.43%)(图 2i—j),东洞庭湖显著高于西洞庭湖(t=1.869,P=0.044)。3个湖区类富里酸组分(C1、C2)贡献率均在 56%之上(P>0.05),其中,类蛋白组分C3贡献率均在23%以上(P>0.05),说明类富里酸物质对水体中DOM的贡献程度最大,其次是类蛋白物质,这与同步荧光分析结果相一致。东洞庭湖较高的类蛋白组分贡献率可能与周围人类活动有关(田泽斌等,2014)。
2.4 荧光指数分析
荧光光谱指数(FI、BIX、HIX)可以表征不同物质来源对DOM的相对贡献程度(Yao et al.,2012;Nie et al.,2017;Qiao et al.,2021)。荧光指数(FI)可以表征DOM的来源及DOM的降解程度。洞庭湖的FI值范围为2.28—2.54,平均值 (2.39±0.08),接近生物来源FI值,说明洞庭湖夏季DOM受内源贡献率较大。生物源指数(BIX)表征自生源对湖泊中DOM的相对贡献程度(Nie et al.,2017)。洞庭湖水体 BIX在 0.87—1.54之间,平均值为(0.97±0.15),表现为较强的自生源特征。腐殖化指数(HIX)表征DOM腐殖化程度(Bu et al.,2019;Qiao et al.,2021),HIX处于1.19—5.74之间,平均值为 (4.61±0.99),整体上表现为较弱腐殖质特征,洞庭湖水体腐殖化程度较低。洞庭湖水体BIX、HIX空间上虽呈现一定的分布规律(图2f和图2g),但通过相关性分析发现,3个湖区间BIX、HIX差异性并不显著(P>0.05)。就空间变异程度来说,洞庭湖东、南、西3个湖区BIX变异系数均小于0.25,主要为结构性因素影响;东洞庭湖的HIX变异系数为0.30,受结构性因素和随机因素共同影响,其余两个湖区HIX值均受结构性影响。
2.5 荧光组分与各水质参数之间的关系
如图6所示,洞庭湖C1、C2、C3、C4间互为极显著正相关关系(P<0.01),值得注意的是,组分C2和 C4的相关系数达到了 1.00(P<0.01),不同组分间可能存在相同的来源或变化趋势(江俊武等,2017)。ρ(COD)、ρ(DOC)、a254和 A250/A365与 4 类组分荧光强度均为显著正相关性(P<0.01),说明荧光强度的分布情况在一定情况上可以反映水体中有机物的含量和相对分子量大小(Fang et al.,2011;吕伟伟等,2018)。4类组分中,a254与类富里酸组分(C1、C2)的相关系数均在0.97以上(P<0.01)(图6),而洞庭湖水体DOM的主要贡献组分为类富里酸,因此,类富里酸是影响洞庭湖DOM丰度的主要物质。

图6 洞庭湖水体DOM的荧光组分间及组分与水质参数间的相关性分析Fig. 6 Correlation analysis between fluorescence components and water quality parameters of DOM in Dongting Lake
通常,受输入源、周围环境及水生生物含量等综合因素的影响,同一湖泊生态系统中不同湖域DOM 的成分、结构及荧光特性也会存在一定差异(吕伟伟等,2018)。3个湖区4类组分与各水质参数的相关分析结果显示,东洞庭湖 4类组分之间及显著相关(P<0.01),且均与 ρ(COD)、ρ(DOC)、a254呈极显著正相关关系(P<0.01)(图7);南洞庭湖区4类组分之间及组分与ρ(DOC)、a254、A250/A365均呈显著相关关系(P>0.05)(图8);西洞庭湖组分之间及组分与各参数间相关性均无显著相关性(P>0.05)。洞庭湖东、南、西3个湖区的4类组分与ρ(COD)、ρ(DOC)、a254和A250/A365之间的相关性不尽相同,这可能与河流输入、水文环境差异和光辐射变化有关,三峡工程的运行对洞庭湖水文、湖泊污染物转化迁移及富营养化等方面的影响同样不可忽视(Lai et al.,2013;Wang et al.,2017;吕伟伟等,2018)。
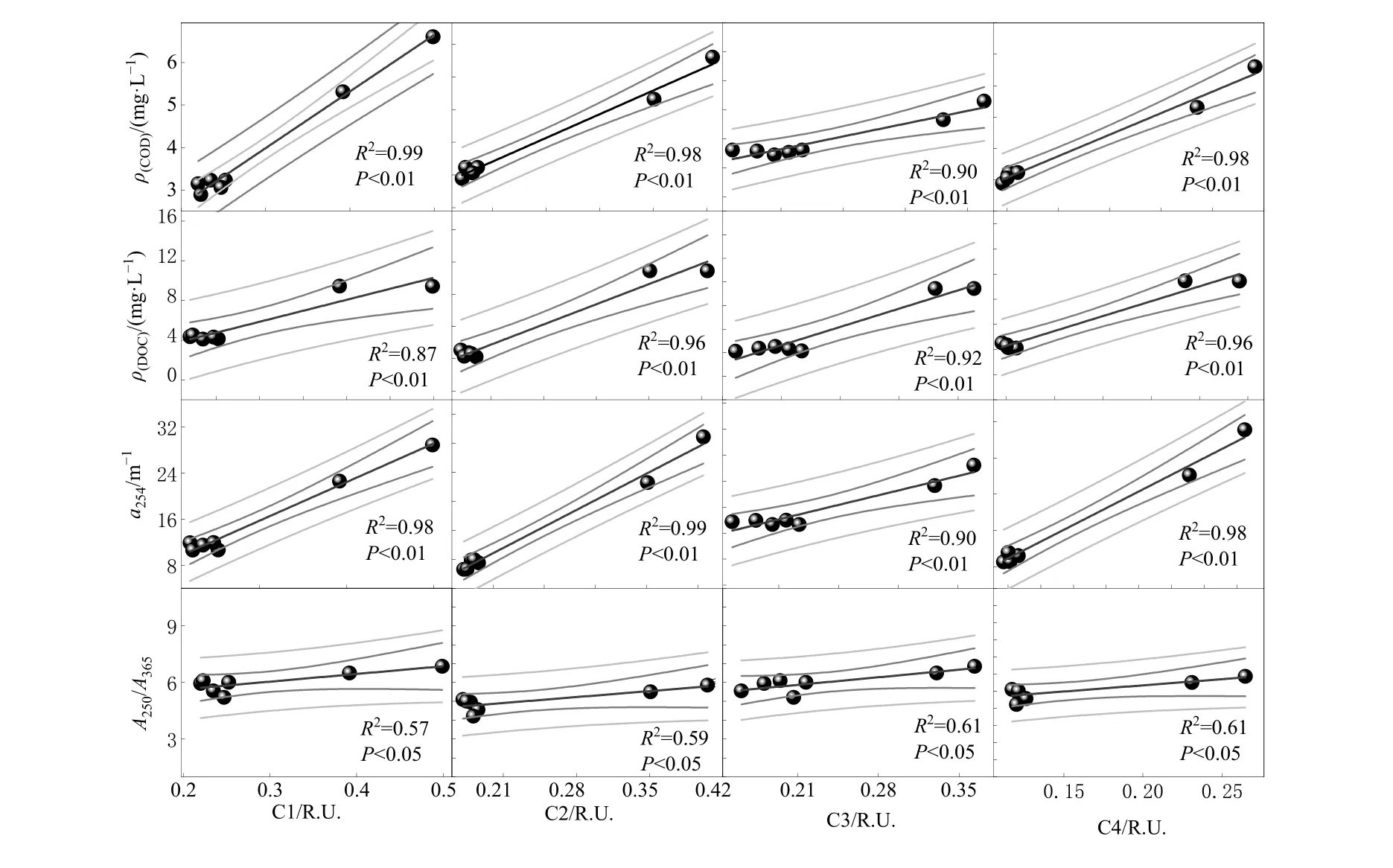
图7 东洞庭湖湖区4组荧光组分与主要水质参数的相关性分析Fig. 7 Correlation analysis between four groups of fluorescence components and main water quality parameters in East Dongting Lake

图8 南洞庭湖湖区4组荧光组分与主要水质参数的相关性分析Fig. 8 Correlation analysis between four groups of fluorescence components and main water quality parameters in South Dongting Lake
3 讨论
3.1 洞庭湖水体DOM的荧光特性
洞庭湖面积广阔,湖泊水体受水文环境、河流汇入、人类排污及内部动植物腐蚀降解释放的等多种因素的影响。相关报道发现,洞庭湖污染程度在不断加深,部分区域水体出现轻度富营养化,入湖河流及周围人类活动是造成湖泊有机污染物积累的主要因素(Li et al.,2016;Dai et al.,2017)。采样时间虽处于雨水丰沛的夏季,但洞庭湖的ρ(COD)、ρ(TN)、ρ(TP)、ρ(Chla)与以往的研究相比均有很大程度的增加,说明洞庭湖污染程度有增大的趋势。组分及荧光指数结果显示,洞庭湖整体以内源输入为主,水体DOM中的类富里酸组分贡献率在56%以上,类蛋白组分C3贡献率在23%以上,说明类腐殖质物质和类蛋白物质为水体DOM中的主要组成部分,类富里酸是影响洞庭湖水体DOM浓度的主要物质。相关性结果显示,洞庭湖表层水体 DOM的4类组分之间均为显著正相关关系(P<0.01),说明水体中的4类组分之间具有相似的来源,联系密切。ρ(DOC)、ρ(COD)、a254和 A250/A365与 4类组分荧光强度均为显著正相关关系(P<0.01)(图 6),与其他吸收参数及组分的相关性较差(P>0.05),表明A250/A365、ρ(DOC)、ρ(COD)、a254可以用来指示洞庭湖水体DOM的荧光变化,湖泊水体在丰水期受陆源输入影响较少,主要受结构性因素影响,水动力扰动、水流速度及方向对湖泊污染物转化迁移及富营养化等方面的影响较大(张光贵,2016)。
3.2 洞庭湖不同湖区DOM的来源
相关性分析结果表明,洞庭湖东、南、西3个湖区 4 类组分与 ρ(DOC)、ρ(COD)、a254和 A250/A365之间的相关性不尽相同,东洞庭湖的组分与参数相关性极显著(P<0.01),其水体DOM中的类蛋白物质、类腐殖质物质含量均表现为东>南>西,这与洞庭湖独特的湖水流向、河流输入、长江之间的顶托作用和沿岸居民活动等不无关系(张光贵,2016)。田泽斌等(2014)发现频繁的人类活动造成的湖底沉积物再悬浮会增加洞庭湖东部水体氮、磷浓度,沿岸人为排放的污染物汇入也会加剧湖水污染。东洞庭湖作为湖水聚集区,大量有机物污染物的经过河流输入再由西、南湖区向东汇聚,与此同时,江与湖之间的顶托作用造成的阻力促使有机物汇集,为东洞庭湖的芦苇、苔草、浮游动植物提供良好的生长环境,生物腐解沉降的有机物质可能经水力扰动、洪水冲刷等作用再悬浮等对东洞庭湖水质造成影响(Lai et al.,2013;张光贵,2016)。另一方面,洞庭湖东部沿岸发达城市频繁的人类活动造成的污染物输入及大量渔业、其他企业的存在会向湖水中输入大量的类蛋白物质,相对而言,丰水期大量河水、雨水的冲刷对南、西部湖区的污染物具有一定的稀释、搬运作用,南、西湖区受污染程度较低,胡光伟亦认为,东洞庭湖水质污染最严重,这与江湖作用、沿岸企业分布及三峡工程运行不无关系(胡光伟等,2019)。
综上,洞庭湖东、南、西3个湖区的彼此联系,相互影响。洞庭湖作为特殊的吞吐性湖泊,相对而言,汛期来自其他西、南两湖区污染物汇集、沿岸人口类活动、江与湖之间顶托作用造成的水流不畅是造成东洞庭湖水体污染物聚积的重要原因,虽然丰水期大量淡水的冲刷、稀释对洞庭湖西、南湖区具有一定的清洁作用,污染程度相对东部较轻,但也需要引起重视,研究发现,三峡工程集中蓄水水流速度下降东部、南部滩涂区可能会增大水华的风险(Dai et al.,2017)。因此,对不同湖区制定不同治理方案,加强排污监管力度等是防止洞庭湖进一步污染的有效措施。
4 结论
(1)洞庭湖水体中的DOM一共含有4类荧光组分,主要为C1和C2(类富里酸组分)、C3(类蛋白组分)、C4(类胡敏酸组分)。同步荧光及各组分荧光强度分析结果表明,类富里酸为水体 DOM组成的主要组分,也是影响洞庭湖水体DOM浓度的主要物质。
(2)地统计分析结果表明,吸收参数A250/A365、a254、ASUV和ASUV-260的空间分布主要受结构性因素影响,湖泊整体以内源输入为主。相关性分析结果显示,洞庭湖4类组分呈极显著相关关系(P<0.01),说明洞庭湖水体 DOM 来源具有同源性。洞庭湖DOM 的 4 类荧光组分与 ρ(DOC)、ρ(COD)、a254、A250/A365相关性显著,说明 ρ(DOC)、ρ(COD)、a254、A250/A365可以用于表征洞庭湖水体DOM的浓度。东洞庭湖较高的类腐殖质物质和类蛋白物质可能源是人为活动及河流输入的共同作用的结果。
(3)洞庭湖东、南、西3个湖区彼此联系,相互影响,东洞庭湖受污染程度相对较高,江与湖之间顶托作用造成的水流不畅及周边企业排污是导致东洞庭湖水体污染较为严重的重要原因。
