乙烯基修饰三苯基三嗪为受体单元的激基复合物发光性能
2022-01-06林武滔
林武滔
(三明学院 资源与化工学院,福建 三明 365004)
第三代有机电致发光材料——热激活延迟荧光(thermally activated delayed fluorescence,TADF)材料逐渐成为OLED材料研究的热点[1]。发光材料应用于电致发光时,其发光效率主要由激子利用率决定,可应用的发光材料主要有荧光、磷光和延迟荧光材料等,其中TADF材料由于可采取全有机结构的方式实现单、三线态激子的100%利用率,具有前二者不可比拟的优势[1]。传统的TADF材料主要由电子给体单元(DONOR,D)和电子受体单元(ACCEPTOR,A)通过形成扭曲结构,保障HOMO-LUMO能级的充分分离以减小单、三线态能级差ΔES-T,从而获得高效的三线态激子利用率[3]。近年来的研究发现,系列空穴传输材料与电子传输材料亦可分别作为电子给体和受体单相互作用形成的激基复合物(exciplex)亦可实现TADF性质[4],D-A单元分属两个分子,使HOMO-LUMO能级充分分离,通常所得Exciplex-TADF的ΔES-T极小,三线态激子利用率较高,不论是作为发光单元还是作为掺杂主体单元都具有优异的发光性能[5]。
2012年日本九州大学 Adachi研究小组首次发现了TADF现象[6]。Adachi研究小组以m-MTDATA为电子给体、3TPYMB为电子受体(图1),获得绿色发光的激基复合物,外量子效率达5.4%,量子产率达26%;此后大量研究人员开始着手于获得量子产率更高的激基复合物发光组合[7-10]。众所周知,发光材料的量子产率与发光单元的共轭结构联系紧密,因此如能采取简便的策略在已有的激基复合物组合的基础上,对其进行简易修饰从而获得新的Exciplex无疑更加便捷。基于此,本论文选择三苯基三嗪(2,4-二苯基-6-(3-乙烯基苯基)-1,3,5-三嗪(TRZ)),以乙烯基对其修饰,拓展共轭程度,与苯基噻嗪(10-苯基-10H-吩噻嗪(P-TZ))、3,6-二叔丁基咔唑(B-CZ)组合形成激基复合物,通过探讨其多方面的发光性能,揭示乙烯基修饰对激基复合物性能的影响。

图1 世界上首次报道的激基复合物发光组合[6]
1 材料与方法
本文所用的实验原料、试剂与仪器如表1~2所示。
表1 实验材料与试剂

表2 实验仪器
1.1 化合物的制备
1.1.1 3,6-二叔丁基-9-苯基咔唑(B-CZ,D1)的制备
依次加入溴苯 (551 mg,3.512 mmol),3,6-二叔丁基咔唑 (1 000 mg,3.6 mmol),(tBu)3PH-BF4(140 mg,0.358 mmol),tBuONa(688 mg,71 684 mmol),Pd2(dba)3(229.7 mg,0.25 mmol),充氮除氧,注入25 mL甲苯,氮气氛围下室温搅拌0.5 h,然后升温至100℃反应8h至单体完全消耗,冷却至室温,加入大量水终止反应,静置、过滤收集有机层,用饱和食盐水洗涤,经无水硫酸镁干燥,浓缩产物经硅胶柱层析分离,石油醚为展开剂,浓缩干燥收得白色固体即为目标产物1 073 mg,产率为85.8%。
1.1.2 10-苯基-10H-吩噻嗪(P-TZ,D2)的制备
溴苯(230.79 mg,1.47 mmol),吩噻嗪(300 mg,1.5 mmol),三叔丁基膦氟化硼盐(43.5 mg,0.15 mmol),Pd2(dba)3(68.67 mg,0.075 mmol),叔丁醇钠(288 mg,3 mmol),加入双口烧瓶,充氮除氧,注入 10 mL甲苯,氮气氛围下室温搅拌0.5 h,然后升温至100℃反应6 h至单体完全消耗,冷却至室温,加入大量水终止反应,静置、过滤收集有机层,用饱和食盐水洗涤,经无水硫酸镁干燥,浓缩产物经硅胶柱层析分离,石油醚为展开剂,浓缩干燥收得淡黄色固体333.7 mg,产率为82.4%。
1.1.3 2,4-二苯基-6-(3-乙烯基苯基)-1,3,5-三嗪(M-TRZ,A)的制备
1-乙烯基-3-苯硼酸(526.59 mg,3.558 mmol),2-氯-4,6-二苯基 d-1,3,5-三嗪(1 000 mg,3.745 mmol),2-二环己基膦-2',6'-甲氧基二苯(S-Phos)(246.01 mg,0.599 mmol),K2CO3(1 033.71 mg,7.490 mmol),四丁基碘化铵(41.9 mg), Pd2(dba)3(68.59 mg,0.075 mmol),加入双口烧瓶,充氮除氧,注入 15 mL 甲苯、5 mL去离子水,氮气氛围下室温搅拌0.5 h,然后升温至100℃反应8 h至单体完全消耗,冷却至室温,加入大量水终止反应,静置、过滤收集得固体再以纯的石油醚(PE)∶乙酸乙酯(EA)=100∶6为展开剂进行过柱纯化,再将所得产物浓缩、以二氯甲烷和甲醇混合溶液重结晶、干燥后收得白色粉末508.3 mg,产率为42.6%。

图2 化合物制备路线图
1.2 紫外-可见光谱法(UV-vis)
选择不同溶剂将化合物配置成 0.1 μmol/L浓度溶液,以石英比色皿为容器在厦门精艺兴业科技有限公司生产的UV-2550型紫外分光光度计进行测试。
1.3 荧光发射光谱法(PL)
1.3.1 溶液荧光光谱
分别配置浓度为0.1 μ mol/L的二氯甲烷(DCM)、乙酸乙酯(EA)、甲苯(TOL)溶液,运用天津港东科技股份有限公司生产的F-320A荧光分光光度计,变化不同激发波长测试其荧光发射光谱。
1.3.2 固体荧光光谱测试
将化合物按照不同的比例进行充分混合后转移至固体样品槽中测试其荧光光谱。
2 实验结果与分析
2.1 化合物的紫外-可见光谱(UV-vis)分析
图3(a)为化合物D1在不同溶剂中的紫外-可见吸收光谱,由图可见,化合物D1一共有两处吸收峰,298 nm处有一强吸收峰,对应于异丁基吸收,在350 nm附近还有两个相对强度较弱的吸收肩峰,分别对应苯基π-π*电子跃迁,咔唑基团的n-π*电子跃迁所致的吸收。由图可知,化合物在TOL、DCM和EA溶剂中具有基本一致的吸收峰,说明其在基态具有类似稳定的吸收行为。其吸收边位于360 nm处,对应D1带隙为3.44 eV。
图3(b)为化合物D2在不同溶剂中的紫外-吸收光谱,由图可见,化合物D2在DCM和EA中分别于258和256 nm处产生较强和相对较弱的吸收峰,对应于苯基π-π*电子跃迁。而在TOL溶剂中,仅观察321 nm处,波长范围250~350 nm之间出现一个吸收峰,对应于吩噻嗪基团的n-π*电子跃迁所致的吸收。由图3(b)可知,在TOL、DCM和EA溶剂中基本表现出一致性的基态行为。随着溶剂极性由小到大,化合物D2的吸收边分别为376、374、374 nm,在TOL、DCM和EA中的带隙分别为3.29、3.32、3.32 eV,随着溶剂极性增大,其带隙亦逐渐增大。
图3(c)为化合物A在不同溶剂中的紫外-吸收光谱,由图可见,化合物A在波长范围250~300 nm之间出现一个吸收峰,对应于乙烯基的π-π*电子跃迁。由图3(c)可知,在TOL、DCM和EA溶剂中,基本表现出一致性的基态行为。随着溶剂极性由小到大,化合物A的吸收边分别为340、340、343 nm,在 TOL、DCM 和 EA中的带隙分别为 3.65、3.65、3.62 eV,随着溶剂极性增大,其带隙基本保持不变。


图3 化合物溶液的紫外-可见吸收光谱图
三个化合物的共轭程度有限,其紫外吸收主要集中在400 nm以下的深紫外短波区域。其中,苯基咔唑和苯基吩噻嗪由于杂原子氮和硫的存在,产生较强的电子离域能力,拓宽了化合物的紫外吸收边,具有更小的带隙。
2.2 化合物荧光光谱分析(PL)
2.2.1 化合物的荧光发光性能
图4(a)为化合物D1在受到300 nm紫外光激发时于TOL、DCM和EA中的荧光发射光谱。不同溶剂中,化合物具有类似的发光行为,在350~400 nm范围内有一蓝色发光光谱,其最大发射峰分别位于352、354、351 nm,并均伴有肩峰位置分别为367、368、365 nm,半峰宽为50 nm。化合物在溶液状态下具有稳定的发光行为,测试范围内,其发光性能受溶剂和激发光谱的影响较小。
图4(b)为系列化合物D2在TOL、DCM和EA溶剂中的荧光发射光谱。由图可见,在受到360 nm紫外光激发时,D2在不同溶剂中均产生天蓝色荧光,对应发射峰分别为441、444、440 nm;半峰宽为90 nm。化合物在溶液状态下具有稳定的发光行为。相比于D1分子,两者具有类似的结构,将D1中的N原子改为S原子,结构由咔唑单元变为吩噻嗪,由于酚噻嗪具有更强的给电子特性,使分子中电子的离域程度增加,化合物的荧光发射峰产生了近100 nm的红移,并且半峰宽增大。结合化合物的紫外数据分析,说明S原子的引入可拓宽化合物的共轭程度,故使其紫外吸收边和荧光发射峰均产生不同程度的红移,但是也观察到D2的荧光发射光谱具有更宽的半峰宽,说明其具有更加弥散且复杂的激发态行为。
图4(c)为化合物A受到265 nm紫外光激发时的荧光发射光谱。区别于以上两种化合物,化合物A在DCM、EA和TOL溶剂中具有不同的发光光谱,其中,在EA和DCM两个极性溶剂中,于短波292和302 nm位置产生一强发射峰,同时在长波352和350 nm处还可观察到一发射尖峰;而在TOL溶液中仅仅观察到于短波302 nm位置的单峰发射。

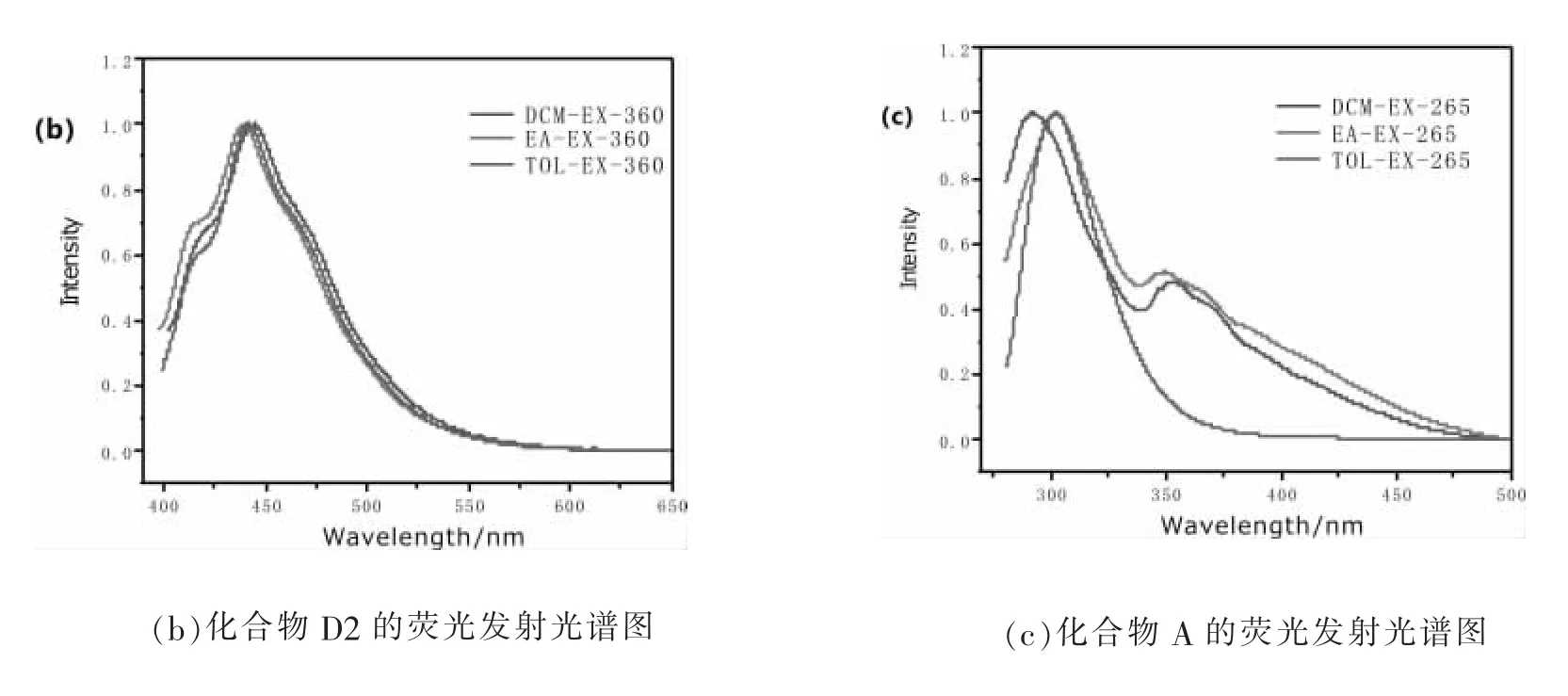
图4 化合物溶液的荧光发射光谱图
在化合物A中,外围的苯环单元与内在的三嗪单元存在分子内的电荷转移,在极性溶剂中,电荷转移效应更加明显,因此在DCM和EA溶液中观察到的长波发射应是源于A分子内电荷转移所对应的荧光发射。相比于前两个电子给体型化合物D1、D2,A的荧光发射峰位置更蓝移,这与其具有更短的紫外吸收边和吸收峰相互匹配。
图5(a)为化合物D1固体采取330 nm激发时的荧光发射光谱图,其发光光谱对应的最大发射峰为368 nm,比溶液状态下的351 nm的发射峰产生了17 nm的红移,主要源于聚集态时化合物π-π*相互作用所致的吸收,其对应色坐标为(0.158 6,0.051 7)(见图5(d))。化合物D2固体采取300 nm激发时其发光光谱对应的最大发射峰为440 nm(见图5(b)),与溶液中的发光类似,说明化合物D2在固态时分子间的相互作用较小或是相互作用对其发光行为影响较小,其色坐标如图5(e)所示为(0,1399,0.1178)。化合物A固体采取280 nm激发时,对应的发射光谱如图5(c)所示,与溶液发光光谱具有较大差别,其对应的发光光谱于340~400 nm范围产生一宽峰,且该发射峰的位置比之溶液状态产生明显红移,这是因为化合物A具有类平面结构,聚集态时易产生分子间相互作用,从而使其溶液和固体状态的荧光发光产生较大变化。其固体荧光色坐标如图5(f)所示为(0.1451,0.0464)。

图5 图5化合物固体的荧光发射光谱图
2.2.2 激基复合物的荧光发光性能
为探讨不同化合物组合形成的激基复合物的荧光发光性能,依据D1和D2给电子性质和化合物A的缺电子性质,将D-A进行相互组合,研究其发光性能。
将化合物D1与A按照物质的量比1∶1进行混合之后,在365 nm紫外灯的照射下可见蓝色发光,其荧光发射光谱如图6(a)所示,在受到360 nm紫外光激发时,其发光峰位置位于392 nm与430 nm位置,对应色坐标为(0.175 4,0.119 2);对比二者单独的发光光谱,发现该混合体系的发射峰发生了明显红移,说明D1与A组合形成激基复合物,且D1-A组合的发光峰波长随着激发波长的红移逐渐红移,表现出类似簇发光化合物的性质。
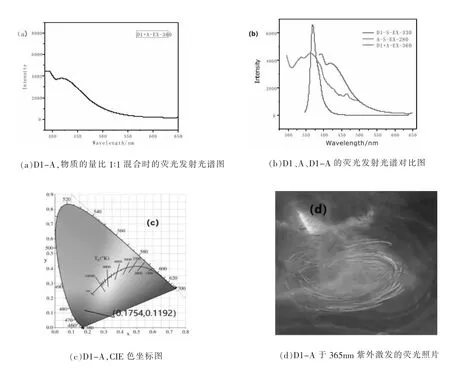
图6 D1-A的荧光发射光谱图
为了深入研究激基复合物的发光性质,进一步选择苯基吩噻嗪(D2)与化合物A进行组合,并通过改变二者的摩尔比例深入研究激基复合物的发光性能。
当按照物质的量比1∶1进行混合时,D2-A组合在365nm紫外灯的照射下发射出可见的明亮黄白光,其荧光发射光谱如图7(a)所示;该复合物于440和540 nm有两处发光峰,两者的发光强度均衡,且于465 nm处伴有并肩峰,其对应色坐标为(0.289 3,0.349 2),处于白光区域。通过对比发现,该混合体系的短波发射峰位置和峰形与D2固体的荧光发射光谱类似,推测其源于化合物D2的发光。而其长波位置的发光可能是源于D2与A形成的激基复合物的发光峰。为了验证以上设想,测试了D2∶A=1∶2(物质的量比)混合物的发光光谱,如图7(b)所示,图中在425 nm附近的发光峰强度明显减弱,主要观察到550 nm处的荧光发射,验证了该处黄光发射源于D2-A激基复合物的发光。值得一提的是,D2-A(物质的量比1∶1)仅仅采取二元比例即获得了覆盖全光谱的白光发射,该白光光谱中,短波发光主要源于D2分子的荧光发射,而长波部分主要源于D2-A组合形成的激基复合物所对应的延迟荧光发光。由于后者具有100%内量子效率,该白光组合具有比以往传统二元荧光材料组合形成的白光更高的理论内量子效率,应用于电致发光具有较好的应用前景。同时,一般激基复合物的形成仅由于给电子单元和拉电子单元按物质的量比1∶1的形式互配即可,本研究结果显示,在D2-A体系中,其激基复合物的形成并非严格按照物质的量比1∶1组合。

图7 D2+A的荧光发射光谱图
2.3 综合分析
由D1的荧光发射光谱(图4(a))可见固体D1的发光峰为350 nm,经光谱转换模拟得到CIE色坐标为(0.158 6,0.051 7),位于深蓝光发光区域。由D2的荧光发射光谱(图4(b))可见固体D2的发光峰为450 nm、落在蓝光范围中,可以得到CIE色坐标为(0.139 9,0.117 8)的蓝色的光。由A的荧光发射光谱(图4(c)可知)可见A的发光峰为350 nm、位于蓝光范围之间,可以得到CIE色坐标为(0.145 1,0.046 4)蓝色的光。由D1+A的荧光发射光谱(图6(a))可知该复合物有425 nm发光峰,峰在蓝光范围之间,可以得到CIE色坐标为(0.175 4,0.119 2)的蓝色发光。从D2+A的荧光发射光谱(图7(a))可见有440与550 nm的发光峰,分别落在蓝光范围与绿光范围之间,可以得到CIE色坐标为(0.289 3,0.349 2)的白色发光。各种化合物的CIE坐标汇总列于表1。

表1 化合物的CIE坐标汇总表
对比D1和D2与A组合,虽然两个组合均可形成激基复合物,且复合物的发光峰比之两个化合物均有所红移。由于D2单元具有更强的给电子特性和更高三线态能级,其与A组合所得的激基复合物发光更明显,应具有更高的量子发光效率,其发射峰比之D2和A单元红移了近100 nm,且激基复合物的发光峰与D2单元发光峰的组合于可见光区域互补,当复合物中存在过量D2单元时,可实现可见光区域良好的覆盖获得了近白光,通过进一步调整二者的比例有望获得纯度更佳的白光。无疑为二元体系白光的组合提供了有益的借鉴。
3 结论
本研究基于激基复合物发光机理,在综合分析了3,6-二叔丁基-9-苯基-咔唑(D1)和10-苯基-10H-吩噻嗪(D2)作为电子给体单元,2,4-二苯基-6-(3-乙烯基苯基)-1,3,5-三嗪(A)作为电子受体单元在基态的吸收发射性能基础之上,将D、A单元进行混合,获得了蓝光、黄光和白光发射的激基复合物组合。吩噻嗪由于具有较大的共轭程度与A匹配可形成黄光发射,通过改变D2与A的混合比例,可获得具有较高理论内量子效率的白光发射。相关研究结果有望拓展应用于制作电致发光器件获得高效的电致白光发射。
