新冠疫情下药物临床试验受试者管理优化
2022-01-04陈中建台宗光朱全刚
崔 贞,陈中建,2,台宗光,2,朱全刚,2*
(1.上海市皮肤病医院Ⅰ期临床研究中心,上海 200443;2.上海中药外用制剂创新工程技术研究中心,上海 200443)
新冠肺炎疫情防控期间,药物临床试验各环节均受到不同程度的影响,其中受试者筛选与入组环节受影响最大。由于疫情防控的影响,一些受试者无法到现场完成筛查、访视和安全性评估。项目中出现一定程度的入组减慢、给药中断、给药超窗、无法追踪不良事件(AE)、数据缺失等,一方面无法保证试验项目进度,另一方面无法保证受试者的安全[1]。为此在临床试验中,通过公众号先后推出两版疫情下的药物临床研究工作指引,利用问卷星、金数据、电话随访、视频通信等线上平台开展线上远程随访、初步筛选和AE追踪工作。同时,研究者积极协调伦理审查允许受试者就近访视。
1 对象与方法
1.1 研究对象回顾性选取2020年1月至2020年10月本院新冠疫情下药物临床试验受试者100例,依据受试者疫情期间管理策略,随机分为信息化管理组(n=50)、常规化管理组(n=50)两组。每组根据受试者参加临床试验的特点和访视内容,分成8个类别。采集受试者的性别、年龄和体重等基本信息。
1.2 纳入和排除标准纳入标准:①符合所参与项目的纳入标准,具有完整的研究病历资料;②经过研究者初步评估,认为具有良好的依从性。
排除标准:①合并精神疾病等影响受试者依从性的严重疾病;②合并免疫系统疾病、内分泌系统疾病、心血管系统疾病、恶性肿瘤等影响受试者安全性的严重疾病。
1.3 研究方法常规化管理组受试者接受临床试验中的常规化管理;信息化管理组受试者在常规管理的基础上加入信息化管理措施,具体操作如下。
① 驭时公众号推送疫情期间临床试验的管理信息。驭时公众号受众多业界内人士关注,具有权威性高、普及面广的优势。本中心先后在驭时公众号发布两版疫情期间的临床试验工作指引,向临床试验项目的申办方、CRO、SMO公司发出警示。
② 问卷星和金数据平台助力改变筛选模式——集中变分散。设计受试者健康问卷及承诺书,获取报名的受试者的基本信息,以及近期的旅居史,目前所在地,来院交通工具等信息,对不符合来院体检的受试者予以劝退,对来院筛选者将原来的一次筛选变为分批分散筛选,在招募广告中告知筛选批次及日期,控制每批次招募人数及筛选人数。筛选前按照报名顺序为受试者匹配精准筛选时间段并告知,各筛选岗位做好流程设计及时间把控,避免同一时间段人员聚集。
③ 电话、视频通信、跨中心多形式访视。通过线上及当地就医等方式促进随访频率的提升,及时跟进受试者的用药安全及疗效。指导受试者有效应对与处理临床试验中的突发情况,并根据情况及时调整治疗方案。通过缓解受试者的焦虑情绪,减少受试者的脱落。
以上信息化管理措施一方面有效保证受试者的安全,另一方面为临床试验的持续进行创造有利条件。
1.4 观察指标①药物临床试验访视分类。根据受试者访视的内容和皮肤科试验药物的特点将访视类型分为八类。类别一:访视只需获得非注射试验药物;类别二:访视只需安全性检查;类别三:访视需要获得非注射试验药物,并进行安全性检查;类别四:访视需要获得非注射试验药物,进行安全性检查,判别疗效;类别五:访视需要获得注射给药,进行安全检查;类别六:访视需要密集采血、给药;类别七:关键访视,统计学上不可缺失;类别八:原定电话访视,无需返院。前期的筛查过程+受试者访视管理的紧急应对模式:访视类别一至三,就近就医;类别四至七:返院就医(特殊情况无法返院,允许就近就医);类别八:无需返院就医[2]。
② 受试者访视完成率。访视完成率= (访视完成例数/总例数) × 100%。
③ 受试者依从性。依照慢性疾病用药依从性测评表编制量表,评价两组受试者的依从性;该量表设20个条目,每条目按完全依从、基本依从、偶尔依从、基本不依从、不依从分别赋值5分,4分,3分,2分,1分。
依从率= (完全依从+基本依从)例数/总例数×100%;
该量表克朗巴哈系数Cronbach’s α信度值为0.782,具有较高的可信度。
④ 受试者满意度。采用问卷调查方式,问卷由20个问题组成,包括病房环境、医护人员服务态度、护理技能、护士问题处理能力等4个维度;总分0~100分,分为不满意(0~59分)、一般(60~79分)、基本满意(80~89分)、非常满意(90~100分)四项。
满意度= (非常满意+基本满意)例数/总例数×100%
经克朗巴哈系数Cronbach’s α检验,量表系数为0.753,具有较高的信度。
1.5 统计学分析采用Excel汇总数据,采用SPSS 21.0进行统计分析。计数资料或率以n或%表示,各项资料采用频率、均值进行描述分析;连续变量之间的两两比较采用t检验;率的比较采用χ2检验; 检验水准α=0.05。
2 结 果
2.1 受试者的一般资料从表1的资料数据可以看出,信息化和常规化管理组受试者之间的一般资料比较差异均不显著(P>0.05)。其中男女比例接近1∶1,年龄均值40岁左右,60岁以上人群分别占40%和36%,两组受试者分类中最多的为类别五,占总数的50%左右。
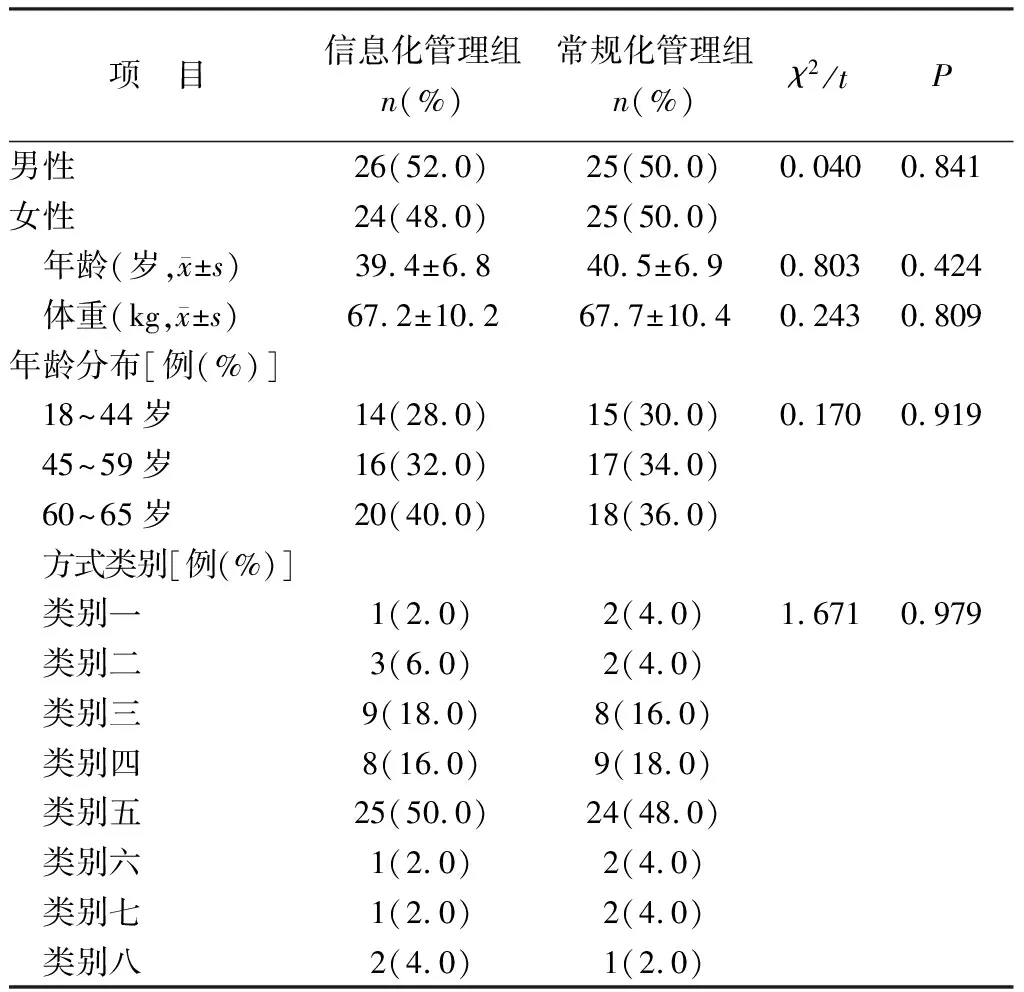
表1 两组受试者的一般资料比较
2.2 两组受试者的访视完成率比较信息化管理组受试者的访视完成率90.0%(45/50)显著高于常规化管理组72.0%(36/50)(P<0.05)(表2)。值得指出的是,在比较关键的四至七类访视中,信息化管理组35例受试者中仅有1例未完成,访视完成率为97.1%,与常规化管理组相比优势明显(表2)。
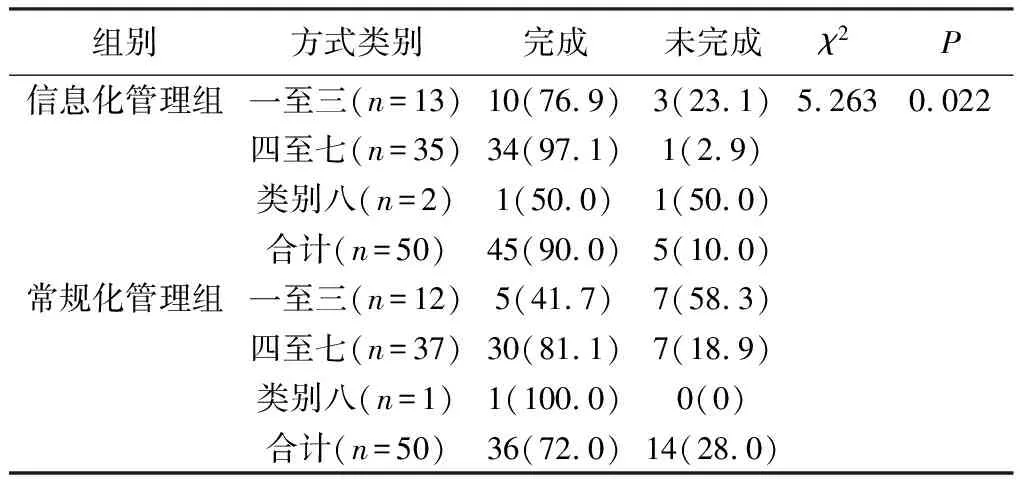
表2 两组受试者的访视完成率比较[n(%)]
2.3 受试者依从性信息化管理组受试者依从性90.00%(45/50)高于常规化管理组64.00%(32/50)(P<0.01)(表3)。通过信息化管理手段,指导受试者有效应对和处理临床试验中的突发情况,及时缓解受试者的焦虑情绪,提高受试者的依从性。

表3 两组受试者依从性[n(%)]
2.4 两组受试者满意度比较信息化管理组受试者满意度94.0%(47/50)显著高于常规化管理组74.0%(37/50)(P<0.01),具体数据见表4。

表4 两组受试者满意度比较[n(%)]
3 讨 论
药物临床试验机构是保护药物临床试验受试者权益的主体[3],机构及研究者在试验过程中应该及时发现安全隐患及风险,充分重视受试者的健康、安全和权益,一方面尽量避免受试者受到伤害,另一方面使受试者最大限度获益[4]。受试者访视贯穿整个试验过程,是临床试验的重要环节。因此,新冠疫情期间进一步强化受试者访视的管理,可以有效地控制受试者的感染风险,提升试验依从性,减少失访现象,避免临床试验数据缺失,保证药物临床试验顺利实施[5]。
在新冠疫情期间的临床试验中,让受试者依据自身情况选取就医方式,之后依据访视类别,通过分类管理有助于受试者完成访视[6]。临床试验中有机结合实际情况和紧急流程指引,依据研究方案科学制定受试者访视的信息化管理策略,可以最大限度地保障受试者权益,并有效保证临床试验的延续性[7]。
本项研究结果表明,信息化管理组在受试者依从性和满意度方面均显著高于常规化管理组。虽然访视完成率检验中两组差值比预期小,样本数量设计偏少,可能对结果产生一定程度的偏差;但是仍可以看出,在访视分类管理过程中,减少受试者的外出,研究者紧密联系受试者,利用信息化手段及时开展远程指导,可使访视的完成率在一定程度上得到保证[8]。现阶段,我国仍处于新冠疫情常态化防控时期,药物临床试验机构应该积极调整管理策略,协助临床试验受试者响应政府号召,减少不必要的外出暴露,从而降低疫情传播风险。科学合理的访视管理一方面能够有效保证临床数据的可溯源性与完整性,另一方面还能够充分保障受试者的健康权益[9]。
综上所述,新冠疫情下药物临床试验受试者信息化管理较常规化管理效果好,值得推广。
