牛痘疫苗接种家兔炎症皮肤提取物治疗糖尿病周围神经病变的Meta分析
2022-01-04张瑶胡占嵩屠莹刘昱邱水晶朱梦晨陈丽娟
张瑶,胡占嵩,屠莹,刘昱,邱水晶,朱梦晨,陈丽娟
2型糖尿病合并周围神经病变通常由血糖持续偏高造成代谢紊乱所导致,进而引起局部循环异常并进一步发展为神经性损害,引起感觉神经和运动功能障碍[1-3]。牛痘疫苗接种家兔炎症皮肤提取物(神经妥乐平)作为一种从兔皮免疫炎症组织中获得的混合物,具有调节免疫功能、神经修复、镇静、镇痛、抗炎等作用[4-5],上市药品分为注射液和片剂两种剂型。多项临床试验证实,作为非蛋白性生理活性物质的神经妥乐平,在神经系统疾病的治疗方面具有一定优势[6-8]。近年来该药已被广泛用于DPN的治疗,但各研究纳入的病例数量较少,所得结论参考价值有限,系统评价也鲜有报道。本研究通过运用Meta分析的方法,评价了神经妥乐平在临床治疗DPN的疗效以及安全性,为该药在临床上安全合理应用提供有效的循证学参考和依据。
1 资料与方法
1.1 检索策略检索循证图书馆、PubMed文献数据库、EMBASE、万方电子数据库、CBM数据库、CNKI,检索时限从各数据库建库起至2019年12月。中文检索词包括“牛痘疫苗接种家兔炎症皮肤提取物”、“神经妥乐平”“糖尿病周围神经病变”“糖尿病”“周围神经病变”;英文检索词包括“neurotropin”“diabetes mellitus”“peripheral neuropathy”“diabetic neuropathy”“diabetic peripheral neuropathy”“DPN”。
1.2 纳入标准(1)研究类型:国内以及国外数据库可检索出公开发表的RCT试验研究,语种限定为中文或英文。(2)研究人群:明确诊断患有2型糖尿病同时合并周围神经病变的病人。依照世界卫生组织(WHO)制定的2型糖尿病诊断标准执行[9],同时病人须明确诊断为合并有周围神经病变,病人的性别、年龄、来源、数量、病情程度不限。(3)干预方法:在临床常规性降糖给药方案的基础上,试验组为在DPN治疗中应用神经妥乐平的病人。对照组病人则采用其他常规药物治疗或其他对症处理措施。(4)结局指标:主要结局指标为临床治疗总有效率。疗效的判定标准由参考相关文献而制定[10],具体标准为:(1)显效:是指病人症状基本得到控制,神经传导的速度增加大于等于5米∕秒,膝、腱反射基本恢复;(2)有效:是指病人症状改善程度较为显著,神经传导的速度增加小于5米∕秒,膝、腱反射可见有一定程度改善但未见完全恢复;(3)无效:是指病人症状未见改善,神经传导速度数值无变化,膝、腱反射未见好转;总有效率的计算公式:显效病人数+有效病人数∕总病例数×100%。次要结局指标包括正中神经运动神经传导速度(单位:m∕s)、胫神经运动神经传导速度(单位:m∕s)和药品不良反应发生率。
1.3 排除标准(1)非中、英文原文的研究;(2)综述;(3)重复论文;(4)非RCT研究;(5)病例报告;(6)回顾性研究;(7)体外实验;(8)动物试验;(9)数据不完整且通过联系作者无法获得的研究。
1.4 文献资料提取与质量评估两位研究人员以相互独立的方式来筛选文献和提取资料,同时进行各研究的质量评估工作。若遇分歧意见时,可由第三名研究人员协助判定。提取资料主要包括作者、年份、研究类型、研究对象特征(年龄、纳入例数、剂量、疗程等)、干预方法、结局指标、安全性指标等。两位研究人员以相互独立的方式依照Cochrane手册(版本5.1)的评估工具评价各文献的偏倚风险。
1.5 统计学方法操作软件RevMan 5.3进行数据处理,根据I2的数值大小来评估异质性,选择所采用的分析模型,当P≥0.1,I2≤50%时,资料异质性较小,用固定效应模型进行分析;若研究间具有异质性(P<0.1,I2>50%),各研究存在异质性,进一步分析其来源,排除明显异质性的影响后,采用随机效应模型进行分析。计量和计数资料分别以均方差(MD)及比值比(OR)作统计量并用95%CI表示,P<0.05代表差异有统计学意义。采用Stata软件(版本15.0)对本研究进行Egger’s及Begg’s检验以评估发表偏倚性。
2 结果
2.1 文献检索结果依照既定的检索方式进行检索,一共检索出219篇文献,剔除133篇重复文章;剔除17篇综述以及非临床研究。严格按照标准筛选后剔除非RCT研究15篇,研究对象和干预方法不符26篇,剔除结局指标不符13篇,剔除数据不完整文献6篇,最终纳入9个研究,合计934例病人。文献筛选步骤如图1所示,研究基本信息特征见表1。

表1 神经妥乐平治疗2型糖尿病合并周围神经病变纳入研究的主要特征

图1 神经妥乐平治疗2型糖尿病合并周围神经病变934例的文献筛选流程
2.2 纳入研究质量评价结果由两名研究人员以相互独立的方式依照Cochrane手册(版本5.1)的评估工具评价各文献的偏倚风险(包括选择偏倚、实施偏倚、测量偏倚、失访偏倚、报告偏倚等),同时利用RevMan的偏倚风险表进行评估,红色:高风险,黄色:不明风险,绿色:低风险。文献经评价后发现,5篇文献显示中等偏倚风险[12-14,16-17],4篇文献显示中低偏倚的风险[11,15,18-19],质量评价结果见图2,3。

图2 神经妥乐平治疗2型糖尿病合并周围神经病变文献的偏倚风险条形图
2.3 Meta分析结果
2.3.1DPN治疗总有效率7项研究[11,13-17,19]报道了神经妥乐平组和对照组对DPN治疗的总有效率,各研究并未出现显著的异质性(P=0.78,I2=0%),选用固定效应模型,将对照组和试验组病人的药物作用效果进行比较,试验组总有效率数值提高有统计学差异[OR=3.91,95%CI:2.64~5.78,P<0.001],见图4。

图4 神经妥乐平治疗2型糖尿病合并周围神经病变934例治疗总有效率的森林图
2.3.2正中神经运动神经传导速度5项研究[12-16]比较了神经妥乐平组和对照组对正中神经运动神经传导速度的影响,各研究出现一定异质性(P<0.001,I2=86%),分析模型选择随机效应模型。数据表明较对照组而言,试验组病人的正中神经传输速度呈现有统计学意义的提高[MD=4.07 m∕s,95%CI:2.12~6.03,P<0.001],见图5。

图5 神经妥乐平治疗2型糖尿病合并周围神经病变934例正中神经运动神经传导速度的森林图
2.3.3胫神经运动神经传导速度4项研究[13-14,18-19]比较了神经妥乐平组和对照组对胫神经运动神经传导速度的影响,各研究并未出现显著的异质性(P=0.26,I2=25%),分析模型选择固定效应模型后发现,相较于对照组,试验组病人传导速度的提高程度 具 有统 计 学差 异[MD=2.93 m∕s,95%CI:2.08~3.79,P<0.001],见图6。
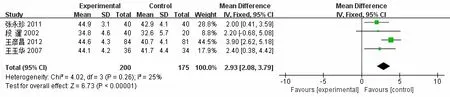
图6 神经妥乐平治疗2型糖尿病合并周围神经病变934例胫神经运动神经传导速度Meta分析森林图
2.3.4安全性共3项研究[15,18-19]对比了试验组和对照组的药品不良反应(ADR)发生率,各研究并未出现显著的异质性(P=0.68,I2=0%),分析模型选择固定效应模型,对结果分析后发现较对照组而言,使用神经妥乐平后试验组病人的不良反应发生率虽不存在统计学意义的差异[OR=3.39,95%CI:1.00~11.50,P=0.05],但数值上却有所增加。见图7。

图3 神经妥乐平治疗2型糖尿病合并周围神经病变文献偏倚风险总图
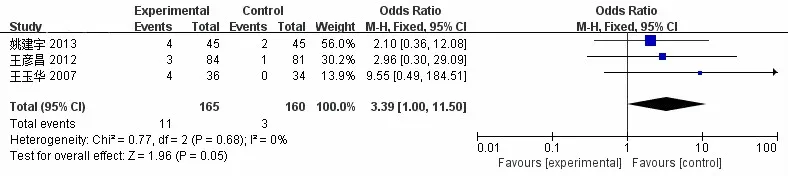
图7 神经妥乐平治疗2型糖尿病合并周围神经病变934例不良反应发生率Meta分析森林图
2.4 发表偏倚分析与敏感性分析将4个结局指标:治疗总有效率、正中神经运动神经传导速度、胫神经运动神经传导速度、药品不良反应发生率采用Egger’s及Begg’s检验进行发表偏倚分析,各结局指标均不存在发表偏倚(P>0.05),敏感性分析采用逐个剔除文献的方法进行,前后的结局指标经比较发现并无差异,提示结果较为准确、可靠和稳定。见表2,3。
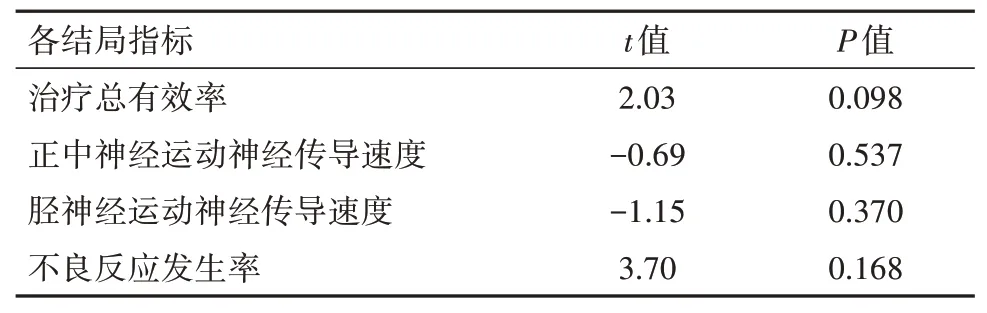
表2 神经妥乐平治疗2型糖尿病合并周围神经病变934例各结局指标的Egger’s检验

表3 神经妥乐平治疗2型糖尿病合并周围神经病变934例各结局指标的Begg’s检验
3 讨论
目前文献报道DPN的患病率大约在10%~90%,该疾病病人多出现周围神经功能减退相关症状,其发病率的数值变化取决于定义神经病变的标准和方法[20-22]。研究显示DPN的发病机制较为复杂,可能与多种因素有关,如神经缺氧缺血、免疫相关因素、神经营养因子缺乏、氧化应激等等[23-24]。由于DPN的发病机制尚不明确,尚无特异性的治疗方法,针对该病的治疗药物也以抗氧化应激类药物如硫辛酸,神经修复类药物如甲钴胺,以及其他改善微循环、镇痛等对症治疗药物为主[25]。尽管DPN的标准治疗方案目前尚未统一,但对糖尿病病人尽早开展诊断和治疗十分关键。神经妥乐平是一种具有神经亲和性的物质,其主要作用是影响神经-免疫-内分泌系统的功能,近年来已在骨科、神经内科、内分泌科等各种神经炎症相关疾病的治疗中被广泛应用。研究表明该药既能激活疼痛的下行抑制系统从而起到止痛效果;又可抑制下丘脑的神经发射活动,保护神经元,恢复突触传递功能[26],可以有效预防和延缓DPN的发生。
本研究系统评价了神经妥乐平治疗DPN的疗效与安全性,最终纳入9篇文献,共934例病人。Meta分析结果显示,在对糖尿病周围神经病变的治疗方面,神经妥乐平组病人较对照组病人给药后的治疗总有效率大幅提高,症状明显缓解且与对照组的差异有统计学意义,提示神经妥乐平在DPN治疗中具有显著优势。肌电图测定正中神经和胫神经运动神经传导速度能较好地反映DPN的临床治疗效果,故本研究选取两者作为次要指标进行分析[27]。结果显示较对照组而言,对于缓解神经传导障碍方面,使用神经妥乐平治疗的病人,其正中神经及胫神经运动神经传导速度的提高幅度呈现有统计学意义的增加。由此可见神经妥乐平对比其他神经病变治疗药物,可以显著改善DPN导致的肢体感觉和运动神经系统症状,具有一定的神经修复作用。纳入文献中所提及的神经妥乐平相关药品不良反应均为头晕、皮疹、面色潮红、胃部不适等轻微不良反应,并无严重ADR发生。神经妥乐平的不良反应发生率虽不存在统计学差异,但数值上却稍有增加。由此可见,该药在疗效指标上虽具有一定优势,但发生药物不良反应的风险也不容忽视,使用中需加以注意。
本研究尚存在的局限性:纳入文献中有多个文献未交代具体随机与分组的方法,有可能发生一定选择性偏倚;研究均未提及分配隐藏内容、部分研究未采用盲法,在实施性方面可能存在一定偏倚;纳入研究对失访没有明确记载,不排除存在失访偏倚可能。本次研究纳入的文献数量以及所涉及病例数均较少,部分文章质量水平有限,故还需要更多大样本、高质量的RCT研究来进一步评价神经妥乐平的有效性和安全性。
综上所述,神经妥乐平具备治疗DPN的药理学基础,对相关文献进行Meta分析,结果显示神经妥乐平对DPN的治疗疗效显著,具有一定的临床应用前景,同时对于其发生不良反应的风险在临床使用中仍需予以重视。
