胰腺实性假乳头状瘤与无功能性神经内分泌肿瘤磁共振成像预测模型的建立
2021-12-27刘芳朱蒙蒙王铁功曹凯孟英豪边云王莉陆建平邵成伟
刘芳 朱蒙蒙 王铁功 曹凯 孟英豪 边云 王莉 陆建平 邵成伟
海军军医大学第一附属医院放射诊断科,上海 200433
胰腺实性假乳头状瘤(solid pseudopapillary tumors of pancreas, SPTs)是一种少见的低度恶性肿瘤,占胰腺原发肿瘤的1%~2%,近年来随着影像检查手段的进步及普及,其发病率有所增加[1-2]。SPTs可通过剜除等局部治疗手段治愈[3],预后良好。胰腺神经内分泌肿瘤(pancreatic neuroendocrine tumors, PNETs)占胰腺肿瘤的2%~10%,预后较SPTs差,且大多数为无功能性肿瘤,根治性切除术是治愈PNETs的唯一潜在的方法[4],同时根据肿瘤的组织学分级,术后需要对部分患者进行靶向治疗、化疗或放疗等[5-7]。由于两者的治疗方法及预后不同,因此术前精确诊断具有重要的临床价值。MRI由于其高分辨率及无辐射等优点,已成为胰腺疾病诊断的主要检查手段[8-9],但是SPTs与PNETs的部分MRI表现重叠,鉴别存在困难。本研究旨在建立鉴别SPTs和PNETs的预测模型,以期提高术前诊断准确率及提供预后信息。
资料与方法
一、一般资料
连续性收集2013年1月至2020年12月间海军军医大学第一附属医院行胰腺肿瘤手术切除并经术后病理证实为SPTs的142例(SPTs组)及PNETs的137例(PNETs组)患者的临床及影像学资料。所有患者均在手术前1个月内行MRI增强扫描。排除标准:(1)术前行放疗、化疗者;(2)MRI资料不全;(3)图像质量差,难以诊断。该研究已通过医院伦理委员会批准。
依据国际预测模型建模共识[10],按照纳入的时间顺序,将2013年1月至2018年12月间106例SPTs和100例PNETs患者归入训练集,2019年1月至2020年12月间36例SPTs和37例PNETs患者归入验证集。
二、MRI扫描方法
患者检查前均禁食禁水4 h。MRI设备采用美国GE公司Signa HDxt 3.0 T、美国GE公司Discovery 750 3.0 T扫描仪和8通道体部线圈。扫描序列:(1)横断面呼吸触发脂肪抑制快速自旋回波T2WI序列。重复时间(repetition time, TR) 6 316 ms,回波时间(echo time, TE)85 ms,矩阵224×320,视野440 mm×440 mm,层数20,层厚5 mm,层间距1 mm。(2)肝脏快速容积成像(liver acquisition with volume acceleration,LAVA)T1WI序列。TR 2.58 ms,TE 1.18 ms,矩阵224×320,无层间距,层厚5 mm,视野440 mm×440 mm。增强扫描采用高压注射器以2.0 ml/s的流率经前臂静脉注入对比剂钆喷替酸葡甲胺(Gd-DTPA) 0.2 ml/kg,注射结束后用20 ml生理盐水以同样流率冲洗。分别于注射对比剂后15、20、40 s行动脉期、门静脉期、延迟期扫描。
三、图像分析
由两位经验丰富的放射诊断科医师独立阅片观察,记录一致的观察结果,意见不一致时经过协商达成共识。观察指标为肿瘤位置,病灶大小、形状、边界,有无囊变,T1WI信号、T2WI信号,强化方式、强化峰值期相、峰值期强化程度,胰胆管是否扩张、胰腺有无萎缩以及有无周围血管、器官侵犯。T1WI内有高信号代表肿瘤内出血;病灶内观察到T2WI水样高信号,增强后无明显强化判定为肿瘤囊变;胰管直径≥3 mm或胆总管直径≥10 mm定义为胰胆管扩张;病灶与血管、器官分界不清视为侵犯血管与器官。所有病灶经手术切除后送病理检查,由两名经验丰富的病理科医师单独盲法阅片,诊断意见不同时经过协商达成一致。
四、统计学处理
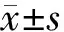
结 果
一、两组患者的临床及MRI影像特征
SPTs组与PNETs组患者的临床及MRI影像特征分析见表1。训练集SPTs组与PNETs组间年龄、性别、肿瘤大小、肿瘤形状、囊变、T1WI信号、T2WI信号、强化峰值期相、峰值期强化程度、强化方式、侵犯邻近器官差异均有统计学意义(P值均<0.05),其余特征差异均无统计学意义。验证集SPTs组与PNETs组年龄、肿瘤形状、囊变、T1WI信号、T2WI信号、强化峰值期相、峰值期强化程度、强化方式差异均有统计学意义(P值均<0.05),其余特征差异无统计学意义。

表1 142例胰腺实性假乳头状瘤患者与137例胰腺神经内分泌肿瘤患者临床及MRI影像特征比较
二、两组患者临床及MRI影像特征的单因素回归分析
单因素分析结果显示(表2),训练集SPTs组与PNETs组的年龄、性别、肿瘤大小、肿瘤形状、是否囊变、T1WI信号、强化峰值期相、峰值期强化程度、强化方式、侵犯邻近器官差异均有统计学意义(P值均<0.05)。验证集的年龄、形状、囊变、T1WI信号、峰值期相强化程度、强化方式差异有统计学意义(P值均<0.05)。

表2 142例胰腺实性假乳头状瘤患者与137例胰腺神经内分泌肿瘤患者临床及MRI影像特征的单因素回归分析
三、预测模型的建立及诊断效能
将上述训练集中单因素回归分析具有统计学意义的10个因素(年龄、性别、肿瘤大小、肿瘤形状、囊变、T1WI信号、强化峰值期相、峰值期强化程度、强化方式、侵犯邻近器官)进一步纳入多因素回归分析,结果显示,年龄、性别、肿瘤大小、T1WI信号、峰值期强化程度、强化峰值期相是6个预测SPTs与PNETs的独立因素(表3),即年龄越大、男性患者、肿瘤体积越小、T1WI不含高信号、强化峰值期相位于动脉期或静脉期、峰值期强化程度高于胰腺实质者更倾向于PNETs。利用这6个因素建立预测模型,预测PNETs概率的公式为:4.31+1.13×年龄+1.31×肿瘤大小-1.29×女性-4.18×T1WI呈高信号+1.28×强化高于胰腺实质-4.69×延迟期强化。

表3 142例胰腺实性假乳头状瘤患者与137例胰腺神经内分泌肿瘤患者临床及MRI影像特征的多因素回归分析
将预测模型可视化为列线图(图1)。列线图在训练集和验证集的AUC值分别为0.99(95%CI0.977~1.000)、0.97(95%CI0.926~1.000)(图2);在训练集的灵敏度、特异度、准确率分别为98.00%、94.34%、96.12%;在验证集的灵敏度、特异度、准确率分别为86.49%、97.22%、91.78%,提示预测模型对SPTs和PNETs的鉴别具有良好的诊断效能。

图1 胰腺实性假乳头状瘤与胰腺神经内分泌肿瘤诊断列线图
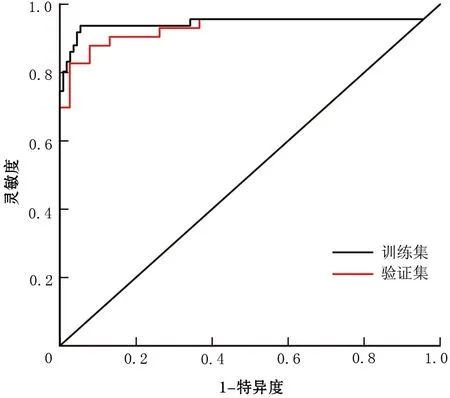
图2 列线图在训练集与验证集中的ROC曲线
四、预测模型的临床应用
为评估预测模型的实际临床应用效果,绘制预测SPTs和PNETs的临床决策曲线(图3),当列线图鉴别两类疾病的阈值>0.05时,列线图较“所有的患者视为PNETs治疗”方案或“所有患者视为SPTs治疗”方案获得更多的净收益,即给患者带来更多的临床获益。图4为临床实际应用中的2个病例,利用预测模型可以准确诊断SPTs和PNETs。

注:PNETs为胰腺神经内分泌肿瘤;SPTs为胰腺实性假乳头状瘤图3 鉴别胰腺实性假乳头状瘤和神经内分泌肿瘤的列线图决策曲线
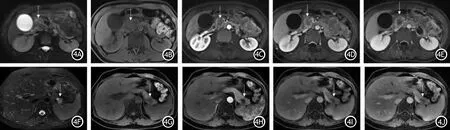
图4 胰腺神经内分泌肿瘤与胰腺实性假乳头状瘤患者的MRI表现。横断面脂肪抑制T2WI示胰头部一枚稍高信号影(↑),病灶长径约24.65 mm(4A),横断面脂肪抑制T1WI示肿块呈低信号(↑,4B),横断面增强示肿块呈轻度强化,强化峰值位于门静脉期,峰值强化程度低于正常胰腺实质(4C~4E),根据列线图诊断为神经内分泌肿瘤的概率约0.8;横断面脂肪抑制T2WI示胰尾部一结节状混杂高信号影(↑),病灶长径约24.80 mm(4F),横断面脂肪抑制T1WI示肿块呈低信号(↑,4G),横断面增强示肿块呈渐进性强化,强化峰值位于延迟期,峰值强化程度低于正常胰腺实质(4H~4J),根据列线图诊断为实性假乳头状瘤的概率>0.9
讨 论
SPTs与PNETs均为胰腺少见肿瘤,近年来随着影像检查技术的发展与普及,两者的发生率也逐渐增多,且常常为偶然发现,无明显临床症状,两者的影像表现具有一定的重叠[8]。以往研究表明,SPTs常见于年轻女性,病灶内常发生出血,增强后呈渐进性延迟轻度强化[11-14]。本研究结果与文献一致,训练集的SPTs患者平均年龄为33岁,其中高达83.02%(88/106)患者是女性,64.15%(68/108)患者病灶内可观察到T1WI高信号(出血),97.17%(103/106)患者病灶强化峰值位于胰腺延迟期,74.54%(89/106)患者病灶强化程度弱于正常胰腺实质。PNETs通常血供丰富,增强后常明显强化,强化峰值以动脉期或门静脉期为著[15-16],本研究结果与之相似,训练集80%(80/100)病灶明显强化,53%(53/100)强化峰值位于动脉期,31%(31/100)强化峰值位于静脉期。PNETs具有一定侵袭性,本研究11%(11/100)患者病灶侵犯邻近器官。SPTs因侵袭性低,完整的手术切除可达到根治性目的[17-18],而PNETs术后常需要进行辅助性放化疗或靶向治疗[19]。因此术前精确诊断对于临床治疗的选择及指导具有重要意义。
术前影像学评估方法较多,但各有利弊。超声内镜引导下细针穿刺术(endoscopic ultrasonography-guided fine-needle aspiration,EUS-FNA)虽然可获得病灶的组织学标本进行病理诊断,但是该检查有创、昂贵,可能产生一系列严重的并发症,且灵敏度并不高,因此在临床上的应用有限[20]。CT、MRI是胰腺病变术前诊断及无创评估的主要影像手段。然而,CT具有辐射,且对病灶内成分的判定价值有限,对于病灶出血、囊变的评估不够敏感。MRI由于其软组织分辨率高,多参数成像,且无辐射,对于出血、囊变等病变的检测较敏感,因此对于两者的评估更优。
虽然已有SPTs与PNETs影像鉴别的相关研究,但结果有一定的局限性,对于两者鉴别仍有一定困难。Wang等[21]利用CT图像特征鉴别SPTs与弱强化的PNETs,通过多因素分析发现,年轻患者、病灶内出现“浮云征”、钙化是SPTs的独立预测因素,3个因素联合诊断的AUC值为0.865。但该研究样本量小,没有对建立的模型进行验证。Liu等[22]通过分析147例PNETs和21例SPTs的超声内镜图像,发现PNETs回声均匀、呈富血供。然而,EUS检查有创,依赖于操作者的水平,并不作为两类疾病诊断的首选检查方式。Li等[23]利用MRI组学分析数据来鉴别SPTs与PNETs,但没有纳入常规的影像学特征,由于影像组学特征不稳定,且缺乏外部验证,使得该模型的临床应用有限。
本研究共收集142例SPTs、137例PNETs患者的临床及MRI数据,样本量高于以往的研究。利用患者常规临床及MRI的6个特征(年龄、性别、病灶大小、T1WI有无高信号、强化峰值期相、峰值期强化是否高于胰腺实质)建立的预测模型,表现出较好的预测能力,且诊断灵敏度、特异度、准确率均较高,并进一步利用决策曲线,满足临床决策的实际需要。
本研究具有以下局限性:(1)回顾性研究,可能存在选择偏倚;(2)诊断模型缺乏外部验证;(3)未纳入与疾病相关的实验室检查指标,如神经元特异性烯醇化、嗜铬素A、突触素等;(4)纳入的样本均是术后病理证实的病例,术前穿刺病理证实的并未纳入,导致病例数减少。未来,本课题组将开展前瞻性多中心的研究,扩大样本量,增加新的模型算法,使研究模型可以进一步推广。
利益冲突所有作者均声明不存在利益冲突
