恩诺沙星注射液细菌内毒素检查(凝胶法)方法学研究
2021-12-23康福忠,于小婷,王猛,杨雪,甄盼盼,程雪娇
康福忠,于小婷,王猛,杨雪,甄盼盼,程雪娇
摘要:参照《中华人民共和国兽药典》2015版一部附录1143细菌内毒素检查法的有关规定,对恩诺沙星注射液内毒素限度及检查方法进行了研究。结果显示,恩诺沙星注射液稀释到800倍及以上时,对细菌内毒素检查无干扰,内毒素限值确定为400EU/mL。对3批样品进行检查,结果均符合规定。本研究建立的细菌内毒素检查方法(凝胶法)可用于恩诺沙星注射液的细菌内毒素检查。
关键词:恩诺沙星注射液;内毒素检查;凝胶法
恩诺沙星属氟喹诺酮类畜禽专用的广谱杀菌药。对大肠杆菌、沙门氏菌、金黄色葡萄球菌、支原体、衣原体等均有良好作用,在兽医临床上被广泛应用。细菌内毒素是革兰氏阴性菌的细胞壁成分,可引起人和动物发热[1-3]。药品如果被细菌内毒素污染会产生严重的安全问题,尤其是对身体机能较差的患病及幼龄动物。因此,控制恩诺沙星注射液中的细菌内毒素含量对于保证产品的安全性非常有必要。笔者对恩诺沙注射液的细菌内毒素检查方法学进行了研究,为该产品细菌内毒素检查提供依据。
1 试验材料
1.1 仪器
单人净化工作台,苏州净化设备有限公司;
101型电热鼓风干燥箱,北京中兴伟业世纪仪器有限公司;
QL-861型旋涡混合器,江苏海门其林贝尔仪器制造有限公司;
DZKW-4恒温水浴锅,北京中兴伟业仪器有限公司;
试验所用玻璃器皿经250℃烘烤1h以上。
1.2 试验药品
细菌内毒素工作标准品,批号:201784,规格:80EU/支,中国食品药品检定研究院;
细菌内毒素检查用水,批号:2010150,规格:5mL/支,湛江安度斯生物有限公司;
鲎试剂(TAL),批号:2008274,灵敏度:0.125EU/mL,规格:0.1mL/支,湛江安度斯生物有限公司;
鲎试剂(TAL),批号:2009213,灵敏度:0.125EU/mL,规格:0.1mL/支,湛江博康海洋生物有限公司;
恩诺沙星注射液,批号:20201001,20201002,20201003,规格:200mg/mL,天津市中升挑战生物科技有限公司。
2 方法与结果
2.1 鲎试剂灵敏度复核试验
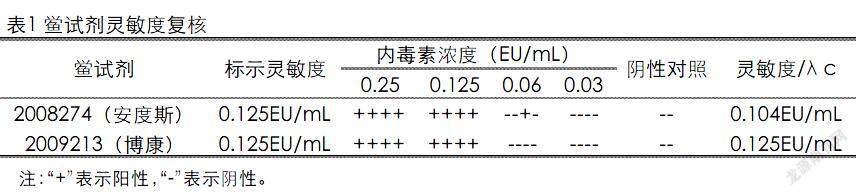
根据《中华人民共和国兽药典》2015版附录1143“细菌内毒素检查法”[4],进行鲎试剂的标示灵敏度复核。结果见表1。结果显示2种不同厂家的鲎试剂的复核灵敏度λc均在0.5~2.0λ之间,符合规定。
2.2 细菌内毒素限值(L)的确定
根据公式:L=K/M[5],其中注射剂K=5EU/kg。M为每千克体重的最大供试品单次剂量,本药品的推荐剂量为:一次量,每10kg体重,猪0.125mL,计算得出M为0.0125mL/kg,进一步计算得出L=400EU/mL,故将恩诺沙星注射液的内毒素限值确定为400EU/ml。
2.3 恩诺沙星注射液最大有效稀释倍数(MVD)的确定
根据公式MVD=cL/λ,其中L为400EU/mL;c为供试品浓度1.0mL/mL(当L以EU/mpL表示时,则c=1.0mL/mL);λ为鲎试剂标示灵敏度,根据市售鲎试劑现有规格,计算出恩诺沙星注射液MVD:MVD 0.5~MVD 0.03分别为800、1,600、3,200、6,400和12,800倍。
前期已进行干扰预实验,供试品稀释到800倍及以上稀释倍数时,供试品溶液对鲎试剂反应无干扰。因此,参考现有鲎试剂的规格(λ=0.125EU/mL),MVD为3,200。
2.4 正式干扰试验
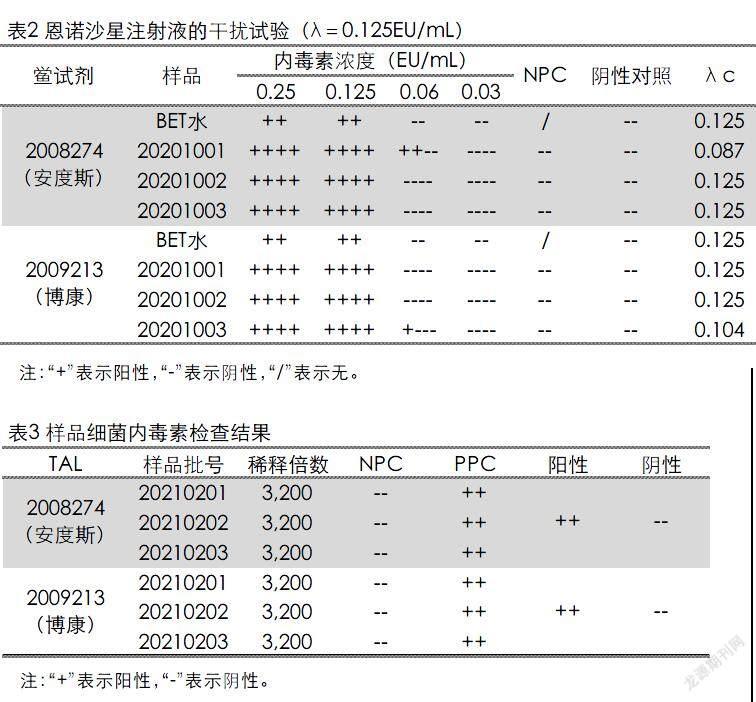
现依法进行正式干扰试验。取3批恩诺沙星注射液,用细菌内毒素检查用水将供试品进行3,200倍的稀释(NPC),依法检测,结果见表2。结果显示三批依法添加内毒素的供试品溶液的反应结果均在0.5~2.0λ之间,依据《中华人民共和国兽药典》2015版附录1143细菌内毒素检查法的要求,认为供试品在该浓度下无干扰作用。
2.5 样品细菌内毒素检查
另取恩诺沙星注射液3批,依法进行内毒素检测,结果见表3。结果表明3个批次的3,200倍稀释的供试品溶液的内毒素含量均小于0.125EU/mL,说明三批恩诺沙星注射液的内毒素含量低于400EU/mL,符合要求。
3 讨论
本试验用两个厂家的鲎试剂对恩诺沙星注射液三个批次的样品进行了干扰试验,结果表明样品稀释至3,200倍的供试品溶液对鲎试剂反应无干扰,确定所采用的方法可行。恩诺沙星注射液可适用细菌内毒素检查法(凝胶法),用灵敏度为0.125EU/mL的鲎试剂按凝胶限度检查法对另外3批样品进行细菌内毒素检查,结果均符合规定。
本研究建立的细菌内毒素检查法适用于天津市中升挑战生物科技有限公司生产的恩诺沙星注射液(20%),该产品为国家五类新兽药,目前市场上未见其他厂家产品,由于不同厂家的处方工艺不尽相同,内毒素检查干扰因素也不相同,因此,未来其他兽药厂家生产的恩诺沙星注射液(20%)应根据实际情况建立与其适应的内毒素检查方法,以便于更好地控制产品质量。
参考文献:
[1] 朗青.无菌原料药头孢噻肟钠细菌内毒素的控制[J].煤炭与化工,2014,37(6):41.
[2] 张虞婷,丁苏苏,李倚云.细菌内毒素的研究进展及其检查法的应用[J].天津药学,2015,27(5):66.
[3] 陈新宇,曹春然,孙圆媛.枸橼酸细菌内毒素检查(凝胶法)方法学研究[J].中国药品标准,2021,22(1):61.
[4] 中华人民共和国兽药典:一部[S].2015年版.2015:200.
[5] 中华人民共和国药典:四部[S].2015年版.2015:154.
