阿帕替尼联合PC方案化疗治疗肺癌合并恶性胸腔积液患者的临床疗效
2021-12-22邢东辉王丽齐仕宇付晓瑞
邢东辉 王丽 齐仕宇 付晓瑞
(1. 上蔡蔡州医院消化肿瘤内科,河南 驻马店 463800;郑州大学第一附属医院肿瘤科,河南 郑州 450000)
恶性胸腔积液属肺癌常见并发症,可导致患者出现胸闷、气闭等不适症状,是患者预后差的标志[1]。铂类药物胸腔灌注联合静脉化疗是目前临床治疗肺癌合并恶性胸腔积液常用方案,可一定程度减少胸腔积液,控制病情进展,但总体治疗效果不够理想。
近年来临床研究发现,肺癌患者血清血管内皮生长因子(VEGF)及受体VEGFR均呈异常高表达状态,可增加血管渗透性,对恶性胸腔积液的形成具有重要作用,需针对其治疗以提升疾病控制效果[2]。其中阿帕替尼属多靶点小分子抗血管药物,对VEGFR-2酪氨酸激酶具有良好抑制作用,在恶性肿瘤治疗中应用广泛[3]。
本研究将阿帕替尼与PC化疗联合应用于肺癌合并恶性胸腔积液患者的治疗,分组从多方面综合分析其应用价值,为临床治疗提供数据参考。现报告如下。
1 资料与方法
1.1 一般资料
选取2018年1月~2020年10月我院肺癌合并恶性胸腔积液患者109例作为研究对象,选例标准如下:
(1)纳入标准:均经胸部X线平片、CT、组织病理学等临床综合检查确诊为原发性非小细胞肺癌,且检查结果显示癌灶转移至胸膜致单侧或双侧癌性胸腔积液,即合并恶性胸腔积液;胸腔积液量均可测量;EGFR等肺癌驱动基因呈阴性或状态不明;卡氏(KPS)评分>70分,预计生存期>3个月;精神、认知状态、依从性良好,可有效配合临床治疗与检查;均知情本研究并签署同意书。
(2)排除标准:合并其他肺部病变或其他组织器官恶性肿瘤;对本研究所用治疗方案存在使用禁忌证或不耐受;合并感染性疾病;凝血功能障碍;心、肝、肾等器官功能不全;既往抗血管药物治疗史或胸腔灌注给药史;合并出血性疾病或潜在出血风险;合并严重内科疾病。
将所选研究对象按随机数字表法分研究组(n=55)、对照组(n=54)。
其中研究组男34例,女21例;年龄47~73岁,平均(60.71S6.04)岁;病理类型:腺癌36例,鳞癌19例;胸腔积液量:<1000 mL 35例,≥1000 mL 20例;KPS评分72~89分,平均(81.16S3.42)分。
对照组男32例,女22例;年龄49~75岁,平均(62.74S5.95)岁;病理类型:腺癌38例,鳞癌16例;胸腔积液量:<1000 mL 36例,≥1000 mL18例;KPS评分74~91分,平均(82.14S3.51)分;两组性别、年龄、病理类型、胸腔积液量、KPS评分等基础资料均衡可比(P>0.05)。本研究经医学理委员会审批通过。
1.2 方法
于给药前1~3 d行超声定位下胸腔穿刺置管引流术;用药治疗期间根据患者个体情况予以补水、维持水电解质平衡、止吐等常规处理。
1.2.1 对照组
采用PC方案化疗:以21 d为1个化疗周期,于每周期第1 d一次性静脉滴注培美曲塞(扬子江药业集团有限公司,国药准字H20143380)500 mg·m-2;于每周期第2 d、9 d、16 d胸腔灌注顺铂(江苏豪森药业集团有限公司,国药准字H20010743)25 mg·m-2,灌注给药后嘱患者每30 min左右更换1次体位,便于药物与胸膜腔充分接触。
1.2.2 研究组
在对照组基础上联合阿帕替尼(江苏恒瑞医药股份有限公司,国药准字H20140103)口服治疗:于每周期第1d~第21 d 餐后0.5 h服用,500 mg·d-1。
两组均连续治疗2个周期后实施疗效评估。
1.3 恶性胸腔积液疗效评估标准
根据胸腔积液减少及维持情况实施评估,其中胸腔积液完全消失并维持4周以上为完全缓解;与治疗前比较,胸腔积液减少50%以上并维持4周以上为部分缓解;与治疗前比较,胸腔积液减少不及50%或增加不及25%为无效;与治疗前比较,胸腔积液增加25%及以上为进展。总有效率=(完全缓解+部分缓解)/总例数×100%。
1.4 观察指标
临床统计:(1)两组恶性胸腔积液治疗总有效率;(2)治疗期间及时详细统计两组毒副反应,并根据WHO抗癌药物毒性反应标准分级。
临床检查:分别于治疗前后采集患者晨起空腹状态下肘外周静脉血约5ml,以3000 r·min-1转速离心10min,分离血清,采用全自动生化分析仪(迈瑞,BS-220型)实施检测;(1)采用电化学发光法测定癌胚抗原(CEA)、糖类抗原125(CA125)、非小细胞肺癌抗原(CYFRA21-1)3项肿瘤标志物水平。(2)采用酶联免疫吸附法(ELISA)测定血清血管内皮因子-A(VEGFA)、血管内皮因子-B(VEGFB)水平。
1.5 统计学处理
通过SPSS22.0软件进行数据处理,计数资料以百分率(%)表示,采用χ2检验,计量资料以均数S标准差(SSD)表示,采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 恶性胸腔积液治疗总有效率
研究组恶性胸腔积液治疗总有效率高于对照组(P<0.05),见表1。
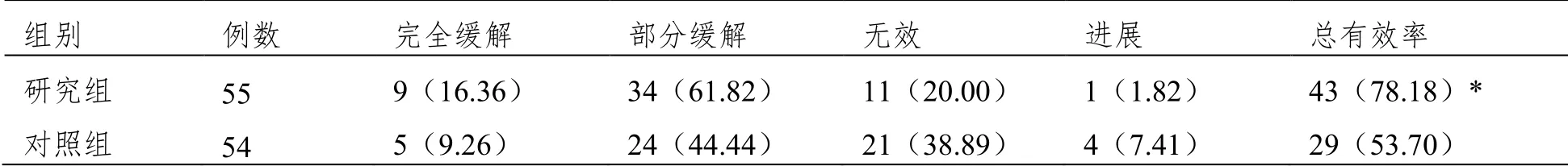
表1 两组恶性胸腔积液治疗总有效率比较n(%)
2.2 肿瘤标志物
与治疗前相比,各治疗组的血清CEA、CA125、CYFRA21-1水平均明显降低(P<0.05),其中研究组更为显著(P<0.05),见表2。
表2 两组血清肿瘤标志物水平比较(±SD)

表2 两组血清肿瘤标志物水平比较(±SD)
注:与同组治疗前比较,aP<0.05;与同期对照组相比,*P<0.05。
组别 例数 CEA(ng·mL-1) CA125(U·mL-1) CYFRA21-1(U·mL-1) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 研究组 55 57.28±6.31 32.35±4.07a* 47.15±6.77 31.72±5.03a* 7.39±0.71 2.88±0.40a* 对照组 54 59.60±6.52 39.57±4.82a 44.93±6.59 41.04±5.76a 7.61±0.75 3.57±0.50a
2.3 血管内皮因子
与治疗前相比,各治疗组的血清VEGFA、VEGFB水平均明显降低(P<0.05),其中研究组更为显著(P<0.05),见表3。
表3 两组血清血管内皮因子水平比较(±SD)

表3 两组血清血管内皮因子水平比较(±SD)
注:与同组治疗前比较,aP<0.05;与同期对照组相比,*P<0.05。
组别 例数 VEGFA(ng·mL) VEGFB(ng·mL) 治疗前 治疗后 治疗前 治疗后 研究组 55 107.04±12.81 83.54±9.08a* 90.26±8.12 73.38±6.17a* 对照组 54 103.38±13.02 90.77±9.94a 93.21±8.35 80.25±6.81a
2.4 毒副反应
统计结果显示,两组均未出现Ⅳ级毒副反应,患者耐受性良好,未影响治疗进程,且两组各毒副反应发生率比较差异均无统计学意义(P>0.05),见表4。
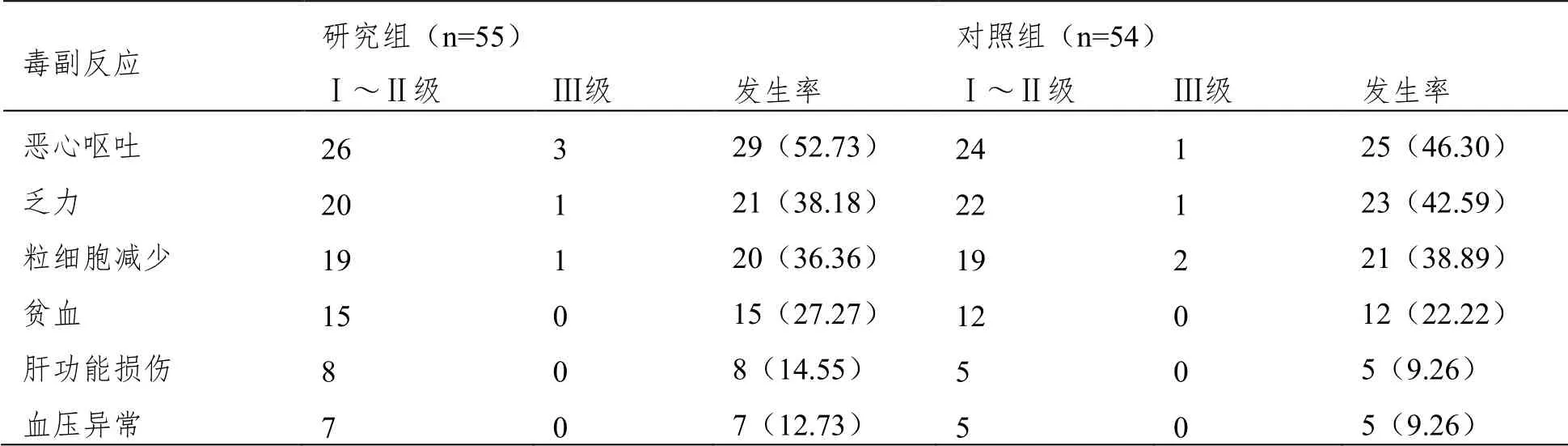
表4 两组毒副反应发生率比较n(%)
3 讨论
恶性胸腔积液是肺癌胸膜转移的结果,肺癌患者中发生率可达15%左右,可加速病情进展,并提示不良预后,是临床治疗重点及难点之一[4]。
培美曲塞是临床治疗原发性肺癌常用抗代谢药物,具有多靶点作用,可对肿瘤核酸物质合成产生抑制作用,进而发挥抗肿瘤效果[5]。而化疗药物胸腔灌注是针对性治疗恶性胸腔积液的主要方法,其中多以顺铂为主,药物进入胸腔后可通过渗透、扩散作用杀伤癌细胞,亦可通过胸膜缓慢吸收入血维持一定有效血药浓度;其与培美曲塞静脉化疗联合可对癌灶及恶性胸腔积液发挥一定控制作用,但存在较大个体差异性,部分患者经治疗后仍无法控制至理想状态[6]。
随病理学研究的不断深入,临床发现,作为最重要的肿瘤血管生长因子,VFGF表达可在肺癌细胞转移至浆膜腔时显著增高,除刺激癌灶新生血管生成外,还可促使浆膜腔毛细血管新生,扩大液体滤过面积,同时增加毛细血管通透性,进而使穿腹膜蛋白浓度升高,促进恶性胸腔积液形成[7]。
基于上述理论指导,本研究将抗血管生成作为主要思路,在PC化疗基础上联合应用阿帕替尼实施治疗。其主要作用靶点为VEGFR-2,可竞争性结合该受体胞内酪氨酸ATP结合位点,抑制VEGF与之结合及酪氨酸激酶活性,进而对新生血管生成发挥良好控制作用,降低肿瘤微血管密度[8]。杨燕峰等[9]相关研究指出,在化疗基础上联合应用阿帕替尼治疗晚期肺癌相关恶性胸腔积液效果显著,可提高治疗有效率,且毒副反应未见明显增多。
本研究结果中,研究组恶性胸腔积液治疗总有效率高于对照组(P<0.05),但两组各毒副反应发生率无明显差异(P>0.05),充分证实了阿帕替尼在肺癌合并恶性胸腔积液治疗中的重要价值。
为深入分析阿帕替尼、PC化疗联合方案提升疾病控制效果的相关机制,本研究在上述结论基础上进一步比较两组肿瘤标志物、血管新生相关因子变化情况。其中CEA、CA125、CYFRA21-1均是目前临床用于诊断、评估肺癌常用肿瘤标志物,其血清水平可有效反映肺癌细胞生长情况[10]。而VEGFA、VEGFB水平升高与肿瘤血管新生、恶性胸腔积液形成直接相关,且可有效反映肿瘤细胞活性[11]。
分析本研究结果发现,阿帕替尼、PC化疗联合方案可显著降低患者肿瘤标志物、VEGFA、VEGFB表达水平,可见其在抑制新生血管生成、控制癌灶进展方面均有积极作用,进而有效减少恶性胸腔积液。阿帕替尼吸收入血后可通过抑制肿瘤血管生成、增殖达到抑制肿瘤生长作用,同时经血液循环到达胸膜,阻断VEGF-VEGFR2通路,调节转移病灶血管内皮细胞,改善血管渗透性,减少恶性胸腔积液[12]。
综上可知,阿帕替尼、PC化疗联合方案可有效控制原发肺癌病灶的同时对并发的恶性胸腔积液发挥良好缓解作用,可有效降低肿瘤标志物及VEGFA、VEGFB表达,增强病情进展控制效果,且不影响治疗安全性。
Vax the world
Madhukar Pai
Earlier this month, while the United Nations (UN) Climate Change Conference convened in Glasgow, countries also gathered at the Global Conference on Health and Climate Change to recognize the climate crisis as a global health crisis-a consequence of increased poverty, food and water insecurity, and infectious disease transmission, among other dangers. Unsurprisingly, both crises are worse in lower-income countries. These countries are also experiencing the greatest number of deaths and collateral damage from COVID-19.
Science. 2021 Nov 26;374(6571):1031. doi: 10.1126/science.abn3081. Epub 2021 Nov 25.
