金属-有机骨架MIL-88A(Fe)及其复合物的合成与高级氧化降解水体有机污染物的研究进展
2021-12-21王茀学王崇臣
王茀学, 王崇臣
北京建筑大学环境与能源工程学院,建筑结构与环境修复功能材料北京市重点实验室, 北京 100044
金属-有机骨架(metal-organic frameworks, MOFs)是一类由中心金属离子为节点、有机配体做组件桥连而成的具多孔网状结构的新兴材料[1-2]. MOFs结构多样且孔径可调,具有独特的物理和化学特性[3-4],在气体储存[5-6]、分离[7-8]、催化[9-10]、医学[11-12]和环境修复[13-14]等众多领域展现出了良好的应用前景. 以环境修复领域为例,MOFs不但能实现对包括重金属、有机污染物的荧光传感检测[15-16],还能通过吸附[17-21]及还原/氧化等过程将各种污染物从环境中去除[22-26].
部分MOFs能被可见光/紫外/紫外-可见光激发产生光生e-(电子)-h+(空穴),显示出潜在的光催化性能,如NH2-UiO-66[27]、ZIF-8[28]等. 促进光生e--h+分离效率是提高光催化性能的有效途径,因此很多研究者通过引入氧化石墨烯[29]、金属氧化物[30]等功能材料实现e-快速转移从而提高光催化效率. Wang等[23]系统综述了MOFs光催化降解有机污染物的研究现状,并提出了其作为光催化剂降解有机污染物所面临的机遇与挑战. 大量研究表明,在光催化体系中添加H2O2、PS (过硫酸盐)等氧化剂时,氧化剂不但能抑制e--h+复合,还能被e-分解产生·OH (羟基自由基)、·SO42-(硫酸根自由基)等具有强氧化性的活性物质,进而氧化降解有机物分子. Du等[31]总结了MOFs及其衍生物活化PS降解有机物研究进展,指出钴和铁基MOFs具有较好的活化效果;Sharma等[32]综述了MOFs及其衍生物用于高级氧化去除染料等有机污染物研究进展,认为铁基MOFs是具有广阔应用前景的异相催化剂;Cheng等[33]总结并对比了铁及其他金属基MOFs类芬顿降解有机物性能,发现MIL (materials of institute lavoisior)系列的铁基MOFs关注度较高. MIL系列的铁基MOFs有MIL-53(Fe)、MIL-68(Fe)、MIL-88A(Fe)、MIL-88B、MIL-100(Fe)和MIL-101(Fe)等,其中由富马酸和Fe(Ⅲ)构筑的MIL-88A(Fe)不但具有较大的高级氧化应用潜力,且被认为是环境友好材料[34]. 当前对MIL-88A(Fe)的研究还处在初期,总结、对比其合成方法有利于促进以MIL-88A(Fe)为代表的MOFs材料的宏量、绿色合成,梳理其在AOPs领域的研究现状并提出发展方向具有重要意义.
MIL-88A(Fe)是一种较具有代表性的MOF材料,其晶体结构类型为六角形(P-62c). 每个Fe(Ⅲ)与6个富马酸配体的μ3-O配位形成Fe—O簇,再由富马酸连接成三聚体,最终形成具有孔和笼(5~7 Å)的三维骨架结构. 丰富的Fe—O簇使其能被可见光激发产生e--h+,在类芬顿、激发PS等体系中表现出较高活性[35-36]. 截至目前,研究者发现MIL-88A(Fe)具有多种形貌,其中最常见的有3种,即r-MIL-88A(Fe)(棒状,rod-like)[35,37]、s-MIL-88A(Fe)(纺锤状,spindle-like)[38-39]和d-MIL-88A(Fe)(钻石状,diamond-like)[40-41]. 研究表明,不同形貌的MIL-88A(Fe)对光具有不同的吸收性能,从而也影响了其对应的催化性能[42],因此通过调节合成条件制备具有不同形貌的MIL-88A(Fe)引起了诸多研究者的关注. 该综述将系统梳理和总结MIL-88A(Fe)及其复合物的合成方法与策略以及形貌控制方法,介绍MIL-88A(Fe)及其复合物在高级氧化方面的研究进展,包括光芬顿、活化PS和催化臭氧氧化去除有机污染物的效率、反应机理等,以期为研究者继续深入发掘MIL-88A(Fe)在高级氧化方面的潜力提供有用信息.
1 合成方法及形貌调控
1.1 MIL-88A(Fe)的合成
1.1.1水/溶剂热法与产物形貌
水/溶剂热法能制备出形貌规整、结晶度高的MOFs材料,是合成MIL-88A(Fe)的常用方法之一[43]. 将FeCl3·6H2O和富马酸按1∶1分散在H2O/DMF(N,N-二甲基甲酰胺)中,在65~150 ℃下加热4~6 h即可得到MIL-88A(Fe)〔见图1(a)〕. 合成条件(如加热温度和溶剂种类)对颗粒尺寸有明显影响,通常以H2O为溶剂且提高反应温度可得到粒径较大的产物. 例如,65 ℃水热反应6 h得到的MIL-88A(Fe)粒径为(250±55)nm,而将温度升至100 ℃时,其粒径达到(915±65)nm[44]. 除对产物的粒径产生影响外,合成条件还对晶体颗粒的形貌产生明显影响. 如图1(b)~(e)所示,65 ℃水热反应4 h得到的MIL-88A(Fe)呈棒状,溶剂换为DMF时(65 ℃)产物为钻石状,将温度升至100 ℃并延长反应时间至12 h,产物则变为纺锤状[40,42].

图1 MIL-88A(Fe)结构及合成条件对其形貌的影响[40,42]Fig.1 The structure of MIL-88A(Fe) and the effects of prepared conditions on the morphology of MIL-88A(Fe)[40,42]
1.1.2超声法
超声法合成过程是在溶剂中产生气泡并快速破裂,形成局部高温,具有合成条件较为简单、耗时短(5~60 min)等优点. 超声波辐射时间是影响颗粒尺寸和晶体形貌的主要因素,适当延长时间有利于增加产物颗粒尺寸. 超声波浴辐射2 h,产物表面粗糙,尺寸较大(长2.7~5.4 μm、宽1.6~3.2 μm);当反应时间缩短至1 h,MIL-88A(Fe)呈现规整的纺锤状,表面光滑,尺寸为1.3 μm×0.55 μm. 此外,超声方式对产物也有一定的影响,如使用脉冲探头辐射超声波反应10 min所得到的MIL-88A(Fe)粒径较小,约为500 nm×180 nm,而相同条件下,使用连续探头辐射超声波方式得到的产物粒径约为900 nm×250 nm[45].
1.1.3微波辅助法
微波辅助法是利用微波辐射的方式对反应液进行加热,分子充分碰撞从而大幅提高反应速率. 该法可在10 min内完成反应,是宏量制备纳米级MIL-88A(Fe)(<100 nm)最简便快速的方法之一[44]. 反应温度和反应时间是影响产物晶体颗粒尺寸和形貌的主要影响因素. 50 ℃下微波辐射2 min所得产物的粒径约20 nm,而80 ℃下反应2 min产物粒径增至100 nm左右[44]. 升高反应温度或延长微波辐射时间会增大产物粒径,但该方法合成的MIL-88A(Fe)因为结晶太快而无规整形貌.
1.1.4室温搅拌法
室温搅拌法是在室温下对反应液进行搅拌,Fe(Ⅲ)和富马酸缓慢反应生成MIL-88A(Fe)粉末. 该法制备的MIL-88A(Fe)为纺锤状,影响产物尺寸的主要因素为反应物初始浓度. 10 mmol的富马酸溶液和等摩尔浓度的FeCl3·6H2O溶液混合,室温搅拌24 h后得到MIL-88A(Fe)尺寸为 1 000 nm×500 nm. 将富马酸配体和FeCl3·6H2O分别增至20 mmol(其他条件不变)时,产物尺寸缩至500 nm×300 nm. 这表明提高反应液浓度有利于缩小产物尺寸[46]. 但是,该方法也面临耗时长(24~72 h)、产率低(25%)、产物难分离及产生废液等问题[47].
1.1.5机械化学法
机械化学法合成MOFs材料无需(或需微量)溶剂、耗时短(10~60 min)、产量大、产物粒径小,被认为是一种绿色的合成方法[43]. 将FeCl3·6H2O和富马酸钠置于研钵中研磨10 min,产物没有规则的形貌[48]. 在研钵中添加FeCl3·6H2O和纯水研磨3 min使金属盐彻底溶解后,再加入富马酸钠并继续研磨10 min,产物为r-MIL-88A(Fe),但没有明显的棱角. 该法的不足之处是产物结晶度较低,且可能含有无定形杂质[22].
水/溶剂热法、超声法、微波辅助法、室温搅拌法和机械化学法合成MIL-88A(Fe)各有优缺点. 水/溶剂热法合成虽然比其他几种方法缓慢,但可得到高质量的MIL-88A(Fe),因此目前应用较为广泛. 超声法、微波法能快速合成尺寸较小的晶体,但其产率不高、产物形貌不规整. 室温搅拌法面临耗时长、产率低及产生废液较多等难题. 机械化学法合成MIL-88A(Fe)无需添加溶剂(或需微量溶剂),且反应后无废液产生,因此更符合绿色化学的发展趋势.
1.2 MIL-88A(Fe)复合物的制备
1.2.1水/溶剂热法
水/溶剂热法制备复合物方法较为简单,将选定的功能材料〔如GO (氧化石墨烯)[49]、g-C3N4(石墨相氮化碳)[50]和ZnO[51]等〕或其前驱体(如Ag3PO4的前驱体为AgNO3和NaH2PO4)加入MIL-88A(Fe)合成体系即可. 该法操作简单,且能保留MIL-88A(Fe)规整的形貌不受破坏,是制备复合物的常用方法.
1.2.2机械研磨法
机械研磨法制备复合物是将MIL-88A(Fe)粉末与功能材料混合,借助机械力使其相互作用并在2种材料交界面形成异质结结构,是制备复合材料的有效方法. 该法制备复合材料能保留MIL-88A(Fe)形貌,无需添加溶剂,具有绿色、经济、操作简单、耗时短(10~60 min)等优点[52].
1.2.3重结晶法
重结晶法是将功能材料进行溶解后与MIL-88A(Fe)分散液混合,功能材料沉积并在MIL-88A(Fe)表面再次结晶而获得复合材料. 以PDINH (3,4,9,10-苝四甲酰二亚胺)为例,将其溶于浓硫酸后与MIL-88A(Fe)的分散液充分混合,PDINH在MIL-88A(Fe)表面沉积、重结晶,最后形成薄层覆盖在MIL-88A(Fe)的外表面[53].
1.2.4光化学还原法
光化学还原法制备金属纳米颗粒负载的MOF复合物具有复合快速、绿色节能等优点[27]. 以FeCl3·6H2O为金属源,在合成体系中添加AgNO3,Ag+可与Cl-反应生成AgCl负载于MIL-88A(Fe)表面. 利用紫外-可见光照射30 min将部分AgCl还原成Ag,最终得到Ag/AgCl@MIL-88A(Fe)[54].
2 MIL-88A(Fe)及其复合物用于高级氧化去除有机污染物
MIL-88A(Fe)表面具有丰富的不饱和位点,在一定程度上能直接活化H2O2和PS产生具有强氧化性的活性物质(如·OH和·SO4-). 光照条件下,MIL-88A(Fe)产生光生e--h+,e-能活化H2O2、PS和臭氧,或将Fe(Ⅲ)还原为Fe(Ⅱ),Fe(Ⅱ)直接活化H2O2等氧化剂,显著提高活性物质的产生速率.
2.1 光芬顿
形貌不同的MIL-88A(Fe)具有相同的红外吸收特征〔见图2(a)〕,但r-MIL-88A(Fe)的(100)晶面衍射峰强度明显高于s-MIL-88A(Fe)和d-MIL-88A(Fe)〔见图2(b)〕[42]. 此外,r-MIL-88A(Fe)对光的吸收波长范围更长,光吸收强度更高且PL (光致发光)强度更低,如图2(c)(d)所示. 太阳光照射50 min后,r-MIL-88A(Fe)光芬顿去除RhB (罗丹明B)的效率更高且速率更快,如图2(e)(f)所示.
除光吸收能力强外,r-MIL-88A(Fe)还具有更低的活化能. 如图3(a)(b)所示,MIL-88A(Fe)的(100)晶面分解H2O2形成·OH的活化能为0.58 eV,低于形成·O2-的活化能(0.86 eV)[40]. 相比之下,(101)晶面活化H2O2形成·OH需要克服更高的能垒(0.84 eV)〔见图3(c)〕. 因此在光芬顿降解苯酚过程中,(100)晶面占比最高的r-MIL-88A(Fe) (60%)具有最快的降解速率与最高的TOF值(转换效率)〔见图3(d)〕.
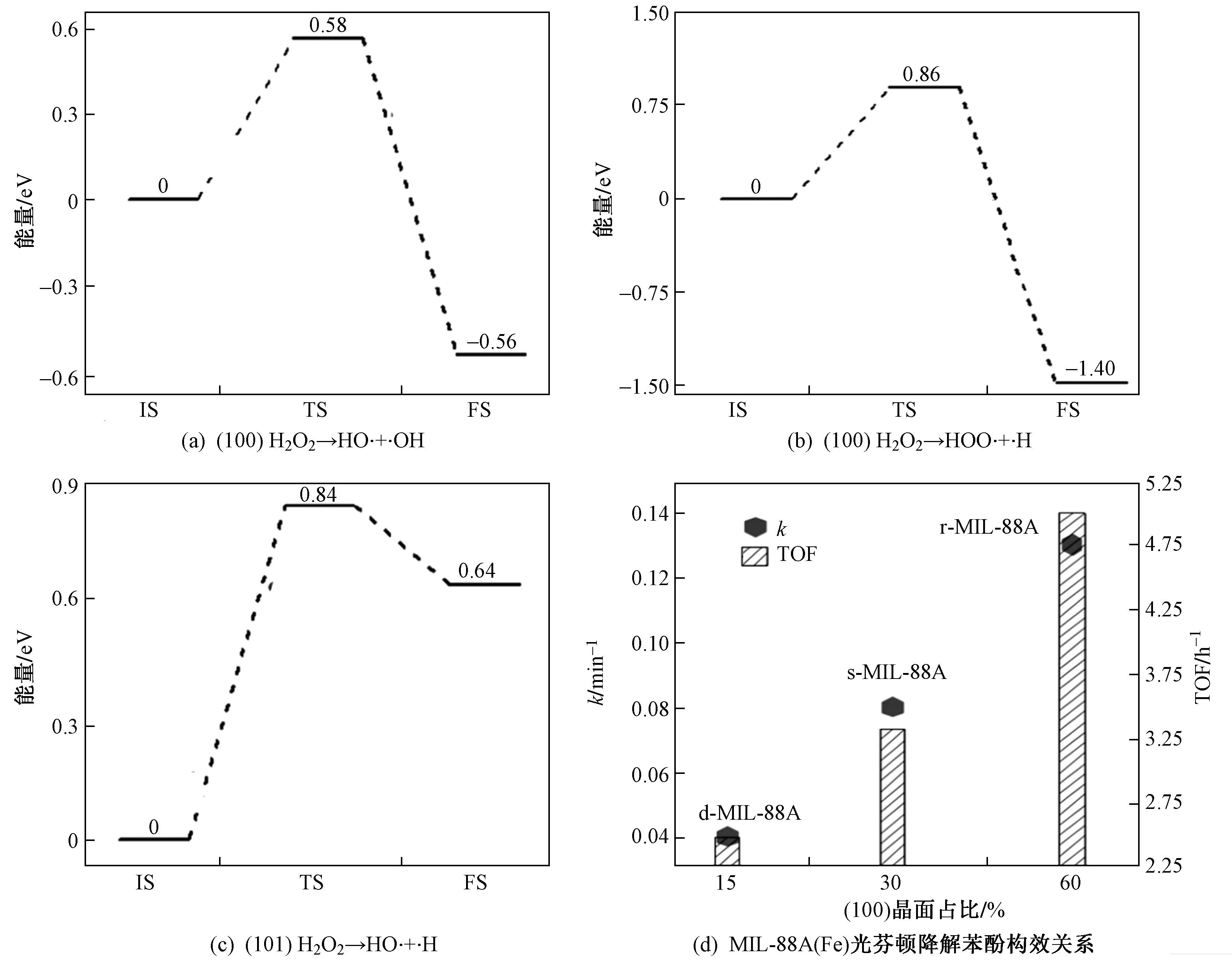
图3 MIL-88A(Fe)活化分解H2O2过程[40]Fig.3 Dissociation process of H2O2 over MIL-88A(Fe)[40]
将合适的功能材料与MIL-88A(Fe)复合是改善其光生电子-空穴分离效率及光芬顿性能的有效手段。Chen等[38]利用机械研磨法将PANI (聚苯胺)与MIL-88A(Fe)复合,PANI@MIL-88A(Fe)复合物在白光下完全去除BPA (双酚A)仅需30 min,比MIL-88A(Fe)快1倍(99%, 60 min). Yang等[55]将Ag3PO4与MIL-88A(Fe)复合,复合物在20 min内降解90.9%的四环素,远高于相同条件下MIL-88A(Fe)对四环素的去除率(52.2%). GO具有优良的电子转移能力,将其与MIL-88A(Fe)复合可有效抑制e--h+复合. GO紧密地包裹在MIL-88A(Fe)表面,负载量为9%(M88/GO-9)时催化剂由橙黄色变成亮黑色,带隙值也从2.58 eV缩至2.19 eV. M88/GO-9光芬顿降解RhB的效率约100%,远高于MIL-88A(Fe)(45%)[56].

注: C和C0分别为溶液的瞬时浓度和初始浓度,单位均为mg/L.图2 不同形貌MIL-88A(Fe)的表征与光芬顿降解RhB性能对比[42]Fig.2 Characterization and photo-Fenton RhB degradation over MIL-88A(Fe)[42]

M88/GO-9+hv→h++e-
(1)
H2O2+e-→·OH+OH-
(2)
e-+O2→·O2-
(3)
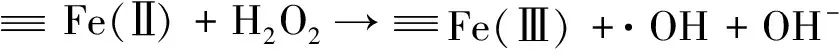
(4)
2.2 活化PS
活化PS〔包括PMS (HSO5-,过一硫酸盐)和PDS (S2O82-,过二硫酸盐)〕是一种SR-AOPs (基于·SO4-的高级氧化法). ·SO4-具有比·OH更长的半衰期(分别为30~40 μs和20 ns)及更高的氧化电位(E0分别为2.5~3.1、1.9~2.7 V)[57],因此其有机物去除率往往高于类芬顿体系.
MIL-88A(Fe)骨架中的Fe(Ⅲ)能直接活化PS产生·SO4-,在无光条件下活化PS对TC-HCl (盐酸四环素)的去除率为60% (90 min),高于无催化剂条件(PS+无光和PS+可见光)和无PS条件(MIL-88A+可见光). 光照条件下,MIL-88A(Fe)对TC的去除率进一步提高,在80 min内可达到99.8%,其原因是光照促进了e-的产生,从而加快PS活化速率〔见式(5)〕. 此外,该体系中·O2-对于降解有机物也具有一定贡献[35].
e-+S2O82-→·SO4-+SO42-
(5)

(6)
(7)
PDINH是一种环境友好的有机半导体材料,具有良好的稳定性和光吸收性能. Yi等[58]利用研磨法制备了PDINH@MIL-88A(Fe)复合物〔PxMy,其中P和M分别为PDINH和MIL-88A(Fe),x和y分别为PDINH和MIL-88A(Fe)占复合物的质量分数〕用于活化PDS降解抗疟疾药物CQ(磷酸氯喹). CQ在30 min的去除率达94.6%,高于相同条件下的MIL-88A(Fe)(约78%)和PDINH(90%). PDS的投加量从0.25 mmol/L增至2.0 mmol/L时,CQ的去除率由92.6%升至95.7%;继续增加PDS投加量,去除率没有增加反而降低,原因是复合物产生的e-有限,无法满足过量的PDS对e-的需求〔见式(8)(9)〕,而过量的PDS会消耗·SO4-〔见式(10)(11)〕.
P25M175+light→e-+h+
(8)
S2O82-+e-→·SO4-+SO42-
(9)
·SO4-+S2O82-→·OH+SO42-+·S2O8-,
k=6.1×105L/(mol·s)
(10)
·SO4-+·SO4-→S2O82-,
k=4.0×108L/(mol·s)
(11)
在pH为3~11范围内CQ都具有较高的去除率(≥90%),但pH=11时反应速率比初始条件(pH=5.04)降低了56.5%,原因是强碱性条件下,·SO4-容易与OH-反应生成氧化电位较低、半衰期较短的·OH,如式(12)所示. DFT (密度泛函理论)计算结果显示,PDINH与MIL-88A(Fe)复合后表面原子的电荷降低了2.339 eV,表明复合物中光生e-的流向是从PDINH到MIL-88A(Fe)[58].
·SO4-+OH-→·OH+SO42-
(12)
P25M175光催化活化PDS降解CQ机理如图4所示,MIL-88A(Fe)和PDINH都能被可见光激发产生e--h+,PDINH的e-转移到MIL-88A后活化PDS产生·SO4-. 此外,O2/·O2-的氧化还原电位(-0.33 eV)[59]低于MIL-88A(Fe)(2.16 eV)和PDINH(1.07 eV)的LUMO (最低未占轨道)电位,因此O2能与e-反应形成·O2-. 除·SO4-和·O2-外,h+及反应过程产生的·OH和非自由基1O2(单线态氧)对降解CQ也有一定贡献.

图4 P25M175光催化活化PDS降解磷酸氯喹(CQ)机理[58]Fig.4 Mechanism of photocatalysis-activated SR-AOP oxidation of CQ (chloroquine phosphate) over P25M175[58]
2.3 催化臭氧氧化
除了光芬顿和活化PS,催化臭氧氧化也是去除水体中有机污染物的有效手段. 通常认为,LAS (Lewis acid sites, 路易斯酸位点)是催化臭氧的主要位点[60]. 在25 ℃时,MIL-88A(Fe)具有3个明显的Py-FTIR (吡啶吸附红外光谱)吸收峰(1 070、1 042 和 1 012 cm-1),分别归属于LAS的ν18a、v12和v1振动[61]. MIL-88A(Fe)光催化臭氧氧化去除4-NP (4-硝基苯酚)仅需15 min时,TOC (总有机碳)去除率为76%. 而在无光照的条件下,MIL-88A(Fe)催化臭氧氧化降解92.9%的4-NP需要30 min,且TOC去除率仅为39%,表明光照在该反应过程具有明显的促进作用. 相比之下,MIL-88A(Fe)光催化降解4-NP效率更为有限,反应30 min去除率仅为23.4%,低于纯臭氧体系(51.4%). 活性物质捕捉试验表明,·OH和·O2-是降解4-NP的主要活性物质,此外1O2也具有一定的作用[61]. 磷酸盐通常被认为是催化剂表面铁位点的屏蔽剂,当反应体系中添加磷酸盐占据LAS[60]后,4-NP的去除率降低了58.6%,证明了LAS在催化臭氧氧化过程中的重要作用.
MIL-88A(Fe)光催化臭氧氧化降解4-NP的机理可以分为两部分[61]:一是MIL-88A(Fe)表面的LAS分解臭氧产生·OH、·O2-和1O2等活性物质〔见式(13)~(18)〕;二是e-〔见式(19)〕与臭氧反应生成·OH、·O2-和1O2进而降解4-NP〔见式(20)〕.
(13)

(14)
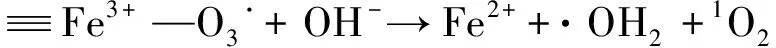
(15)
(16)
·OH2+OH-→H2O+·O2-
(17)

(18)
MIL-88A(Fe)+hv→e-+h+
(19)
O3+e-+H2O→1O2+·O2-+·OH
(20)
MIL-88A(Fe)的形貌对其光芬顿降解有机物的效率存在较明显的影响,(100)晶面占比最高的棒状形貌具有最高的活性,但形貌对活化PS、催化臭氧氧化效率是否有影响尚待研究. 氧化剂投加量和溶液初始pH是影响MIL-88A(Fe)高级氧化效率的主要因素. 氧化剂投加量较少时,体系中产生的活性物质有限,且不利于光生电子的转移,而过多的氧化剂则会淬灭活性物质;降低pH往往有利于促进光芬顿和活化PS反应. 臭氧本身具有较强的氧化性,能直接氧化分解部分有机物,将其与MIL-88A(Fe)耦合可明显增加其对有机物的去除率.
除催化活性较高、稳定性好,生物毒性低也是MIL-88A(Fe)能用于环境修复领域的重要因素. 在10%葡萄糖溶液中加入30 mg/kg的MIL-88A(Fe)后通过静脉注射至雌性大鼠体内,7 d后未观察到大鼠死亡或明显的中毒迹象[62]. 与对照组相比,大鼠的体重和行为无明显区别. 病理检查显示,试验组与对照组大鼠器官(包括心脏、肾脏和大脑)重量无明显差异,但脾脏、肝脏和肺出现异常. 值得注意的是,给药7 d后这些器官的重量逐渐恢复到正常值. 体内分布研究显示,纳米级的MIL-88A(Fe)被降解为铁和富马酸,最后随尿液和粪便排出体外. 在给药7~15 d期间,尿液和粪便中排除的铁含量较低;给药15 d后,给药剂量的47%(铁)经尿液和粪便排出. 服用MIL-88A(Fe)约2周后,大鼠体内铁稳态恢复到正常生理值,远少于服用氧化铁纳米颗粒所需恢复时间(7周). 静脉注射1 d后,大鼠肝脏和脾脏中富马酸含量约22wt%,但7 d内其浓度明显降低. 总而言之,MIL-88A(Fe)在光芬顿、活化PS和催化臭氧氧化方面具有较大的应用潜力,能有效降解染料、PPCPs (药物及个人护理品)和苯酚类等有机物(见表1). 因此,MIL-88A(Fe)可用于环境修复.

表1 MIL-88A(Fe)及其复合物用于高级氧化去除有机污染物
3 结论与展望
MIL-88A(Fe)是一种以Fe(Ⅲ)为节点、富马酸为桥连配体的环境友好型多孔MOF,其合成方法(水/溶剂热法、超声法、微波法和室温搅拌法等)多样、形貌易于调控且易于制备复合物. 利用水/溶剂热等方法可将MIL-88A(Fe)与其他功能材料进行复合,有效提高其光生e-转移效率. 高级氧化体系中添加的氧化剂 (如H2O2、PS和臭氧等)不仅能生成·OH、·SO42-和·O2-等活性物质,还能抑制光生e--h+复合. MIL-88A(Fe)具有较宽的pH适用范围,不易团聚且水稳定性和化学稳定性良好,因此可循环多次使用并保持高的催化活性.
虽然MIL-88A(Fe)及其复合物在可见光下具有良好的类芬顿去除有机污染物性能,但目前仍面临成本较高、Fe(Ⅲ)还原速率慢等关键问题. 此外,粉末状的催化剂用于光芬顿体系难以实现回收再利用,不利于实际污水处理. 活化PS产生的·SO4-具有比·OH 更高的氧化能力和更长的半衰期,且适用的pH范围更宽,但其持续输入的过硫酸盐对水环境的潜在风险还有待研究. 臭氧本身氧化性较强,且具有难闻的鱼腥味,吸入后有害人体健康. 因此,上述3种高级氧化的方法各有利弊.
总之,MIL-88A(Fe)作为新兴高级氧化催化剂得到了广泛的关注和研究.考虑到MIL-88A(Fe)用于AOPs还处于起步阶段,今后的发展存在无限可能. 基于笔者所在研究团队在MOFs尤其是MIL-88A(Fe)用于环境修复领域的长期工作积累,认为MIL-88A(Fe)今后的发展方向和趋势有以下几个方面:① MIL-88A(Fe)颗粒纳米化. 通常认为,纳米级催化剂具有更高的催化活性. ②合成绿色化. 研究已表明,MIL-88A(Fe)可在水溶液中合成,无须使用有机溶剂. 但水热法、超声法等合成后依然产生大量的废液. 机械研磨法合成无需溶剂(或仅需微量溶剂),因此有望实现绿色合成. ③应用负载化. 粉末状的MIL-88A(Fe)难以从水体中回收再利用,尤其将其尺寸缩小至纳米级,回收难度会增加. 将MIL-88A(Fe)负载于基质上能有效解决该问题. ④研究实用化. 目前的研究大多以实验室配置的溶液为目标污染物,今后应注重实际污水的处理. ⑤环境效应研究. 目前虽然已有论文报道其对大鼠的生理毒性,但其对不同生物不同时期(如哺乳动物的孕期、哺乳期等)的影响尚待系统研究. 大多数论文只研究MOFs去除污染物的效率,却很少研究MOFs本身的环境效应. 因此,今后的研究还应关注MIL-88A(Fe)等MOFs用于AOPs后对环境是否造成潜在的、长期的危害.
