大粒径磺酸基固相萃取填料的制备及其对弱碱性非法添加物的吸附性能评价
2021-12-17李爽文湘郡滕鑫丁星宇李壹熊晓辉
李爽,文湘郡,滕鑫,丁星宇,李壹,熊晓辉
(南京工业大学 食品与轻工学院,江苏 南京,211816)
β-受体激动剂,俗称瘦肉精,包括盐酸克仑特罗、特布他林、沙丁胺醇、莱克多巴胺等在内的十几种化合物[1-2]。将此类药物添加在动物饲料或饮水中能有效促进禽畜生长,提高胴体瘦肉率[3],但其残留物被人体过量摄入后,会出现胸闷、头痛、四肢麻木等诸多不良反应,长期食用还可诱发恶性肿瘤[2-4],因此我国农业部第176号公告已经明令禁止在饲料和动物饮用水中使用β-受体激动剂。三聚氰胺,是一种三嗪类含氮杂环有机化合物,化学式为C3N3(NH2)3,被广泛用作化工原料,不可被添加到食品当中[5],但因其较高的氮含量(66%左右),被一部分不法商贩恶意添加进奶制品中冒充蛋白质[6-7]。这些食品安全问题受到社会各界的广泛关注,而如何高效快速地检测出食品中可能存在的有害物质也成为研究的热点。
目前常用于β-受体激动剂和三聚氰胺的检测方法主要有液相色谱串联质谱法[8-9]、气相色谱串联质谱法[10-11]、拉曼光谱法[12-13]、免疫分析法[14-15]等。目前液相色谱串联质谱法是在定量检测β-受体激动剂和三聚氰胺中应用最广泛的方法。但由于食品样品基质的复杂性,往往使得直接测定样品中微量、痕量污染物较为困难,不仅准确度难以达到要求,对于仪器的损害也较大[16-17]。因此,在用仪器对样品进行检测之前的前处理过程就显得格外重要[18]。固相萃取技术(solid phase extraction,SPE)以其高效、便捷和实用等众多优点,在样品前处理方式中占据了重要的位置[19-21]。
随着检测分析行业对固相萃取的使用需求不断增加,固相萃取填料呈现多元化发展,其中以聚苯乙烯(polystyrene,PS)为代表的有机高分子聚合物基质固相萃取填料,因其比表面积大、表面反应力强、吸附能力强及性质稳定等优点[22-23],自出现以来就倍受分析者们的青睐。已有的磺酸基阳离子固相萃取填料大多采用浓硫酸磺化聚苯乙烯的方法,LI等[24]在用均匀的磺化聚苯乙烯微球作为模板制备可生物降解的壳聚糖中空微球时发现,用浓硫酸作为磺化剂,PS表面的磺酸基经过20 h的反应才饱和。WENG等[25]发现以浓硫酸为磺化剂的反应,需过量的硫酸才能反应完全。该方法耗费反应试剂,通常需要过量硫酸才能与聚苯乙烯反应完全[26],反应时间较长,反应温度较高;且填料粒径多在60~100 μm,进行固相萃取时耗时长,经常因样品基质黏稠堵塞柱管。本研究以聚苯乙烯微球为基质,以氯磺酸为磺化剂对其表面进行磺化修饰,得到磺酸基阳离子固相萃取填料,即磺化的聚苯乙烯(sulfonated polystyrene,SPS),并对填料的粒径、磺酸基担载量进行优化。结合高效液相色谱联用质谱法,用β-受体激动剂和三聚氰胺评价其吸附性能,对其在实际样品中的应用能力进行评价,并结合Miscellaneous设计和响应面法,找到应用于实际样品时,满足检测要求的材料最佳担载量。本研究对制备大粒径磺酸基阳离子固相萃取填料时节约试剂用量、节省反应时间、降低反应温度,前处理时有效缩短固相萃取时间等方面具有重要实际意义。
1 材料与方法
1.1 仪器与试剂
Pure扫描电子显微镜,荷兰Phenom公司;Vario ELcube元素分析仪,德国Elemental公司;Mastersizer 3000超高速智能粒度分析仪,英国Malvern公司;Nicolet IS5傅立叶红外光谱仪、UItiMate3000高效液相色谱-TSQ Quantum Access MAX三重四极杆质谱联用仪,美国Thermo Fisher公司。
PS微球(平均粒径:170 μm),南京麦科菲高效分离载体有限公司;PS微球(平均粒径:40 μm),无锡知益微球科技有限公司;空固相萃取柱(规格:3 cc/60 mg),深圳逗点生物技术有限公司;盐酸克仑特罗、莱克多巴胺、沙丁胺醇、克仑特罗-D9、莱克多巴胺-D6、沙丁胺醇-D3、三聚氰胺标准品,坛墨质检国家标准物质中心;甲醇和甲酸(色谱纯),美国Sigma-Aldrich公司;氯磺酸、四氯化碳(CCl4)、乙醇、四氢呋喃(均为分析纯),国药集团化学试剂有限公司。
3种β-受体激动剂及其同位素内标分别用甲醇配制成100 μg/mL的单标标准贮备液,-18 ℃避光保存;分别吸取适量的单标标准贮备液,用甲醇逐级稀释成1 μg/mL的混合标准液,-18 ℃避光保存。三聚氰胺标准品用甲醇配制成1 μg/mL的单标标准贮备液,-18 ℃避光保存。
1.2 SPS的制备
采用超纯水、乙醇和四氢呋喃洗涤PS微球,以除去PS表面的悬浮剂、单体和低分子物质,然后用乙醇洗涤5次,并真空干燥至恒重。将干燥的PS-DVB微球(2 g)添加到四颈烧瓶中,用CCl4(20 mL)溶胀3 h后,边搅拌边加入一定量的氯磺酸。在一定温度下反应结束后,将材料依次用乙醇和超纯水洗滤至中性,然后在水中浸泡过夜。次日,将材料用水洗滤至中性,用乙醇洗滤5次,并真空干燥24 h。
1.3 SPS的表征
使用Phenom Pure扫描电子显微镜观察微球形貌;采用溴化钾压片法制片,使用红外光谱仪测定微球表面官能团性质;使用Mastersizer 3000超高速智能粒度分析仪表征粒径分布。硫含量分析采用氧瓶燃烧、硫酸钡电位滴定法进行。根据公式(1)、公式(2)分别计算微球的担载量和磺化度:
(1)
(2)
式中:LA,担载量,mmol/g;X,硫元素质量百分比;MS,硫元素摩尔质量,g/mol;DS,磺化度,%;MPS,苯乙烯摩尔质量,g/mol;WSPS,磺化后SPS微球的质量,g;WPS,磺化前PS微球的质量,g。
1.4 固相萃取小柱的制备
在3 mL针筒型聚丙烯空柱管底部填入筛板,称取60 mg填料填入柱中,适度振实、振平后,填料上端由筛板封住,用配套的装柱推杆压实,得到固相萃取柱。
1.5 不同PS微球制备固相萃取柱
分别选取2种粒径不同PS微球,其平均粒径分别为170和40 μm,比较其磺化的难易程度,并按1.2节和1.4节方法制备固相萃取柱,比较其对3种β-受体激动剂和三聚氰胺的动态吸附能力。
1.6 样品处理
β-受体激动剂的样品处理方法按照GB/T 22286—2008《动物源性食品中多种β-受体激动剂残留量的测定 液相色谱串联质谱法》[27]进行。三聚氰胺样品参照GB/T 22388—2008《原料乳与乳制品中三聚氰胺检测方法》[28]中第二法的方法进行前处理。
1.7 仪器条件
1.7.1 分析β-受体激动剂仪器条件
色谱条件:色谱柱为Kinetex LC Column C18(100 mm×2.1 mm,2.6 μm);柱温30 ℃;进样体积10 μL;流动相A为0.1%甲酸水,流动相B为乙腈;梯度程序如下:0~1 min,97% A;1~3.5 min,97%~70% A;3.5~4.5 min,70% A;4.5~6.4 min,70%~25% A;6.4~6.5 min,25%~5% A;6.5~8.2 min,5% A;8.2~8.3 min,5%~97% A;8.3~10 min,97% A。流动相的流速设置为0.4 mL/min。
质谱条件:电喷雾离子源正离子电离(ESI+),电喷雾离子源温度500 ℃,毛细管电压5 500 V,雾化器流量为55 L/min。3种β-受体激动剂在多反应监测模式下的质谱检测参数见表1。

表1 三种β-受体激动剂的串联质谱检测参数Table 1 Tandem mass spectrometry detection parameters of three β-receptor agonists
1.7.2 分析三聚氰胺仪器条件
色谱条件:色谱柱为Thermo AccucoreTMHILIC(100 mm×2.1 mm,2.6 μm);柱温40 ℃;进样体积10 μL;流动相A为2 mmol/L甲酸铵水溶液,流动相B为乙腈;梯度程序如下:0~2 min,10% A;2~4 min,10%~50% A;4~5 min,50% A;5~5.2 min,50%~10% A;5.2~7 min,10% A。流动相的流速设置为0.4 mL/min。
质谱条件:电喷雾离子源正离子电离(ESI+),定量离子:127.1>85.2,定性离子:127.1>68.4;毛细管电压3 500 V,离子源温度350 ℃,雾化器温度300 ℃;裂解电压77 V;定量离子的碰撞能量为17 V,定性离子的碰撞能量28 V。
1.8 填料最佳担载量的选择
1.8.1 β-受体激动剂的最佳担载量选择
应用Miscellaneous设计和响应面法研究2个自变量填料担载量和加标浓度对3种β-受体激动剂回收率的影响,运用Design-Expert V8.0.6.1软件设计方案,建立回归模型,通过计算得到应用于实际猪肉样品时,满足检测要求应选择的材料最佳担载量。1水平担载量数值选用实验制备所得最高担载量(表2、表3)。根据实际情况调整,170 μm填料的担载量选用0、1.39、3.05 mmol/g;40 μm填料的担载量选用0、0.86、2.24 mmol/g。
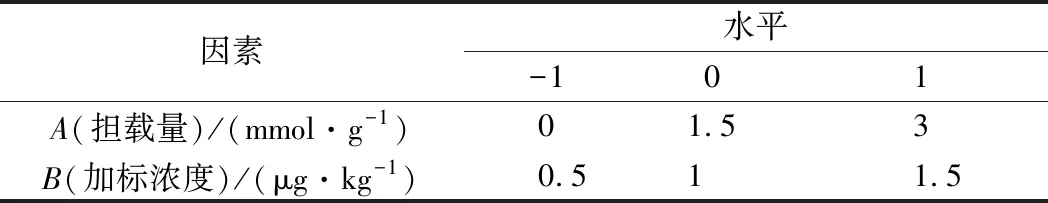
表2 170 mm SPS应用于β-受体激动剂的Miscellaneous 试验因素水平表Table 2 Levels and factors designed for 170 mm SPS fillers applied to β-receptor agonists Miscellaneous

表3 40 mm SPS应用于β-受体激动剂的Miscellaneous 试验因素水平表Table 3 Levels and factors designed for 40 mm SPS fillers applied to β-receptor agonists Miscellaneous
1.8.2 三聚氰胺的最佳担载量选择
方法同1.8.1节,试验因素水平如表4、表5所示。

表4 170 mm SPS应用于三聚氰胺的Miscellaneous 试验因素水平表Table 4 Levels and factors designed for 170 mm SPS fillers applied to melamine Miscellaneous
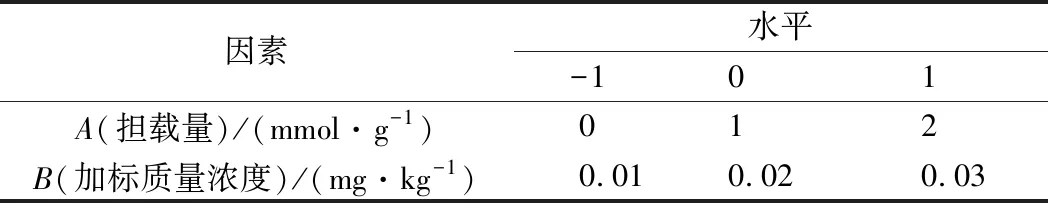
表5 40 mm SPS应用于三聚氰胺的Miscellaneous 试验因素水平表Table 5 Levels and factors designed for 40 mm SPS fillers applied to melamine Miscellaneous
2 结果与讨论
2.1 微球的表征
2.1.1 SEM表征
使用扫描电子显微镜观察材料的形貌。如图1所示,改性后的SPS与PS对比,微球仍然保持良好的单分散性和球形度,形态无明显变化。从图1-a(1 300×、2 300×)系列可以看出,改性后的微球表面出现了大量凸起的颗粒物,这是由于磺酸基成功修饰到苯环上导致的。

a-170 μm的微球;b-40 μm的微球图1 PS和SPS的SEM表征图Fig.1 SEM of PS and SPS
2.1.2 红外光谱表征
通过红外光谱对获得的产物进行表征。由图2可知,与PS相比,SPS多出3个新峰:1个宽峰位于3 400 cm-1处,这归因于被磺酸基团吸附的水分子的振动;位于1 168和1 034 cm-1处的2个峰,可以归因于C—S键,表明产物的苯环上引入了磺酸基团;苯环C—H在1 715 cm-1处的吸收峰得到增强,并且随着磺化度的增加,它成为一个宽而强的吸收带[29]。

图2 PS和SPS的红外光谱Fig.2 FTIR spectra of PS and SPS
2.1.3 粒径分布
通过表征微球的粒径(图3),可以获得磺化前后微球的单分散性和粒径变化。PS微球在磺化处理之前具有良好的分散性,并且在用2种磺化剂处理后,粒径均略有增加,单分散性变得更好,这是由于苯环上成功接枝磺酸基导致的。
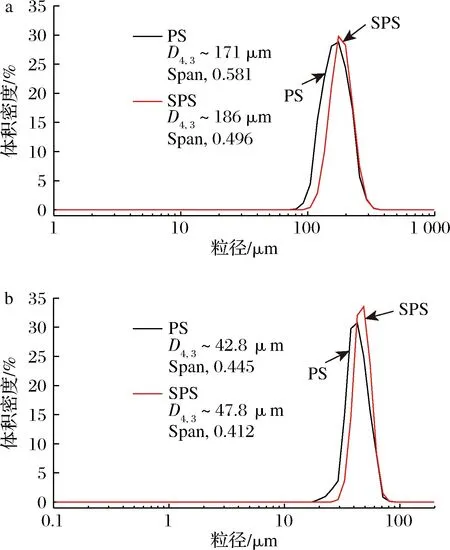
a-170 μm的PS,SPS;b-40 μm的PS,SPS图3 PS和SPS的Malvern Mastersizer粒径分布图Fig.3 Malvern Mastersizer droplet size distribution of PS and SPS
2.1.4 产物的元素分析
通过元素分析确定了SPS微球的元素组成,改性处理后,出现了大量PS微球元素组成中不存在的硫元素。使用元素分析结果,根据1.3节计算微球的担载量,判定以下反应条件的优化。
2.1.5 担载量的优化控制
2.1.5.1 反应时间对担载量的影响
在25 ℃、PS微球与氯磺酸摩尔比为1∶1的条件下进行机械搅拌反应,探究担载量与磺化时间之间的关系。结果如图4所示,磺化反应速度非常快,随着反应时间的增加,担载量迅速增大,170 μm微球反应5 min即可达到3.05 mmol/g的担载量。5 min后,担载量随反应时间的延长变化不大。反应条件相同时,170 μm PS比40 μm PS更容易被氯磺酸改性。

图4 SPS微球担载量随时间的变化图Fig.4 The chang of loading capacity of SPS microspheres with reaction time
2.1.5.2 PS载体磺酸基担载量的可控性
在25 ℃条件下反应5 min,通过改变氯磺酸与PS微球的摩尔比,研究氯磺酸用量对PS载体担载量的影响,结果见图5。担载量随氯磺酸用量的增加而增大,并且呈近似线性关系(170 μm SPS:y=3.15x+0.08,R2=0.968 0;40 μm SPS:y=2.47x-0.28,R2=0.986 9)。将担载量按照1.3节公式(2)换算成磺化度,则磺化度与氯磺酸用量也呈近似线性关系。由图5-b可知,已得到的微球最大担载量3.05 mmol/g,对应的磺化度为39.56%,如果氯磺酸含量持续增加,理论上磺化度接近100%时将不再增大,对应的PS载体担载量此时会出现峰值。反应条件相同时,170 μm SPS比40 μm SPS担载量更高,170 μm的PS更容易被氯磺酸改性。可见,氯磺酸的磺化具有良好的规律性,可以根据需要,通过控制氯磺酸的用量制备出不同磺化程度的磺化聚苯乙烯微球。
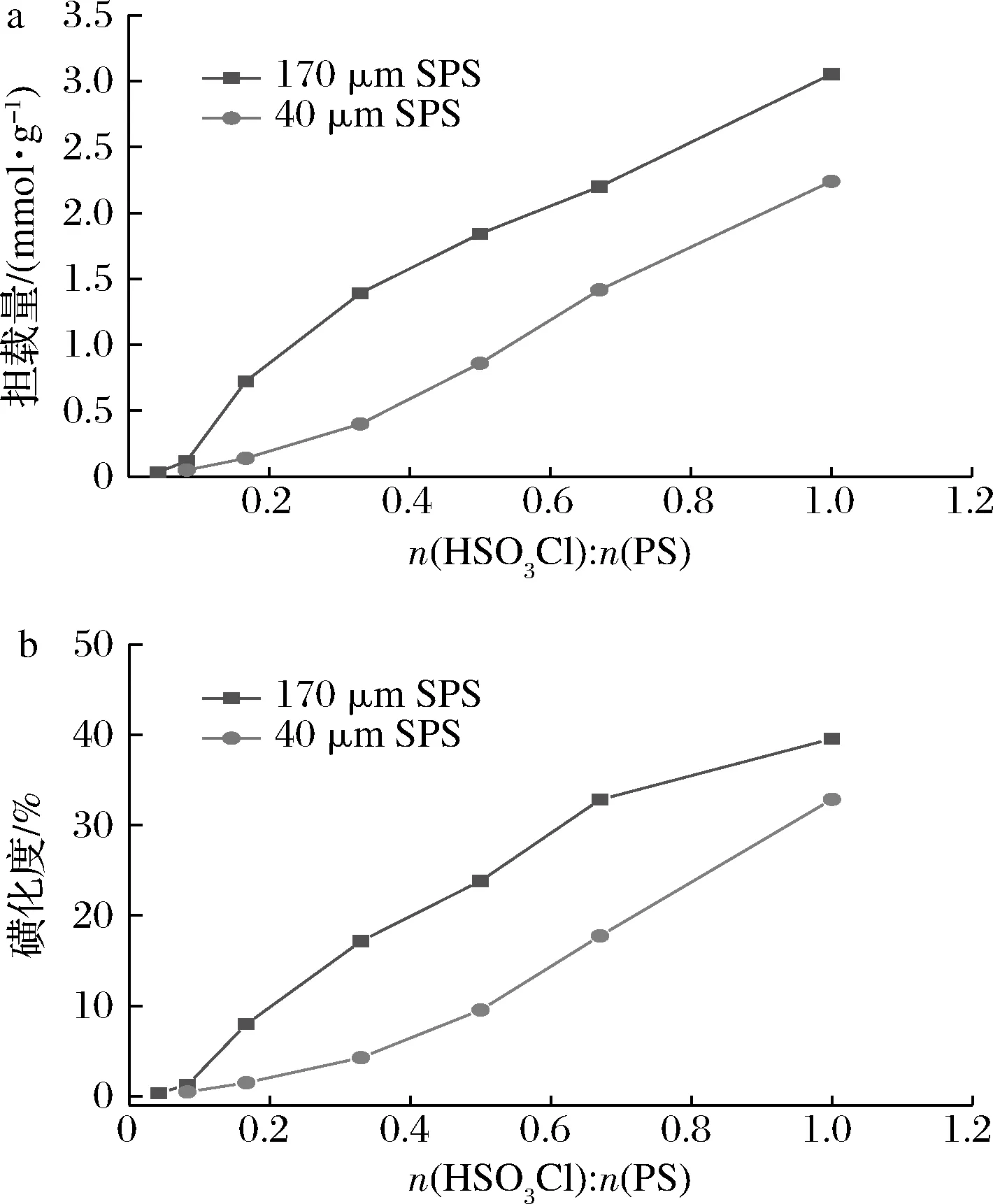
图5 氯磺酸用量对反应结果的影响Fig.5 Effect of sulfonating agent amount on reaction注:图中n为摩尔
2.1.6 材料的动态吸附能力
2.1.6.1 170 μm SPS填料的最佳担载量
按照1.6节的实验方法,依照实验因素水平表2、表4分别进行13次试验,以回收率为指标,各因素组合下3种β-受体激动剂及三聚氰胺回收率的结果分别如表6、表7所示。
(1)回归方程与方差分析
以克仑特罗、莱克多巴胺、沙丁胺醇、三聚氰胺回收率为响应值建立的二次回归方程分别如公式(3)、(4)、(5)、(6)所示:
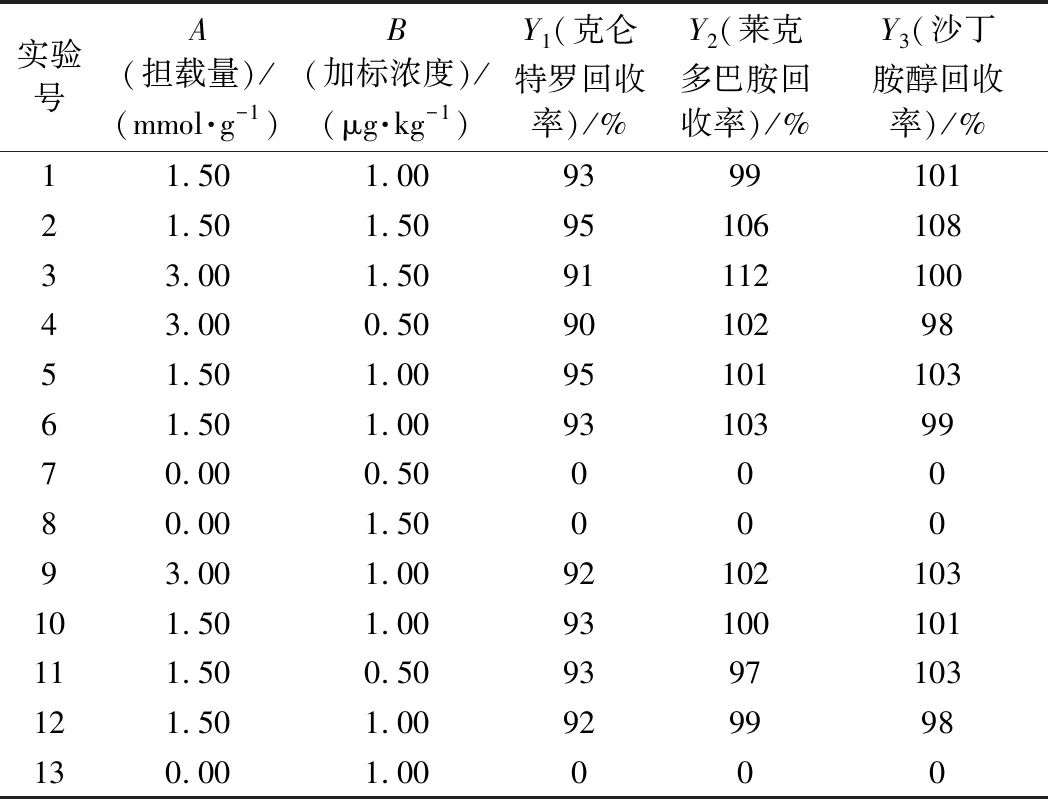
表6 β-受体激动剂的Miscellaneous试验设计方案与结果Table 6 Experimental design and results by Miscellaneous of β-agonists

表7 三聚氰胺的Miscellaneous试验设计方案与结果Table 7 Experimental design and results by Miscellaneous of melamine
Y1=-0.22+93.83A+0.08B+0.36AB-21.25A2+0.13B2
(3)
Y2=5.19+96.86A-14.19B+3.15AB-21.64A2+7.72B2
(4)
Y3=4.64+102.91A-12.85B+0.74AB-23.43A2+7.03B2
(5)
Y4=-6.32+30.47A+272.83B
(6)
方差分析表明:所得的回归方程显著程度非常高,Y1、Y2、Y3、Y4模型的F值分别为4 957.65、1 204.8、587.84、635.73,Y1、Y2、Y3的P值均<0.05,Y4的P值<0.000 1,表明该模型具有统计学意义。Y1、Y2、Y3、Y4的相关系数R2值分别为0.999 7、0.998 8、0.997 6、0.992 2,说明实测值与预测值拟合程度良好。失拟项值分别为0.373 2、0.339 6、0.075 5、0.668 1,均大于0.05,无失拟因素存在。因此该模型可以用于分析各因素对于3种β-受体激动剂及三聚氰胺回收率的影响,并优化预测满足检测条件的最佳担载量。
Y1、Y2、Y3、Y4模型中因素A(担载量)的P值均<0.000 1,因素B(加标浓度)的P值分别为0.278 1、0.008 2、0.349 3、0.059 5,因此,可得出各单因素对3种β-受体激动剂及三聚氰胺回收率影响的顺序为:A(担载量)>B(加标浓度)。
(2)各因素的交互作用分析
回归方程模拟二因素对3种β-受体激动剂及三聚氰胺的回收率影响见图6。

图6 170 μm SPS填料的Y=(A,B)的响应曲面图Fig.6 Responsive surface plot of Y=(A,B) for 170 μm SPS fillers
通过对三维响应曲面图的分析,可以更加直观地找出不同的变量因素制成的小柱对于3种β-受体激动剂回收率的影响。在图6中,曲面的高度越高,颜色越深,则代表着回收率越好。其中Y4的响应曲面较为平整,说明因素担载量与加标浓度之间无交互作用。可以看出,加标浓度对3种β-受体激动剂及三聚氰胺的回收率的影响甚微;而固相萃取填料的担载量对回收率起着重要的作用。随着填料担载量的增加,3种β-受体激动剂和三聚氰胺的回收率均逐渐增大,在1 mmol/g左右时,3种β-受体激动剂的回收率已达到80%,在2.7 mmol/g左右时三聚氰胺的回收率达到80%,已基本满足检测的要求,随后担载量继续增加,回收率变化不再明显。
(3)实验验证
为使3种β-受体激动剂的回收率均在80%~120%,目标值接近100%,利用本模型得出最佳担载量为1.38 mmol/g。此条件下,加标浓度为0.5 μg/kg时,模型对克仑特罗、莱克多巴胺、沙丁胺醇的回收率的预测值分别为89%、95%、98%。为了验证本模型预测值的准确性,进行回归模型的验证实验。根据实际制备得到的填料进行调整,选用担载量为1.39 mmol/g的SPS填料装柱,进行3次平行实验,取平均值。实际测得克仑特罗、莱克多巴胺、沙丁胺醇的回收率分别为88%、97%、97%,与预测结果接近,说明优化结果可信,对确定最佳担载量有实际指导作用。
为使三聚氰胺的回收率在80%~120%,目标值接近100%,利用模型得出最佳担载量为3 mmol/g。此条件下,加标浓度为0.01 mg/kg时,模型对三聚氰胺的回收率的预测值为87%。根据实际制备得到的填料进行调整,选用担载量为3.05 mmol/g的SPS填料装柱,进行3次平行实验,取平均值。实际测得三聚氰胺的回收率为88%,误差较小,说明优化结果可信,对确定最佳担载量有实际指导作用。
2.1.6.2 40 μm SPS填料的最佳担载量
实验及分析方法同2.1.6.1。为使3种β-受体激动剂的回收率均在80%~120%,目标值接近100%,利用本模型得出最佳担载量为0.81 mmol/g。此条件下,加标浓度为0.5 μg/kg时,实际测得克仑特罗、莱克多巴胺、沙丁胺醇的平均回收率分别为87%、82%、81%。为使三聚氰胺的回收率在80%~120%,目标值接近100%,利用模型得出最佳担载量为2 mmol/g。根据实际制备得到的填料进行调整,选用担载量为2.24 mmol/g的SPS填料装柱,此条件下,加标浓度为0.01 mg/kg时,实际测得三聚氰胺的回收率为83%,与预测值之间误差较小,说明优化结果可信,对确定最佳担载量有实际指导作用。
2.1.7 应用性能评价
将制备的填料的动态吸附能力与同类型Waters Oasis®MCX和安谱(CNW)MCX填料进行了比较,以提取猪肉中的β-受体激动剂和奶粉中的三聚氰胺。根据2.1.6的结果,在相同条件下,使用最佳担载量的填料对0.5 μg/kg加标猪肉样品进行SPE吸附,170 μm的填料的担载量选用1.39 mmol/g,40 μm的填料的担载量选用0.86 mmol/g。使用填料对0.01 mg/kg加标奶粉样品进行SPE吸附时,170 μm的填料的担载量选用3.05 mmol/g,40 μm的填料的担载量选用2.24 mmol/g。实验结果见图7,结果表明,自制的填料性能均达到国际水平,对3种β-受体激动剂的回收率为81%~97%,相对标准差(relative standard deviation,RSD)为3.22%~8.98%。对三聚氰胺的回收率为82%~88%,RSD在2.45%~2.97%。从RSD结果可以看出,自制的材料在3个平行实验中具有良好的平行性。其中,沙丁胺醇的提取平行性甚至优于CNW小柱。因此,本实验制备的SPS填料适合猪肉中3种β-受体激动剂药物和奶粉中三聚氰胺的富集和纯化,可以推广使用。Waters Oasis®MCX填料的平均粒径为60 μm,安谱(CNW)MCX填料的平均粒径为100 μm,2种商品化填料以及自制的40 μm填料在前处理实际样品时均因为粒径较小容易产生堵塞柱管、过柱时间长等问题,而本实验制备的170 μm填料则避免了这些问题,具有样品溶液过柱流畅、缩短固相萃取时间的优势。
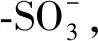
图7 自制填料与MCX填料的比较Fig.7 Comparison of the self-synthetic sorbents with MCX sorbents
3 结论
本研究制备了担载量可控的磺酸基阳离子固相萃取填料(磺化聚苯乙烯),并将其应用于β-受体激动剂和三聚氰胺的检测分析当中。以PS微球为载体材料,以氯磺酸为磺化剂,制备了磺化聚苯乙烯微球,并对其粒径和担载量进行优化。通过控制磺化剂用量,可实现在0~3.5 mmol/g内磺酸基担载量定量化可控。已有的磺酸基阳离子固相萃取填料大多采用传统的浓硫酸法进行磺化反应,且填料的粒径在60~100 μm,合成时间长、成本高,应用于前处理时易堵塞小柱,固相萃取时间长。本研究为填料的制备提供了一种新的思路,即使用氯磺酸作为磺化剂,制备更大粒径(170 μm)的填料。采用该方法制备填料,大粒径微球更易被磺酸基改性,且反应温度低,磺化剂用量少,反应时间短,产品性能质量可控,成本大大降低;在满足检测要求的条件下,前处理过程中使用该填料,不易堵塞小柱,能够缩短固相萃取时间。结合响应面软件,得到满足检测条件的填料最佳担载量。分析猪肉样品中β-受体激动剂时,170 μm的填料的担载量选用1.39 mmol/g;分析奶粉样品中三聚氰胺时,170 μm的填料的担载量选用3.05 mmol/g。本研究制备的最佳担载量填料对3种β-受体激动剂的回收率为88%~97%,相对标准偏差为5.23%~8.99%;对三聚氰胺的回收率为88%,相对标准偏差为2.97%。填料性能满足痕量检测的要求,可应用于实际食品样品中β-受体激动剂和三聚氰胺的浓缩富集。
