原发性肝癌患者术前营养相关指标与患者主观整体评估评分的相关性研究
2021-12-17李晨琪顾杨娟葛瑞良刘建伟曹翔
李晨琪,顾杨娟,葛瑞良,刘建伟,曹翔
原发性肝癌(以下简称肝癌)是指发生于肝细胞或肝内胆管上皮细胞的恶性肿瘤,是全球范围内癌症相关死亡的第4 大因素,且发病率位居世界第6[1]。 在我国,肝癌每年约导致38.3 万人死亡,占世界肝癌死亡病例数的一半以上[2]。 既往研究发现肝癌患者营养不良发生率高[3],而我国大部分肝癌患者合并有慢性肝炎或肝硬化等基础疾病,更增加了其营养不良的发生率[4]。 肝癌患者术前存在营养不良会增加术后发生感染、腹水、肝性脑病甚至死亡的风险[5⁃6]。 因此,术前应对肝癌患者进行常规营养评估,及时发现患者的营养不良状况并给予营养支持,从而改善其手术预后情况。
患者主观整体评估(patient⁃generated subjective global assessment, PG⁃SGA)量表是美国Ottey[7]专门为恶性肿瘤患者设计的营养状况评估方法,并被美国肠外肠内营养学会推荐为评估肿瘤患者营养状况的首要工具,且普遍应用于肿瘤患者中[8]。 本研究通过PG⁃SGA 量表对原发性肝癌患者进行术前营养评估,同时测定血液中葡萄糖(glucose, Glu)、视黄醇结合蛋白(retinol⁃binding protein,RBP)、前白蛋白(prealbumin, PA)、血红蛋白(hemoglobin, HGB)、肌酐(creatinine, Cr)以及体质量指数(body mass in⁃dex,BMI)水平,并进行比较分析,探讨其相关性以及能够反映肝癌患者术前营养不良的相关指标的诊断价值,旨在为准确评估肝癌患者营养状况及相关干预措施的制定提供依据。
1 对象与方法
1.1 研究对象
本研究为一项前瞻性、观察性单中心研究。 纳入2016 年12 月至2017 年3 月于海军军医大学附属东方肝胆外科医院接受治疗的120 例肝癌患者作为研究对象,其中男性107 例(89.2%),女性13 例(10.8%);年龄(51.8 ±9.7)岁,范围22 ~72 岁。纳入标准:(1)术前临床诊断为肝癌并得到术后病理证实;(2)肝癌系初发且未接受过任何抗肿瘤治疗;(3)年龄≥18 岁;(4)无交流障碍,能准确回答问题,能自主站立,且配合本次研究。 排除标准:(1)术前合并其他部位肿瘤而导致主要器官受损;(2)因自身原因没有接受治疗即出院;(3)血液肌酐水平≥100 μmoI/L;(4)术前腹部B 超提示存在腹水。本研究经过患者及家属知情同意并签署同意书,并通过医院伦理委员会批准。
1.2 研究方法
1.2.1 PG⁃SGA 营养评估 本研究采用PG⁃SGA 量表对每个纳入研究的患者在入院24 h 内完成术前营养评估[9]。 PG⁃SGA 评分由2 个部分组成:第一部分为患者自评表,包括体质量、进食情况、症状以及活动和身体功能;第二部分为医务人员评估表,包括疾病的相关诊断、应激状态及体格检查。 2 个部分相加后的最终得分被视为营养评估的总得分,总得分越高则说明患者营养不良情况越严重。 得分≥4 分被评定为营养不良[10]。
1.2.2 评估质量控制 为了防止产生偏倚,本研究由2 名专业的营养医师对患者进行营养评估。 在评估前,营养医师进行培训并统一评分标准,具体操作方法参考石汉平等[10]编撰的《PG⁃SGA 肿瘤患者营养状况评估操作手册》,每个病例评估时间不得少于10 min。若出现主观不确定性的打分,则记录在评估量表空白处,并由2 名营养医师共同讨论后确定最终得分。
1.2.3 血液生化指标检测 患者入院后次日清晨,在未接受任何药物治疗的基础上,空腹抽取静脉血,检测Glu、RBP、PA、HGB、Cr 水平。
1.2.4 人体测量学指标检测 患者统一使用经校准后的秤测量身高、体质量。 患者入院后第2 天清晨空腹并排空大、小便,穿着统一的单薄病员服、脱鞋测量,身高读数精确到0.5 cm,体质量读数精确到0.5 kg。 BMI 的计算方法为体质量(kg)/[身高2(m2)]。 1 ~3 个月体质量变化及2 周内饮食情况均经过反复询问患者及其亲属所得。
1.3 统计学处理
使用SPSS 23.0 软件进行统计学分析。 计量资料采用均数± 标准差(±s)表示,组间比较采用t检验;计数资料采用率表示,组间比较采用连续性修正的χ2检验;双变量相关性分析,采用Pearson 相关检验;采用受试者工作特征(receiver operating characteristic, ROC)曲线判断检测指标血液RBP、PA、Cr、BMI 对PG⁃SGA 评分判定营养不良的诊断价值。P<0.05 表示差异有统计学意义。
2 结果
2.1 PG⁃SGA 评分情况
分别对每位患者的PG⁃SGA 评分进行统计,其中最低分为1 分,最高分为22 分,得分为(4. 3 ±3.3)分。 并将其按得分情况分为非营养不良组(PG⁃SGA 得分<4 分)和营养不良组(PG⁃SGA 得分≥4 分)。 2 组患者的性别(χ2=0.218,P=0.871)和年龄(t=-1.407,P=0.162)比较差异均无统计学意义。 见表1。

表1 120 例原发性肝癌患者PG⁃SGA 评分分组情况
2.2 血液生化指标及人体测量学指标的比较
通过比较非营养不良组与营养不良组各项营养相关指标的差异发现,营养不良组患者的BMI 以及血液RBP、PA、Cr 水平均显著低于非营养不良组,差异有统计学意义(P<0.001);而2 组患者的血液Glu 和HGB 水平比较差异均无统计学意义(P>0.05)。 见表2。
表2 不同营养状况的原发性肝癌患者血液生化指标及人体测量学指标均值的比较(±s)
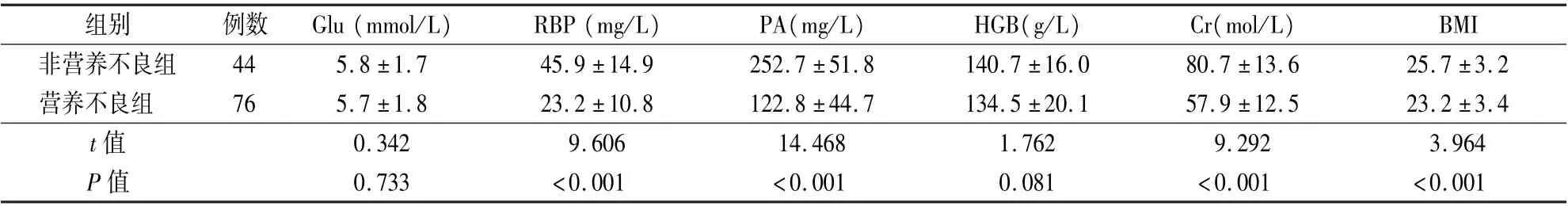
表2 不同营养状况的原发性肝癌患者血液生化指标及人体测量学指标均值的比较(±s)
注:Glu 为葡萄糖,RBP 为视黄醇结合蛋白,PA 为前白蛋白,HGB 为血红蛋白,Cr 为肌酐,BMI 为体质量指数
组别例数Glu (mmol/L)RBP (mg/L)PA(mg/L)HGB(g/L)Cr(mol/L)BMI非营养不良组445.8±1.745.9±14.9252.7±51.8140.7±16.080.7±13.625.7±3.2营养不良组 765.7±1.823.2±10.8122.8±44.7134.5±20.157.9±12.523.2±3.4 t 值0.3429.60614.4681.7629.2923.964 P 值0.733<0.001<0.0010.081<0.001<0.001
2.3 PG⁃SGA 评分与营养相关指标的相关性研究
通过绘制散点图,发现肝癌患者术前PG⁃SGA总得分与BMI 以及血液RBP、PA、Cr 之间存在线性相关趋势。 见图1 ~4。 进一步采用Pearson 相关检验得出,原发性肝癌患者术前PG⁃SGA 评分与RBP(r=-0. 526,P<0. 001)、PA(r=-0. 636,P<0.001)、Cr(r=-0. 612,P<0. 001)及BMI(r=-0.219,P=0.016)均存在负相关关系。
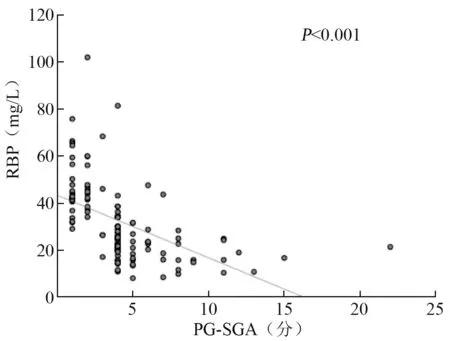
图1 RBP 与PG⁃SGA 评分的相关性散点图
2.4 营养相关指标对PG⁃SGA 评分分组预测诊断结果
为判断BMI 以及血液RBP、PA、Cr 水平对肝癌患者术前营养不良的诊断价值,将其与PG⁃SGA 评分分组做ROC 诊断曲线,结果显示,BMI 及血液RBP、PA、Cr 对应的曲线下面积分别为0.925(P<0.001)、0. 979(P<0. 001)、0. 906(P<0. 001)、0.701(P<0.001),提示以上指标均可以对PG⁃SGA评分分组进行预测诊断。 当BMI 以及血液RBP、PA、Cr 水平临界值分别为31.35 mg/L、189.5 mg/L、68.50 μmol/L 及23.16 时,即出现血液RBP≤31.35 mg/L、PA≤189.5 mg/L、Cr≤68.50 μmol/L 或BMI≤23.16 其中之一时,可诊断为存在营养不良。 见表3、图5。
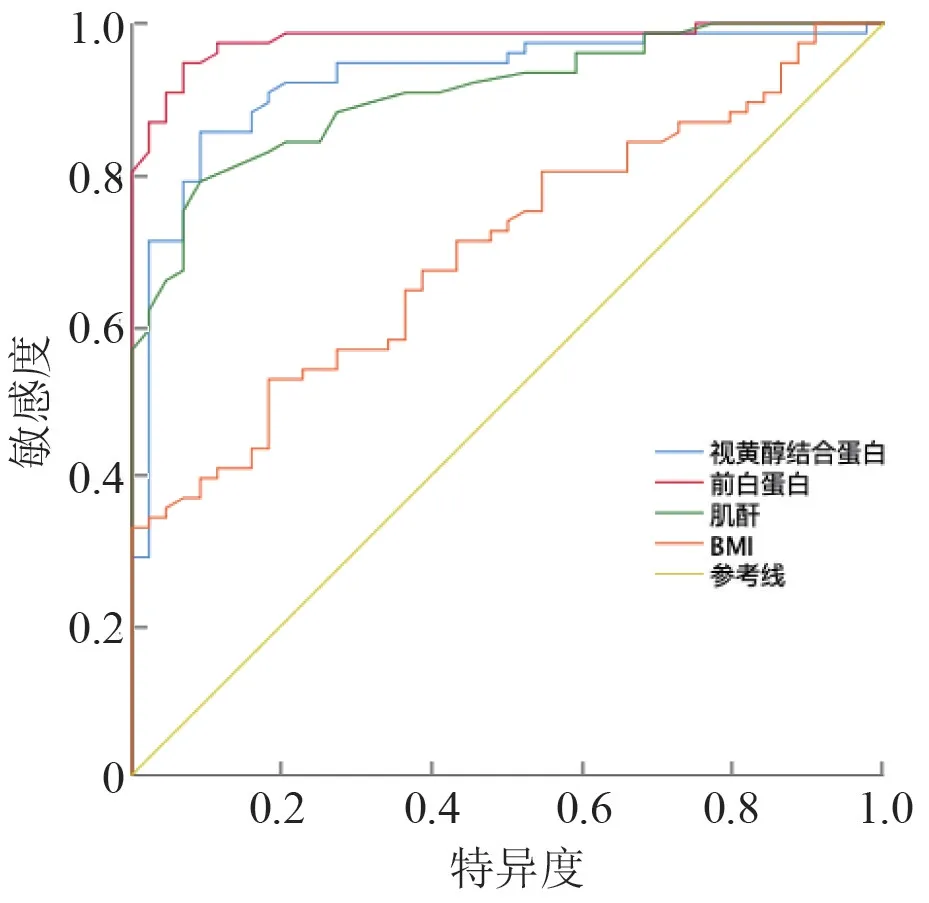
图5 各项检测指标对PG⁃SGA 评分分组的ROC 特征

表3 各项指标对PG⁃SGA 评分分组预测诊断结果
3 讨论
2015 年欧洲临床营养和代谢学会(European So⁃ciety for Clinical Nutrition and Metabolism, ESPEN)把营养不良的定义局限于能量和宏量营养素(蛋白质) 不足[11],而营养不良在肝癌患者中较为常见[12]。 本研究纳入的120 例患者中, 男性占89.2%,这是由于部分男性有嗜酒等不良生活习惯及性激素的诱因而导致肝癌的发病率远高于女性[13]。 本研究通过采用PG⁃SGA 量表对120 例肝癌患者术前进行营养评估,结果显示PG⁃SGA 得分0 ~3 分区间共有44 例,得分≥4 分共有76 人(63.3%),此结果与Ni 等[14]的研究一致,表明肝癌患者术前营养不良发生率高,应高度重视对营养不良患者的早期筛查并及时进行营养干预。
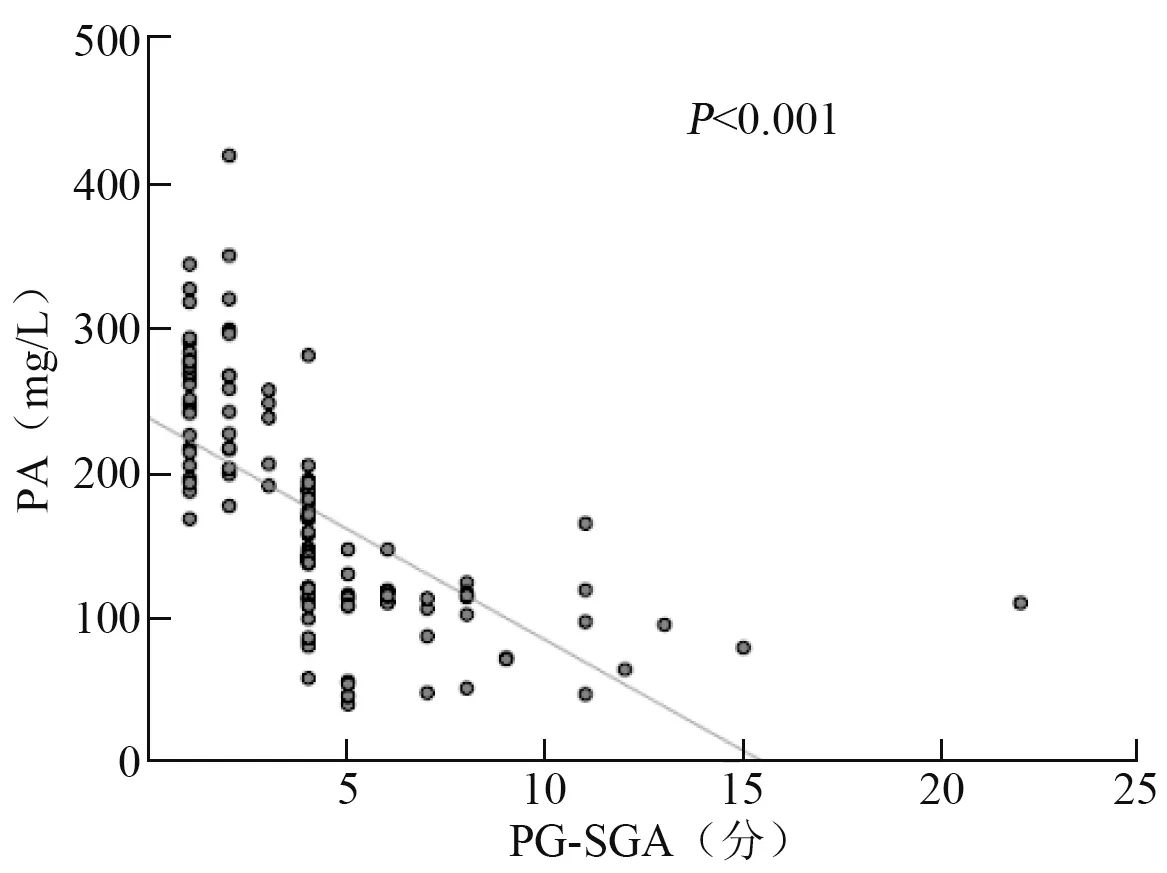
图2 PA 与PG⁃SGA 评分的相关性散点图

图3 Cr 与PG⁃SGA 评分的相关性散点图
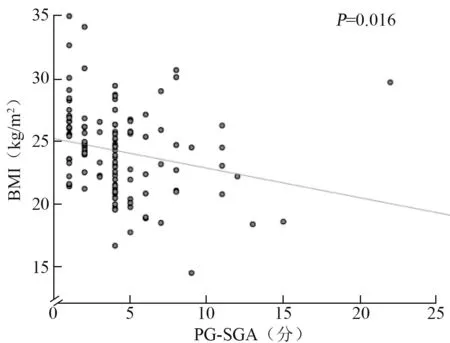
图4 BMI 与PG⁃SGA 评分的相关性散点图
BMI 以及血液RBP、PA、Cr 是传统的营养相关指标。 RBP 和PA 均属于半衰期较短的快速转化蛋白[15],其中RBP 的半衰期约为12 h[16],PA 的半衰期约为1.9 d[17],其水平变化能够灵敏地反映出肝脏的合成功能。 在肾功能正常的前提下,当肝脏功能受损的患者存在蛋白质营养不良时,体内蛋白质的供给与消耗出现失衡,蛋白质储备减少,从而导致Cr 水平的下降[18]。 体质量是能够体现肿瘤患者营养状况的一项重要指标[19],而由身高和体质量得出的BMI 被认定为最常用的营养不良筛查方法之一[11]。 本研究对2 组患者的营养相关指标进行比较发现,营养不良组患者的BMI 以及血液Glu、RBP、PA、HGB、Cr 水平均低于非营养不良组,提示这些检测指标可能在原发性肝癌患者发生营养不良的过程中发生了变化,但血液Glu 和HGB 水平在营养不良组和非营养不良组之间的差异无统计学意义。
本研究进一步将2 组有显著性差异的4 项检测指标(RBP、PA、Cr、BMI)与PG⁃SGA 评分进行Pear⁃son 检验,结果显示其均与评分呈负相关,BMI 以及血液RBP、PA、Cr 水平越低,其PG⁃SGA 得分越高,营养状况越差,该结果与既往研究结果基本一致[15⁃17,20]。 该结果表明,结合BMI 以及血液RBP、PA、Cr 的测定能够更好地识别肝癌患者的营养不良状况,及时进行术前营养干预。
为了进一步判断诊断价值,本研究对4 项检测指标绘制ROC 曲线,结果发现,当血液RBP≤31.35 mg/L、PA≤189.5 mg/L、Cr≤68.50 μmol/L 或BMI≤23.16 时,可能存在营养不良。 对应的曲线下面积提示4 项检测指标中血液PA 水平对肝癌患者营养不良诊断价值最优,其次为RBP,而BMI 诊断价值最差,其原因可能为肝癌患者合并腹水会干扰体质量的数据,从而导致BMI 与营养不良的不一致性[21]。 因此,本研究排除了术前腹部B 超提示存在腹水的患者。 但由于肝癌患者机体组织的受损存在不平衡的可能性,部分患者即使已经存在严重的营养不良但也无体质量明显下降[22⁃23]。
综上所述,肝癌患者术前有较高的营养不良发生率。 本研究发现BMI 以及血液RBP、PA、Cr 水平与PG⁃SGA 存在负相关,对原发性肝癌患者术前进行营养评估时联合上述4 项检测指标可以提高预测不良结局的水平,降低患者因营养问题而导致不良结局的风险,值得引起临床医生重视。 但由于本研究收集的样本量较少,结果有局限性,需要增加样本数量后做进一步证实。
