焚烧条件对模拟城市生活垃圾焚烧污染物二噁英的影响
2021-12-14张楷文张海军高肖汉吕雪川
张楷文,刘 旭,,张海军,高肖汉,吕雪川,张 磊,*,王 胜,*
(1.辽宁石油化工大学 石油化工学院,辽宁 抚顺 113001;2.中国科学院大连化学物理研究所 洁净能源国家实验室,辽宁 大连 116023)
中国国民经济的迅猛发展和城市化程度的不断加深,城市生活垃圾的数量逐年增长[1]。目前,人均生活垃圾产生量达到1.2 kg/d 左右,预计到2025年,这一数字将进一步上升到1.42 kg/d,因此,生活垃圾的无害化处理已经成为城市化进程中的重要任务[2]。生活垃圾的无害化处理一般采用填埋法和焚烧法[3]。焚烧法相比填埋法能更好地实现生活垃圾减量,再利用和无害化[4]。由于城市生活垃圾组成的复杂性,在焚烧过程中会产生重金属污染物、气态污染物、二噁英污染物等二次污染物。其中,二噁英(PCDD/Fs)已被证实是毒性最强、严重危害人类健康的一类种类繁多的芳烃类化合物[5]。近年来,随着人们对环境保护的高度重视,如何抑制垃圾焚烧过程中PCDD/Fs 的生成已成为焚烧法处理城市生活垃圾的关键性问题。研究表明,PCDD/Fs 在垃圾焚烧过程中生成的化学路径有两个:一是高温500–800 ℃下气相生成;二是低温200–400 ℃异相生成[6,7]。当前实现垃圾焚烧过程二噁英控制的方法主要有三种:一是通过垃圾分类,减少城市生活垃圾中Cu、Fe 等金属的存在,从源头减少Cu、Fe 对二噁英生成反应的催化促进作用[8,9]。二是改变燃烧条件。生活垃圾中富含碳元素,其不完全燃烧会产生大量苯的同系物及不饱和烃,这些物质经过氯代化反应会生成二噁英前驱体氯苯、氯酚、含氯烃类等。Christelle 等[10]等使用低浓度氯酚研究二噁英的形成,研究发现水的存在明显抑制了PCDD/Fs 的形成。Yu 等[11]利用TiO2基V2O5/WO3催化剂低温氧化PCDD/Fs,同时探究了含水量对PCDD/Fs 破坏率的影响。研究发现,适量水蒸气的引入(3%)会促进脱氯,同时产生羟基自由基,从而增加了PCDD/Fs 的破坏率。当引入8%的水蒸气反而促使PCDD/Fs 的破坏率低于无水体系。三是添加抑制剂。添加碱性物质或含硫、氮化合物作为二噁英催化抑制剂,可以有效抑制二噁英的生成[12]。
本实验采用在焚烧过程中加入廉价的镍基催化剂、水以此改变焚烧条件,进一步探究焚烧条件对生活垃圾焚烧污染物二噁英的影响。
1 实验部分
1.1 模拟生活垃圾焚烧实验
模拟生活垃圾焚烧实验在自行搭建的固定床反应器中进行。反应管采用定制的薄壁钢管(刚玉内衬)。用K 型镍铬-镍硅热电偶分别测量反应管中心(反应温度)和反应管出口的温度变化,实验装置图见图1。
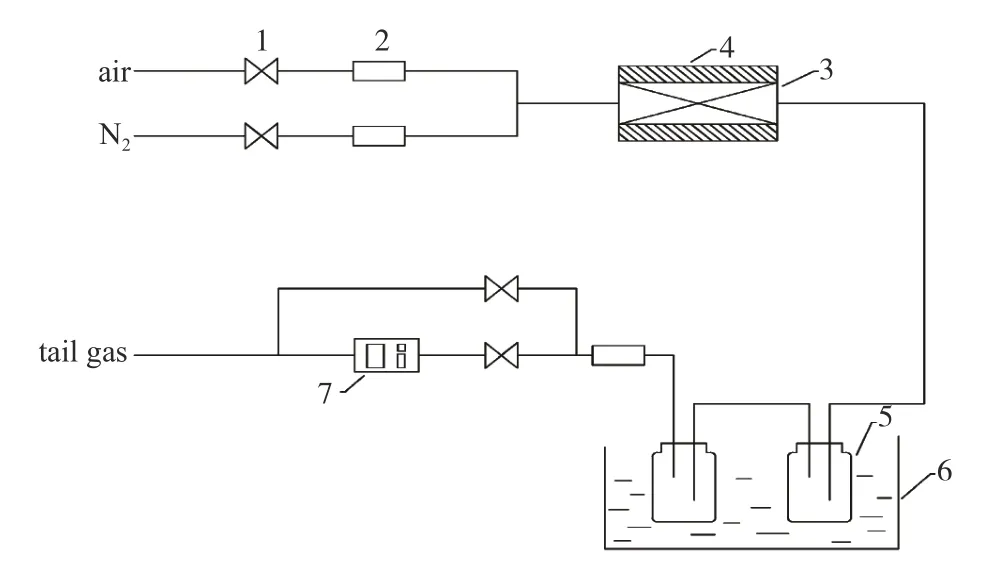
图1 实验装置示意图Figure 1 Schematic diagram of the experimental setup
通过前期对所在城市生活垃圾进行取样分析,自制出与实际城市生活垃圾具有相同碳元素、氢元素和氯元素含量的模拟城市垃圾(各组分质量分数分别为木屑78.6%、聚乙烯15.4%、聚氯乙烯6%)。取模拟城市生活垃圾50 g 放入反应管中迅速将其置入管式电阻炉中(炉温700 ℃),进口空气流量2.5 L/min。反应尾气用装有70 mL 无水乙醇的吸收罐吸收尾气中的有机物质及二噁英,将吸收了有机物的液体称为吸收液。为了避免乙醇和有机物夹带,用装有100 mL 水的吸收罐进一步吸收挥发的乙醇;然后用冷凝罐冷凝过饱和的水和乙醇,经分液后的气体称为尾气。尾气经体积流量计后,进入烟气分析仪(德国IMR4000)分析尾气中各气体组分浓度。
分别考察无添加、加入15 g 工业Ni/Al2O3催化剂、加入10 mL 水、加入10 mL 水和15 g 工业Ni/Al2O3催化剂对反应温度、尾气流量及各组分浓度、各类二噁英浓度和毒性的影响。四组实验分别依次编号为1(No added)、2(Ni/Al2O3)、3(H2O)和4(H2O-Ni/Al2O3)。本实验涉及到催化剂用量和水的添加量,这是在课题组前期探索工作基础上得到的。
1.2 吸收液中二噁英分析方法
首先在吸收液中滴加二噁英提取内标10 μL,用氮吹仪浓缩至溶液不再减少。后加入20−30 mL甲苯(分析纯)超声20 min。用旋蒸仪将溶液浓缩至1 mL 左右后加入浓硫酸(优级纯)4−6 mL,120 r/min震荡3 h。随后用20−30 mL 正己烷(农残级)活化硅胶柱(由上至下依次填装无水硫酸钠6 g,硅胶0.9 g,碱性硅胶3 g,硅胶0.9 g,44%酸化硅胶6 g,硅胶0.9 g,硝酸银硅胶3 g,无水硫酸钠10 g),活化后将样品移入层析柱中,保持流出速率1 滴/秒。流出液经旋蒸至3 mL 左右后过氧化铝柱(由上至下依次填装无水硫酸钠2 g,氧化铝10 g,无水硫酸钠2 g,活化步骤同上),保持流出速率1 滴/秒。流出液经旋蒸仪浓缩至1 mL 左右,氮吹浓缩至静干,最后加入提取内标定容至10 μL。
分析液采用同位素稀释-高分辨气相色谱-高分辨质谱联用法(HRGC/HRMS),分别分析样品中的多氯联苯、多氯萘、二噁英类物质。
分析仪器采用Waters Autospec Premier GC/MS高分辨气相色谱质谱联用仪。色谱:Rtx5MS 色谱柱,进样温度280 ℃,进样体积1 μL;质谱:电子轰击离子源(EI),温度260 ℃,选择性离子检测(SIM)。
1.3 吸收液中有机物分析方法
取吸收液50 mL 用氮吹仪浓缩至溶液不再减少。加入15 mL 二氯甲烷,置于冰浴中超声20 min,静置取上清液;重复3 次得到萃取液。将萃取液在30 ℃下旋转蒸发至3 mL 左右,经过滤膜、凝胶净化系统(GPC),收集21−50 min 的流出组分;将其在30 ℃下旋转蒸发至1 mL 左右,再装样于无水硫酸钠和硅胶填装的层析柱(由下而上依次装填3 g 无水硫酸钠、10 g 硅胶、5 g 无水硫酸钠),用60 mL 正己烷/二氯甲烷(体积比=1∶1)混合液淋洗,收集流出液并将其由旋蒸仪浓缩至10 mL左右;加入3 g 铜粉超声10 min,取上清液,氮吹浓缩至近干,用1 mL 正己烷溶解定容,经0.22 μm 有机滤膜过滤后得到分析液。
分析仪器采用赛默飞TraceUltraDSQ 气相色谱-质谱联用仪。色谱:J&KDB-5ms 色谱柱,进样温度260 ℃,进样量1 μL;质谱:电子轰击离子(EI)源,温度230 ℃,全扫描检测。
1.4 二噁英毒性当量计算
二噁英的毒性当量计算按公式(1)计算,其中某种二噁英的毒性当量等于其质量浓度与其毒性当量因子的乘积[13]。
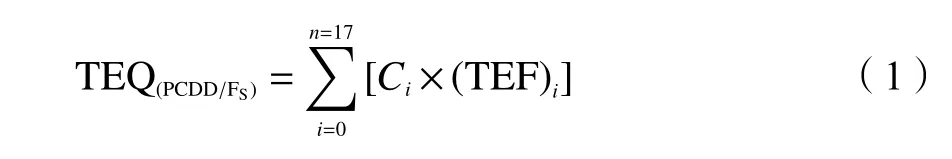
式中,Ci—第i种2,3,7,8-氯取代二噁英的质量浓度,ng/L;
(TEF)i—第i种2,3,7,8-氯取代二噁英毒性当量因子。
1.5 PCDDs/PCDFs 抑制率计算
PCDDs/PCDFs 抑制率计算按公式(2)计算,其中某多氯代二苯并对二噁英(PCDDs)或多氯代二苯并呋喃(PCDFs)的抑制率等于实验1 所测PCDDs或PCDFs 与实验2、3、4 中的质量浓度差与实验1 所测其质量浓度的比值。
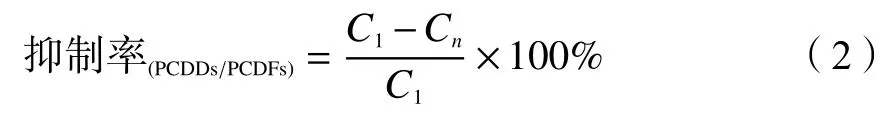
Cn—实验n(n=2、3、4)所测PCDDs/PCDFs 质量浓度,pg/L;
C1—实验1 所测PCDDs/PCDFs 质量浓度,pg/L。
2 结果与讨论
2.1 反应温度分析
图2 为反应温度随反应时间的变化。实验1 和实验2 分别经610 和721 s 达到700 ℃,实验3 和实验4 经834 s 达到700 ℃。实验3 和实验4 反应升温速率低于实验1 和实验2,这是由于水蒸发需要吸收热量。实验3 反应温度最终稳定温度高于其他三组实验15 ℃左右,说明水的加入会影响焚烧过程热效应。
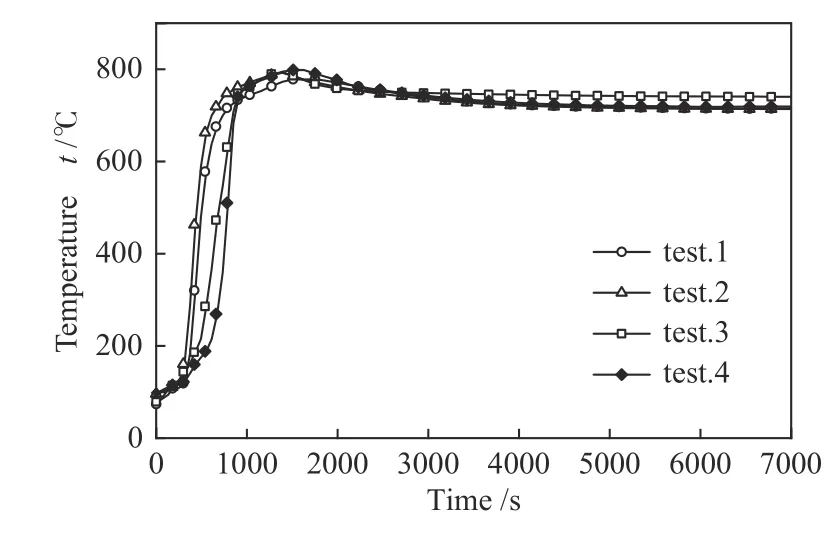
图2 反应温度随反应时间的变化Figure 2 Temperature change of the reaction
图3 为反应管出口温度随反应时间的变化。四组实验反应管出口温度升温速率基本相接近。3500 s 后四组实验出口温度趋于稳定,实验1 反应管出口温度高于其他三组实验15 ℃左右,说明焚烧条件的改变对焚烧反应燃烧后区域的温度范围造成影响,从而影响尾气中气相有机物的组成,减少二噁英前驱物的生成。
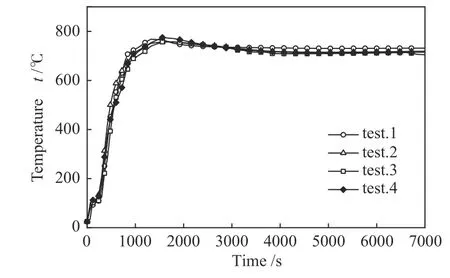
图3 反应管出口温度随反应时间的变化Figure 3 Temperature change of reaction tube outlet
2.2 焚烧过程尾气流量分析
图4 为模拟垃圾焚烧过程中尾气流量随反应时间的变化。在实验1 中尾气流量经468 s 达到峰值4.04 L/s,焚烧1070 s 尾气流量趋于平稳,而在焚烧2375 s 时出现一个明显的流量突增。在实验2中尾气流量开始上升至93 s 时出现流量突减,并在190 s 出现上升过程的最低点后继续增加,于256 s 达到流量峰值5.47 L/s,焚烧780 s 尾气流量趋于平稳,在焚烧3662 s 时出现一个明显的流量突增。在实验3 中尾气流量经471 s 达到峰值4.90 L/s,焚烧900 s 尾气流量趋于平稳。在实验4 中尾气流量开始上升至170 s 时出现流量突减,并在250 s 出现上升过程的最低点后继续增加,于304 s 达到流量峰值5.64 L/s。
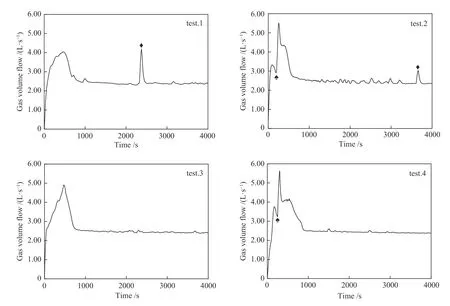
图4 焚烧反应过程中的尾气流量随反应时间的变化Figure 4 Exhaust gas flow during incineration reaction
实验2 和实验4 出现上升过程的最低点可能是由于反应受传热控制,导致了尾气流量下降。实验1 和实验2 出现两个气量突增过程,而实验3 和实验4 无气量突增,这可能由于水的加入使模拟垃圾床层更紧凑不易塌陷。在实验4 中,尾气流量峰值相比其他三组实验均有所增加,这是由于加入水或催化剂可以促进大分子有机物向小分子有机物转化,小分子有机物的换算系数高于大分子有机物的换算系数,从而造成尾气流量的增加[14]。
2.3 焚烧尾气中各气体组分的含量变化
图5 是尾气中CO 摩尔分数随反应时间的变化。在四组实验中CO 均在37 s 时开始产生,此时四组实验反应管内温度均低于100 ℃,说明此时管内垃圾发生不完全燃烧反应。随着焚烧时间的延长,CO 摩尔分数迅速延长,分别在246、280、228、210 s 时达到峰值。由CO 的增加可以间接表明从头合成过程中PCDD/Fs 的形成[15,16],此时反应出口温度在200 ℃以上,满足二噁英从头合成反应发生在燃烧后低温区域温度(200–400 ℃)[17]。当反应温度高于200 ℃,CO 摩尔分数也逐渐降低,这是由于反应管内部分物料由不完全燃烧反应逐步转变为完全燃烧反应。
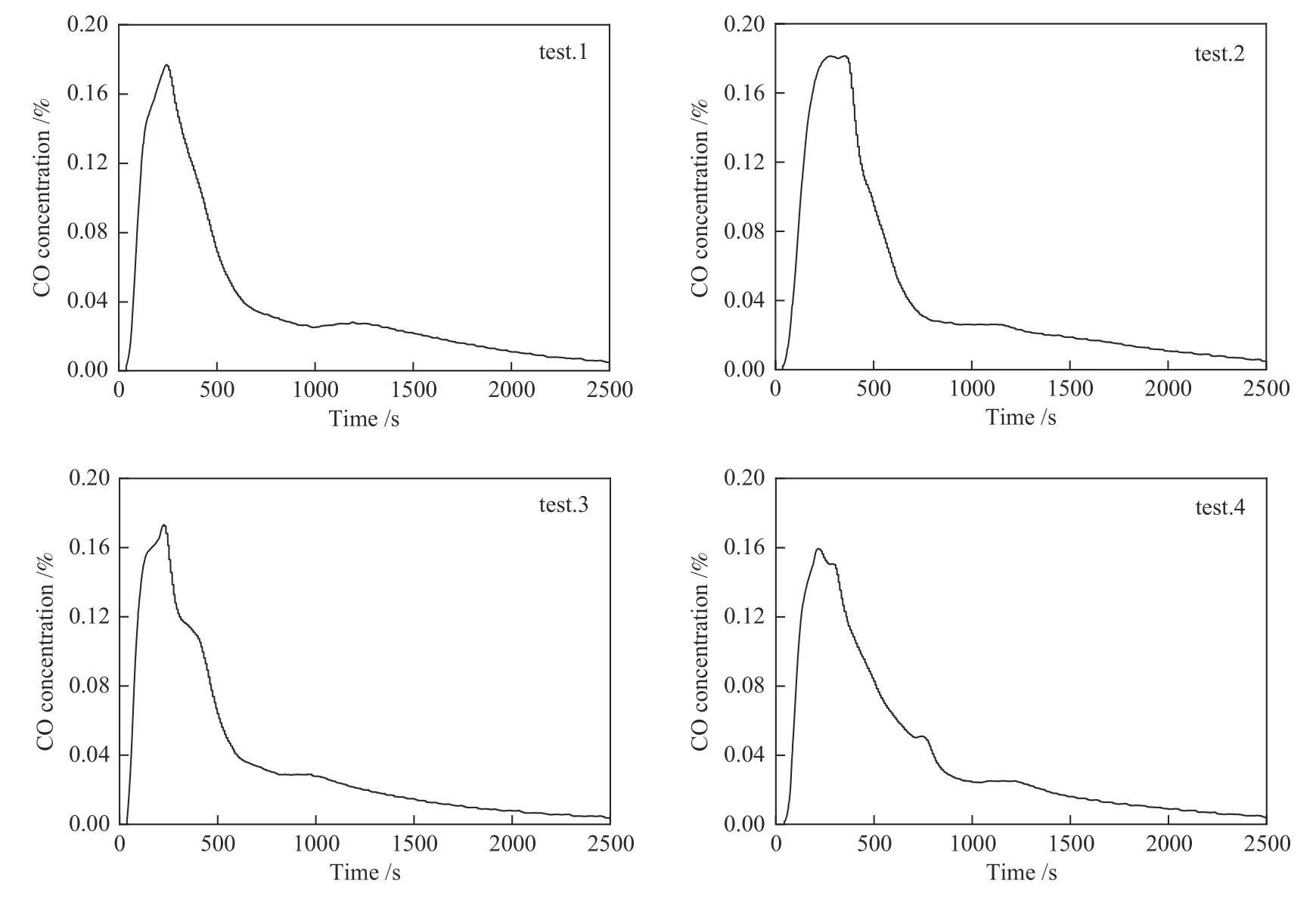
图5 尾气中CO 摩尔分数随反应时间的变化Figure 5 Change of CO concentration in exhaust gas
图6 为尾气中H2摩尔分数随反应时间的变化。开始反应665 s 后H2被检测出,四组实验H2摩尔分数均在3.01×10−2左右。无 论是水还是催化剂的加入对H2的生成都起促进作用,其中水和催化剂共同作用效果更明显。随着H2摩尔分数的升高,实验1、2 和3 的CO 摩尔分数有所降低,而实验4 在705 s 时CO 摩尔分数有显著升高。说明实验1、2 和3 发生的是烃类裂解脱氢的过程,而不是气化过程[18],而实验4 在焚烧反应过程中同时发生烃类裂解脱氢和气化过程。在H2生成的同时CO2的摩尔分数在逐渐降低,在H2消失后CO2摩尔分数又增加,说明烃类在催化剂和水共存的燃烧条件下裂解脱氢反应优先于气化过程。
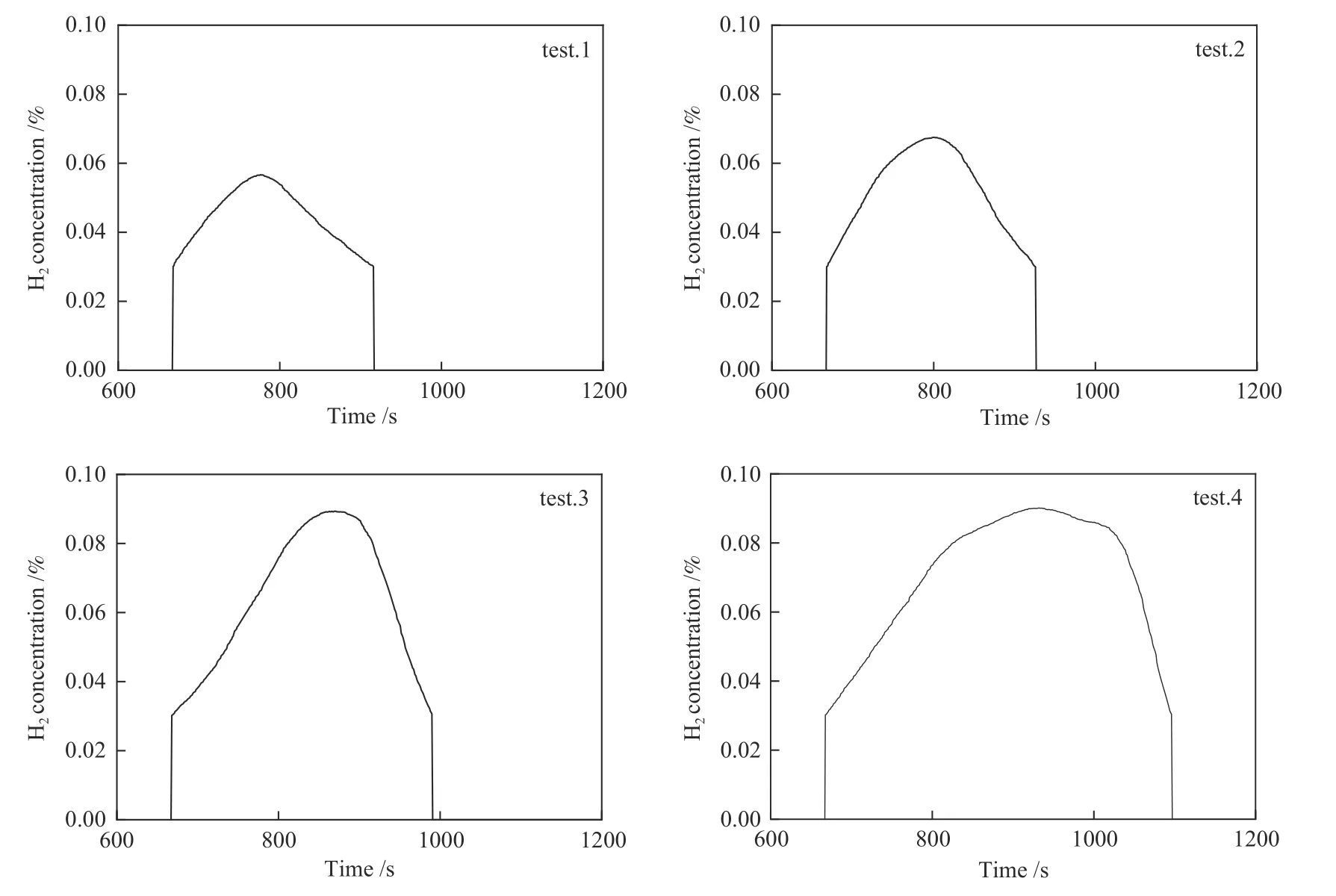
图6 尾气中H2摩尔分数随反应时间的变化Figure 6 Change of H2 concentration in exhaust gas
图7 为尾气中烃类摩尔分数随反应时间的变化。由于垃圾组分中含碳量高,热解过程中生成的烃类复杂,以总烃摩尔分数计。烃类在398 s 时开始生成,在700 s 后摩尔分数逐渐降低。无论是实验2 中单独加入催化剂,还是实验3 单独加入水,对烃类的生成影响均不大。但在实验4 中尾气烃类峰值低于其他三组,可能是因为水提供了充足的氢源,催化剂促进了多碳烃类有机物的催化裂解反应[19],两者协同作用下使得大分子烃类裂解生成小分子烃类。由图10、图11 含碳有机物的分布规律可进一步证明焚烧过程中大分子烃类不断地向小分子烃类转化。
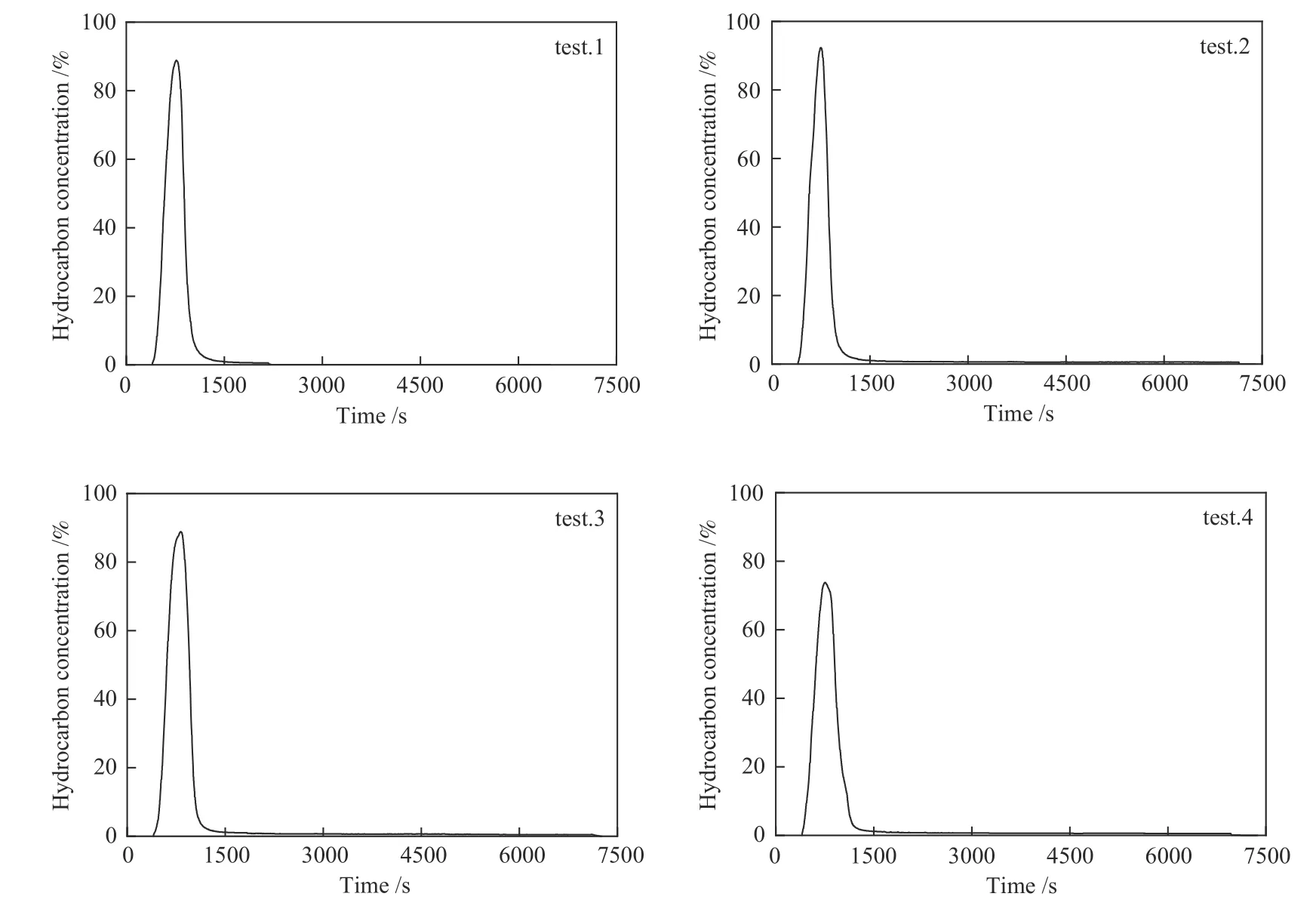
图7 尾气中烃类摩尔分数随反应时间的变化Figure 7 Change of hydrocarbon concentration in exhaust gas
2.4 吸收液二噁英分析
表1 为吸收液中多氯代苯并对二噁英和多氯代苯并呋喃质量浓度。由表1 可以看出,在不同焚烧条件下均生成了17 种二噁英同系物,并且在垃圾焚烧过程中水、镍基催化剂的加入对不同的多氯代苯并对二噁英和多氯代苯并呋喃的抑制作用不尽相同。
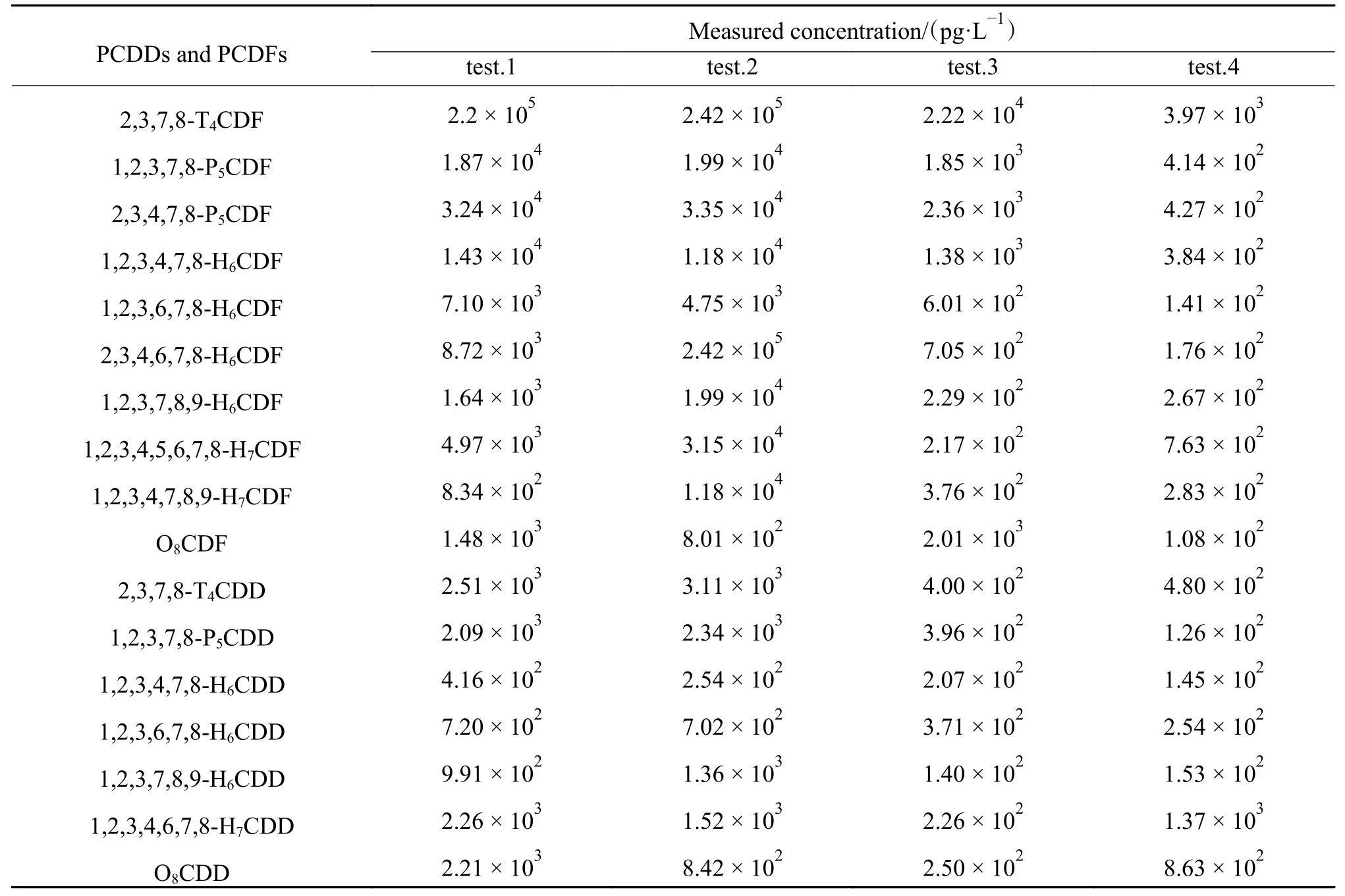
表1 多氯代二苯并对二噁英和多氯代二苯并呋喃质量浓度表Table 1 PCDDs and PCDFs concentration distribution
表2 为不同燃烧条件下吸收液中多氯代苯并对二噁英和多氯代苯并呋喃的抑制情况。由表2可以看出,在实验2 中催化剂的加入对四氯代苯并对二噁英和四氯代苯并呋喃、五氯代苯并对二噁英和五氯代苯并呋喃起促进生成作用。在实验3 中水的加入虽然促进了八氯代苯并对二噁英的生成,但对其他多氯代苯并对二噁英和多氯代苯并呋喃的生成均有很好的抑制作用。在实验4 中水和催化剂共同作用对检测的17 种多氯代苯并对二噁英和多氯代苯并呋喃的生成均有抑制作用,二噁英总抑制率可达80.7%,多氯代二苯并对二噁英平均抑制率可达到91.51%,其中,2,3,4,7,8-P5CDF 抑制率高达98.7%。对多氯代二苯并呋喃平均抑制率可达到69.9%,其中,对1,2,3,7,8-P5CDD 抑制率高达94.0%。
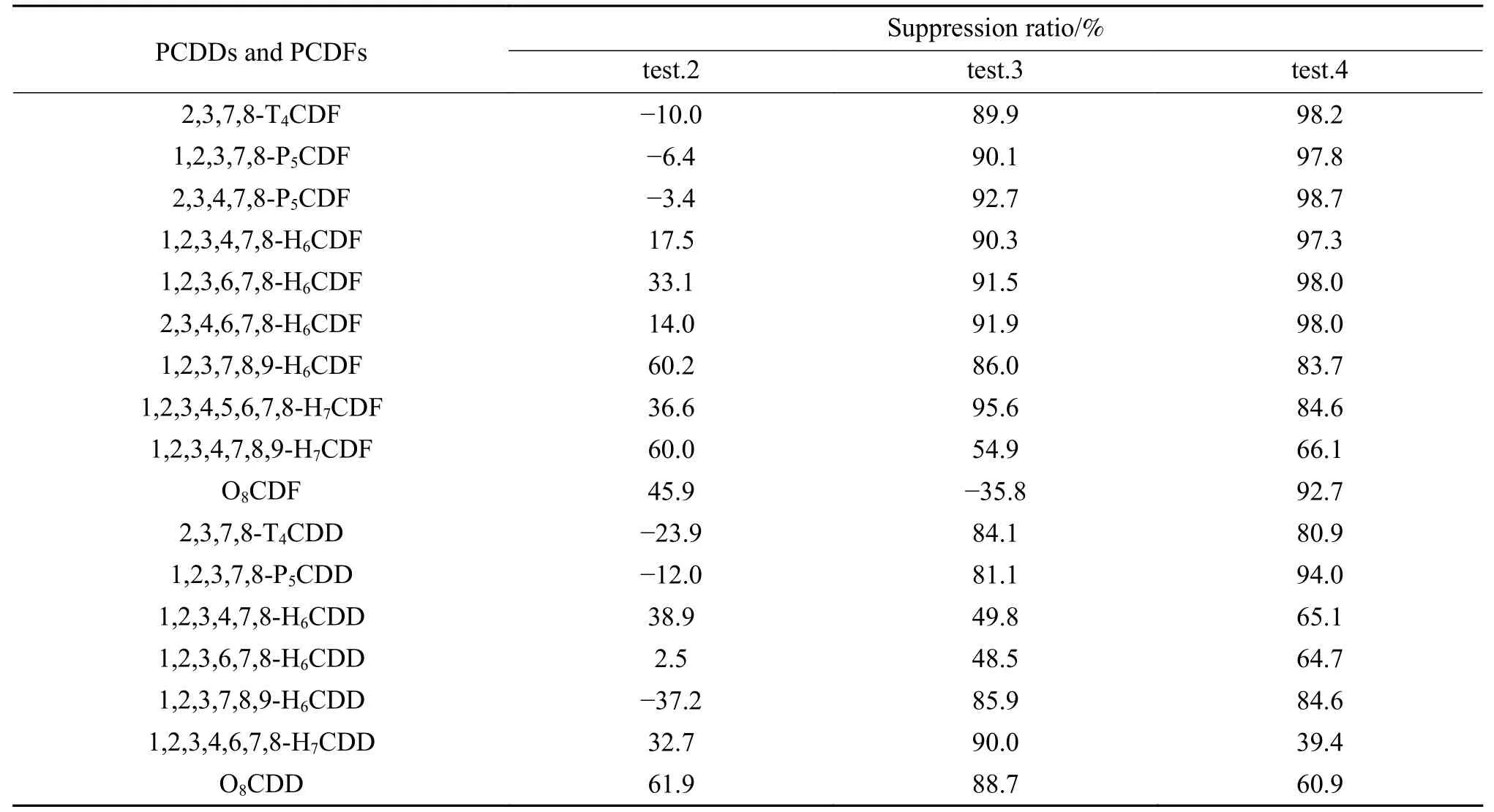
表2 多氯代二苯并对二噁英和多氯代二苯并呋喃抑制率Table 2 Suppression ratio of PCDDs and PCDFs
2.5 二噁英当量毒性分析
图8 为二噁英类物质总当量毒性图。由图8可见,在实验2 中Ni/Al2O3催化剂的加入会使总当量毒性升高4.3%,这是由于实验2 促进了毒性强的四氯代二噁英及四氯代呋喃的生成,因此,总毒性当量较实验1 有所增加。在实验3 中水加入会使总毒性当量降低90%,在实验4 中催化剂和水共同作用下对二噁英类物质总毒性当量降低最为显著可达98%。
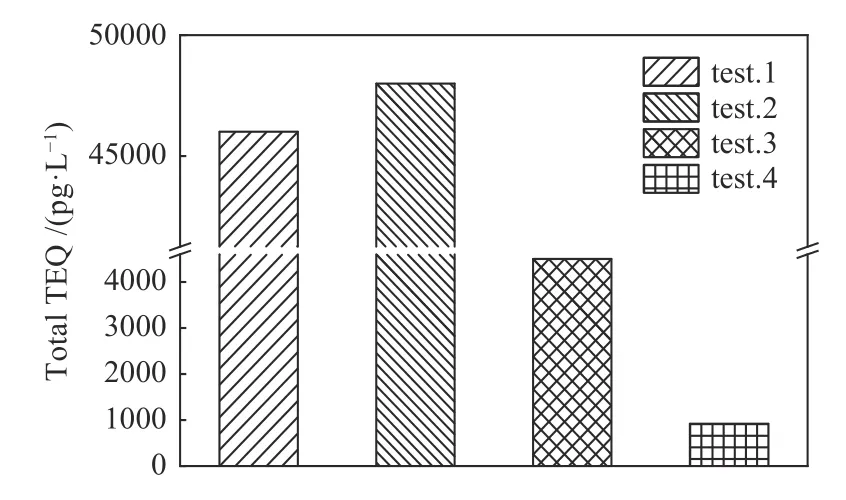
图8 总毒性当量图Figure 8 Total toxicity equivalent graph
图9 为各类二噁英和呋喃毒性当量图。从图9可以看出,水的添加对毒性较强的二噁英和呋喃的毒性当量均减少。Ni/Al2O3催化剂的添加对七、八氯代苯并对二噁英和七、八氯代苯并呋喃的毒性有降解作用,但对其他多氯代苯并对二噁英和多氯代苯并呋喃毒性均有促进作用。催化剂和水共同作用降解毒性效果明显,尤其对毒性高的四氯代二噁英和呋喃都降低了98%左右。由于二噁英具有较为复杂的形成机理,本研究发现催化剂的加入,特别是水的加入能够显著抑制二噁英的生成。主要是因为在含水气氛下,可能会发生气相中间碳氢化合物的重整反应,形成还原性气体,从而减少了二噁英的生成。课题组先前的研究也表明,还原性气氛有助于抑制二噁英的生成[20];在该反应过程中,反应的速控步骤应该是水蒸气和碳氢化合物的水蒸气重整反应,催化剂的加入能够加速这一反应。这就是催化剂和水蒸气的协同效应,而单独加入催化剂对反应的促进作用有限。
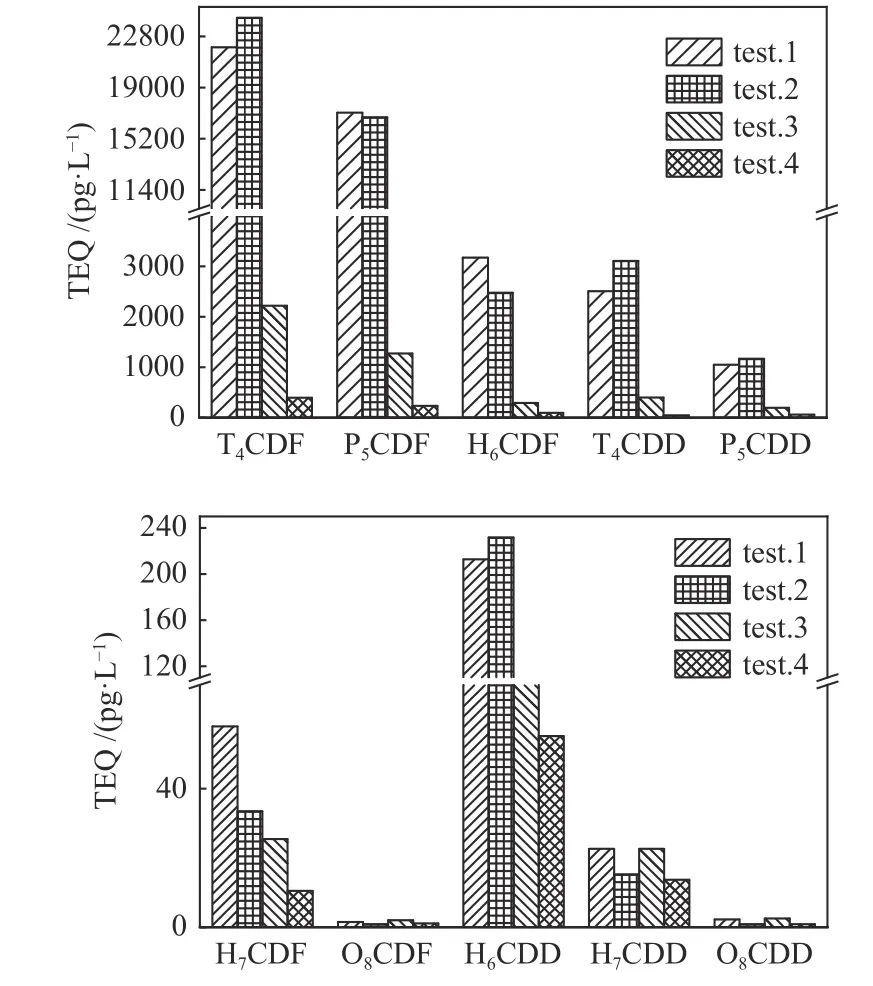
图9 各类二噁英和呋喃毒性当量图Figure 9 Toxic equivalent graphs of various dioxins and furans
2.6 吸收液有机物分析
图10、图11 为吸收液中含碳有机物分布。通过质谱定性分析发现,Ni/Al2O3催化剂和水蒸气共同作用促进大分子有机物转化为小分子有机物,C10 以上的大分子物质完全消失,C8 和C9 分子被断开,C4 和C5 明显增多,检测出的烃类种类也减少一半。水的加入促进了C6 以上的大分子物质向小分子物质的转化,其中,C6 和C8 的转化效果最为显著。催化剂的加入促进了C6、C7、C8 等大分子有机物的降解。
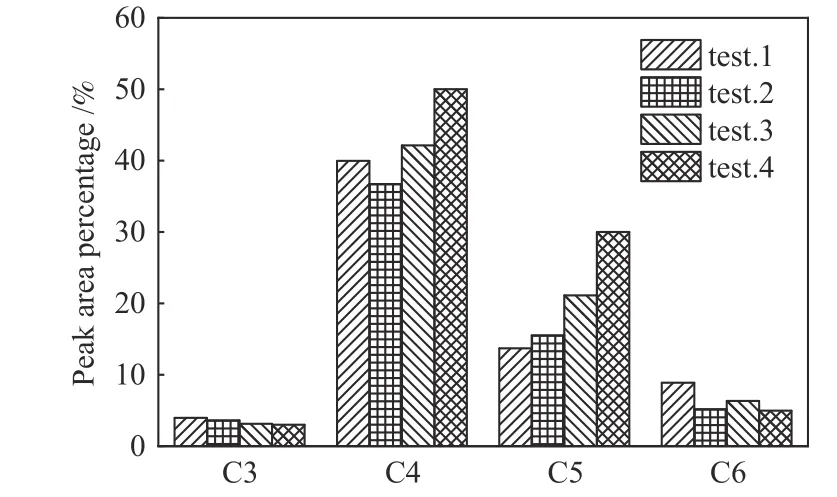
图10 吸收液中C3−C6 有机物的分布Figure 10 Concentration of C3−C6 organic matter in absorbent
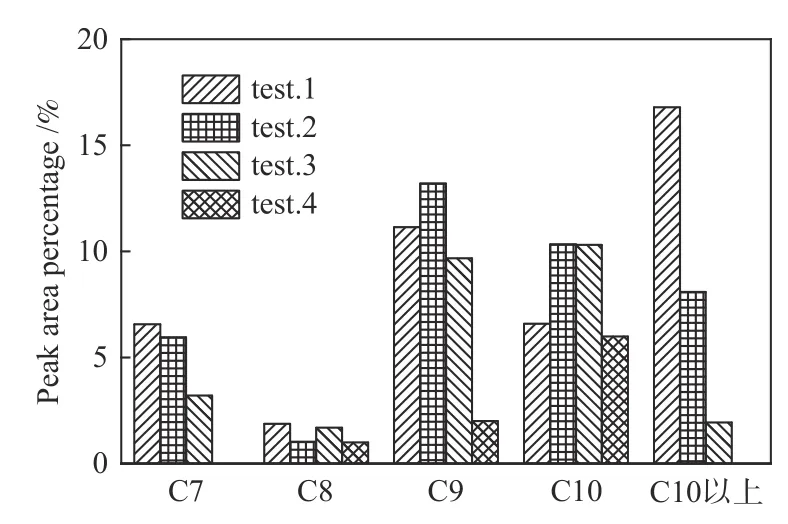
图11 吸收液中C6 以上有机物的分布Figure 11 Concentration of organic matter above C6 in absorbent
3 结论
通过改变模拟城市生活垃圾焚烧实验的焚烧条件(加入镍催化剂、水),分析反应温度、焚烧尾气流量、尾气组分、吸收液二噁英含量、二噁英当量毒性、吸收液有机物分布的变化,探究不同燃烧条件对生活垃圾焚烧副产二噁英生成的影响。结果表明:
焚烧过程中加入水和镍催化剂可以有效抑制17 种二噁英类物质的生成,二噁英生成总抑制率达到80.7%。对生成的二噁英总当量毒性降低98%。
焚烧过程中加入水和镍催化剂促进了生活垃圾的完全燃烧,焚烧尾气H2增加,CO 降低,促进了焚烧过程中大分子烃类裂解为小分子烃类,从而减少了二噁英前驱物的生成。
不同于现有有关二噁英的研究,常采用氯酚、氯苯等化合物通过前驱物合成二噁英并探究其抑制方法。笔者通过前期对所在城市生活垃圾进行取样分析,模拟出与生活垃圾元素含量相同的模拟生活垃圾,将其进行焚烧处理并在焚烧过程中探究二噁英抑制方法,期望使抑制方法更具可实现性。
