局部进展期口腔鳞癌术后容积旋转调强放疗与固定野调强放疗剂量分布研究*
2021-12-09刘骁蕾侯栋梁王秀楠
刘骁蕾,房 彤,侯栋梁,王 钦,王秀楠
(首都医科大学附属北京世纪坛医院放疗科 100038)
口腔癌为最常见的头颈肿瘤之一,绝大多数为鳞癌。我国每年新发病例约4.6万例[1]。早期患者预后较好,但中晚期患者预后较差,5年总生存率仅约50%。手术是局部中晚期口腔癌最有效的治疗方法,术后放疗的加入可明显降低中晚期口腔癌局部复发率和远处转移率,提高患者5年生存率[2]。固定野调强放疗(fixed-field intensity modulated radiotherapy,FF-IMRT)已广泛应用于口腔癌术后放疗[3]。近年来,容积旋转调强放疗(volumetric modulated arc therapy,VMAT)也逐渐应用治疗头颈肿瘤。临床工作中,口腔鳞癌往往与其他头颈肿瘤进行综合研究,关于口腔鳞癌独立研究较少。由于口腔鳞癌有多个原发部位,邻近器官不同和生理腔隙复杂,导致口腔鳞癌靶区变化较多,与其他头颈肿瘤靶区相差较大。本研究比较口腔鳞癌术后VMAT与FF-IMRT的计划计量学差异。
1 资料与方法
1.1 一般资料
回顾性选择2018年11月至2019年9月本院收治的局部进展期口腔癌术后放疗患者。纳入标准:年龄18~70岁;卡氏功能状态评分(KPS评分)≥70分;TNM分期(8th分期)Ⅲ~ⅣB期;术后病理为鳞癌;颈部淋巴结pN2或N3,双侧Ⅱ、Ⅲ、Ⅳ、Ⅴa或(和)Ⅴb区颈部淋巴结阳性;无放疗禁忌证。随机选择16例口腔癌患者放疗前定位图像进行研究。本研究通过本院伦理委员会审批(2018年科研伦审第40号),患者及家属签署知情同意书。
1.2 方法
1.2.1模拟定位
患者在定位前理发,口腔科就诊洁牙,处理龋齿。舌和口底的口腔癌患者予以口含器,保护软腭远离照射区域。采用仰卧位,选用合适角度的头枕,热塑头颈肩固定面罩,自由呼吸状态下使用荷兰Phillips公司螺旋Big Bore CT模拟机行放疗前定位。扫描范围从颅底至气管分叉,扫描层厚3 mm,予以静脉增强造影。扫描后图像传至美国Varian Eclipse 计划系统。
1.2.2靶区和危及器官勾画
将入组患者放疗前定位图像重新复制。按照RTOG指导勾画靶区,临床靶体积(CTV)包括瘤床、手术区域和双侧颈部淋巴结(Ⅱ、Ⅱ、Ⅲ、Ⅳ、Ⅴ区)。CTV在前后外放0.3 cm,上下外放1 cm并收至皮下3 mm,形成计划靶体积(planning target volume,PTV)。危及器官包括腮腺、脊髓、脑干。所有患者靶区及危及器官均由1名放疗科副主任医师重新勾画。整合口腔临床检查和放疗前1个月内头颈CT和MRI影像学检查,必要时加用PET-CT图像,进行CTV准确勾画。
1.2.3处方剂量和计划设计
2名高年资物理师各选取8套靶区制作放疗计划,对每例患者分别设计FF-IMRT计划和VMAT计划。CTV处方剂量要求60 Gy分30次,每次2 Gy。处方剂量覆盖必须大于95%PTV(不设为95%),最大剂量小于110%。FF-IMRT计划采用7个野均分共面照射,机架角度为0°、 51°、 103°、154°、 206°、 257°、 309°。VMAT计划采用双弧照射,顺时针181°~179°,再逆时针179°~181°。加速器使用美国Varian公司的Trilogy加速器,6 MV X线。
1.2.4计划评估
使用剂量体积直方图(DVH图)评估靶区和危及器官的剂量分布。靶区评估参数包括均匀度指数(HI)=(D2-D98)/D50,其中D2、 D98和D50分别是覆盖2%、98%和50%PTV体积的剂量[4-5]。适形度指数(CN)=VT,ref/VT×VT,ref/Vref,其中VT是靶区的体积,VT,ref是100%处方剂量覆盖PTV体积,Vref是受照射的体积[5]。CN值越接近1,放疗计划的适形度越好。HI值越小,PTV均匀度越好[6]。V50%/VPTV指数中V50%是50%剂量线在体内所包围的体积,VPTV是靶区体积。危及器官评估参数包括腮腺Dmean和接受30 Gy照射体积百分比(V30)、脊髓受照最高剂量(Dmax)和脑干Dmax。
1.3 统计学处理
2 结 果
2.1 基本情况
16例患者年龄(53.6±9.2)岁,主要为男性(87.5%),原发部位以舌癌多见(50%),临床分期以ⅣA最多见(75%),见表1。
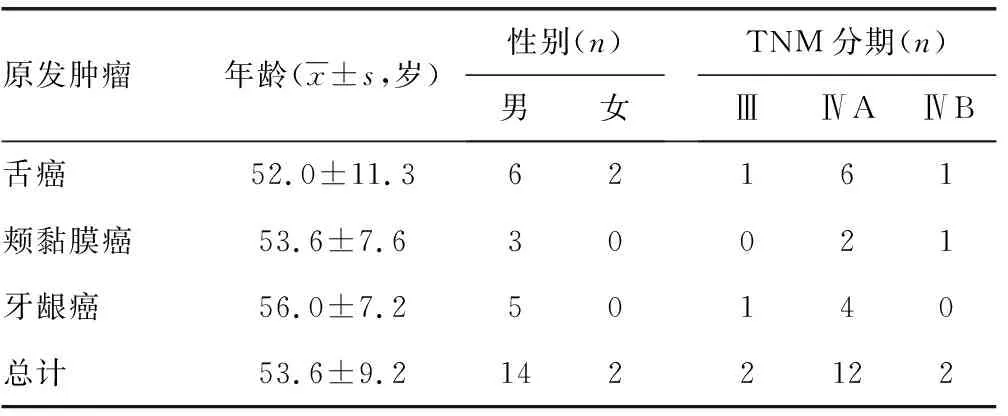
表1 患者基本情况
2.2 两组靶区剂量对比
VMAT组和FF-IMRT组的CN比较差异无统计学意义(P=0.084)。VMAT组的HI(0.107±0.013)明显高于FF-IMRT组(P<0.001),V50%/VPTV较FF-IMRT组明显下降(P<0.001),见表2、图1。DVH图显示VMAT组的100%~110%处方剂量的体积分布明显大于FF-IMRT组,VMAT组靶区剂量热点较FF-IMRT增多。
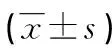
表2 两组靶区评估参数比较
2.3 两组机器跳数比较
VMAT组的机器跳数为(562±99)MU,明显少于FF-IMRT组(1 433±282)MU,差异有统计学意义(P<0.001),见表2。
2.4 两组危及器官受照剂量比较
VMAT组双侧腮腺、脊髓、脑干受照剂量较FF-IMRT组明显降低,差异有统计学意义(P<0.05),见表3。
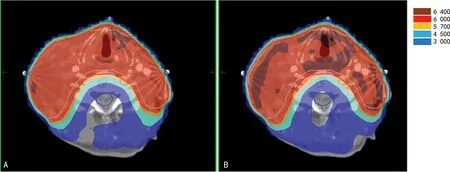
A:FF-IMRT;B:VMAT。
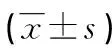
表3 两组危及器官受照剂量比较
3 讨 论
术后放疗是提高高危口腔鳞癌患者的局部控制和生存率的重要手段[7]。但是放疗不良反应是患者心理排斥和中断治疗的主要因素。因此,在临床应用中,不仅强调最大程度地杀灭恶性肿瘤细胞,还应尽可能的保护正常器官[5]。
FF-IMRT相较传统三维适形放疗技术,剂量均匀度和适形度较好,能明显改善对周围正常组织损伤,但是由于FF-IMRT计划分野过多,引起治疗时间过长[8-10]。VMAT作为一种新的IMRT技术,放射子野更小、精度更高,放射剂量率较FF-IMRT明显升高。本研究显示,VMAT组机器跳数较FF-IMRT组减少了60.1%,技术上治疗时间明显缩短。前期基础研究显示,X射线引起DNA双链断裂(DSB)导致细胞损伤和细胞周期停滞;如DNA持续受损,细胞将持续停滞于细胞周期,最终引起细胞凋亡;然而肿瘤细胞常伴有修复通路基因过表达,导致DSB修复能力增加,从而产生放疗耐受性[11-13]。因此虽然与VMAT接受相等剂量,FF-IMRT因为放疗时间增加,可能引起肿瘤细胞DSB修复增多,进而导致放疗疗效降低。同时,由于VMAT治疗时间缩短,可降低患者因治疗保持强迫体位的不适感,更好保持体位,减少体位移动、呼吸等对放疗精确性的影响。
FF-IMRT剂量率较VMAT低,患者受照低剂量区增加,可能增加放疗并发症。V50%/VPTV可用于评估剂量在体内外扩程度。本研究结果显示,VMAT组V50%/VPTV较FF-IMRT组明显下降,FF-IMRT可能较VMAT的不良反应增加。VMAT比FF-IMRT对正常组织保护更好,双侧腮腺、脊髓和脑干受照剂量明显下降。虽然本研究入组病例分期较晚,存在腮腺受侵病例,腮腺整体受照剂量较高,但VMAT的腮腺受照剂量仍较FF-IMRT明显下降。HE等[14]针对647例鼻咽癌回顾性分析显示,应用VMAT治疗较FF-IMRT腮腺V30降低2%,脑干、脊髓降低0.6~3.5 Gy。
同时,本研究发现VMAT的适形度与FF-IMRT相似,而均匀度较FF-IMRT下降。关于头颈肿瘤VMAT和FF-IMRT适形度和均匀度结果各异。部分研究认为VMAT可达到比FF-IMRT更优的适形度[15-17]。NAGARAJAN等[18]研究通过比较30例头颈肿瘤的靶区计划,发现VMAT的均匀度低于FF-IMRT。VMAT的均匀度下降可能与VMAT热点体积(≥107%处方量的体积)分布增多相关;也可能与口腔癌的生理结构相关。LEUNG等[19]发现不同原发部位头颈肿瘤的FF-IMRT与VMAT靶区适形度和均匀度差异性不同,如低危区口腔癌和喉癌靶区VMAT适形度和均匀度与FF-IMRT相似;而鼻咽癌靶区二者虽适形度相似,但FF-IMRT的均匀度优于VMAT。提示原发肿瘤的解剖和危及器官的不同特点,可能影响靶区剂量分布。但由于本研究入组数量有限,未包括所有原发部位,因此结论不适用于所有口腔鳞癌患者,亟待进一步更全面的研究。
综上所述,对于Ⅲ~ⅣB期口腔鳞癌术后放疗首选VMAT,其保护危及器官较好,治疗时间明显缩短。但FF-IMRT具有靶区均匀度好且治疗费用低廉的优点,因此对于不具备VMAT的基层医疗机构,FF-IMRT仍值得临床上推广。
