波罗蜜叶片突变体叶绿素含量测定和超微结构观察
2021-12-08周丹,罗灿,于旭东,蔡泽坪,吴繁花
周丹,罗灿,于旭东,蔡泽坪,吴繁花


摘 要:波罗蜜(Artocarpus heterophyllus)是一种热带果树,至今对其突变体的研究少有报道。本研究以波罗蜜叶片为试验材料,探究其葉片出现白化和返绿现象的可能原因。(1)用分光光度计法、比色法测定波罗蜜叶片突变体和正常绿叶的叶绿素及叶绿素前体物质含量;(2)用叶绿素酶Elisa试剂盒测定叶绿素酶活性;(3)用透射电子显微镜对叶绿体的超微形态结构进行观察。研究结果表明:(1)不同叶色所产生的叶绿素a含量、叶绿素b含量、叶绿素总含量、类胡萝卜素含量均存在显著差异;(2)波罗蜜叶片突变体和正常绿叶的叶绿素合成前体物质含量之间并没有出现显著性差异;(3)对波罗蜜叶片的叶绿素酶活性进行测定时,发现其活性出现显著差异,但对其叶绿素含量的差异性并没有产生较大影响;(4)观察波罗蜜叶片内叶绿体超微形态结构时,发现正常绿叶的叶绿体形态完好且数量较多,白化叶和返绿叶的叶绿体内部结构存在缺陷,其原因是叶绿体基粒构建阶段受阻;基于测定波罗蜜叶片中的叶绿素、叶绿素前体物质含量和叶绿素酶活性,并观察波罗蜜叶片内叶绿体的超微形态结构,对得到的数据结果进行比较分析。本研究推测是在叶绿素合成阶段,原脱植基叶绿素合成叶绿素时受阻及叶绿体发不良导致波罗蜜出现白化和返绿现象,为今后进一步综合研究波罗蜜突变体提供理论依据。
关键词:波罗蜜;叶绿素;叶绿素前体物质;叶绿素酶活性;超微结构
中图分类号:S667.8 文献标识码:A
Determination of Chlorophyll Content and Observation of
Ultrastructure in Leaves of Mutants of Artocarpus heterophyllus
ZHOU Dan1,2,3,4, LUO Can1,4, YU Xudong1,2,3,4*, CAI Zeping1, WU Fanhua1
1. College of Forestry, Hainan University, Haikou, Hainan 570228, China; 2. Key Laboratory of Genetics and Germplasm Innovation of Tropical Special Forest Trees and Ornamental Plants (Hainan University), Ministry of Education, Haikou, Hainan 570228, China; 3. Key Laboratory of Germplasm Resources Biology of Tropical Special Ornamental Plants of Hainan, Haikou, Hainan 570228, China; 4. Hainan Sub-platform of National Forest Genetic Resources Platform, Danzhou, Hainan 571737, China
Abstract: Artocarpus heterophyllus is a tropical fruit, and so far there are few reports on its mutants. In this study, the leaves of A. heterophyllus were used as the experimental materials to explore the possible reasons for the albinism and regreening of the leaves. The contents of chlorophyll and chlorophyll precursors in leaf mutants and normal green leaves were determined by conventional methods. The activity of chlorophyllase was determined by Elisa kit. The ultrastructure of chloroplast was observed by a transmission electron microscope. Chlorophyll a content, chlorophyll b content, total chlorophyll content and carotenoid content produced by different leaf colors were significantly different. There was no significant difference in the content of chlorophyll synthesis precursors between the mutant and the normal green leaves. In the determination of chlorophyll enzyme activity of the leaves, although there was a significant difference in its activity, it had no significant effect on the difference in chlorophyll content. When observing the ultrastructure of chloroplasts in the leaves, it was found that the chloroplasts in the normal green leaves were intact and had a large number, and the internal structure of chloroplasts in the albino leaves and the regreening leaves was defective, because the chloroplast grana construction stage was blocked. Based on the determination of chlorophyll, chlorophyll precursor content and chlorophyll enzyme activity in the leaves, the ultrastructure of chloroplast in the leaves was observed, and the data were compared and analyzed. In this study, it was speculated that during the chlorophyll synthesis stage, the blocked synthesis of chlorophyll by pchlide and the poor chloroplast development led to the albinism and regreening of A. heterophyllus, which would provide a theoretical basis for further comprehensive study of A. heterophyllus mutants.
Keywords: Artocarpus heterophyllus; chlorophyll; chlorophyll precursor substance; chlorophyll enzyme activity; ultrastructure
DOI: 10.3969/j.issn.1000-2561.2021.10.025
植物的白化病会导致植株生长缓慢,矮化甚至死亡。植物产生的白化现象与植物叶绿体的发育不良和叶绿素合成途径受阻都十分相关[1-2]。植物叶绿体内含有多种光合色素,是高等植物进行光合作用的主要场所[3]。叶绿体发育不良或结构存在缺陷,会使植物叶绿素的合成受到影响,最终导致植物光合过程受阻。叶绿素的合成从起始物质L-谷氨酰-tRNA到最终产生叶绿素a和叶绿素b,中间过程涉及多种物质和酶的参与[4],例如,叶绿素前体物质中的δ-氨基乙酰丙酸(ALA)、原脱植基叶绿素(Pchl)等,其中任何一种叶绿素前体物质的合成受阻,最终都会影响合成的叶绿素含量。例如:钟小兰和马均等[5]在红苞凤梨(Ananas bracteatus)金边嵌合体白化细胞中发现尿卟啉原含量与正常绿叶相比显著减少,而其后的前体物质含量均显著地低于正常绿叶前体物质的含量,最终导致叶绿素含量显著下降。在叶绿素合成和降解过程中,如果其中任何一步发生障碍,就可能导致植物的叶色产生异常现象。在叶绿素降解过程中,叶绿素酶是一种关键酶,它可以加速叶绿素的降解,因此叶绿素酶活性的高低也会对叶绿素含量产生影响[6]。
目前,关于植物白化的研究有很多,在一些模式植物中已鉴定出白化病的表型,例如,在木本植物中的茶树(Camellia sinensis)[7];在草本植物中的烟草(Nicotiana tabacum)[8]、水稻(Oryza sativa)[9]、拟南芥(Arabidopsis thaliana)[10]等,但导致白化病产生的原因,仍未得到充分研究。作为热带果树的波罗蜜(Artocarpus heterophyllus),是海南省重要的经济植物,其带有白化病的苗木会对其产量造成一定影响。尽管目前有一些关于波罗蜜白化病的研究,但多集中在幼苗解剖观察、生理指标的测定和形态的观察等[11],很少有研究关注到波罗蜜叶绿素合成代謝途径和叶绿体发育机制的方面。
由于白化现象和返绿现象在植物形态中表现出明显的性状差异,因此在植物种子培育工作中可以作为一种标记性状,在植株幼苗期就可观察性状差异。另外,植物的白化现象和返绿现象对研究植物的抗病机制也有重要的作用和意义。目前,在波罗蜜叶片突变体筛选抗病基因中也有了相关研究[12]。因此,本研究以波罗蜜的叶片为研究材料,测定波罗蜜叶片突变体和正常绿叶叶片内的叶绿素、叶绿素合成前体物质的含量和叶绿素酶活性,观察植物叶片内叶绿体的超微形态结构,以探究波罗蜜叶片出现白化和返绿现象的可能原因,为进一步探究波罗蜜突变体叶绿素合成代谢途径、叶绿体发育机制提供理论依据。
1 材料与方法
1.1 材料
以波罗蜜的正常苗(正常生长的健康苗)、白化苗(萌芽时即患有白化病的幼苗)及返绿苗(萌芽时患有白化病,在生长发育一段时间后,叶片出现返绿现象的幼苗)作为研究材料(图1),波罗蜜的种子收集自海南省儋州市海南大学儋州校区(1095 E,195 N)。从带有隐性白化遗传基因的波罗蜜母株成熟果实中剥离出种子,挑选饱满的种粒,种植于培养桶中并在室外自然环境下进行培养。当幼苗生长到30 d后,随机挑选生长一致的正常苗、白化苗及返绿苗,并选取幼苗顶端向下的第三、第四片生长成熟的叶片作为试验材料,测定叶绿素含量、叶绿素合成前体物质含量及叶绿素酶活性,试验重复3次以上。
1.2 叶绿素及其前体物质含量的测定
1.2.1 δ-氨基乙酰丙酸含量的测定 δ-氨基乙酰丙酸(ALA)含量测定参照Dei[13]的方法,使用电子天平(AR323CN)称取新鲜波罗蜜叶片,剪碎、研磨。用Ehrlich-Hg试剂,黑暗条件下显色15 min,利用分光光度计(ZG-EU-2200R)在波长553 nm测定OD值。
1.2.2 胆色素原、尿卟啉原Ⅲ、粪卟啉原Ⅲ含量的测定 胆色素原(PBG)、尿卟啉原Ⅲ(UroⅢ)、粪卟啉原Ⅲ(CoprogenⅢ)含量测定参照Bogorad[14]的方法,称取新鲜波罗蜜叶片,剪碎并用液氮充分研磨,加入缓冲液提取,利用分光光度计测定波长553 nm、测水相405.5 nm、测盐酸相399.5 nm处的OD值。
1.2.3 原卟啉Ⅸ、镁原卟啉Ⅸ和原脱植基叶绿素含量的测定 原卟啉Ⅸ(ProtoⅨ)、镁原卟啉Ⅸ(Mg-ProtoⅨ)原脱植基叶绿素(Pchl)含量的测定参照Hodgins等[15]的方法,称取新鲜波罗蜜叶片,剪碎、研磨。最后利用全波长酶标仪(BioTek Epoch)测定波长在575、590、628 nm的OD值。1.2.4 叶绿素含量的测定 叶绿素含量的测定参照张治安[16]的方法,称量新鲜波罗蜜叶片,剪碎、研磨、过滤。用紫外分光光度计(UV-1800PC)在波长665、649、470 nm下测定吸光度。
1.3 叶绿素酶活性的测定
分别取波罗蜜白化叶、正常绿叶和返绿叶的叶片,按照植物叶绿素酶Elisa试剂盒说明书的方法,测定叶绿素酶活性。利用酶标仪(瑞士帝肯IF50)在450 nm波长处测定各孔的OD值。
1.4 叶绿体超微形态观察
为确定波罗蜜叶片中叶绿体结构是否完整,对波罗蜜叶片细胞内的叶绿体进行超微结构观察。参照杨勇骥等[17]的方法,对波罗蜜叶片进行取材及样品的制备。用莱卡UC-6型超薄切片机进行超薄切片,最后用透射电子显微镜(日立HT-7700)观察,并拍照记录。
1.5 统计分析
试验数据采用Excel 2016软件进行整理和制表,采用Duncans新复极差法进行显著性测验(P<0.05)。
2 结果与分析
2.1 波罗蜜的叶色观察
波罗蜜叶片突变体是一个自然突变体,现对其叶片表型性状进行观察。如图2所示,在相同环境下生长的波罗蜜幼苗,其叶片长、宽的大小表现为白化叶<返绿叶<正常绿叶。波罗蜜白化苗表现出植株叶片全部白化,植株的长势与正常植株相比较弱;波罗蜜返绿苗呈现出叶片由白色变为淡绿色;波罗蜜的正常苗是在植株的整个生长过程中都表现为绿色。
2.2 叶绿素及其前体物质含量的测定
2.2.1 叶绿素前体物质含量的测定 为探究波罗蜜叶片叶绿素合成过程中是否发生障碍(图3),对叶绿素合成的前体物质δ-氨基乙酰丙酸、胆色素原、尿卟啉原Ⅲ、粪卟啉原Ⅲ、原卟啉Ⅸ、镁原卟啉Ⅸ和原脱植基叶绿素等含量进行测定(表1),将得到的数据进行比较和分析。将波罗蜜正常绿叶中各物质的含量定为100%,与白化叶、返绿叶测得的含量进行比较(图4),结果显示:波罗蜜叶片突变体和正常绿叶叶绿素前体物质含量之间没有出现显著性差异(P>0.05)。
2.2.2 葉绿素含量的测定 叶绿素是光合色素的一种,在植物光合过程中,它对光能有吸收、转化的作用[18]。测定波罗蜜叶片突变体和正常绿叶的光合色素含量,并对数据结果进行比较分析(表2)。结果显示:波罗蜜正常绿叶叶片内的叶绿素a(Chl a)、叶绿素b(Chl b)、类胡萝卜素(Car)含量显著高于白化叶、返绿叶(P<0.05);返绿叶叶片内的叶绿素a、叶绿素总含量显著高于白化叶(P<0.05),白化叶、返绿叶叶片内的叶绿素b、类胡萝卜素含量没有出现显著性差异(P>0.05);波罗蜜叶片突变体和正常绿叶的叶绿素a/b、类胡设正常绿叶各物质含量为100%,白化叶、返绿叶的各物质含量换算成相应各物质含量的百分数。
萝卜素/叶绿素总含量的比值也无明显差异(P> 0.05)(图5)。结合图4和图5,可以初步推测叶绿素合成在Pchlide→Chlide→Chl a→Chl b之间发生了障碍。
2.3 叶绿素酶活性的测定
植物叶绿素的降解过程一般可分为3个阶段[19](图6)。在叶绿素降解过程中,叶绿素酶是一种关键酶[20],一般认为,它的活性越高,会加快叶绿素的降解。由图7可知,正常绿叶叶片内的叶绿素酶活性显著高于白化叶、返绿叶(P<0.05),可达1425.7 U/mL,约为白化叶叶绿素酶活性的2.3倍,约为返绿叶的1.4倍;返绿叶叶片内的叶绿素酶活性显著高于白化叶(P<0.05),可达到994.4 U/mL,约为白化叶叶绿素酶活性的1.6倍(白化叶叶片内的叶绿素酶活性为623.6 U/mL)。结合表2和图7的数据结果,通过对波罗蜜不同叶色的叶绿素酶活性进行测定,发现正常绿叶的酶活性最高,其叶绿素的含量也是最多的,说明酶活性的高低没有对叶绿素含量产生较大的影响;返绿叶的酶活性高于白化叶的酶活性,其叶绿素的含量也高于白化叶,说明叶绿素酶活性的高低不是直接影响叶绿素含量存在差异性的主要因素,而是其叶绿素合成量减少所致。因此可以推测叶绿素降解并不是引起波罗蜜叶片出现白化和返绿现象的主要原因。
2.4 叶绿体超微形态观察
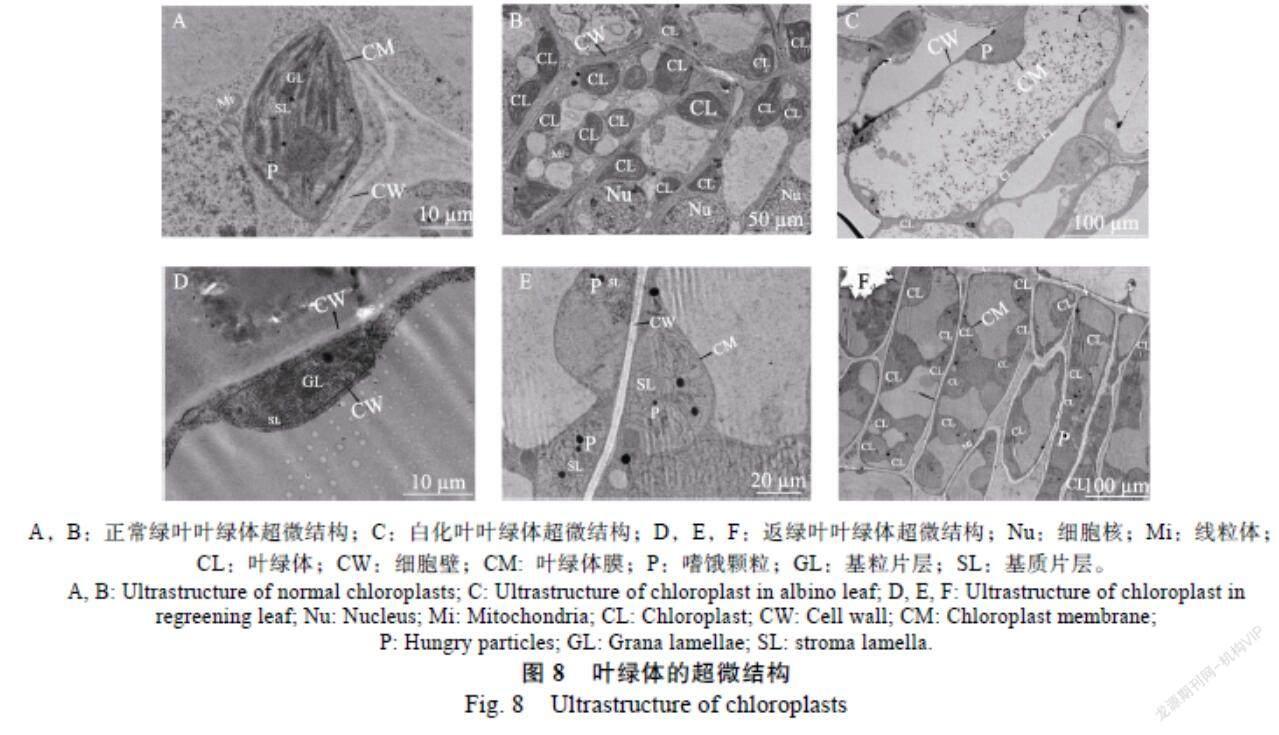
通过观察波罗蜜叶片内叶绿体形态结构的变化,可以发现环境条件变化和波罗蜜叶片之间的适应性[21]。将波罗蜜叶片进行染色制片,观察叶片内叶绿体的形态结构。由图8可知,正常绿叶的细胞内叶绿体形态完好且数量较多,叶绿体膜结构完整,内部片层结构和垛叠层数都较多,排列整齐且清晰。(图8A、图8B);在白化叶的细胞中,叶绿体数量极少且内部结构出现明显缺陷,叶绿体内部结构完全模糊化(图8C);返绿叶中的细胞内有极少结构较为良好的叶绿体,形状多为长椭圆形,叶绿体被膜结构完整,含有少量基粒类囊体结构,其结构垛叠大致整齐,但其基质类囊体结构排列较为松散(图8D);返绿叶中的大多数叶绿体结构出现明显缺陷,体积膨胀,形状多为圆形(少数为长椭圆形),叶绿体膜结构完整,基粒片层结构完全消失,基质片层结构排列散乱(图8E、图8F)。
3 结论
植物叶绿素的合成过程从起始物质L-谷氨酰- tRNA到最终产生叶绿素a和叶绿素b一共要经历16步[22],如果在这个合成途径中的任何一个环节发生障碍,则障碍之前的前体物质会积累,进而导致其含量增加;而其后的物质含量会迅速下降。本文通过对一系列前体物质含量进行测定,结果表明:波罗蜜中的白化叶、正常绿叶和返绿叶的前体物质含量从δ-氨基乙酰丙酸(ALA)到原脱植基叶绿素(Pchl)并没有出现显著性差异,类似的结论在白肋烟(Burley21)和马里兰烟(Md609)叶片中也有发现,刘彩云等[23]研究发现在这2种叶片中,其叶绿素前体物质的含量之间没有明显的差异,但最终形成的叶绿素a、b含量出现显著差异性。因此,初步认为波罗蜜叶绿素合成的障碍是发生在Pchlide→Chlide→Chl a→Chl b之间。类似的研究结果在水稻突变体中也有发现,徐培洲等[24]研究发现水稻突变体W1叶绿素合成受阻可能发生在Pchlide到Chlide。
通过对波罗蜜叶片突变体的前体物质含量进行比较分析,发现波罗蜜的白化叶、正常叶、返绿叶之间没有显著差异。介于此,本研究从叶绿素降解的角度,测定比较了波罗蜜不同叶片的叶绿素酶活性的高低。结果表明,波罗蜜叶片的叶绿素酶活性虽然存在显著差异,但对其叶绿素含量的差异并没有产生较大影响,说明叶绿素酶活性的高低不是直接影响叶绿素含量存在差异性的主要因素,而是其叶绿素合成量减少所致。类似的研究结果,陈友根等[25]曾在甜瓜属(Cucumis)正反交杂种的叶绿素酶活性测定中,发现叶绿素降解不是发生黄叶突变体的主要原因,而是其叶绿素合成量减少所致。
植物叶绿体的发育大致经历5个阶段,包括前质体阶段、造淀粉体阶段、变形虫状质体阶段、前基粒质体阶段和成熟叶绿体阶段[26]。在这个过程中任何一个阶段发生障碍,都可能造成叶绿体发育不良或者结构存在缺陷。植物叶色突变的产生与叶绿体的发育不良和叶绿素合成受阻紧密相关[27-28]。本研究通过观察波罗蜜叶片内的叶绿体超微形态结构,发现白化叶内的叶绿体数量极少,叶绿体内部结构出现明显缺陷,其体内结构完全模糊化;返绿叶中的细胞内有极少结构较为良好的叶绿体,大多数叶绿体结构发育不良。推测波罗蜜叶片在白化期和返绿期,叶绿体在发育过程中其基粒构建阶段受阻,使其发育不良,进而导致波罗蜜叶片发生变化。类似的研究结果在安吉白茶突变体中也有发现,杨荧等[29]研究发现安吉白茶是其叶绿体发育不良而导致安吉白茶叶白化。
4 结论
植物叶片表现出的白化现象与植物叶绿体的发育不良和叶绿素合成途径受阻都十分相关。通过测定波罗蜜叶片突变体和正常绿叶的叶绿素、叶绿素合成前体物质含量和叶绿素酶活性,并观察波罗蜜叶片内叶绿体的超微形态结构,发现波罗蜜的白化叶和返绿叶中的叶绿体结构异常,同时叶绿素合成在Pchlide→Chlide→Chl a→Chl b之间发生了障碍,本研究推测是因为叶绿素合成阶段受阻及叶绿体发育不良导致波罗蜜出现白化和返绿现象。波罗蜜叶片突变体材料对研究波罗蜜的叶绿素合成过程、叶绿体的发育、光合作用和培育优良波罗蜜品种都具有重要意义。因此,对于波罗蜜突变体的叶绿素合成代谢途径与叶绿体发育机制,还有待进一步深入研究。
参考文献
[1] 涂美艳, 宋海岩, 陈 栋, 等. 川中丘陵区碱性土对GF677和毛桃叶片光合特性及叶绿素荧光参数的影响[J]. 山地学报, 2018, 369(1): 153-162.
[2] 黄小贞, 赵懿琛. 拟南芥PGK基因家族功能的初步分析[J]. 山地农业生物学报, 2017, 36(1): 12-17, 35.
[3] 刘聪利, 魏祥进, 邵高能, 等. 水稻叶色突变分子机制的研究进展[J]. 中国稻米, 2012, 18(4): 15-21.
[4] Beale S I. Green genes gleaned[J]. Trends in Plant Science, 2005, 10(7): 309-312.
[5] 钟小兰. 红苞凤梨金边嵌合体白化细胞叶绿素合成限速基因挖掘[D]. 雅安: 四川农业大学, 2015.
[6] Fernandez-Lopez J A, Almela L, Almansa M S, et al. Partial purification and properties of chlorophyllase from chlorotic citrus limon leaves[J]. Phytochemistry, 1992, 31(2): 447-449
[7] 李娜娜. 新梢白化茶树生理生化特征及白化分子机理研究[D]. 杭州: 浙江大学, 2015.
[8] 孙敬三, 朱至清, 李守全. 烟草缺绿突变体的质体发育和超微结构[J]. 遗传学报, 1982, 9(2): 147-150, 172.
[9] 尚丽娜, 陈新龙, 米胜南, 等. 水稻温敏型叶片白化转绿突变体tsa2的表型鉴定与基因定位[J]. 作物学报, 2019, 45(5): 662-675.
[10] 郭 彦, 张文会. 拟南芥白化突变体反射光谱及色素含量研究[J]. 安徽农学通报, 2018, 24(14): 16, 77.
[11] 付 影, 于旭东, 蔡泽坪, 等. 菠萝蜜白化突变体的性状研究[J]. 热带作物学报, 2018, 39(6): 1081-1086.
[12] 郑李婷, 于旭东, 蔡泽坪, 等. 波罗蜜叶绿素缺失突变体次生生长茎抗病基因的筛选[J]. 分子植物育种, 2020, 18(22): 7348-7355.
[13] Dei M. Benzyladenine-induced stimulation of 5-aminolev-uli?nic acid accumulation under various light intensities in levulinic acid-treated cotyledons of etiolated cucumber[J]. Physiologiae Plantarum, 1985, 64(2): 153-160.
[14] Bogorad L. Porphyrin synthesis[J]. Methods in Enzymology, 1962, 5: 885-895.
[15] Hodgins R, Van Huystee R B. Rapid simultaneous estimation of protoporphyrin and Mg-porphyrins in higher plants[J]. Journal of Plant Physiology, 1986, 125(3-4): 311-323.
[16] 張治安. 植物生理学实验指导[M]. 北京: 中国农业科技出版社, 2004: 15-23.
[17] 杨勇骥. 医学生物电子显微镜技术[M]. 上海: 第二军医大学出版社, 2012: 13-35.
[18] 史典义, 刘忠香, 金危危. 植物叶绿素合成、分解代谢及信号调控[J]. 遗传, 2009, 31(7): 698-704.
[19] 沈成国, 张福锁, 毛达如. 植物叶片衰老过程中叶绿素降解代谢研究进展[J]. 植物学通报(增刊), 1998, 15: 41-46.
[20] Smadar H S, Tamar A, Tzahi A, et al. Chlorophyllase is a rate-limiting enzyme in chlorophyll catabolism and is posttra?nsl?ationally regulated[J]. The Plant Cell, 2007, 19: 1007-1022.
[21] 郑敏娜, 李向林, 万里强, 等. 水分胁迫对6种禾草叶绿体、线粒体超微结构及光合作用的影响[J]. 草地学报, 2009, 17(5): 643-649.
[22] Diter W, Simon G. Chlorophyll biosynthesis[J]. The Plant Cell, 1995, 7: 1039-1057.
[23] 刘彩云, 刘洪祥, 杜传印. 白肋烟和马里兰烟叶绿素酶活性测定及其基因表达的实时定量PCR分析[J]. 中国农学通报, 2011, 27(3): 139-142.
[24] 徐培洲, 李 云, 袁 澍, 等. 叶绿素缺乏水稻突变体中光系统蛋白和叶绿素合成特性的研究[J].中国农业科学, 2006, 39(7): 1299-1305.
[25] 陈友根, 崔 利, 陈劲枫. 甜瓜属正反交杂种叶绿素生物合成与代谢研究[J]. 植物生理学报, 2013, 49(5): 452-456.
[26] 陈湘宁, 李玉湘, 李继耕. 水稻、小麦花药培养白化苗质体亚显微结构和蛋白质的研究[J]. 遗传学报, 1988, 15(2): 95-101, 164.
[27] Chen T, Zhang Y D, Zhao L, et al. Fine mapping and candidate gene analysis of a green-revertible albino gene gra(t) in rice[J]. Journal of Genetics & Genomics, 2009, 36(2): 117- 123.
[28] Li C, Zheng Y, Zhou J, et al. Changes of leaf antioxidant system, photosynthesis and ultrastructure in tea plant under the stress of fluorine[J]. Biologia Plantarum, 2011, 55(3): 563-566.
[29] 杨 荧, 吕立堂, 赵德刚. 安吉白茶白化叶和返绿叶叶绿体超微结构和叶绿素及其前体物含量的比较[J]. 山地农业生物学报, 2019, 38(6): 71-75, 79.
責任编辑:白 净
