HPLC-FLD法同时测定直服丹参粉中黄曲霉毒素B1、B2、G1、G2
2021-12-08阳文武王文婷张华熊有明
阳文武 王文婷 张华 熊有明
【摘 要】 目的:建立HPLC-FLD同时测定直服丹参粉中黄曲霉毒素B1、B2、G1、G2的方法。方法:样品70%甲醇提取液的分析采用Inertsustain C18色谱柱(4.6 mm× 150 mm,5μm),柱温:35 ℃,以甲醇-乙腈-水(40∶[KG-*3/5]18∶[KG-*3/5]42)为流动相,流速为1.0 mL/min,激发波长为360 nm,发射波长450 nm。结果:黄曲霉毒素B1、B2、G1、G2线性范围分别为9.3~46.5 pg、3.0~15.0 pg、9.3~46.5 pg、3.5~17.5 pg,平均回收率分别为95.1%、90.2%、95.4%、93.3%,RSD分别为1.7%、2.2%、1.6%、1.3%,检测限分别为2.0、1.0、2.0、1.0 ng/kg。50批样品中有9批次检出黄曲霉毒素,检出率为18.0%,均符合相关参考限量标准。结论:该方法简便准确、重复性好,可用于丹参粉的质量控制。
【关键词】 丹参粉;黄曲霉毒素B1、B2、G1、G2;高效液相色谱-荧光法
【中图分类号】R917 【文献标志码】 A【文章编号】1007-8517(2021)20-0048-05
Simultaneous Determination of Aflatoxins B1, B2, G1, G2 in Powder of Salvia Miltiorrhiza by HPLC-FLD
YANG Wenwu WANG Wenting ZHANG Hua XIONG Youming*
Wanzhou Institute for Food and Drug Control in Chongqing,Chongqing 404000,China
Abstract:Objective Establish an HPLC-FLD method for simultaneous determination of aflatoxins B1, B2, G1, G2(AFB1, AFB2,AFG1,AFG2)in powder of Salvia miltiorrhiza.Methods The analysis of 70% methanol extract of this samples were performed on a 35 ℃ thermostatic Inertsustain C18 column (4.6 mm×150 mm, 5 μm), methanol-acetonitrile-water (40∶[KG-*3/5]18∶[KG-*3/5]42) as mobile phase, flow rate of 1.0 mL/min, excitation wavelength of 360 nm, emission wavelength of 450 nm. Results The AFB1, AFB2,AFG1,AFG2 have a good linear relationship in the range of 9.3~46.5 pg、3.0~15.0 pg、9.3~46.5 pg、3.5~17.5 pg, and the correlation coefficients r all were 0.9999. The average recoveries were 95.1%,90.2%,95.4% and 93.3%, respectively .The RSD were 1.7%,2.2%,1.6%,and1.3%, respectively. The method detection limits were 2.0, 1.0, 2.0 and 1.0 ng/kg,respectively. Aflatoxins were detected in 9 batches of 50 batches of samples, the detection rate was 18.0, and conformed to the relevant reference limit standards. Conclusion The method is simple, accurate and reproducible, and can be used for the quality control of Salvia miltiorrhiza powder.
Key words:Powder of Salvia Miltiorrhiza;AFB1; AFB2;AFG1;AFG2; HPLC-FLD
丹參粉是唇形科植物丹参(Salvia miltiorrhiza Bge.)干燥根及根茎制成的粉末,具有活血祛瘀、通经止痛、清心除烦、凉血消痈之功效[1]。丹参喜气候温和、空气湿润、土壤肥沃的环境,且其药用部位直接与土壤接触,易感染真菌[2-4]。黄曲霉毒素是由黄曲霉和寄生曲霉中产毒菌株产生的一类致癌性物质,是目前为止发现的毒性最大的真菌毒素,其毒性相当于砒霜的68倍,对人体及动物器官尤其是肝脏损害严重[5]。在植物来源的药材中主要污染AFB1、AFB2、AFG1、AFG2,其中AFB1 被公认为是主要的有毒物质,从2010年版《中国药典》开始,就对部分中药规定:AFB1不得过5 μg/kg,AF(B1+B2+G1+G2) 总量不得过10 μg/kg [1]。目前,关于直服丹参粉中真菌毒素含量测定的研究鲜有报道,而丹参粉配伍三七粉直接泡服已成为预防和治疗心脑血管疾病的常用方式,因此对丹参粉中黄曲霉毒素的含量水平进行监测对确保人民用药安全具有十分重要的意义。
1 仪器与材料
1.1 仪器 LC-20A液相色谱仪(包括 LC-20AT 型四元泵、 SIL-20A 型进样器、RF- 20A xs型荧光检测器、CTO-20A 型柱温箱,日本岛津株式会);SDLA-B-1101型超纯水机(重庆圣德利医疗器械研究有限公司);Waters固相萃取装置(美国沃特世公司);AB204S型天平(万分之一,瑞士METTLER TOLEDO公司);SIGMA4-16S离心机(德国SIGAM公司);T25 digital ULTRA-TURRAX分散机(德国IKA公司)。
1.2 材料 乙腈、甲醇,均为色谱纯(DIKMA科技公司);AFB1 、AFB2、AFG1、AFG2混合对照品溶液浓度分别为0.93、0.30、0.93、0.35μg/mL(批号:610001-201703,中国食品药品检定研究院)。黄曲霉毒素免疫层析亲和柱(Pribolab公司);水为超纯水。50批丹参粉样品购自重庆市不同区县的不同药店(S1丹参粉,重庆康迪药业有限公司,批号180701;
S2丹参粉,成都康美药业生产有限公司,批号181201331;
S3丹参粉,云南向辉药业有限公司,批号F20190405;
S4丹参,成都市祺隆中药饮片有限公司/包装打粉;
S5丹参,四川圣上大健康药业有限公司/包装打粉;
S6丹参,四川圣上大健康药业有限公司/包装打粉;
S7丹参,四川/散装打粉;
S8丹参粉,重庆康迪药业有限公司,批号181101;
S9丹参粉,太极集团四川绵阳制药有限公司,批号1805002;
S10丹参粉,云南向辉药业有限公司,批号F20190108;
S11丹参粉,东方红西洋参药业(通化)股份有限公司,批号190301;
S12丹参粉,云南七丹药业股份有限公司,批号1903004;
S13丹参粉,太极集团四川绵阳制药有限公司,批号1707002;
S14丹参粉,太极集团四川绵阳制药有限公司,批号1905001;
S15丹参粉,重庆慧远药业有限公司,批号181201;
S16丹参粉,北京深港药业有限公司,批号1801006;
S17丹参粉,云南向辉药业有限公司,批号20190108;
S18丹参,成都科欣药业有限公司,批号180401/包装打粉;
S19丹参,四川圣上大健康药业有限公司,批号180801/包装打粉;
S20丹参粉,四川国强中药饮片有限公司,批号181001;
S21丹参,四川同正堂中药饮片有限公司,批号181001/包装打粉;
S22丹参粉,安徽省泽华国药饮片有限公司,批号181001;
S23丹参,希美(重庆)制药有限公司,批号190401/包装打粉;
S24丹参粉,云南向辉药业有限公司20180522;
S25丹参粉,上医正念堂(成都)医药科技有限公司,批号190601;
S26丹參粉,北京同仁堂(安国)中药饮片有限责任公司,批号1904008;
S27丹参粉,黄冈金贵中药产业发展有限公司,批号8050103;
S28丹参,安徽协和成药业饮片有限公司,批号19030406/包装打粉;
S29丹参,成都科欣药业有限公司,批号180401/包装打粉;
S30丹参粉,洪雅县瓦屋山药业有限公司,批号181001;
S31丹参,四川中江/散装打粉;
S32丹参,山东,批号180901/包装打粉;
S33丹参,四川中江/散装打粉;
S34丹参,四川中江/散装打粉;
S35丹参,四川中江/散装打粉;
S36丹参粉,成都康美药业生产有限公司,批号181102011;
S37丹参粉,成都康美药业生产有限公司,批号181201851;
S38丹参粉,重庆康迪药业有限公司,批号180301;
S39丹参粉,通化德济参药业有限公司,批号20180801;
S40丹参粉,成都康美药业生产有限公司,批号180700061;
S41丹参粉,成都康美药业生产有限公司,批号181201331;
S42丹参粉,云南向辉药业有限公司,批号F20180140;
S43丹参粉,重庆康嘉药业有限公司,批号190201;
S44丹参粉,重庆康迪药业有限公司,批号180901;
S45丹参粉,云南七丹药业股份有限公司,批号1901001;
S46丹参粉,云南七丹药业股份有限公司,批号1906010;
S47丹参粉,云南向辉药业有限公司,批号F20190405;
S48丹参粉,太极集团四川绵阳制药有限公司,批号1812004;
S49丹参粉,湖北金贵中药饮片有限公司,批号A190101;
S50丹参粉,重庆康迪药业有限公司,批号180601)。
2 方法与结果
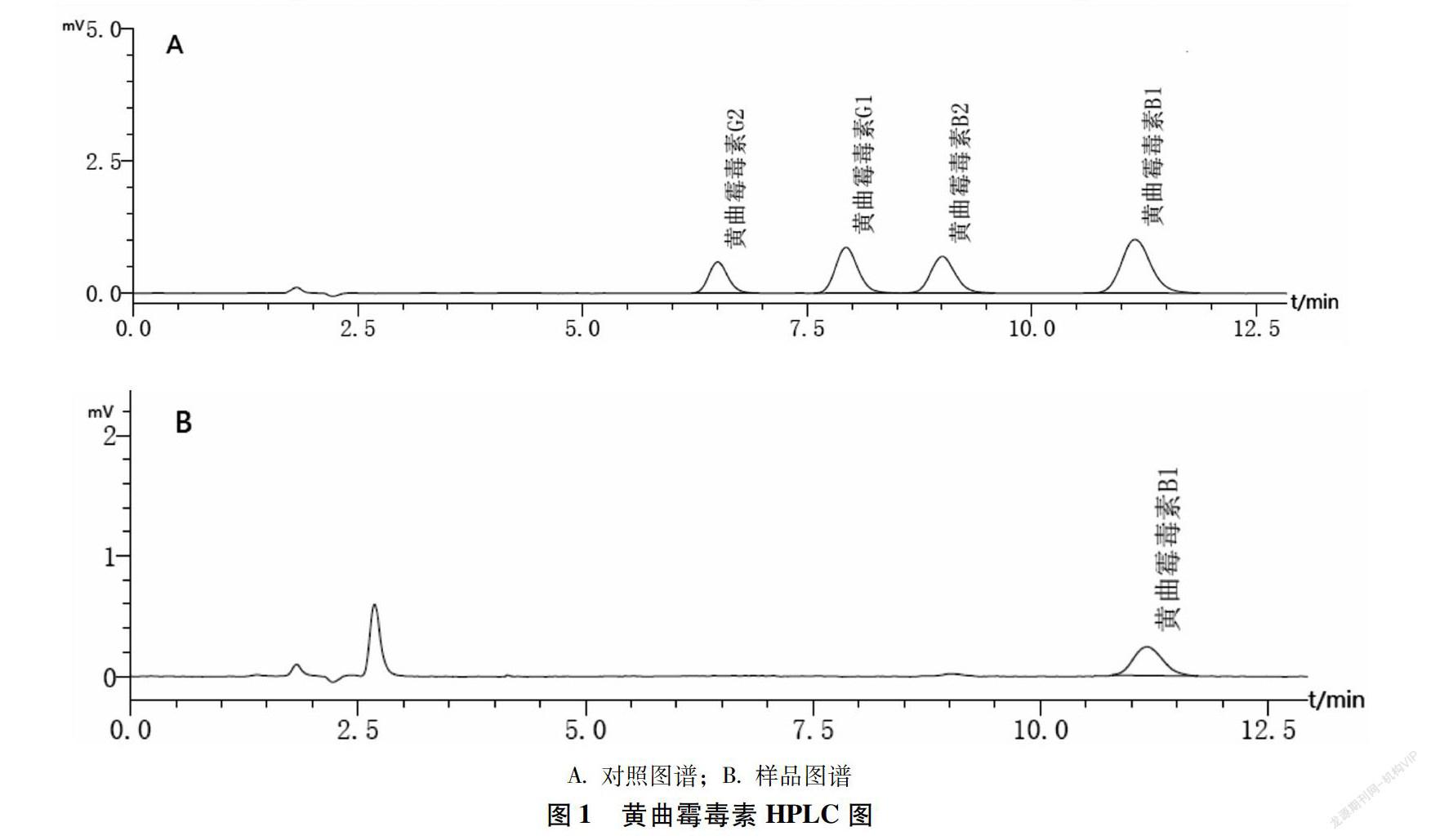
2.1 色谱条件 色谱柱:Inertsustain C18(4.6 mm× 150 mm,5 μm);柱温:35 ℃;其余按《中国药典》2015年版四部通则2351黄曲霉毒素测定法中规定设置[6]。在上述色谱条件下,AFB1 、AFB2、AFG1、AFG2色谱峰分离度>1.5(如图1所示)。
2.2 对照品溶液配制 精密量取黄曲霉毒素混合对照品溶液100 μL于50 mL量瓶中,用甲醇定容至刻度,摇匀,精密吸取不同体积溶液,注入液相色谱仪,测定峰面积。
2.3 样品溶液制备 取丹参粉10 g,精密称定,按《中国药典》2015年版四部通则2351黄曲霉毒素测定法中供试品溶液制备的方法进行处理[6]。精密吸取各供试品溶液20 μL,注入液相色谱仪,测定峰面积。
2.4 方法学考察
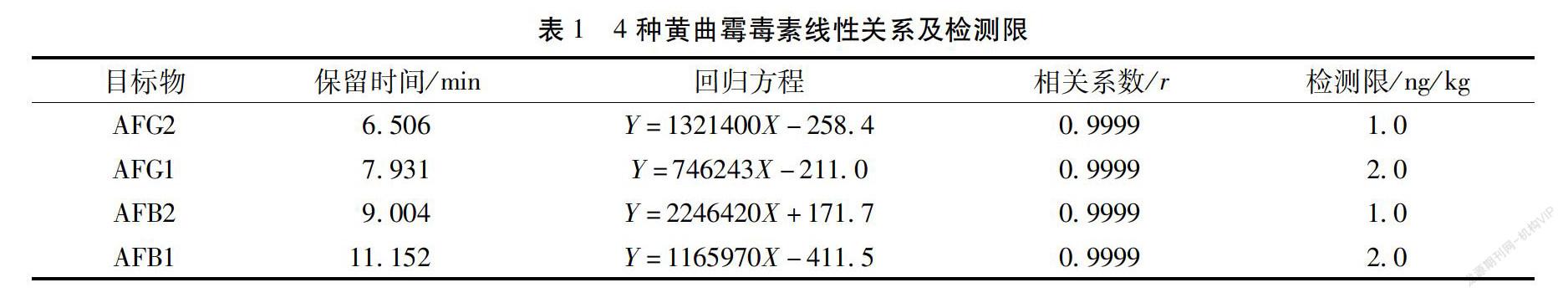
2.4.1 线性关系及检测限 分别精密吸取上述混合对照品溶液5、10、15、20、25 μL,注入液相色谱仪,测定峰面积,以峰面积为纵坐标,进样量为横坐标,绘制标准曲线,结果见表1。由结果可知,AFB1、AFB2、AFG1、AFG2进样量分别在9.3~46.5 pg、3.0~15.0 pg、9.3~46.5 pg、3.5~17.5 pg范围内线性关系良好。在空白基质中依次加入较低浓度的混合对照品溶液后进行测定,以每种化合物的3倍信噪比(S/N=3)确定方法的检出限。结果见表1。
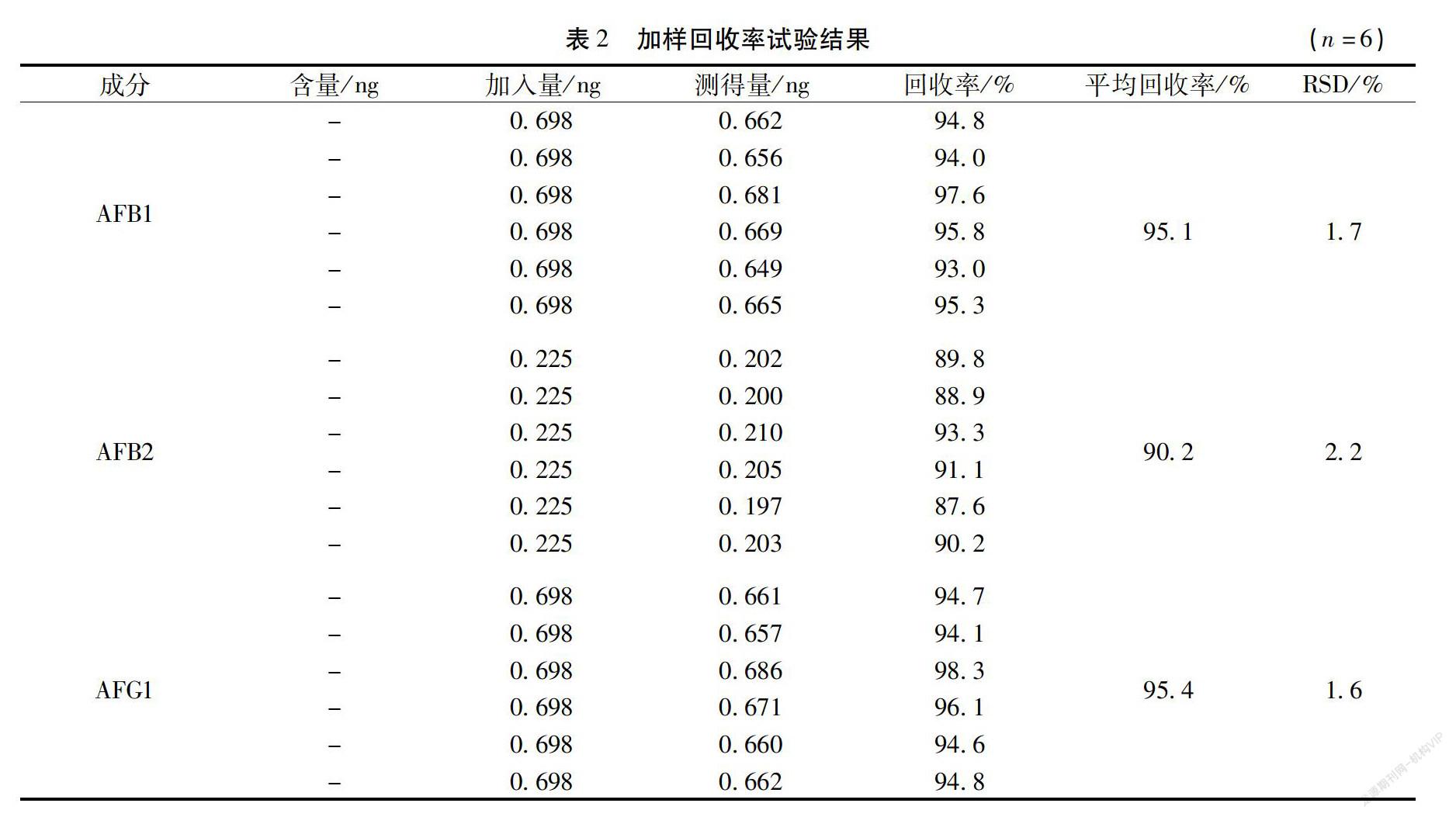
2.4.2 加样回收率试验及精密度 精密称取已知含量(AFB1、AFB2、AFG1、AFG2均未检出)的丹参粉6份,每份约5 g,精密加入混合对照品溶液0.375 mL,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,计算加样回收率,AFB1 、AFB2、AFG1、AFG2的平均回收率分别为95.1%、90.2%、95.4%、93.3%,RSD分别为1.7%、2.2%、1.6%、1.3%,表明方法精密度满足分析要求。结果见表2。
2.5 样品测定 取50批丹参粉,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,外标法定量。结果表明,50 批样品中有9批次检出AFB1,检出率为18.0%,但都低于药典部分药材限量标准,在这9批当中有两批检出AFG1,有1批检出AFG2,所有样品均未检出AFB2,结果见表3。
3 讨论
《中国药典》2015年版四部通则2351黄曲霉毒素测定法中的色谱条件,只规定了色谱柱的类型,没有规定色谱柱的品牌、型号,该试验考察了Diamonsil C18 柱、中普红C18柱、Agilent ZORBAX SB-C18柱和Inertsustain C18柱对黄曲霉毒素分离效果的影响,最终选取Inertsustain C18柱(4.6 mm× 150 mm,5 μm),在此色谱柱条件下,黄曲霉毒素峰形良好,分离度大于1.5。该试验采用的方法操作步骤简便、快速灵敏、重现性好,适用于大批量丹参粉中黄曲霉毒素的快速检测。
丹参粉不仅可以治疗疾病,还有养生保健的功效,很多心脑血管病患者每年都会直接泡服大量丹参粉。虽然该试验检测出AFB1的9批样品均符合药典限量标准,但AFB1性质稳定,耐高温,不易分解,容易在人体内积蓄,长期服用含有AFB1的丹参粉,很有可能引起身体不适,甚至会有患癌症的风险,而《中国药典》2015年版一部中丹参的检验项目未包含黄曲霉毒素,为提高丹参粉的质量,保证人民用药安全,应加强对丹参粉中黄曲霉毒素的监控。分析结果发现,药厂生产的丹参粉黄曲霉毒素含量较低,可能与其经过专业设备加工消毒后密封包装有关[7-8],但这类产品价格昂贵,大部分居民都是购买丹参后,自己打粉,没有消毒灭菌,储存过程中经常暴露在空气中,在相对湿度较高时,很容易滋生微生物,甚至产生毒素,严重威胁老百姓的身体健康。针对这一情况,应做更进一步的研究,以期为人民群众的用药安全保驾护航。
参考文献
[1]国家药典委员会. 中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:76.
[2]王文丽,徐晖,陈慧芝,等. 15种中药材表面真菌污染的分离与分子鉴定[J]. 中国中药杂志,2013(38):1910-1914.
[3]王铁霖,关巍,孙楷,等. 丹参常见病害的病原、发病规律及综合防治[J]. 中国中药杂志,2018,43(11):2402-2406.
[4]谭婧,郑润生,王文丽,等. 中药饮片中黄曲霉毒素和玉米赤霉烯酮的液質联用检测分析[J].时珍国医国药, 2012(23): 2469-2472.
[5]郭丽敏, 段启, 刘涛. HPLC法测定制何首乌中黄曲霉毒素B1、B2、G1、G2的含量[J]. 甘肃医药, 2015,34(8): 618-621.
[6]国家药典委员会. 中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015.
[7]张振凌,张爱婷,张红伟,等. 加热炮制对中药饮片黄曲霉毒素B1含量的影响[J]. 中华中医药杂志,2009,24(4):527-529.
[8]张超,马越,赵晓燕,等. 热处理对玉米粉中黄曲霉毒素B1含量变化的影响[J]. 中国粮油学报,2012,27(11):10-13.
(收稿日期:2021-03-05 编辑:刘 斌)
