中国南海软珊瑚附生真菌Acremonium sp. SCSIO41216 的次级代谢产物研究
2021-12-04张涵谭雁鸿杨斌刘永宏李云秋
张涵, 谭雁鸿, 杨斌, 刘永宏, 李云秋
1. 桂林医学院, 广西 桂林 541004;
2. 中国科学院南海海洋研究所热带海洋生物资源与生态重点实验室, 广东 广州 510301;
3. 南方海洋科学与工程广东省实验室(广州), 广东 广州 511457
海洋生物的生存环境具有高压、高盐度、寡营养、低温但相对恒温(火山口附近有高温、极地地区还有超低温)、有限的光照和有限的含氧量等特点。生存环境决定了海洋生物在新陈代谢等方面具有显著的特点, 造成海洋生物次级代谢的途径和酶反应机制与陆地生物有许多不同之处, 使海洋生物成为资源丰富、保存完整、最具有新药开发潜力的新领域(Shao et al, 2010)。由于许多海洋天然产物在结构上与微生物天然产物相同或极其相似, 共附生于海洋无脊椎动物的微生物被认为可能是这些化合物的真正生产者(Blunt et al, 2018)。目前据文献报道, 珊瑚来源的真菌代谢产物不仅具有化学结构多, 还具有生物活性性的多样性。
枝顶孢属真菌分布广泛, 代谢产物结构丰富且表现出广泛的生物学活性: 包括抗微生物、细胞毒性、抗肿瘤、免疫抑制、抗氧化、抗炎、抗疟疾、植物毒性、杀虫和酶抑制活性等, 是一个具有巨大潜力的资源宝库 (Xie et al, 2010; Tian et al, 2017)。Chen 等(2018)从海绵来源的枝顶孢属真菌中分离得到化合物(R)-4-((R)-hydroxy(4-nitrophenyl)methyl)oxazolidin-2-one (compounds 2)对棉铃虫具有一定的杀虫活性, LC50值为0.56±0.03mg·mL-1。Olesya I.Zhuravleva 等从海参来源的枝顶孢属真菌中分离得到化合物virescenoside A 可抑制尿素酶活性, 其IC50为138.8μmol·mL-1; 化合物Virescenoside Z10可显著降低脂多糖(lipopolysaccharide)刺激的巨噬细胞中的活性氧(reactive oxygen species, ROS)生成,在浓度为10μmol·L-1时可使巨噬细胞ROS 含量降低45% (Zhuravleva et al, 2019)。但目前国内外对软珊瑚来源的枝顶孢属真菌的报道较少。
1 材料与方法
1.1 仪器与试剂
主要仪器包括旋转蒸发仪(EYELAN-1100V-W型,日本东京理化株式会社), AV-500、AV-700 核磁共振仪(德国Brucker 公司), HITACHI L-2400 半制备HPLC(日本日立公司), ZYJ-S 型超净工作台(苏州净化设备有限公司), 中压制备柱色谱仪(Buchi 公司产品 C615/605), HR-ESM-MS (德国Brucker 公司)。主要试剂包括薄层色谱硅胶(青岛海洋化工厂), 10~40目和100~200 目正相硅胶(烟台江友硅胶开发有限公司), 反相硅胶(Merck 公司)及分析纯级化学试剂(广州化学试剂厂和天津市富宇精细化工有限公司)等。
1.2 菌株发酵培养
菌株Acremoniumsp. SCSIO41216 共附生软珊瑚为短指软珊瑚(Sinulariasp.), 采集地点为海南省三沙市七连屿附近海域(16°55′10.0″N, 112°20′5.5″E),采集时间为2015 年5 月。
该菌株通过DNA 扩增和ITS 区序列与GenBank数据库比较鉴定为枝顶孢菌属(Aremoniumsp.)编号SCSIO41216, 保存于中国科学院南海海洋研究所热带海洋生物资源与生态重点实验室。
将保藏于4℃的菌株接种到PDA 琼脂固体斜面培养基上, 置于28℃培养箱培养7d。用接种针挑取适量孢子, 接种到含 15mL MB 培养液(麦芽粉15g,海盐2.5g, 蒸馏水1000mL, pH=7.4~7.8)的150mL 三角烧瓶中, 在25℃, 转速180r·min-1摇床条件下培养3d。将培养好的种子液分别接种到40 瓶灭菌后的大米培养基(大米200g, 海盐2.5g, 蒸馏水250mL)中静置培养60d。
1.3 提取与分离
发酵完毕后菌株用两倍体积丙酮浸泡2d, 然后将大米捣碎, 超声15min, 用8 层纱布进行减压过滤,滤液减压浓缩以除去丙酮。然后再用两倍体积乙酸乙酯萃取3 次, 浓缩后得到乙酸乙酯相粗浸膏。滤渣继续用乙酸乙酯提取3 遍, 浓缩后合并以上乙酸乙酯部分得总粗浸膏(120g), 粗浸膏采用中压色谱进行分离, 用100~200 目硅胶拌样, 流动相为石油醚∶乙酸乙酯(V:V= 100 : 0 ~ 1 : 1, 流速50mL·min-1)梯度洗脱得到第一部分, 再用石油醚∶乙酸乙酯∶甲醇(V:V:V= 20 : 20 : 1 ~ 0 : 0: 100,流速50mL·min-1)梯度洗脱得到第二部分。两部分通过薄层色谱法(TLC)检识合并得11 个馏分。其中Fr.6 经反相中压色谱(ODS) (VMeOH:VH2O= 20 : 80 ~100 : 0)梯度洗脱得8 个子馏分, Fr.6-2 经半制备液相(VMeOH:VH2O= 55 : 45)得到化合物3 (29.1mg),Fr.6-5 经半制备液相(VMeOH:VH2O= 60 : 40)得到化合物5 (13.7mg)。Fr.7 经反相中压色谱(ODS)(VMeOH:VH2O= 20 : 80 ~ 100 : 0)梯度洗脱得6 个馏分, Fr.7-4经半制备液相(VMeOH:VH2O= 56 : 44)得化合物2(6.4mg)。Fr.10 经反相中压色谱(ODS)(VMeOH:VH2O=20 : 80 ~ 100 : 0)梯度洗脱得4 个馏分, Fr.10-2 经半制备液相(VMeOH:VH2O=49 : 51)得化合物4 (4.6mg),Fr10-3 经半制备液相(VMeOH:VH2O= 54 : 46)得化合物 1 (5.3mg)其中 Fr.11 经反相中压色谱(ODS)(VMeOH:VH2O= 20 : 80 ~ 100 : 0)梯度洗脱得5 个子馏分, Fr.10-3 经半制备液相(VMeOH:VH2O= 60 : 40)得到化合物6 (5.3mg), Fr.10-3 经半制备液相(VMeOH:VH2O= 26 : 74)得到化合物7 (24.5mg)。化合物1~7结构如图1。
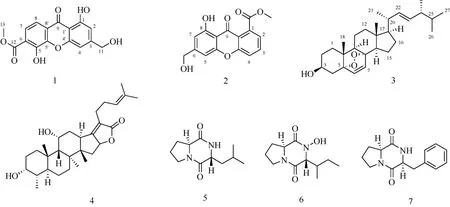
图1 化合物1—7 的结构Fig. 1 The chemical structures of compounds 1-7 from Acremonium sp.
2 结构鉴定
2.1 化合物1
黄色针状晶体, 可溶于甲醇、氯仿等有机溶剂,熔点204℃,1H-NMR (700 MHz, CD3OD)δ: 7.36 (1H,d,J= 7Hz, H-8), 7.25 (1H, d,J= 7Hz, H-7), 6.93(1H,brs, H-4), 6.68 (1H, brs, H-2), 4.66 (2H, s, H-11), 3.95(3H, s, OCH3);13C-NMR (175 MHz,CD3OD)δ: 182.4(C-9), 172.4 (C-12), 162.6 (C-1), 159.9 (C-4′), 157.6(C-3), 153.3 (C-5), 148.6(C-5′), 130.0 (C-7), 120.6(C-8), 119.1 (C-6), 118.2 (C-8′), 108.3 (C-2), 107.9(C-1′), 105.2 (C-4), 64.5(C-11), 52.9 (OCH3)。核磁数据与文献对照基本一致, 故化合物 1 鉴定为fischexanthone (Tan et al, 2012)。
2.2 化合物2
黄色非晶形固体, 可溶于甲醇、氯仿等有机溶剂,1H-NMR (700 MHz,CD3OD)δ: 7.88 (1H, dd,J=6.9Hz, H-3), 7.69 (1H, dd,J= 6.9, 2.6Hz, H-2), 7.38(1H, dd,J= 6.9, 2.6Hz, H-4), 7.04 (1H, s, H-5), 6.80(1H, s, H-7), 4.70 (2H, s, H-11), 3.98 (3H, s, H-13);13C-NMR (175 MHz, CD3OD)δ: 181.9 (C-9), 171.4(C-11), 162.8 (C-8), 157.5 (C-4′), 157.4 (C-5), 154.8(C-6), 134.8 (C-1), 123.9 (C-4), 120.7 (C-4), 118.4(C-8′), 109.1 (C-7), 108.7 (C-8′), 105.4 (C-5), 64.3(C-11), 53.5 (C-12)。核磁数据与文献对照基本一致,故化合物 2 鉴定为 sydowinin A (Goddard et al,2014)。
2.3 化合物3
白色不定型粉末, 可溶于甲醇、氯仿等有机溶剂, [ ɑ]25D-2.8 (c= 0.001, MeOH),1H-NMR (700 MHz,CDCl3) δ: 6.50 (1H, d,J=8.5Hz, H-7), 6.24 (1H, d,J=8.5Hz, H-6), 5.20 (1H, dd,J=15.3, 7.4Hz, H-23),5.15 (1H, dd,J=15.3, 8.3Hz, H-21), 3.92-3.98 (1H, m,H-3), 0.99 (3H, dd,J=6.6Hz, H-21), 0.90 (3H, d,J=6.8Hz, H-28), 0.87 (3H, s, H-19), 0.80-0.81 (9H, m,H-27, H-18, H-26);13C-NMR (175 MHz, CDCl3) δ:135.6 (C-6), 135.3 (C-22), 132.4 (C-23), 130.9 (C-7),82.3 (C-5), 79.6 (C-8), 66.6 (C-3), 56.3 (C-17), 51.8(C-14), 51.2 (C-9), 44.7 (C-13), 42.9 (C-24), 39.9(C-20), 39.5 (C-12), 37.1 (C-4), 37.0 (C-10), 34.8 (C-1),33.2 (C-25), 30.2 (C-2), 28.8 (C-16), 23.5 (C-11), 21.0(C-21), 20.8 (C-15), 20.1 (C-27), 19.8 (C-26), 18.3(C-19), 17.7 (C-28), 13.0 (C-18)。核磁数据与文献对照基本一致, 故化合物 3 鉴定为(22E)-5α,8α-epidioxyergosta-6,22-dien-3β-ol (Hybelbauerová et al, 2008)。
2.4 化合物4
白色晶体, 可溶于甲醇、氯仿等有机溶剂, 熔点112℃,+12.3 (c= 0.001, MeOH),1H-NMR (700 MHz, CD3OD)δ: 5.14 (1H, m, H-24), 5.05 (1H, dd,0=4.3, 11.0, H-16), 4.33 (1H, d,J= 2.3, H-11),3.65-3.66 (2H, m, H-3, H-13), 2.30-2.39 (3H, m,Ha-23, Ha-15, Ha-1), 2.13-2.25 (4H, m, Hb-23, H-22,H-5), 2.04 (1H, dt,J= 3.0, 14Hz, Ha-12), 1.80-1.88(2H, m, Ha-2, Hb-12), 1.66-1.74 (6H, m, H-27, Ha-7,Ha-6, Hb-2), 1.60 (3H, s, H-26), 1.46-1.53 (6H, m,H-30, H-9, H-4, Hb-1), 1.13-1.19 (3H, m, Hb-15, Hb-7,Hb-6), 0.99 (3H, s, H-19), 0.91 (3H, d,J=6.8, H-28),0.82 (3H, s, H-18);13C-NMR (175 MHz, CD3OD)δ:178.9 (C-21), 173.4 (C-17), 133.8 (C-25), 124.4(C-20), 124.0 (C-24), 83.9 (C-16), 72.4 (C-3), 68.1(C-11), 56.7 (C-14), 51.7 (C-9), 42.1 (C-8), 39.5(C-13), 38.5 (C-10), 38.0 (C-4), 36.7 (C-5), 34.9(C-15), 33.3 (C-12), 32.3 (C-7), 31.0 (C-1), 30.8 (C-2),28.4 (C-22), 25.9 (C-27), 24.9 (C-23), 24.1 (C-19),23.0 (C-30), 22.6 (C-6), 20.3 (C-18), 17.8 (C-26), 16.5(C-28)。核磁数据与文献对照基本一致, 故化合物4鉴定为 16-O-去乙酰基夫西地酸内酯(Rastrup-Andersen et al, 2002)。
2.5 化合物5
白色晶体, 可溶于甲醇、氯仿等有机溶剂, 熔点137.6℃, [ ɑ]25D-29.3 (c= 0.001, MeOH),1H-NMR(500 MHz, CD3OD)δ: 4.26 (1H, t,J= 1.2, 6.8, H-9),4.12(1H, m, H-6), 3.52-3.49 (2H, m, H-3), 2.27-2.33(1H, m, Ha-5), 1.96-1.83 (3H, m, H-4, Hb-5),2.06-1.96 (2H, m, Ha-10, H-11), 1.54-1.48 (1H, m,Hb-10), 0.97 (3H, d,J= 3.15, H-12), 0.95 (3H, d,J=3.0, H-13);13C-NMR (125 MHz, CD3OD)δ: 172.8(C-1), 168.9 (C-7), 60.3 (C-6), 54.6 (C-9), 46.4 (C-3),39.4 (C-10), 29.1 (C-5), 25.8 (C-11), 23.6 (C-4), 23.3(C-12), 22.2 (C-13)。核磁数据与文献对照基本一致,故化合物5 鉴定为环-(S)-脯氨酸-(R)-亮氨酸 (Yang et al, 2009)。
2.6 化合物6
白色固体, 可溶于甲醇、氯仿等有机溶剂, [ ɑ]25D-15.2 (c= 0.001,MeOH),1H-NMR (500 MHz, CD3OD)δ: 4.20 (1H, t,J= 6.5, H-9), 4.07 (1H, brs, H-6),3.60-3.54 (1H, m, Ha-3), 3.53-3.57 (1H, m, Hb-3),2.36-2.30 (1H, m, Ha-5), 2.20-2.13 (1H, m, H-10),2.05-2.00 (1H, m, Ha-4), 1.96-192 (2H, m, Hb-4, Hb-5),1.49-1.41 (1H, m, Ha-11), 1.36-1.30 (1H, m, Hb-11),1.08(3H, d,J= 7.2, H-12), 0.93 (3H, t,J= 7.4);13C-NMR (125 MHz, CD3OD)δ: 172.5 (C-1), 167.6(C-7), 61.3 (H-6), 60.0 (H-9), 46.2 (C-3), 37.1 (C-11),29.6 (H-5), 25.5 (C-10), 23.3(C-4), 15.6 (C-12), 12.6(C-13)。核磁数据与文献对照基本一致, 故化合物6鉴定为环-(S)-脯氨酸-8-羟基-(R)-异亮氨酸 (Yang et al, 2009)。
2.7 化合物7
黄色固体, 可溶于甲醇、氯仿等有机溶剂, [ ɑ]25D-27.4 (c= 0.001, MeOH),1H-NMR (500 MHz,CD3OD)δ: 7.32-7.24 (5H, m, H-2′, H-3′, H-4′, H-5′,H-6′), 4.47 (1H, t,J= 5.5, 4Hz, H-9), 4.10 (1H, dd,J= 9.5, 6.5Hz, H-6), 3.59-3.53 (2H, m, H-3), 3.42-3.37(1H, m, Ha-10) ,3.20 (1H, t,J= 5Hz, Hb-10),2.14-2.08 (1H, m, Ha-5), 1.86-1.79 (2H, m, H-4),1.25-1.17 (1H, m, Hb-5);13C-NMR (125 MHz, CD3OD)δ: 170.9 (C-7), 166.9 (C-1), 137.4 (C-1′) , 131.0(C-2′), 129.5 (C-3′), 128.1 (C-4′), 60.1 (C-6), 57.7(C-9), 46.0 (C-3), 38.2 (C-10), 29.4 (C-5), 22.8(C-4)。核磁数据与文献对照基本一致, 故化合物7 鉴定为环-(L)-脯氨酸-(L)-苯丙氨酸 (Furtado et al, 2005)。
3 讨论与结论
本文对中国南海软珊瑚来源真菌Acremoniumsp. SCSIO41216 的次级代谢产物进行了分离鉴定,共分离出 7 个单体化合物: fischexanthone (1);sydowinin A (2); (22E)-5α, 8α-epidioxyergosta-6,22-dien-3β-ol (3); 16-O-去乙酰基夫西地酸内酯 (4);环-(S)-脯氨酸-(R)-亮氨酸 (5); 环-(S)-脯氨酸-8-羟基-(R)-异亮氨酸 (6); 环(L)-脯氨酸-(L)-苯丙氨酸(7)。化合物1—7 均首次从海洋软珊瑚来源的枝顶孢属真菌中分离获得。
根据文献报道, 化合物1 对禾谷镰刀菌具有中等的抗菌活性, MIC 值为474.68μmol·L-1(Wang et al,2020)。化合物2 对人结肠癌细胞, 神经母细胞瘤细胞有细胞毒性, IC50值为124.30 和117.80μmol·L-1(Hayashi et al, 2018)。化合物3 显示出许多有前途的生物学特性, 包括免疫抑制剂、抗疟原虫、抗细菌、抗病毒、抗炎, 以及抗肿瘤活性(Hybelbauerová et al,2008)。化合物4 对金黄色葡萄球菌有抑制作用, 抑制率为48.64% (Salimova et al, 2018)。Yang 等(2009)使用MTT 法检测了化合物5 和6 对人肝肿瘤细胞(SGC-7901)、人胃肿瘤细胞(HepG2)、人卵巢肿瘤细胞(HeLa)进行了细胞毒活性测试, 结果表明化合物5 和6 对3 种肿瘤细胞均无活性。化合物7 对人食管肿瘤细胞(ECA-109)、人体宫颈肿瘤细胞(Hela-S3)和人胰腺肿瘤细胞(PANC-1)三种肿瘤细胞株表现出较弱的体外细胞毒性, 抑制率在50%~65%之间(Lin et al, 2020)。
通过以上研究可以发现, 该属真菌的次生代谢产物种类多样, 具有丰富的化学多样性。但关于海洋软珊瑚来源枝顶孢属真菌的报道较少, 本文丰富了海洋软珊瑚来源的枝顶孢属真菌代谢产物的多样性, 也说明了从枝顶孢属真菌次生代谢产物中挖掘出有独特活性的化合物的潜力巨大, 为后续药物先导化合物的发现与研究提供了参考。
