一种银耳固体饮料的开发及工艺优化*
2021-12-01欧亚龙许晓燕
周 州,罗 舒,宋 怡,欧亚龙,许晓燕
(四川省中医药科学院,四川 成都 610041)
银耳(Tremella fuciformis) 是一种药用价值极高的食药兼用真菌,既是天然功能食品,又是食品加工中的天然添加剂[1],有“菌中之冠”的美称。银耳多糖是重要的生物活性物质,可以通过激活免疫细胞来提高机体的免疫功能,使吞噬细胞吞噬能力提升,增加淋巴细胞活性从而提高其抗肿瘤、预防肠道疾病等功效[2]。银耳倍受消费者喜爱,因而近年来以银耳为原料研制的食品推陈出新,如银耳保健醋、银耳姜汁乳饮料、银耳饼干等[3-5]。
枸杞是众所周知的进补中药材,相关产品已经走入千家万户,受到消费者青睐。枸杞多糖是枸杞的主要生物活性成分,被证实具有保护生殖系统、免疫调节、延缓衰老、抗辐射及抗缺氧等功效[6]。郭华等[7]研究表明,枸杞多糖具有增进紫杉醇对人卵巢癌HO-8910PM细胞的抗癌能力。
《本草纲目》记载芦根有清热生津、除烦、止呕、利尿的功效。现代的研究表明,芦根中含有VB1、VB2、VC以及蛋白质、脂肪、碳水化合物、天冬酰胺等多种营养物质[8],同时芦根多糖具有抗氧化、抗结石、改善脂质代谢、保护肝脏肾脏等多种作用[9]。自古至今,民间常有芦根绿豆饮、芦根饮等自制保健饮品。
基于具有减缓女性卵巢早衰功能的临床试验组方,以组方中的主要原料银耳、枸杞、芦根为研究对象,制备了一种固体饮料,产品命名为卵复春。通过介绍该固体饮料制备工艺过程和稳定性试验结果,提供最佳提取工艺、浓缩方式、颗粒性质及稳定性结果,以期为相关功能食品的研究与生产提供参考。
1 材料与方法
1.1 材料与试剂
银耳、枸杞、芦根等中药材,购自四川千方中药饮片有限公司;D-无水葡萄糖标准品,批号为PS010303,购自成都普思生物科技股份有限公司。
1.2 仪器与设备
UV-2860s紫外可见分光光度计,尤尼柯(上海)仪器有限公;DZF-6020真空干燥箱,上海精宏实验设备有限公司;RE-52AA/52B旋转蒸发仪,上海亚荣生化仪器厂;JOYA-8000T喷雾干燥机,上海乔枫实业有限公司;KXH-101-2A电热鼓风干燥箱,上海科析试验仪器厂;AL104电子分析天平,梅特勒-托利多国际贸易(上海)有限公司;YP1201N电子称,上海精密科学仪器有限公司;SHH-250SD药品稳定性实验箱,上海建恒仪器有限公司。
1.3 方法
1.3.1 多糖测定方法
参考《中国药典》第一部(2015版)中硫酸蒽酮法进行测定[10]。
1.3.2 提取工艺
1) 单因素试验
浸泡时间:称定银耳等药材共66 g,加水660 mL,分别浸泡0、30 min、60 min、90 min后回流提取60 min,共2次。过滤,合并滤液,浓缩,定容至2 000 mL,测定总多糖含量。
料液比:称定银耳等药材共66 g,分别按料液比 1∶8、1∶10、1∶15、1∶20、1∶25 加水,浸泡 60 min后回流提取60 min,共2次。过滤,合并滤液,浓缩,定容2 000 mL测定总多糖含量。
提取时间:称定银耳等药材共66 g,加水660 mL,浸泡60 min后,按30 min、60 min、90 min、120 min回流提取,共2次,过滤,合并滤液,浓缩,定容至2 000 mL,测定总多糖含量。
提取次数:称定银耳等药材共66 g,加水660 mL,浸泡60 min后回流提取60 min,分别提取1次、2次、3次、4次。过滤,合并滤液,浓缩,定容至2 000 mL,测定总多糖含量。
2) 正交试验
基于单因素试验结果,选择料液比、提取时间和提取次数3个因素,各设3个水平,按照L9(34)正交表安排试验,见表1。
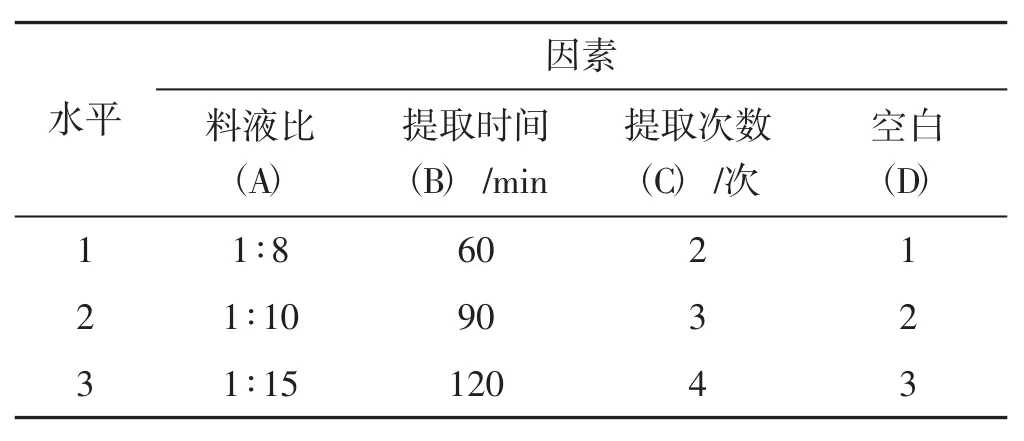
表1 提取工艺因素水平Tab.1 Factors and levels of extraction technology
如表1所示水平因素进行试验,以多糖和干膏得率为指标对提取工艺进行综合评价。
设定多糖含量权重为70%,干膏得率权重为30%,综合评分(Z,%) 计算公式为:
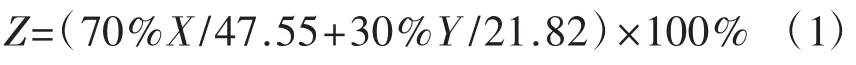
式中:X为多糖含量(mg·g-1);Y为干膏得率(%)。
1.3.3 除杂工艺
产品形式为方便食品,因此提取液仅需除去固体微粒。芦根、银耳、枸杞等药材采用水提法,有较多的杂质,因此采用高速离心法(16 000 r·min-1离心15 min)除去水提取液中的固体微粒体系。
1.3.4 浓缩工艺
药材提取液需要进一步浓缩成一定相对密度的浸膏。采用减压浓缩的方法,将提取液在浓缩温度70℃~80℃、真空度0.08 MPa~0.1 MPa的条件下进一步浓缩,制成一定相对密度1.08~1.10(60℃) 的浸膏[11-12]。
1.3.5 干燥工艺
药材浸膏采用中药常用的喷雾干燥方法[13]继续加工。该方法浸膏粘壁损失少、颗粒干燥。确定喷雾干燥工艺为:控制进料温度50℃~60℃,料液密度1.08〜1.10(60℃),进风温度为185℃〜195℃,出风温度为95℃〜105℃。
1.3.6 制粒
采用湿法制粒。加入47.4%麦芽糊精作为填充剂,以70%乙醇制备软材,20目筛制粒,60℃干燥至水分<4%,16目筛整粒。
1.3.7 临界相对湿度测定
分别取湿法制粒所得颗粒14份,每份约0.5 g,置于已干燥至恒重的称量瓶中,精密称定。将14份样品分为7组,每组各2份,分别为样品1和样品2。将称量瓶盖揭开,将7组样品分别置于7种不同相对湿度的干燥器中,25℃恒温培养箱中放置72 h。取出称量瓶,加盖后精密称定,计算吸湿百分率,绘制相对湿度曲线图。
吸湿百分率(H,%)计算公式为:
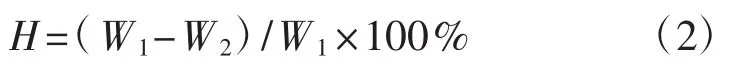
式中:W1表示吸湿前样品重量(mg);W2表示吸湿后样品重量(mg)。
1.3.8 颗粒流动性
采用测定休止角的方法考察颗粒流动性。具体方法为固定漏斗法:将3只漏斗竖直串连并固定于水平放置的坐标纸上方,测量漏斗口距坐标纸的距离;小心地将制成的颗粒沿漏斗壁倒入最上面的漏斗中,直到坐标纸上形成的颗粒圆锥体尖端接触到漏斗口为止。由坐标纸读出圆锥底部的直径(D),重复测定5次,休止角(tgα,°)计算公式为:

式中:H指漏斗口距坐标纸的距离(cm);D为圆锥底部直径(cm)。
1.3.9 包装
本品颗粒具有一定的吸湿性,采用铝塑复合袋进行包装。
1.3.10 稳定性试验
1) 加速试验
将中试产品置于加速条件,即温度(40±2)℃、相对湿度(75±2)%条件下放置6个月,每月取样检查。
2) 长期试验
将中试产品,置于室温条件下放置18个月,每月取样检查。
3) 感官评价法
取适量中试产品置于白色瓷盘中,在自然光下观察色泽和状态,嗅其气味;用温开水漱口后品其滋味。
4)水分及重金属测定方法
水分测定按照GB 5009.3食品安全国家标准食品中水分的测定[14]的方法进行;重金属铅、砷、汞的测定分别按照GB/T 5009.11食品安全国家标准食品中总砷及无机砷的测定[15]、GB 5009.12食品安全国家标准食品中铅的测定[16]和GB/T 5009.17食品安全国家标准食品中总汞及有机汞的测定[17]的方法进行。
5) 微生物测定
分别按照GB 4789.2食品安全国家标准 食品微生物学检验菌落总数测定[18]、GB 4789.3食品安全国家标准食品微生物学检验大肠菌群计数[19]、GB 4789.4食品安全国家标准食品微生物学检验沙门氏菌检验[20]、GB 4789.10食品安全国家标准 食品微生物学检验金黄色葡萄球菌检验[21]和GB 4789.15食品安全国家标准食品微生物学检验霉菌和酵母计数[22]进行测定。
2 结果与分析
2.1 提取工艺单因素试验及正交优化结果
2.1.1 提取工艺单因素试验结果
得到的总多糖含量以每克生药含量计,单因素试验结果详见表2。
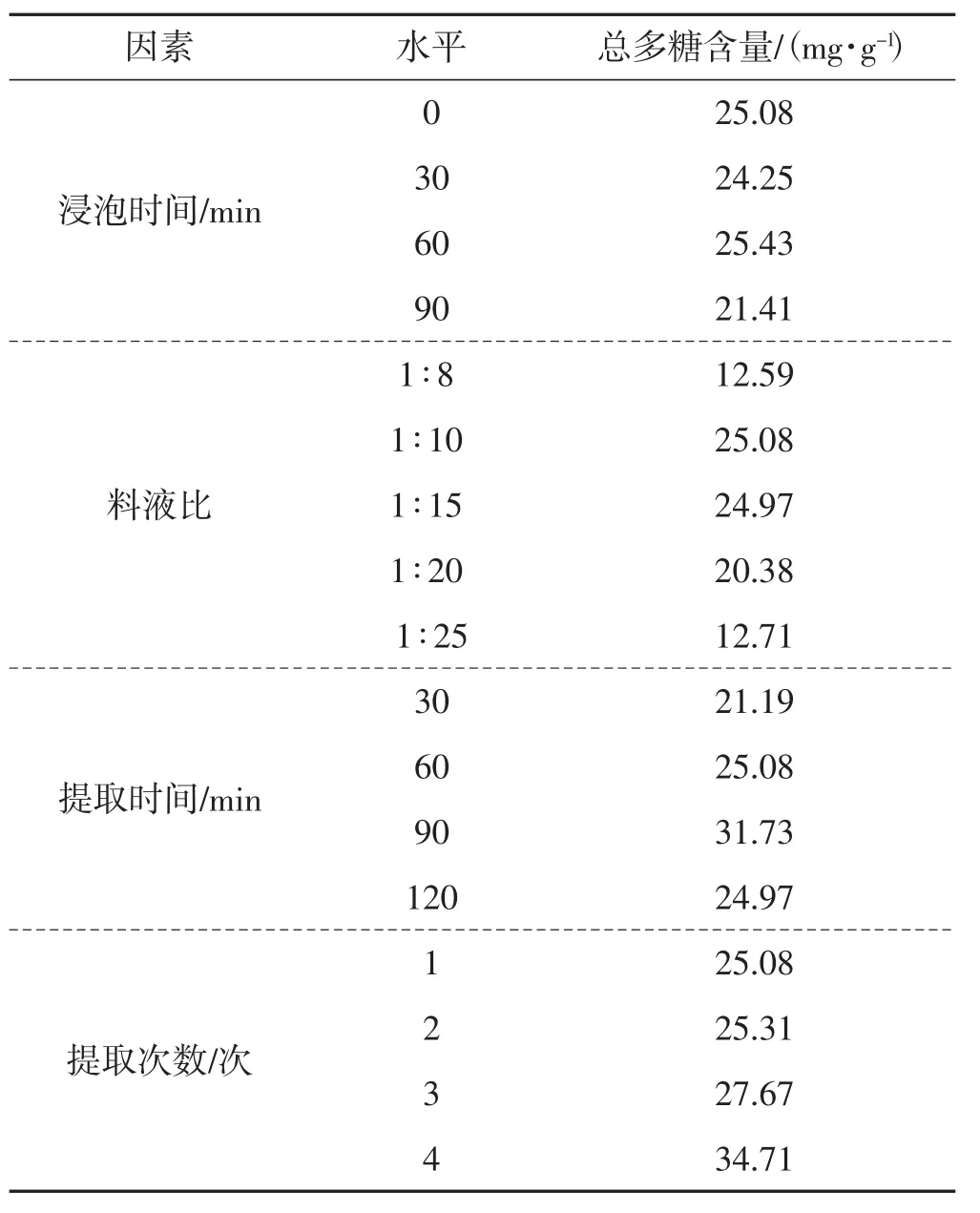
表2 提取工艺单因素试验结果Tab.2 Experiment results of extraction technology
由表2可知,浸泡时间为60 min时,总多糖得率最高;料液比为1∶10时,总多糖含量最高;提取90 min时,总多糖含量最高;随着提取次数的增加,总多糖含量逐渐增大。
2.1.2 提取工艺正交试验结果
正交试验结果见表3。

表3 提取工艺正交试验结果Tab.3 Orthogonal test results of extraction technology
如表3所示,影响芦根等药材提取的因素顺序为:A>C>B,3种因素的影响在方差上显著意义不大,通过直观分析可知以A3B1C2组合最佳。因B的影响差异较小,故验证试验采用A3B1C2和A3B1C3进行,试验结果见表4。
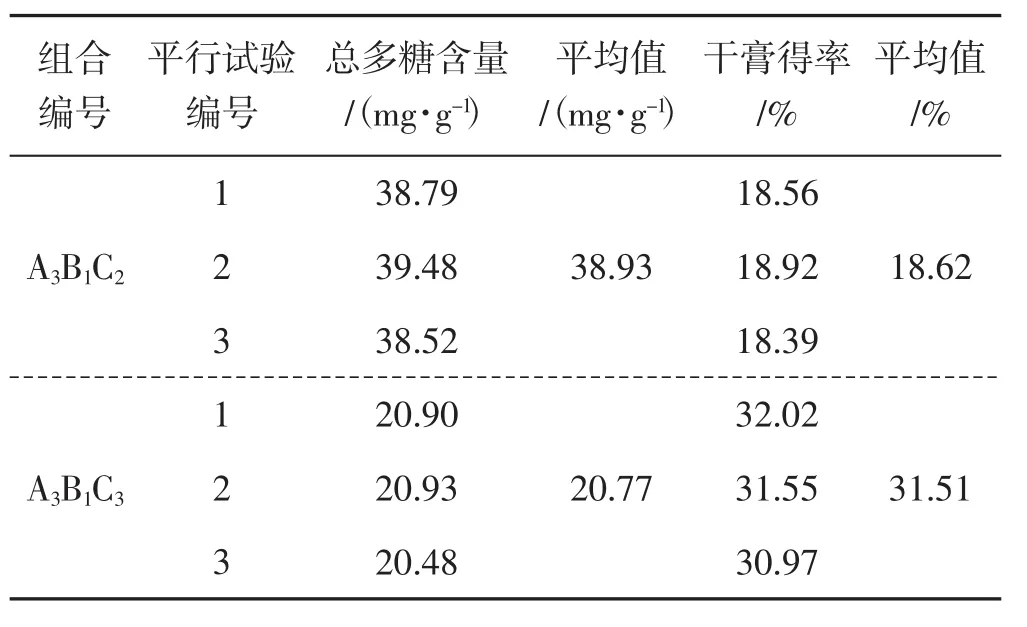
表4 验证试验结果Tab.4 Verification of experimental results
如表4结果显示,验证试验中A3B1C2组合最优。综合正交试验和验证试验结果,表明组合A3B1C2为最佳组合。
2.2 临界相对湿度的测定结果
临界相对湿度分析结果见表5,临界相对湿度曲线见图1。
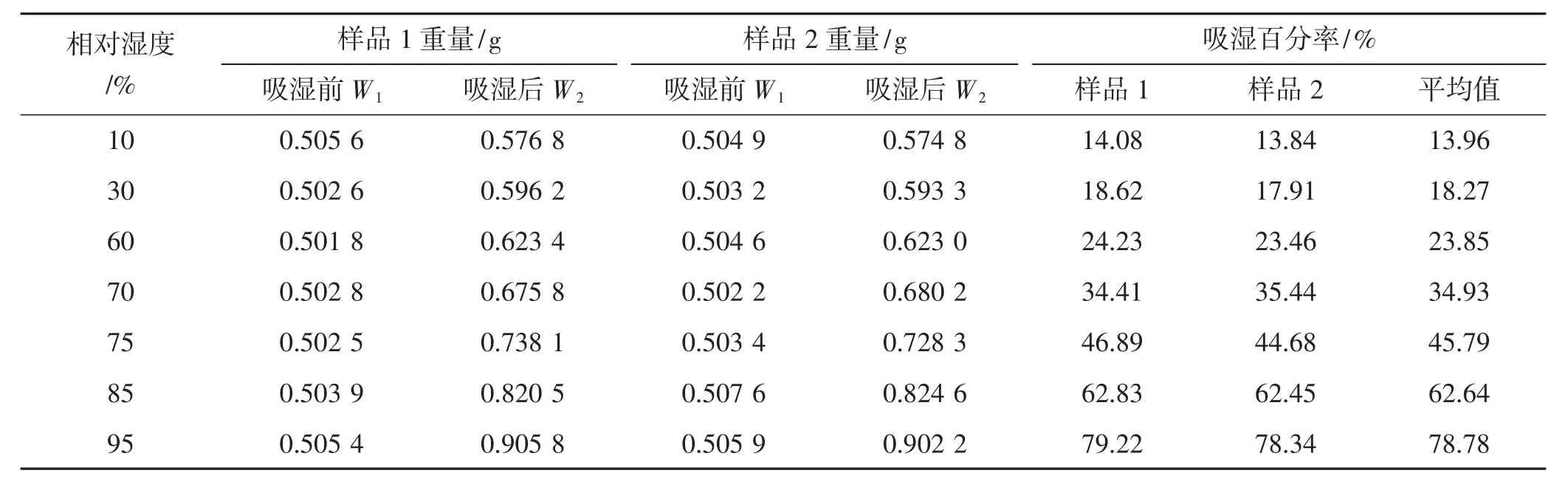
表5 各种相对湿度条件下颗粒吸湿结果Tab.5 Moisture absorption results of particles under various relative humidity conditions
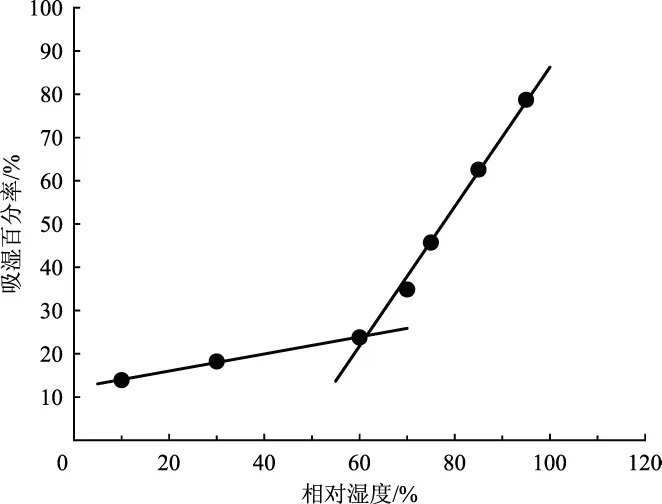
图1 临界相对湿度曲线图Fig.1 Critical relative humidity curve
由表5可知,随着相对湿度的提高,颗粒吸湿百分率有逐渐增大的趋势。由图1可知,本品颗粒的临界相对湿度为64.3%。因此推测本品在生产过程中,当室温为25℃时,要求生产车间(包括制粒车间和分装车间)的相对湿度应控制在60%以下。
2.3 颗粒流动性结果
试验得出3个样品的休止角分别为35.68°、35.72°、35.89°,平均值为35.76°。本品颗粒休止角小于40°,说明流动性良好。
2.4 稳定性试验结果
恒温恒湿加速试验结果见表6,长期试验结果见表7。
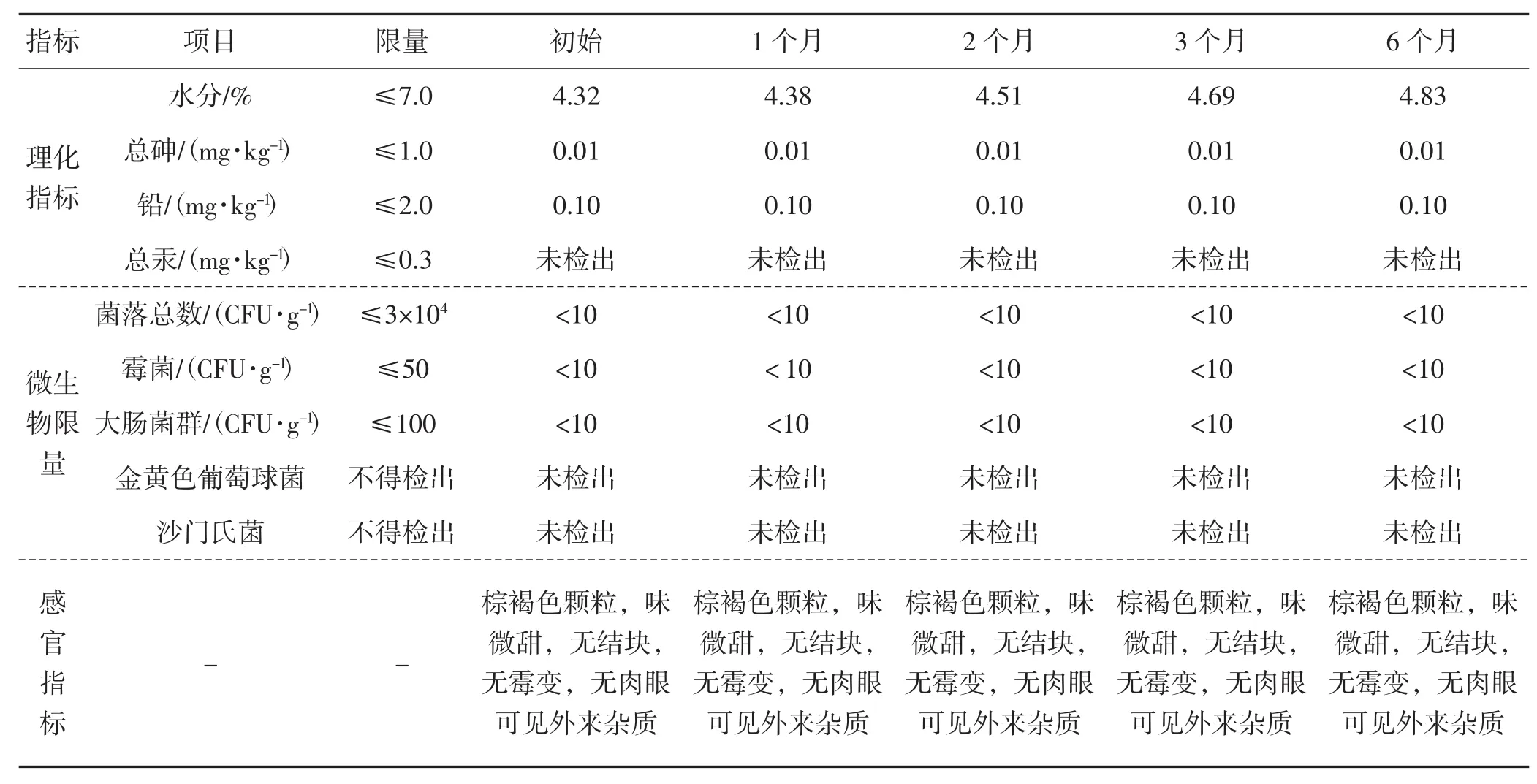
表6 恒温恒湿加速试验结果Tab.6 Constant temperature and humidity accelerated test results
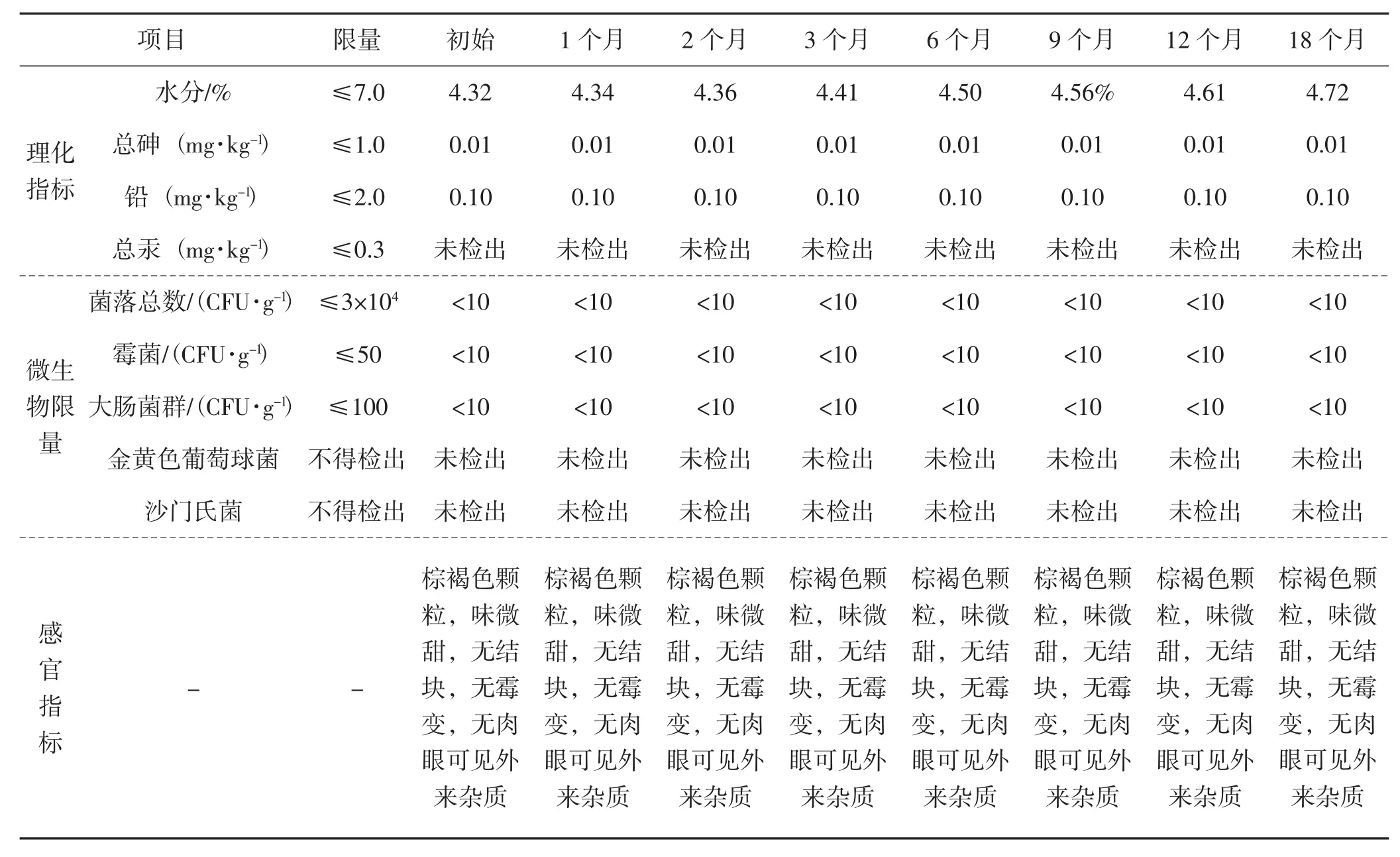
表7 长期稳定性试验结果Tab.7 Long-term stability test results
由表6、表7可以看出,制得的成品在加速期(起始时间、1个月后、2个月后、3个月后、6个月后)和长期(起始时间、1个月后、2个月后、3个月后、6个月后、9月个月后、12月个月后、18月个月后)的感官均良好,水分随着时间增加略有增长,但是均符合GB 5009.3国家标准规定。测试期内,成品重金属含量变化趋势一致,总砷含量为0.01 mg·kg-1,铅含量为 0.1 mg·kg-1,总汞含量为00.1 mg·kg-1。微生物限量变化趋势一致,菌落总数含量<1×10 CFU·g-1、霉菌<1×10 CFU·g-1、大肠杆菌<1×10 CFU·g-1,金黄色葡萄球菌和沙门氏菌均未检出。
3 结论
通过对芦根、银耳、枸杞等药材的提取工艺进行正交优化,对成品颗粒的临界相对湿度和流动性以及稳定性进行考察,获得了卵复春固体饮料制备方法。
试验表明,以粗多糖为指标的药材组合最佳提取工艺条件为:料液比1∶15、提取时间60 min、提取4次。该制备方法制得的卵复春固体饮料颗粒临界相对湿度为64.3%(25℃),颗粒休止角<40°,且稳定性良好,能够为同类药食同源食品开发提供工艺参考。
