盐分对土壤氨挥发与反硝化速率的影响
2021-11-25史祯琦佘冬立陈心逸夏永秋
史祯琦,佘冬立①,陈心逸,夏永秋
(1.河海大学农业科学与工程学院,江苏 南京 210098;2.中国科学院南京土壤研究所/ 土壤与农业可持续发展国家重点实验室,江苏 南京 210008)
海岸滩涂盐碱地是重要的土地后备资源。1985至2016年,我国东部沿海共围垦滩涂9 310.6 km2,对保障耕地占补平衡与国家粮食战略安全起到重要作用[1]。然而,海涂围垦区盐碱地土壤结构差、肥力水平低,农业生产对化肥依赖度高,肥料利用率远低于非盐碱地土壤;加之围垦区普遍采用大水灌溉洗盐压碱,土壤钠盐含量季节与年际变化明显[2],随着钠盐含量变化,围垦区土壤氮素生物地球化学循环过程也必然发生改变。
氨挥发与反硝化过程是农业土壤氮素消纳的重要途径,其速率在沿海生态系统和内陆生态系统之间差异明显。对分布在闽江口道庆州的淡水沼泽湿地和沿海鳝鱼滩沼泽湿地进行研究发现,淡水沼泽湿地反硝化速率〔(32.72±19.15) μmol·m-2·h-1,以N2计〕显著高于沿海沼泽湿地反硝化速率〔(4.97±2.64) μmol·m-2·h-1,以N2计〕(P<0.05)[3]。影响氨挥发和反硝化速率变异的因素众多,目前关于温度、pH、氧化还原电位(Eh)、有机碳与活化氮有效性等环境因素的影响已开展较多研究。其中,pH 是影响氨挥发的重要因素,环境中铵态氮浓度和氨挥发损失量均与pH呈正相关关系[4]。同时,陈巍等[5]对重盐土脱盐-返盐过程的研究表明,盐分变化对pH有显著影响。
关于盐分变化对氮素循环过程的影响规律及机制还有待深入研究[6-7]。随着上覆水或底泥中盐离子(如Cl-、Na+、SO42-、Mg2+)浓度增大,盐分含量增高,底泥反硝化速率表现出不同的响应规律[8]。有研究表明,盐分含量变化在0~36 g·kg-1范围的河口地区,底泥反硝化速率与盐分含量呈显著负相关关系[9];然而FEAR等[10]对美国Eutrophic Neuse河口区盐度梯度上反硝化的研究表明,反硝化速率与盐分含量并未呈现显著相关关系。李建兵等[11]通过室内恒温培养实验,发现盐分促进NH3挥发;但也有研究表明,在中度盐渍化土壤中,施肥后氨挥发总量主要由施氮深度决定,且施氮情况下,低盐度对脲酶活性无影响,高盐度反而促进脲酶活性[12]。
盐分变化可能成为解释沿海生态系统与内陆生态系统氮素循环过程速率差异的重要影响因素[8]。笔者研究拟通过培养试验,测定淹水土壤氨挥发与反硝化特征,进一步明确盐分变化对海涂土壤氨挥发和反硝化的影响规律,为合理开发利用海涂资源、提高氮肥利用效率等提供理论基础。
1 材料与方法
1.1 供试土壤和试验设计
供试土壤取自江苏如东掘港镇六总村(32°12′ N,120°42′ E),位于如东县外侧黄海滩地,为亚热带海洋性季风气候区,围垦年限为60 a,主要为农业用地,作物类型为水稻,灌溉方式为淹灌,所施氮肥以尿素为主。土壤类型为粉砂土,母质为海相淤积物,土壤砂粒(粒径0.05~2 mm) 、粉粒(粒径0.002~<0.05 mm)和黏粒(粒径<0.002 mm) 质量分数分别为13.7%、81.3%和5.0%,土壤基本理化性质:pH为7.2,含盐量为0.24 g·kg-1,w(铵态氮)为0.12 mg·kg-1,w(硝态氮)为0.08 mg·kg-1,w(总有机氮)为0.21 mg·kg-1,w(有机碳)为3.1 g·kg-1。
研究盐度对氨挥发和反硝化的影响,需要进行覆水土壤室内培养试验。根据土壤特性及研究目的,经盐分淋洗处理后,参考滨海盐土分级标准〔非盐化土壤,含盐量(g·kg-1)≤1;轻度盐化土壤,>1~2;中度盐化土壤,>2~4;重度盐化土壤,>4~6;盐土,>6〕[13],设置低盐度处理<1 (即不做盐分淋洗处理,CK)、1、2 g·kg-1和高盐度处理4、10 g·kg-1共5个NaCl盐分梯度,每个处理重复3次。供试土壤经风干、过5 mm孔径筛后,通过多次喷洒NaCl溶液并混匀进行盐分处理,将处理后土壤填入培养盆(PVC,厚度为5 mm,内部尺寸为340 mm×270 mm×130 mm)中,共计15个样品,添加足量碳源(每盆1.2 g C6H12O6)和氮源〔每盆0.9 g CO(NH2)2〕,培养7 d后,测定各处理氨挥发、反硝化速率及水土环境因子。
1.2 氨挥发、反硝化速率及水土环境因子测定
采用通气法[14]测定氨挥发速率(连续7 d),收集装置为PVC圆管,内径15 cm,高20 cm,装有不锈钢网架以控制海绵放置高度。将圆管垂直插入沉积物,保证水土界面以上部分大于10 cm。将两块厚度2 cm、直径16 cm的海绵的一面用15 mL磷酸甘油溶液浸润(50 mL磷酸混合40 mL丙三醇后定容至1 000 mL制成磷酸甘油溶液),将下海绵置于网架上,浸润一面面向土壤,吸收氨挥发气体;将上海绵与管口齐平,浸润一面面向空气,使两块海绵均与圆管紧密贴合。24 h后,将装置中的下海绵装入加有300 mL 2.0 mol·L-1氯化钾溶液的塑料瓶中,完全浸没,气浴振荡1 h后,采集浸提液50 mL,测定浸提液中铵态氮含量。氨挥发速率(RNH3-N,μmol·m-2·h-1,以NH3计)计算公式为
(1)
式(1)中,M为平均每天吸附的氨气(NH3-N)质量,mg;A为收集装置横截面积,m2;D为每次收集的时间,h。
采用膜进样质谱法测定反硝化速率[15]。利用无扰动沉积物采样器(PVC,内径8 cm,外径9 cm,高27 cm)采集各处理上覆水及0~10 cm原状沉积物,底部用橡胶塞密封。沿玻璃棒缓慢加入与上覆水氮素含量一致的硝酸钾溶液直至柱体内充满液体,拧好盖子,调整直至柱体中没有任何气泡,将柱体置于模拟原位淹水环境的培养装置中,连接进水管和出水管。淹水平衡4~6 h后,分别在0、2、4、6和8 h时取样,采用膜进样质谱仪测定c(N2)/c(Ar)比值。水样N2浓度计算公式为
c(N2)=fc×[c样品(N2)/c样品(Ar)] ×c理论值(Ar)。
(2)
式(2)中,fc为校正因子,即c(N2)/c(Ar)的标准水样理论值与实测值的比值。在密闭培养体系中,反硝化主产物N2浓度随培养时间延长而增加。将不同培养时间水样N2浓度和时间进行线性回归,斜率为沉积物柱上覆水中N2浓度变化速率(图1),μmol·L-1·h-1,以N2计;结合沉积物柱样横截面积(m2)与上覆水体积(L),即得反硝化速率,μmol·m-2·h-1,以N2计[15]。
同时测定上覆水及土壤理化性质,采用流动分析仪(TRACCS2000,Skalar Analytical,Breda,the Netherlands)测定无机氮(全氮、铵态氮和硝态氮)浓度;采用便携式多参数测试仪(Hach Company,Loveland)测定溶解氧(DO)浓度、pH;采用土壤电导率仪测定土样浸提液、上覆水电导率(EC)。取表层土样10 g,提取土样DNA,采用荧光Q-PCR绝对定量法,使用QIAGEN质粒提取试剂盒提取重组菌质粒,采用NanoDrop测定PCR产物浓度。获得各处理表层土壤环境中反硝化相关微生物丰度,将执行亚硝酸盐还原过程的nirK型亚硝酸盐还原酶基因以及能催化氧化亚氮生成氮气的nosZ型氧化亚氮还原酶基因作为反硝化微生物的代表基因。
采用Excel软件整理试验数据,采用SPSS 25.0软件进行线性回归分析和不同处理间差异显著性分析及检验,采用Origin 2017软件绘图。
2 结果与分析
2.1 不同盐度处理氨挥发和反硝化速率特征
氨挥发速率随盐度升高而递增(图2),其速率(以NH3计)变化范围为293.92~353.45 μmol·m-2·h-1, CK处理盐度最小,10 g·kg-1处理最大。当盐度为1、2、4和10 g·kg-1时,氨挥发速率分别比对照增加1.9%、3.8%、11.5%和20.3%。由氨挥发速率增幅可知,低盐度条件下,盐度升高对氨挥发过程促进作用不明显(P>0.05);高盐度条件下,氨挥发速率增大较为显著(P<0.05)。
反硝化速率随盐度升高而递减(图2),其速率(以N2计)变化范围为301.91~498.58 μmol·m-2·h-1,CK处理盐度最大,10 g·kg-1处理最小。当盐度为1、2、4和10 g·kg-1时,反硝化速率分别比对照降低13.2%、27.9%、34.6%和39.4%。由反硝化速率降幅可知,低盐度条件下,盐度升高对反硝化速率限制作用较明显;高盐度条件下,反硝化速率降低并不显著。
2.2 不同盐度处理水土环境因子特征
土壤盐分含量变化导致上覆水及沉积物中环境因子发生变化,进而对氨挥发和反硝化过程产生影响。不同处理间各环境因子差异显著性分析结果(表1)表明,上覆水中硝态氮浓度随盐度增大而显著降低(P<0.05),上覆水铵态氮浓度随盐度增大而显著增大(P<0.05)。盐度对上覆水pH无显著影响,<1~10 g·kg-1盐分梯度下上覆水pH变化范围为7.46~7.67,呈弱碱性。上覆水DO浓度与盐分梯度呈正相关关系,但未达显著性水平(P<0.05)。EC随盐度提高而显著增大(P<0.05),变化范围为1 016.67~3 780.00 μS·cm-1,当盐度为1、2、4和10 g·kg-1时,EC分别为对照的1.04、1.33、2.03和3.72倍。
沉积物土壤中硝态氮浓度随盐度增大而增大,土壤铵态氮浓度随盐度增大而降低,两者浓度变化范围分别为0.90~0.93和28.69~30.99 mg·kg-1,但土壤铵态氮和硝态氮浓度随盐度变化均未达显著水平(P>0.05)。表层土壤pH和EC随着盐度提高均显著增大(P<0.05),与对照相比,各加盐处理表层土壤pH平均增大4.6%,EC平均增大82.7%。
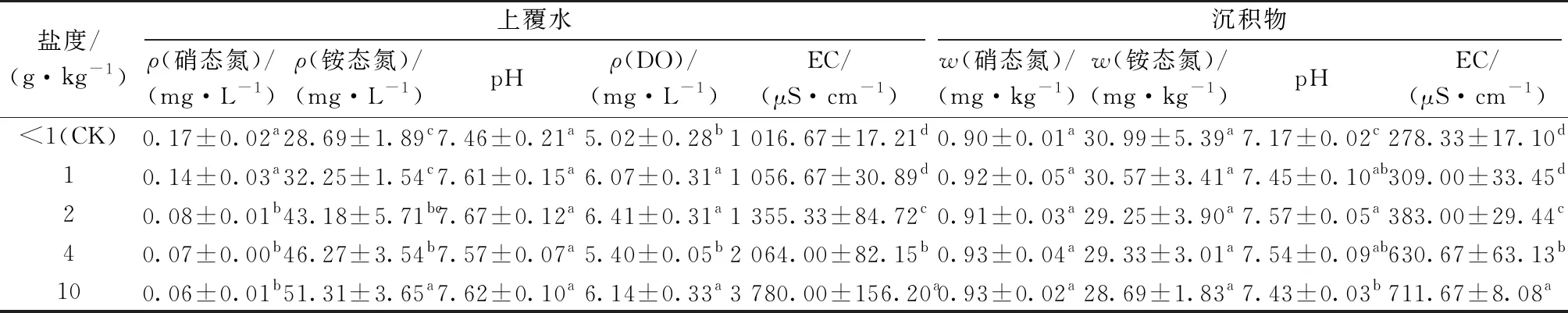
表1 不同盐度和水土环境因子的关系
2.3 不同盐度处理土壤反硝化微生物特征
将nirK和nosZ基因型反硝化细菌作为代表基因具有典型性。随着盐度的提高,nirK和nosZ基因丰度下降,两者丰度变化范围分别为123.11~242.93和16.32×103~24.54×103copies·mg-1,10 g·kg-1盐度处理均最小。与对照相比,盐度为1、2、4和10 g·kg-1处理nirK基因丰度分别降低9.6%、19.4%、42.8%和49.3%,nosZ基因丰度分别降低21.4%、29.9%、33.0%和33.5%(图3)。相关性分析结果表明反硝化速率与nirK和nosZ基因丰度均呈显著正相关关系(图4),相关系数分别为0.71和0.73(P<0.01),进一步证明反硝化过程是由微生物主导的生化反应。
上述结果与反硝化速率随盐度变化而变化的关系相符,其本质是反硝化细菌受盐分抑制,从而导致反硝化速率降低。低盐度条件下,反硝化细菌对盐度增高较为敏感,盐分水平持续提高,反硝化优势微生物对盐分水平的响应程度下降,与反硝化速率变化趋势一致。
3 讨论
土壤盐分变化对海涂盐碱土氮素循环过程具有显著影响。土壤氨挥发速率与盐分水平之间存在显著正相关关系,随盐分水平提高呈显著增大趋势,这与徐万里等[16]和梁飞等[17]的室内培养试验结果一致;AWAD EL-KARIM等[18]也认为一定盐度范围内土壤盐渍化加剧氨挥发的氮素损失,但在低盐度条件下(1、2 g·kg-1),盐分变化对氨挥发速率的影响不显著,其原因主要是低盐度对脲酶活性影响较小[19]。氨化过程首先是在胞外酶的作用下将高相对分子质量可溶性有机氮转化为低相对分子质量可溶性有机氮,其中,一部分通过微生物生命活动代谢产生氨,另一部分则在环境中进行脱氨作用产生氨气[20]。硝化作用对土壤盐度十分敏感,随着土壤含盐量增加,硝化作用受到抑制[16],但NEJIDAT[21]研究不同盐度对12种不同土壤硝化过程的影响,结果表明,由于不同环境下硝化细菌种群不同,故对盐分的耐受性不同。DANCER等[22]和段争虎等[23]都认为土壤pH值是影响氨挥发的重要因素,随着pH值增加氨挥发速率增加。笔者试验中上覆水中硝态氮浓度随着盐度增加而降低,表明硝化作用的确受到一定程度抑制,导致铵态氮在沉积物界面富集,而上覆水和沉积物铵态氮浓度与盐度的关系进一步证明了土壤高盐度减弱了沉积物土壤对 NH4+的吸附能力,促进 NH4+向水体释放[24],同时pH随着盐分的增大而增大,总体呈碱性,促进了NH4+向NH3的转化,氨挥发速率则显著增加。因此,氨挥发速率随盐度的增大而增大,实质上是盐分变化通过影响pH、氮素浓度等环境因素综合作用的结果。
盐分变化引起的土壤反硝化速率差异一方面归结于盐离子化学作用改变土壤中NH4+吸附和释放过程,调节NH4+可利用性进而影响土壤反硝化速率[25]。高盐度减弱了土壤对NH4+的吸附能力,导致硝化细菌(amoA)受到可利用NH4+的限制,进而影响反硝化过程[24]。另一方面,更多学者将盐分对脱氮过程的影响归因于脱氮微生物对盐分胁迫的耐受性差异[26],盐分通过生理机制直接影响反硝化菌活性,如高钠盐环境易导致细胞发生质壁分离,从而抑制细胞活性。笔者研究结果表明,nirK和nosZ基因型反硝化细菌丰度与盐度(即Na+浓度)呈显著负相关关系,表明高盐度抑制微生物活性,高盐度造成的高渗透压使微生物脱水,进而导致细胞失活,同时抑制微生物代谢酶活性[27],这与李佳霖[28]对河口区沉积物反硝化的研究结果一致;但对美国 Eutrophic Neuse河口不同盐度沉积物反硝化过程的研究结果表明,不同盐度底泥反硝化速率差异并不显著[10],其主要原因是不同反硝化细菌对盐分的耐受度不同,当盐度高出一定范围后,一部分不耐受反硝化菌型持续死亡,另一部分菌型却能够存活并继续主导反硝化过程[9]。反硝化过程的两个关键功能基因nirS和nirK表现出对高盐分环境具有不同的耐受性,在淡水河流环境中以nirK基因型反硝化菌为主,而在高盐分水体环境中nirS基因型反硝化菌丰度更高[26]。PIAO等[29]对沿海滩涂湿地的调查发现,nosZ群落α分支耐高盐度环境能力显著高于β和γ分支,盐度成为影响nosZ群落组成的关键性因素。因此,盐分对反硝化的影响已由简单的对速率影响研究逐渐发展到对驱动脱氮过程的微生物群落结构特征及活性影响的相关研究。沿海地区受海水入侵影响,在降雨入渗和地下水强烈蒸发等共同作用下,水分运动过程中伴随有频繁的“脱盐”与“返盐”过程,农田土壤水盐化学环境动态变化明显,势必成为影响土壤反硝化菌种群结构、丰度和活性的关键性因子。因此,“脱盐”与“返盐”过程的频繁交替对反硝化的影响机制探索将成为沿海地区水文过程驱动下氮素生物地球化学循环研究的重要突破口之一。
4 结论
土壤盐分变化对沿海滩涂盐碱土氮素循环过程具有显著影响。盐度升高减弱了沉积物对 NH4+的吸附能力,同时pH与含盐量呈正相关,总体呈弱碱性,促进了NH4+向NH3的转化,最终导致土壤氨挥发速率随盐度升高而显著增大;盐度升高抑制反硝化细菌活性,同时又使可利用NH4+(氮源)减少,直接影响反硝化过程,最终导致土壤反硝化速率随盐度升高而显著降低。
