PDCA循环在我院药品不良反应监测中的效果研究
2021-11-16程振田周芸袁祥萍单丽妮
程振田,周芸,袁祥萍,单丽妮
(潍坊市益都中心医院,山东 潍坊 262500)
用药安全问题是目前全球共同关注的焦点,1972年世界卫生组织明确了药品不良反应(adverse drug reaction,ADR)的定义,即正常剂量的药物用于预防、诊断、治疗疾病或调节生理功能时出现的有害的和与用药目的无关的反应[1-2]。随着社会医疗体系的不断完善,患者接受的药物治疗日益复杂,同时,药物治疗所导致的不良反应事件也在不断增多,严重者甚至可直接威胁患者的生命安全[3]。保障人体用药安全,维护人民身体健康和合法用药的权益,是《中华人民共和国药品管理法》的立法宗旨,《药品管理法》(2019年修订版)第八十一条规定:医疗机构应当经常考察本单位使用的药品质量、疗效和不良反应,发现疑似不良反应的,应及时向药品监督管理部门和卫生健康主管部门报告。开展ADR监测工作是医疗机构的责任和义务,也是预防ADR发生、促进临床合理用药的重要手段[4]。
PDCA循环又称戴明环,是质量保证体系运转的基本方式,亦是质量管理应遵循的科学程序,主要包括计划(plan,P)、执行(do,D)、检查(check,C)、处理(action,A)4个阶段。通过不断发现实际应用中出现的问题,找到引发问题的原因并总结经验,采取相关措施进行处理,通过不停地修改使工作步骤、思想方法逐渐实现科学化、系统化、条理化,达到提高管理质量的目的[5]。
我院自2012年开展ADR监测工作以来,由于部分科室医务人员报告意识薄弱,填报流程不熟悉等问题,使得医院近几年出现ADR上报数量少,新的及严重的报告数量少、参与上报科室少、病程记录率低等现象。本研究自2019年1月起,将PDCA循环应用于ADR监测实践中,经过2个循环后明显提高了我院ADR监测报告的上报数量及质量。
1 资料与方法
1.1 资料来源 收集我院国家药品不良反应监测系统中运用PDCA循环干预前(2017—2018年)和2个循环干预后(2019—2021年)上报的有效ADR报告(均为市药品不良反应监测中心接收的报告),进行研究分析。
1.2 研究指标 ADR上报总数量、新的及严重的ADR上报数量(下称新/严数量)、上报科室数、病程记录率。
1.3 PDCA循环实施过程 采用PDCA循环对我院ADR上报工作进行干预,通过对ADR上报数量、新/严数量、上报科室数及病程记录率等数据的统计,分析PDCA循环干预前后我院ADR上报情况的变化[6-7]。
1.4 2019年
1.4.1 计划(P) 通过分析我院2017—2018年的ADR上报情况发现,存在的主要问题为上报总数少、新/严数量少、上报科室少、病程记录率低,药品不良反应监测小组人员利用头脑风暴法,对上述问题产生的原因进行了分析,结果以鱼骨图(见图1)标示:医务人员不了解ADR上报为免责行为,担心引发医疗纠纷;培训不到位,医务人员不能准确判断相关事件是否为ADR,无上报意识,不熟悉上报流程,未及时将其记录于病历;ADR制度不完善,未明确具体要求,未做到专人负责;上报流程复杂,效率低;无有效奖惩方案。

图1 2019年我院ADR上报数量及质量不达标原因鱼骨图
根据存在的问题,药品不良反应监测小组制定相关对策:①修订ADR上报制度,明确上报要求;②进行相关知识培训,提高医务人员对ADR的认识;③建立有效奖惩方案;④及时向临床反馈上报情况,对存在问题的报表进行告知;⑤完善ADR上报流程及药物说明书查询系统。
1.4.2 执行(D) 针对我院ADR监测工作现状制定相关政策,采取以下具体改进措施:
①修订并完善ADR上报制度,明确上报要求:制定科室上报目标,各临床科室每月1份;在各临床科室设置管理员,负责科室药品不良反应上报、汇总及分析等相关工作;明确填报原则及报表填报要求,可疑即报,发生的ADR记录于病程中,无病程记录者不予上报。
②进行ADR相关培训:进行2次ADR知识培训,对相关定义、可能性关系判定、上报要求、上报流程等内容进行培训,提高医务人员认识。
③建立有效奖惩方案:每季度对临床科室上报情况进行汇总,根据完成情况对科室进行奖惩,完成目标(3份)者每份奖励30元,未完成目标者,每缺少一份扣100元。
④及时反馈上报情况,将总结情况在质量报告中公布:每季度上报工作结束后,对各科室上报情况进行分析,包括是否为合格报表及报表征存在问题,通过办公系统及时通报各临床科室;同时对上报内容进行分析,通过质量安全简报反馈于各临床科室。
⑤完善ADR上报流程及药物说明书查询系统:我院所有的不良事件由质量控制科统一管理,在ADR上报及退回修改时均需通过质量控制科转发。2019年简化ADR上报流程,临床科室直接上报于药学部,减少质量管理科转发,提高上报效率;引进合理用药系统,可查询我院配备药品信息。
1.4.3 检查(C) 该阶段主要对相关改进措施实施后我院的ADR上报情况进行分析,以便及时发现相关措施执行中的问题,主要方法为:每季度对药品不良反应上报情况,通过办公系统进行公示,并在质量简报中进行分析,将完成情况及存在问题反馈于各临床科室;对各科室每季度ADR上报情况进行单独考核,并及时落实奖惩。
1.4.4 处理(A) 每季度对上报ADR报表者进行奖励,鼓励医务人员上报;针对检查阶段发现的问题,进一步制定并修改相关措施,进入下一个PDCA循环。
1.5 2020年
1.5.1 计划(P) 通过分析我院2019年的ADR上报情况发现,与2018年上报情况相比,上报总数、新/严数量、上报科室、病程记录率均有所上升,PDCA循环有效。但上述几项指标仍未达到预期目标值,进入下一个PDCA循环。
药品不良反应监测小组再次对问题原因进行了分析,结果以鱼骨图(见图2)标示:奖惩缺乏力度,科室不重视;培训仅针对科室管理员,普通医务人员不了解ADR相关知识,无上报意识;临床科室仅管理员上报,不能及时发现所有ADR;上报ADR报表时需使用多个程序,过程烦琐;对于新/严ADR未给予特别奖惩。
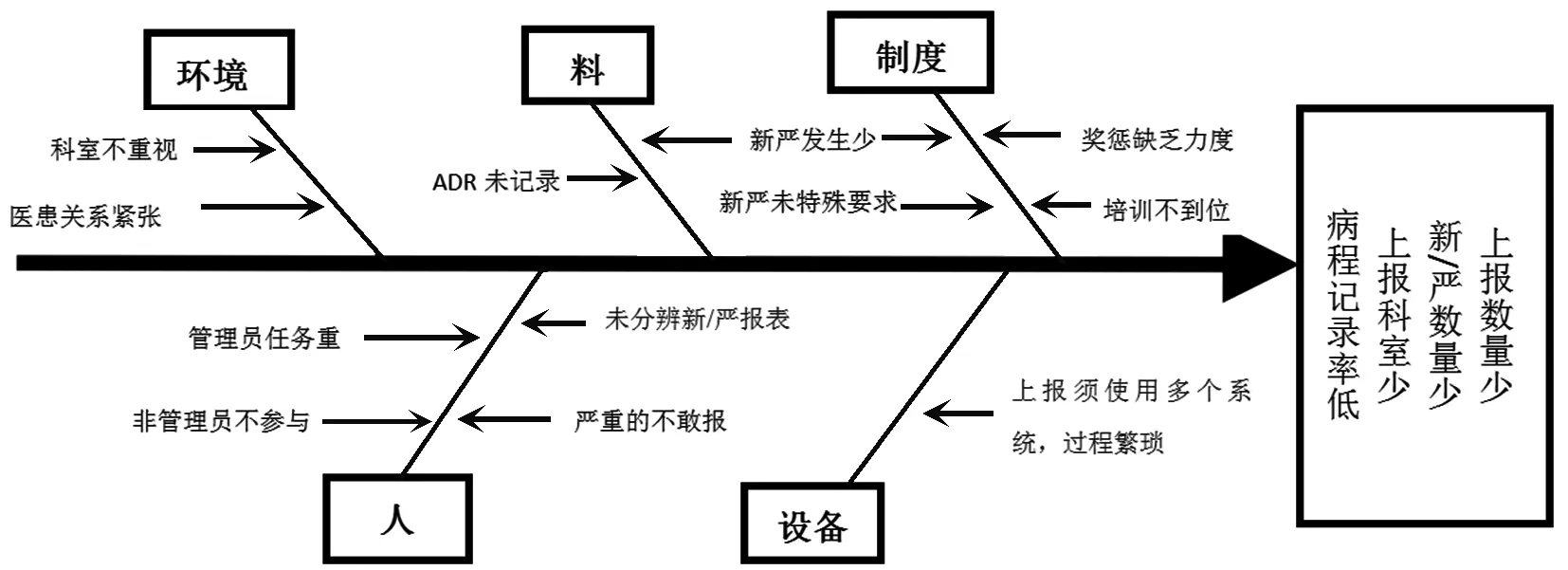
图2 2020年我院ADR上报数量及质量不达标原因鱼骨图
药品不良反应监测小组制定相关对策:①将ADR上报纳入综合目标考核,建立有效绩效考核方案;②更新及完善ADR上报系统;③修订ADR上报制度,赋予新/严报表更多分值,鼓励上报新/严ADR;④进行新/严ADR相关知识培训,提高医务人员的认识;⑤对于上报数量多、报表质量好的个人,优先推荐评选市ADR上报先进个人。
1.5.2 执行(D) 针对我院ADR监测工作现状制定相关政策,采取以下具体改进措施:
①纳入综合目标考核,建立有效绩效考核方案:将ADR上报情况纳入科室综合目标考核,并进行单独考核,满分3分。如未完成上报数量,扣罚科室相应绩效工资。
②引进中国医院药物警戒系统,完善流程:2020年我院引入并安装中国医院药物警戒系统(CHPS),对报表填写项目进行定义和规范;将CHPS系统与我院各系统进行对接,可直接调用各系统数据,减少上报人员工作复杂;修改上报流程,增加退回报表功能,使上报流程进一步完善。
③修订并完善ADR上报制度,赋予新/严报表更多分值:一般的报表0.5分/份,新/严报表1分/份。
④进行ADR相关培训:安排2次ADR知识培训,对新/严报表相关定义、制度改变、CHPS系统使用方法、上报流程改变等内容进行培训,提高医务人员认识及积极性。
⑤对于上报数量多、报表质量好的个人,优先推荐评选市ADR上报先进个人。
1.5.3 检查(C) 该阶段主要对相关改进措施实施后我院的ADR上报情况进行分析,以便及时发现相关措施执行中的问题,主要方法为:每季度对药品不良反应上报情况,通过办公系统进行公示,并在质量简报中进行分析,将完成情况、存在问题及CHPS系统使用情况反馈于各临床科室;对各科室每季度ADR上报情况进行单独考核,并与科室绩效挂钩。
1.5.4 处理(A) 2020年重新修订《药品不良反应/事件监测及报告制度》,完善上报流程,对于上报数量为零的科室进行重点宣教;针对检查阶段发现的问题,进一步制定并修改相关措施:每季度对科室进行单项绩效考核,提高科室重视度,鼓励医务人员上报,并于必要时针对相关问题进行下一个PDCA循环。
2 结果
2.1 药品不良反应上报情况 结果见表1。本市市场监督管理局为我院制定指标为:ADR上报总数量为500份/年、新/严数量分别为100份和75份。我院为三级甲等医院,开放床位1 200张。2020年我院年住院患者6万人次,门诊患者药物处方50万人次,有能力完成制定指标。
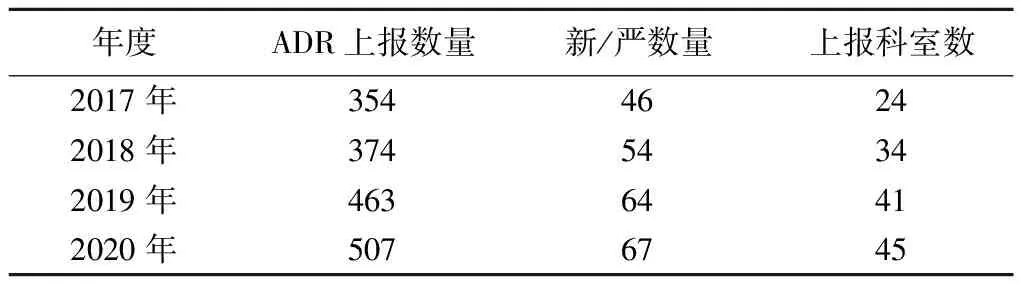
表1 2017—2020年ADR上报情况
①上报数量达到市场监督管理局制定指标。2017—2018年,即PDCA循环干预前,我院分别为354份和374份,未达到市场监督管理局制定指标。运用PDCA循环进行干预后,2019年上报数量有所提高,达到了463份;经过第二个PDCA循环后,2020年上报数量为507份,达到本市市场监督管理局制定的指标。
②新/严数量未达到市场监督管理局制定指标,继续进入下一个PDCA循环进行干预。2017—2018年,即PDCA循环干预前,新/严数量分别为46份和54份,未达到市场监督管理局制定指标。经过2个PDCA循环干预后,2019年及2020年新/严数量提高到64份及67份,但仍未达到本市市场监督管理局制定的指标。2021年将进入下一个PDCA循环,持续改进。
③上报科室数量有所提高。我院共50个临床科室,2017—2018年,即PDCA循环干预前,我院分别有24个和34个临床科室参与ADR上报。经过两次PDCA循环后,2020年有45个科室参与上报,仅有5个科室未参与上报。2021年将针对未参与上报科室重点开展培训。
2.2 药品不良反应病程记录率 结果见表2。病程记录率达到三级医院评审标准要求。2017—2018年,即PDCA循环干预前,我院ADR病程记录率分别为75.42%和79.95%,不符合三级医院评审标准要求。运用PDCA循环进行干预后,2019年病程记录率提高到92.44%;经过第二个PDCA循环后,2020年病程记录率已达100%,符合三级医院评审标准要求。
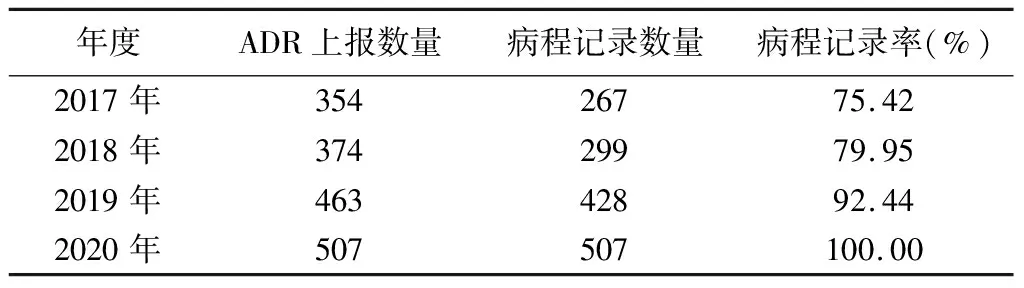
表2 2017—2020年ADR病程记录率情况
2.3 不足
2.3.1 ADR报告率低 结果见表3。WHO的统计数据表明:全球每年住院患者中 ADR 的发生率为 10%~20%,其中,因严重 ADR 导致的病死率约为5%[8]。我院2020年上报率为0.09%,仍有较大提高空间。
2.3.2 门诊患者上报比例低 结果见表4。2020年我院门诊处方人次远高于住院人次,而我院ADR报表中,12例为门诊患者上报,495例为住院患者上报,门诊患者占比仅为2.37%,2021年需关注门诊患者ADR情况。
3 讨论
PDCA循环是一种可全面改善管理质量的科学程序及通用模型[9],我院的 ADR 上报和监测工作自引入 PDCA循环管理模式后,在医院高度重视及多学科、多部门、多专业的相互协作下,通过完善制度、加强监督培训、建设信息系统等措施,提高了全院医务人员对 ADR上报的重视程度,ADR上报数量及质量均显著改善。对ADR上报工作中存在的不足,可进入下一个PDCA循环,持续改进。
医院上报ADR可帮助国家药品监督管理局统计数据,及时识别临床风险信号,预防严重药品不良反应的发生,对于促进临床用药的合理性和安全性具有重大意义,为了提高医院ADR监测的力度和质量,应积极运用新型管理模式对监测工作进行干预[10],并通过干预措施的实施,可提升全体医务人员对于药品不良反应的发现、报告、评价及预警能力,为评价、整顿和淘汰高风险药品提供临床依据,为探索构建医院药品不良反应监测预警体系提供安全用药保障,从而达到保障临床用药的合理性与安全性。
