全后腹膜动脉优先入路在全胰十二指肠切除术中的应用
2021-11-11汪小祥熊光冰秦仁义
汪小祥,熊光冰,冀 旭,王 敏,朱 峰,秦仁义
(华中科技大学同济医学院附属同济医院胆胰外科,湖北 武汉,430030)
1942年,Rockey完成了世界首例全胰腺切除术(total pancreatectomy,TP)[1]。虽然全胰腺切除术在胰腺疾病外科治疗中具有重要作用,但不如胰十二指肠切除术(pancreaticoduodenectomy,PD)、胰体尾切除术的应用广泛。究其原因,主要是全胰切除术后患者的内外分泌功能障碍极大影响了术后生活质量[2-3];同时,术后并发症发生率增加、围手术期死亡率上升,令人望而却步[4]。近年,随着手术技术的进步及围手术期管理水平的提高,以及各种中-长效胰岛素、高效胰酶制剂的应用,全胰切除术重新步入了胰腺外科医生的视野[5]。研究表明,与部分胰腺切除术相比,其短期、长期生存效益并无明显差异[6-8]。目前,关于全胰切除术的研究较多,其在临床中的应用也越来越多,手术指征[9-10]的把控也更为严格,但关于腹腔镜全胰切除术的报道却极少,对于TP手术路径的探讨更是少见。本文回顾分析2014年2月至2020年6月在我院行全胰十二指肠切除术的34例患者的临床资料,术中均采用全后腹膜动脉优先入路,现对其疗效进行评价。
1 资料与方法
1.1 临床资料 2014年2月至2020年6月华中科技大学同济医学院附属同济医院胆胰外科施行全胰十二指肠切除术34例;其中男21例,女13例;平均(52.88±11.32)岁。34例患者术后病理结果为胰腺癌24例,非胰腺癌10例。患者术前常规接受全腹增强CT检查,了解病灶位置、侵及范围,判断肿瘤与血管关系,排除远处转移,评估可切除性。术前有吸烟史3例、饮酒史4例;术前合并糖尿病7例,合并黄疸6例,CA19-9升高18例。34例均成功经全后腹膜动脉优先入路行全胰十二指肠切除术,其中10例行腹腔镜手术,24例行开腹手术。
1.2 手术方法 腔镜组:采用5孔法施术,脐下穿刺10 mm Trocar作为观察孔,左侧锁骨中线脐上置入12 mm Trocar作为主操作孔,分别于右侧锁骨中线脐上12 mm、左右肋缘下穿刺5 mm Trocar作为辅助操作孔。开腹组:取上腹正中切口,左绕脐,逐层切开入腹。术中探查排除肝脏、胃、大网膜、肠系膜及盆腔等处转移后,手术入路采用全后腹膜动脉优先入路。(1)打开胃结肠韧带,显露胰腺,分离胃结肠韧带至结肠肝曲。于胰腺下缘分离出肠系膜上静脉(superior mesenteric vein,SMV)。在胰颈部、SMV之间,由下向上作隧道式分离。于胰腺上缘游离解剖肝总动脉、肝固有动脉、胃十二指肠动脉、胃右动脉并清扫淋巴结,离断胃右动脉及胃十二指肠动脉。显露门脉,沿肝固有动脉向上清扫肝十二指肠韧带内淋巴结。(2)做扩大的Kocher切口至屈氏韧带,于左肾静脉汇入下腔静脉夹角上方、腹主动脉前方找到肠系膜上动脉(superior mesenteric artery,SMA)根部,纵行切开动脉鞘,解剖SMA,完全离断SMA与胰腺钩突系膜,直至SMA跨越十二指肠处,仅留SMV/门静脉与肿瘤及剩余钩突组织相连。(3)向左侧清扫肝总动脉周围至腹腔干,继续向左分离,显露脾动脉根部,并结扎、切断。距幽门4 cm的胃窦部切断胃。逆行切除胆囊,切断肝总管,清扫肝门部。距屈式韧带15 cm处切断空肠,将近侧空肠断端由肠系膜上动静脉后方穿过,进一步紧贴血管壁,由上、下两端分离SMV与胰头之间的纤维组织。(4)在胰腺上下缘、后方分别向左侧分离,分离出脾静脉与冠状静脉分支,离断脾静脉,继续向左侧游离胰腺体尾部。清扫腹腔干左侧淋巴结,分离转向前下方,完全清扫SMA周围。结扎胃短血管,游离脾上极,离断脾膈、脾肾、脾结肠韧带,整块切除标本。(5)消化道重建:按Child术式分别行胆肠、胃肠吻合。若必须合并切除一段门静脉时,则在标本摘除前一步完成。非计划性TP,常规以动脉优先入路行PD,术中离断胰颈后,切缘常规送快速病理学检查,若切缘阳性,则改行TP。其中,计划性全胰腺切除术20例,非计划组14例。
1.3 观察指标及随访 (1)治疗情况:记录手术方式、手术时间、术中出血量、术后病理学检查结果、淋巴结清扫数量及转移情况、术后并发症、住院时间等。(2)随访情况:随访截至2021年5月7日,主要调查患者生存情况。
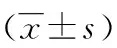
2 结 果
2.1 术中指标 手术时间平均(411.47±116.36)min;中位术中出血量为800(300,1 275)mL;其中计划性TP 20例(58.8%),非计划性TP 14例(41.2%)。常规TP(切除范围包括胰头部、颈部及体尾部,十二指肠及第一段空肠,胆囊及胆总管,脾及脾动静脉,淋巴结清扫:可包括胃窦、幽门,Gerota筋膜、部分结肠系膜,但不包括结肠切除)29例;扩大TP 3例,其中1例联合横结肠切除,1例门静脉切除并重建,1例SMV切除并重建;保留脾脏的全胰切除术2例。
2.2 术后指标 34例患者中8例(23.5%)发生术后并发症,其中胃排空障碍7例(20.6%),术后出血1例(2.9%),胃肠瘘1例(2.9%),腹腔感染2例(5.9%),肺部感染2例(5.9%),无胆漏。术后并发症严重程度按Clavien[11]系统进行分级,Ⅲ级及以上并发症共3例(Ⅲ级并发症1例,Ⅴ级并发症2例),其中1例因呼吸衰竭行气管插管治疗;1例患者术后第3天腹腔少量出血,介入治疗未能找到出血点,保守治疗有效,但合并严重胃排空障碍、肺部感染;1例因严重胃排空障碍导致营养不良于术后49 d死亡。无术后30 d死亡病例,无二次手术病例。术后平均住院(23.21±8.03)d。
2.3 术后病理检查结果 胰腺癌患者共24例,其中胰腺导管腺癌19例,胰腺腺泡细胞癌1例,胰腺黏液性囊腺癌1例,胰腺导管内乳头状黏液瘤(intraductal papillary mucinous neoplasm,IPMN)恶变3例。胰腺癌组R0切除率为91.7%(22例),R1切除2例。按第8版美国癌症联合委员会TNM分期系统进行分期,T分期:T1~T2期10例,T3~T4期14例,N分期:N0期16例,N1期7例,N2期1例,TNM分期:ⅠA期1例,ⅠB期6例,ⅡA期9例,ⅡB期7例,Ⅲ期1例。发生神经或血管侵犯7例,31例肿瘤直径≥3 cm,淋巴结转移5例,中位清扫淋巴结数量8(3,18)枚。
非胰腺癌患者10例,其中胰腺囊性肿瘤5例,包括IPMN 2例,胰腺实性假乳头状瘤伴神经侵犯1例,胰腺浆液性微囊腺瘤1例,胰腺黏液性囊腺瘤并胰管内结石形成1例;胰腺神经内分泌肿瘤3例,其中2例为胰岛素瘤,均为G2级别,1例分期为T3N0M0、ⅡA期,1例T3N1M0、ⅡB期;慢性硬化性胰腺炎1例,伴局部脓肿形成;另1例原发灶来源于胃,为胃低分化腺癌侵及胃壁全层、十二指肠及胰腺组织。
2.4 腔镜手术与开腹手术的比较 腹腔镜组手术时间、术中出血量、术后并发症发生率均优于开腹组。见表1。
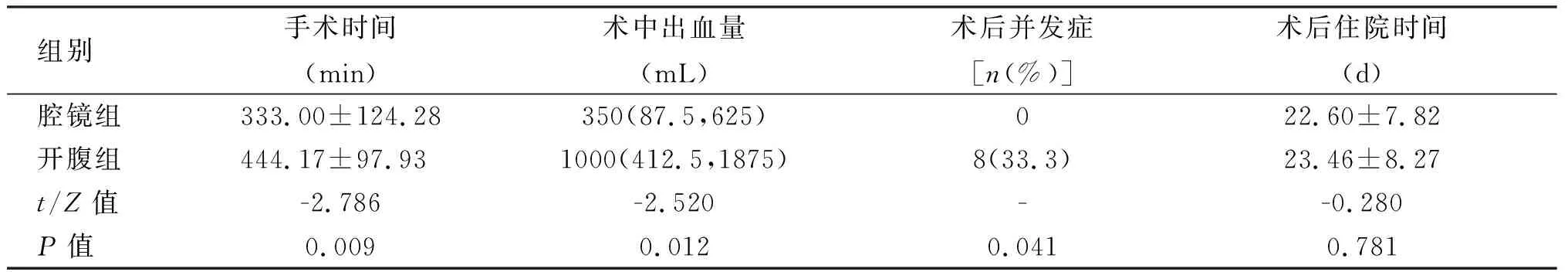
表1 腹腔镜与开腹手术相关指标的比较
2.5 随访与生存情况 33例患者得到随访,随访截至2021年5月,胰腺癌组中位生存期为15个月;总体中位生存期为26.5个月。胰腺癌组13例死亡,1例死于术后并发症,余者死于肿瘤复发;非胰腺癌患者中2例死亡,其中1例属于神经内分泌肿瘤(T3N1M0),1例属于胃低分化腺癌侵及胰腺、周围组织。见图1。
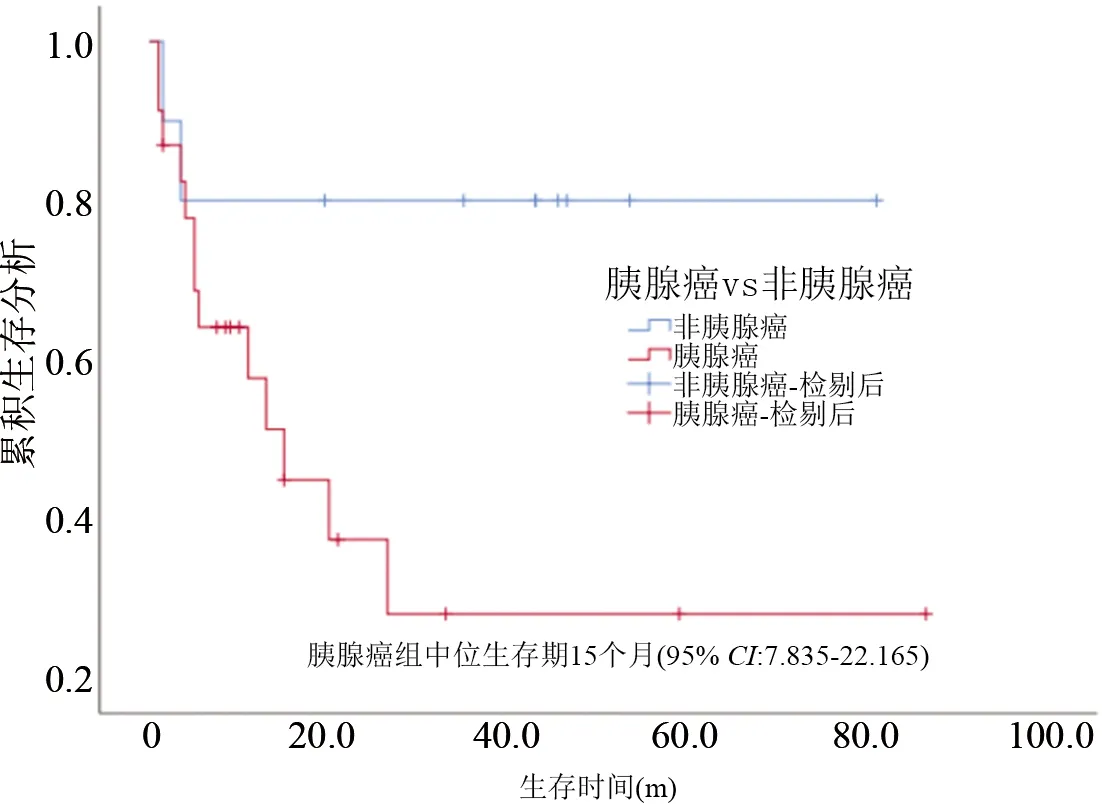
图1 全胰切除术后生存期
3 讨 论
在胰腺外科发展初期,胰腺癌曾被认为是多中心发生[12],而全胰切除术不仅能避免术后胰瘘的发生,还能做到根治性切除,因此风靡一时。但在此后很长一段时间,因全胰切除术后患者预后较差,一度被外科医生所摒弃。近年才重新步入我们的视野。
目前,关于全胰切除术的手术指征尚无统一标准[9-10],尤其腹腔镜全胰腺切除的适应证。本研究中心总结如下:胰腺癌位于胰体部,侵犯脾动脉、胃十二指肠动脉,但未侵及肝总动脉,也无SMA侵犯、肝转移或腹膜种植转移等导致不能切除的因素,是全胰切除术最典型的适应证;其他适应证包括胰腺内有多发性肿瘤或肿瘤呈弥漫性分布,如IPMN、胰腺神经内分泌肿瘤、肾癌多发性胰腺转移等;甚至PD术后,如残余肿瘤复发,也可切除残胰。本组病例中,大部分患者的病理诊断为胰腺导管腺癌,共19例。我们可以发现,最后病理诊断为IPMN的患者共5例,其中浸润性IPMN 3例。表明随着近年对IPMN认识的不断加深[13],对于主胰管型、弥漫性IPMN,全胰切除术的应用比例在不断增加。
实施TP一个很重要的原因是为了达到R0切除,以得到更好的术后生存。除术前评估即决定行计划性TP的患者,绝大部分非计划性TP患者,是由于术中胰颈切缘阳性或可疑阳性[14],而由PD改行TP。本研究中,胰腺癌组10例患者因胰颈切缘阳性或术中探查发现肿瘤位于颈体部而由PD改行TP;其余14例为胰头癌合并胰体尾萎缩或合并胰体尾病变或肿瘤位于胰颈体部,术前即决定行TP。对于非胰腺癌病例,大部分因肿瘤呈多灶性分布,而行全胰十二指肠切除术。
胰腺钩突的处理是PD与TP的重点与难点,胰腺钩突的解剖位置特殊,且易受SMA的影响,我们将这一切缘称为钩突系膜切缘或“SMA切缘”[15]。传统入路对钩突的处理主要为先游离SMV,将SMV推向左侧后,再沿SMA右侧游离钩突。SMA切缘右侧是最容易出现阳性切缘的部位,但传统“SMV优先处理方式”很难保证SMA切缘阴性,从而很难达到R0切除。而对于胰腺癌患者而言,R0切除与其预后息息相关[16]。此外,静脉壁薄,如果肿瘤压迫或侵犯SMV,在剥离受肿瘤压迫静脉过程中极易发生静脉破裂大出血,不仅影响手术安全性,还可引起肿瘤播散,增加术后复发的可能性。因此,胰腺钩突、SMA的处理尤为重要。早在2006年,Pessaux等[17]就提出了后入路的动脉优先处理,而我院胆胰外科近年进一步提出了“全动脉优先离断法”[18]在胰腺交界性可切除胰头癌中的应用。本研究中,TP患者均采用全后腹膜动脉优先入路,一方面,因胰头部的血供主要来自胰十二指肠上、下动脉、钩突动脉,胰十二指肠上动脉发自胃十二指肠动脉,胰十二指肠下动脉、钩突动脉主要来自SMA与脾动脉。优先解剖SMA,完全离断SMA与胰腺钩突,即可将胰头部的动脉血供优先离断,减少了出血量,防止了术中大出血,保障了术中安全;此外,对于需合并切除SMV/门静脉的患者,也能做到从容不迫;另一方面,达到了肿瘤切除的根治性,提高了胰腺癌的R0切除率。而事实结果证明,本研究中胰腺癌组R0切除率高达91.7%,充分显示了“全后腹膜动脉优先入路”的优越性。但此术式的不足在于:(1)如果患者肥胖或肿瘤巨大,游离十二指肠会很困难,从全后腹膜入路无法显露SMA,甚至有造成十二指肠破裂的可能;(2)如果胰头部炎症粘连严重,同样不易分离。动脉优先入路的方式有很多,除后腹膜入路,还包括经钩突入路、肠系膜入路、左后入路、前入路等,因此联合多种动脉入路行TP来解决复杂的胰腺肿瘤,值得进一步探索。
全胰切除术的安全性与可行性一直是国内外学者研究的热点。在早期,其安全性受到广泛质疑。一些研究甚至指明全胰切除术可增加术后并发症发生率与病死率[4],这可能由早期手术经验欠缺、围手术期管理水平不成熟所致。笔者总结了近5年关于全胰切除术后并发症发生率与死亡率报道的文献[19-22],其术后并发症发生率为37%~59%,Clavien-Dindo分级≥3级并发症发生率为23%~32%,30 d或90 d死亡率为2%~8%。而我们的研究结果显示,术后并发症发生率为23.5%,≥3级并发症发生率为8.8%,无术后30 d死亡病例,低于文献报道。值得一提的是,Stoop等[22]对比了2008~2015年行TP的63例患者与2016~2017年行TP的82例患者的资料,结果发现手术量的增加可降低术后并发症发生率与术后病死率,尤其合并血管切除或重建的患者。这也反映了随着手术经验的增加,手术结果能显著改善。
远期效果是评估TP疗效的重要指标。近期研究结果显示[8,16,23-24],胰腺癌TP术后的中位生存期为15~18个月。其中Johnston等[16]回顾分析了美国国家癌症数据库1988~2011年行胰腺癌全胰十二指肠切除术的2 582例患者的临床资料,单变量生存分析结果显示,术后中位生存期为15个月,术后1、3、5年生存率分别为60%、22%、13%。本研究中患者的中位生存期为15个月,与之一致。其次,多项研究结果显示全胰十二指肠切除术的预后与肿瘤类型、肿瘤分期、分化程度、淋巴结清扫数量、淋巴结阳性数量、是否R0切除、术后辅助化疗、术中腹腔冲洗细胞是否阳性等多种因素相关[16,25]。
腹腔镜技术自问世以来,因其优越性已成为众多术式的标准,目前大多数胰腺手术均能在腹腔镜下完成。然而,腹腔镜TP因解剖复杂,位置深在,周围血运丰富,难度系数较大,已成为胰腺外科乃至腔镜外科最具挑战性的手术之一。目前国内外关于腹腔镜TP[26-27]的文献报道较少,且多为个案报道,但也充分说明了其可行性与安全性。本研究中共10例患者行腹腔镜TP,其中胰腺癌6例,胰腺神经内分泌肿瘤2例,IPMN 1例,慢性硬化性胰腺炎1例,患者均恢复良好出院。腹腔镜手术具有康复快、创伤小、疼痛轻、美容效果好等优势,对于术前CT诊断怀疑的局部进展期胰腺癌,我们也可通过腹腔镜探查明确能否行根治性手术。
腹腔镜手术可获得开腹手术无法比拟的手术视野,其独特的放大作用,对淋巴结廓清更彻底,但其劣势在于暴露困难,一旦出血不容易控制,对手术入路要求较高。我们将腹腔镜技术与“动脉优先入路”理念[17-18]相结合,可做到扬长避短,利用其独特的手术视角,从后方优先解剖SMA,先行控制胰头血供,可显著减少术中出血。胰腺作为后腹膜器官,要想充分显露SMA,必须大范围游离结肠肝曲,而腔镜视角下只需小范围游离即可,这也是其优势之一。但腹腔镜下“全后腹膜动脉优先入路”的TP对术者要求高,其学习曲线长,推广难度较大。
本研究对比了腔镜与开腹TP,发现腔镜组手术时间、术中出血量、术后并发症发生率均优于开腹组,其他方面两组差异无统计学意义。由于手术例数较少,尚需更多的研究证实,但也在一定程度上反映了腹腔镜技术的优越性。我们还发现腔镜组术后未发生并发症,而TP后最主要的并发症为胃排空延迟,这表明腹腔镜技术可能降低术后胃排空延迟发病率。因此关于腹腔镜与开腹TP的对比研究有待进一步探索。
TP后严重代谢并发症的发生曾是困扰外科医生的难点。“脆性糖尿病”[28]的发生,外分泌功能不足导致的腹泻及糖尿病带来的一系列慢性并发症(心脑血管病变、糖尿病肾病、糖尿病性视网膜病变、神经病变)均是影响术后生活质量的因素。但得益于长效胰岛素、胰酶制剂的应用,这些都已不再是难题。现有的研究结果显示,TP与PD术后患者生活质量并无明显差异[2-3]。本研究的不足在于回顾性研究未能收集患者术后胰岛素用量、胰酶制剂用量,也未能对患者术后生活质量各方面进行具体量化。
综上,TP作为胰腺肿瘤的根治性手术方式之一,其适应证范围会越来越大。根据目前的报道与我们的经验,全胰十二指肠切除术是安全、可行的,我们提倡采用“动脉优先入路”的手术方式。因本研究属于单中心回顾性研究,样本量有限,统计结果偏倚较大,且在患者术后生存质量方面缺乏调查,数据不足,因此TP的近期、远期疗效仍需大样本多中心的前瞻性随机临床试验结果验证。
