人工关节与仿生软骨材料的表面改性及其摩擦学研究进展
2021-11-08赵蔚祎赵晓铎张云雷麻拴红马正峰蔡美荣周峰
赵蔚祎,赵晓铎,张云雷,麻拴红,马正峰,蔡美荣,周峰
(1.中国科学院兰州化学物理研究所,兰州 730000;2.中国科学院大学,北京 100049)
人体内天然髋、膝关节润滑系统主要由关节面、关节腔、关节骨、关节囊和关节滑液等共同组成,其中,关节头与关节臼被一层富有弹性的软质关节软骨包裹。以膝关节为例,健康人体内膝关节能够承受7~9 倍的人体重量[1-2],局部接触应力高达18 MPa[3],在如此高载荷的运动条件下,膝关节处的摩擦系数可低至0.001~0.03[4]。然而,受年龄增长、过度磨损、部分先天性疾病等多种因素的影响,人体内氨糖软骨素的含量不断降低,软骨细胞分解速度大于其合成速度,软骨内胶原纤维断裂,这些都会导致关节软骨的磨损与退化,进而出现糜烂、脱落等问题,关节出现疼痛、肿胀等症状,最终演变为骨关节炎[5-7]。骨关节炎现已成为世界头号致残性疾病,对受损关节进行修复重建,恢复关节面完整性及其功能,防止关节退变,始终是亟待解决的难题之一。
关节软骨包含<5%的软骨细胞、60%~85%的间隙流体,以及胶原纤维与蛋白质多糖[8-9]。软骨优异的力学性能依赖于纳米/微细胶原纤维构成的有序分层组织纤维结构[10-11],其结构如图1 所示。每一层都有不同的纤维排列、细胞形态以及新陈代谢活动[12]。浅表层紧邻关节腔,软骨细胞呈扁平状[13],平行于软骨表面,高度密集的胶原纤维相互垂直排列,整体有序平行于软骨表面,以承受关节运动中的剪切力[14];中间层的软骨细胞呈圆形,胶原纤维随机分布,起到了承担载荷并均衡地传递到深层区的作用[8];深层区,软骨细胞成串定位在此层中[15],直径较大的胶原纤维彼此平行排列,整体垂直于关节面,使得在增强整体抗压能力的同时,也有助于将软骨固定到软骨下骨表面[8]。

图1 人体软组织中软骨的高度有序结构示意图[10]Fig.1 Schematic diagram of the highly ordered structure of cartilage in human soft tissues[10]
由于关节系统在受损、病变后很难自愈,目前人工关节置换手术已经成为临床治疗此类疾病的主要途径[16]。人工关节假体是用金属、陶瓷、高分子聚合物等材料制作的关节组件,取代损坏的天然关节。然而,假体材料不具备自然生物的代谢作用,且大量的临床医学研究己证实,人工关节的磨损是关节失效的重要原因之一。以聚乙烯人工关节假体为例,随着使用时间的增加,假体表面会产生大量的聚乙烯磨屑,磨屑的堆积会诱发假体周围产生一系列不良生物反应(如骨溶解等),最终导致假体因无菌松动而失效[17]。此外,患者在首次进行关节置换手术10~15 年后,还需进行关节翻修更换的手术,会给患者再次带来身体上的伤害。随着全球老龄化时代的来临,人们对人工关节假体的需求量与日俱增,积极开展人工关节假体仿生设计并考量其摩擦学与抗磨损特性,将有助于延长假体使用寿命,降低患者痛苦。
目前常见的人工关节制作材料有金属、陶瓷、聚合物、水凝胶等,在发展过程中展现了出各自的优点与不足。随着材料学的不断发展与对治疗的总结,各类材料在性能不断改进的同时,也提出了新的挑战。在对材料进行仿生设计的同时,使用不同技术手段对材料进行表面改性处理,既使材料表面得到了优化,又不改变材料本身所具有的优异机械性能。因此,仿照人体天然关节润滑系统组成结构,设计并制备具有减摩抗磨特性的人工关节配副,将有助于延长人工关节的使用寿命,提高患者幸福感,并且对于我国关节假体制造业具有一定的积极意义。
1 硬质人工关节替换材料
1.1 金属材料人工关节
到目前为止,金属人工关节的材料主要有奥氏体不锈钢、钴基合金、钛合金等。奥氏体不锈钢316L(AISI,相当于国产不锈钢00Cr17Ni14Mo2)具有易加工、强度高等优点,是人类最早用于人工关节杆和关节头的制作材料。然而,随着不锈钢人工关节在人体内使用时间的增加,其表面易发生腐蚀与磨损,材料中释放出的镍会引起人体的过敏反应[18]。此外,奥氏体不锈钢的耐磨性较差,易产生磨屑颗粒,进而造成假体松动,最终导致植入假体失效[19]。
随着金属材料的不断发展,不锈钢现已逐渐被钴基合金、钛合金等材料所替代。与奥氏体不锈钢材料相比,钴基合金材料通过碳化物的弥散或形变诱导亚稳态γ 相向马氏体ε 相转变,来实现高强度与更高的耐磨性[20]。但是,钴基合金在体液环境中不断被侵蚀与摩擦,易引起钴、铬、钼等元素溶出,致使机体细胞凋亡与组织坏死等一系列并发症[21]。研究结果表明,通过不同表面处理技术可有效增强钴基合金的耐磨性。Akihiko Chiba 等[22]使用等离子渗氮对钴铬钼(Co-Cr-Mo)合金进行表面改性,发现处理后的样品磨痕宽度较窄,证明磨损率比未处理样品更低。Kazuhiko Ishihara 等[23]用光引发聚合,将聚2-甲基丙烯酰氧乙基磷酸胆碱(PMPC)接枝到Co-Cr-Mo 合金表面,在牛血清蛋白和纯水中与关节软骨对磨时,摩擦系数(COF)均小于0.01,并且表面修饰过的Co-Cr-Mo 合金具有很好的稳定性和生物相容性,可以有效防止关节软骨的退化。然而,316L 不锈钢和钴基合金都具有远高于人体骨骼的弹性模量,这也会导致植入后引起应力屏蔽效应和松动[24]。
自1950 年以来,钛及其合金因生物相容性较好、弹性模量低、比强度高而被广泛应用于生物医用材料,目前在人工关节领域中应用最广泛的是Ti-6Al-4V 合金,虽然具有优异的耐腐蚀性,但其耐磨性较差,从而影响了其使用寿命[25]。钛合金虽然生物相容性优异,但由于其生物惰性,且成分与周围骨骼有很大的不同,导致钛合金在体内仅能通过骨钉之类的机械手段进行固定,而无法利用更强的化学键合进行骨整合。此外,由于人体内环境的复杂性,钛合金表面钝化膜在受到应力以及体液的共同作用下,会发生剥离与溶解,释放出的物质可能会对人体产生毒性或引起炎症等问题[26]。因此,多种表面改性方法被用来提高钛合金植入体的性能。Pan 等人[27]在钛合金表面电镀Ni-P 镀层,发现未处理的钛表面摩擦系数在0.6左右且波动大,电镀Ni-P 镀层后,摩擦系数基本稳定在0.45。另外,Di 等人[28]采用磁控溅射在钛合金表面沉积TiAlN 涂层,TiAlN 涂层试样的磨损量只有钛合金基体磨损量的20%。Choudhury 等人[29]研究了用于人工髋关节的功能性类金刚石涂层的耐久性,结果表明,与没有涂层的同类材料相比,沉积类金刚石涂层的Ti-6Al-4V 的磨损显著降低。钛合金表面常见的生物活性陶瓷涂层有羟基磷灰石、β-磷酸三钙等,此类生物活性涂层能够促进新骨组织生长,并抑制金属离子进入周围骨组织[30-32]。研究证明,具有羟基磷灰石涂层的钛合金植入物相较空白钛合金,更容易生成类骨组织[31]。研究者利用氢氧化钠与热处理对钛合金样品进行处理后,如图2 所示,钛合金表面会形成梯度分布的钛酸钠,通过将其浸泡在模拟体液(SBF)中形成骨状磷灰石[33-35]。这种方法已经在动物模型中进行了一定的研究,其极大地促进了骨整合[36]。β-磷酸三钙涂层易在体内降解,其降解会参与新骨的形成,促进骨组织的生长[37-38]。同时,为了进一步提高钛合金的耐蚀性与在人体内长期服役的稳定性,常用钝化(热氧化)、激光表面改性等方法进行处理。Güleryüz 等[39]研究了Ti-6Al-4V 的最佳氧化条件,发现经氧化处理的Ti-6Al-4V 在600 ℃氧化60 h 后具有优异的耐蚀性,耐磨性是未处理Ti-6Al-4V 的25倍。相关研究发现[40-41],Cp-Ti 和Ti 合金的激光表面重熔可以诱导一层细小的马氏体和一层钛氧化物(如TiO、TiO2和Ti2O3),从而提高耐蚀性和耐磨性。
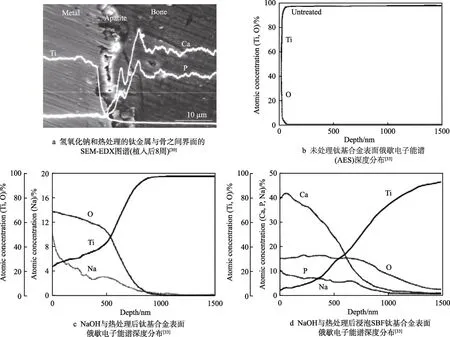
图2 钛合金表面生物活性陶瓷涂层表征[30,33]Fig.2 Characterization of bioactive ceramic coatings on titanium alloys: (a) SEM-EDX profile of the interface between the NaOH- and heat-treated titanium metal and a bone (8 weeks after implantation)[30]; AES depth profiles of the surface of titanium before (b) and after (c) the NaOH and heat treatments, and after subsequent soaking (d)[33]
1.2 陶瓷材料人工关节
陶瓷材料硬度高、生物相容性好、耐磨性与耐腐蚀性能优异,在人工关节领域中应用最广泛的是氧化铝(Al2O3)、氧化锆(ZrO2)陶瓷等。
Al2O3陶瓷是第一批应用于人工关节的陶瓷材料[42],然而在临床使用过程中,陶瓷关节由于韧性低、脆性大,一旦内部有微小裂纹,过载或应力集中就会使裂纹迅速扩展,最终导致关节假体破裂。近年来国内外有关学者开展了大量的Al2O3陶瓷增韧研究工作,如利用纳米氧化锆ZrO2相变增韧或微裂纹增韧等,取得了显著效果[43]。
氧化锆陶瓷的弹性模量较低,生物相容性也很优异[44],在断裂韧性方面优于氧化铝陶瓷。但ZrO2陶瓷属多相材料,有单斜、四方和立方3 种晶体结构,在特殊环境下易发生晶型转变,宏观上致使材料体积和形状发生变化,形成裂纹,最终导致材料破裂。对ZrO2陶瓷进行稳定化处理可以有效解决上述问题,通常在加工过程中加入氧化钙和氧化镁进行增韧处理来控制相变,从而提高ZrO2陶瓷稳定性。ZrO2陶瓷经增韧处理后,韧性大大提高[45]。
是小偷、强盗入室行凶?还是遭遇歹人偷袭?都不是。是儿子吃完晚饭切了个西瓜,顺手就将刀扔在了床上,半夜起夜回来,倒头进被窝,正巧被刀给扎中了胸口。
为了进一步优化陶瓷材料的性能,研究者们通过在陶瓷材料上加工表面织构,提高了陶瓷材料的抗磨性与摩擦性能[46-47]。在干摩擦状态下,一定的表面织构可以起到储存磨屑与减摩的作用;在液体润滑过程中,表面织构除了减摩,其表面形成的润滑膜还可以起到一定的承载作用。Andreas 等[48]利用微细电火花加工技术,在Al2O3增韧ZrO2陶瓷材料表面制备微米级织构化导电层,确定了表面织构的最大可达长径比以及电火花铣削加工的工艺参数。Stanciuc 等[49]利用飞秒激光微加工,在钇稳定的四方氧化锆多晶(3Y-TZP)生物惰性陶瓷表面制备了一定的图案,得出了材料稳定性、循环性与图案直径以及深度之间的关系,发现图案在直径为30 μm、深度为10 μm 时,可最大化地促进人骨髓间质干细胞的成骨,减少骨质流失。
1.3 高分子人工关节
应用于人工关节领域的高分子材料主要有超高分子量聚乙烯(UHMWPE)和聚醚醚酮(PEEK)等。UHMWPE 易于加工,成本较低,常用于制作人工关节臼杯组件。但是UHMWPE 关节在体内长期使用后,会产生大量的磨屑,磨屑扩散到假体周围会激活并释放大量的溶骨因子,使人工关节产生无菌松动[50]。因此,需要对UHMWPE 进行表面改性以提高其减摩耐磨性能。目前常用的UHMWPE 表面改性方法主要有辐射交联、离子注入和表面接枝。
辐射交联是指利用各种辐射手段引发UHMWPE表面长链间相互交联,从而提高表面力学性能。Tcherdyntsev 等[51]研究了辐照、定向拉伸和填充对UHMWPE 结构和性能的影响,结果表明,当辐照强度为20 Mrad 时,材料机械性能最佳。离子注入是指通过等离子体处理UHMWPE 表面,链断裂产生长寿自由基,而后形成一定的交联结构,可提高UHMWPE表面的硬度与抗磨损性能。Perni 等[52]首次证明,氦/氧低温等离子体可用于增强UHMWPE 抗磨损性能而不损失其本身细胞相容性。低温等离子体引发了UHMWPE 链的高密度交联,使得材料表面刚度增加,抗磨损性能有所提高。Binnur[53]利用氩等离子体对UHMWPE 和维生素E 稳定的UHMWPE(VE UHMWPE)进行表面改性研究,在25%牛血清中进行销盘摩擦对比实验,结果显示,改性处理后,材料的表面润湿性和耐磨性均有所提高,传统UHMWPE的摩擦系数下降趋势高于VE UHMWPE。表面接枝是指通过辐照引发材料表面产生自由基,加入单体与自由基反应,通过接枝具有不同性能的单体,使得在保留原材料优良特性的基础上,还具有一定的功能。Xiong 等[54]研究了利用紫外辐射,将MPDSAH([2-(甲基丙烯酰基氧基)乙基]二甲基-(3-磺酸丙基)氢氧化铵)两性离子单体接枝在UHMWPE 粉末表面,发现接枝亲水性高分子聚合物有助于形成水润滑膜,从而提高UHMWPE 的润滑性。Hirosji Kawaguchi 等[55]将PMPC 接枝到UHMWPE 表面,通过髋关节模拟器进行力学模型测试。结果显示,PMPC 移植显著降低了摩擦系数与磨损量(图3),并且可以有效地预防假体周围骨溶解和无菌性假体松动。
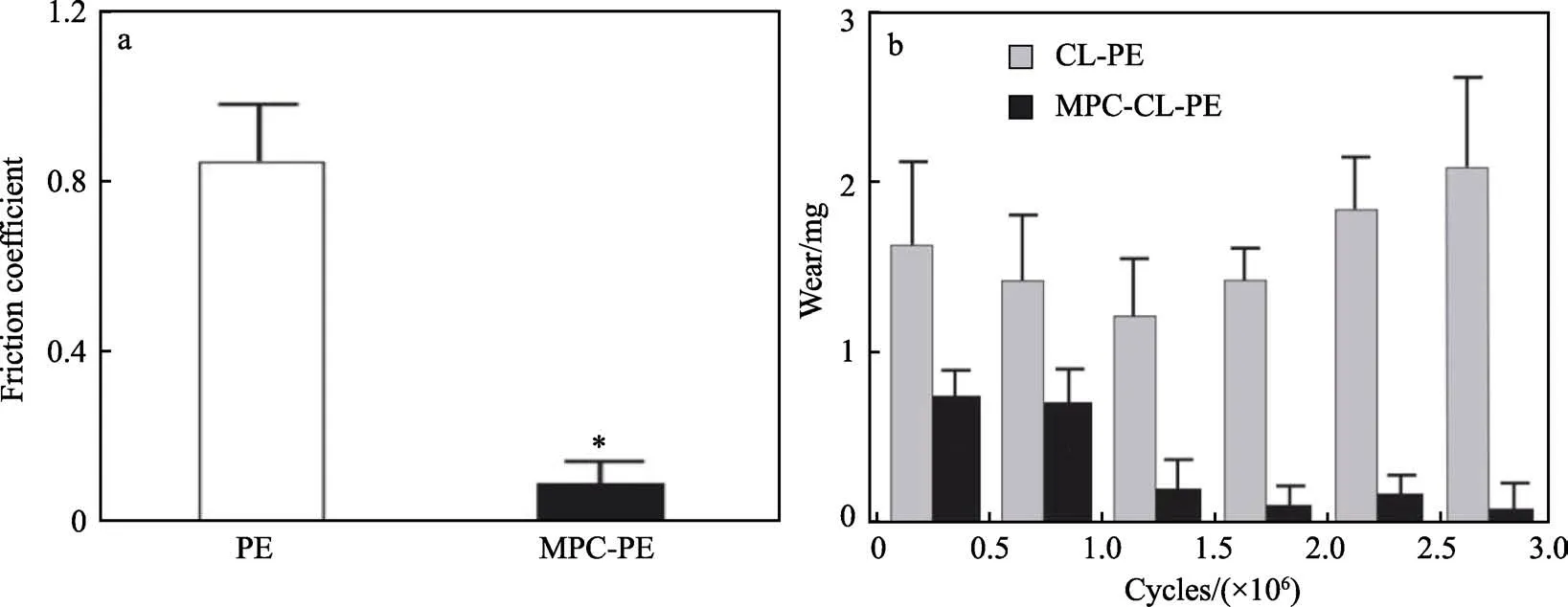
图3 平面PE 表面接枝PMPC 聚合物刷前后的摩擦系数(a)及PMPC 修饰关节模拟器内衬的磨损量(b)(间隔为5×105 转)[55]Fig.3 Friction coefficient before and after graft of PMPC polymer brush on plane PE surface (a) and wear amount of PMPC modified joint simulator lining (5×105 RPM interval) (b)[55]
PEEK 是一种性能优异的热塑性特种工程塑料,具有自润滑、无毒、生物相容性优异等特点。但PEEK表面光滑疏水,呈现生物惰性,无法进行骨整合。因此,近年来研究人员通过填充改性[56]、纤维增强[57]、表面改性[58]等多种方法改善PEEK 的性能。Sharma等[59]通过静压法将未改性和等离子体改性碳纤维(CF)与PEEK 进行复合。结果显示,等离子体改性提高了碳纤维与PEEK 基体的粘附性,界面剪切强度提高了22%,耐磨性提高了26%。Zhao 等[60]通过表面磺化处理在PEEK 上制备出了三维多孔纳米结构网络。经过丙酮处理后的PEEK,由于多孔结构和SO3H 官能团的作用,在体内外均表现出明显的生物活性与细胞相容性。
综上所述,目前传统材料体系的界面接触状态为硬-硬、硬-软接触。这就会更加容易导致磨损并产生磨屑,甚至激发人体分泌溶骨因子使骨溶解,导致假体失效。同时,目前的人工关节使用的材料模量远高于软骨和骨组织,这导致关节系统产生应力屏蔽效应,骨皮质变薄,加重骨质疏松,最终使得关节系统松动、失效等问题[61]。为了解决这些问题,研究者们受到关节软骨的启发,开展了材料仿生设计与制备的研究,并应用于硬质人工关节材料表面,制备出软硬结合的新型仿生人工关节[62]
2 水凝胶仿生关节软骨材料及其表面润滑改性
高分子水凝胶通常是由具有亲水性质的高分子链段,通过化学或者物理交联作用形成的具有三维网络结构的粘弹性聚合物。它可吸收并且储存大量的水,但其自身不溶于水,具有“湿且软”的特点[63]。水凝胶的结构形态与生物体内软组织相似,具有良好生物相容性和应用安全性的水凝胶广泛应用于创伤敷料[64]、关节软骨修复[65]等领域。但是,常规的合成水凝胶材料能量耗散机制单一,承载、抵抗蠕变和耐疲劳能力较差,与天然软骨相差甚远,限制了其在组织工程领域中的进一步推广。因此,只有提高了水凝胶的机械性能,才能使其具有人工关节软骨的力学特性[66],在此基础之上,对其表面进行润滑改性,以降低滑动界面的摩擦系数,方可媲美天然关节软骨,有望用作人工关节软骨材料。
2.1 高性能本体水凝胶软骨材料
研究人员现已开发出一系列具有高强度和良好韧性的水凝胶体系,其优异的力学性能可以归因于断裂时网络中引入的牺牲键有效地耗散了能量,如双网络(DN)水凝胶[67-69]、纳米复合水凝胶[70]和离子交联水凝胶[71-73]等。

图4 BC-PVA-PAMPS 水凝胶性能[77]Fig.4 Comparison chart of com pressive strength, tensile strength and modulus of BC-PVA-PAMPS hydrogel and other hydrogelsb (a); BC-PVA-PAMPS hydrogel can withstand 100 pounds of kettlebells weight (b); PAMPS-PDMAAm, PVA and BC-PVA-PAMPS hydrogels before and after 100 pounds compression (c)[77]
2.2 水凝胶软骨材料的表面润滑改性
尽管目前的研究已经将水凝胶的机械性能提高到了接近软骨的水平,但是水凝胶仿生软骨材料力学强度的提升往往以网络微结构的致密化为代价,进而导致表面水化度降低、润滑性能变差。事实上,天然的关节软骨是一种典型的层状多孔结构材料,且其表面分布着大量的糖基水化大分子链。软骨受压时,内部水分能够渗透到表面与水化大分子链和关节滑液一起起到润滑功能,而层状的生化结构则有利于缓冲压力、耗散应力和提供动态承载功能。因此,发展先进的表面改性方法,对高性能本体水凝胶软骨材料表面进行润滑处理,设计制备类似软骨的多层仿生材料,是同时实现水凝胶软骨材料表面润滑和本体承载的有效途径。
受关节软骨层状结构的启发,Yao 等人[84]将聚乙烯醇(PVA)与β-磷酸三钙(β-TCP)共混,制备了一种新型的双层水凝胶,以作为软骨替代物。在旋转模式下进行摩擦学测试,发现该水凝胶的表面润滑性能与天然软骨相似(摩擦系数~0.05)。然而,这类材料通常较为坚硬,在较大的接触应力下进行摩擦会导致材料磨损严重。Lin 等人[85]利用不对称界面聚合制备了一种基底高强度、表面高含水的双层水凝胶。施加外载时,高强度的基底保证了高承载性能,而高含水量的表面则保证了水润滑性能,从而减小摩擦磨损(图5a)。Lu 等人[86]通过使用一锅法同时聚合,得到了一种可用于骨软骨缺损修复的双层水凝胶(图5b),上层明胶甲基丙烯酰胺-聚多巴胺(GelMA-PDA)水凝胶作为软骨修复层,下层明胶甲基丙烯酰胺-聚多巴胺/磷酸钙(GelMA-PDA/HA)水凝胶作为软骨下骨修复层。同时将转化生长因子TGF-β3 固定在上层诱导软骨再生,而骨形态发生蛋白2(BMP2)固定在下层诱导骨再生。由于上层和下层之间界面的共价结合,两层很好地结合在一起。此外,水凝胶中的PDA 提供了非共价键,以进一步改善上层和下层之间的界面结合。这种双层水凝胶韧性较好,因为这些共价键和非共价键协同增强水凝胶。体外和体内试验表明,这种水凝胶有利于骨软骨缺损的修复。

图5 双层结构模拟水凝胶示意图[85-86]Fig.5 Double structure simulation hydrogel showing intention[85-86]
天然关节软骨表面的刷状水化分子链能够增强表面层状多孔结构的水化能力,使得关节在高载荷下实现低摩擦[1]。因此,通过表面接枝亲水聚合物刷的方法制备水凝胶上表层,以提高界面水化能力,是实现减摩抗磨的良好策略。最初,研究者通过物理吸附将聚合物刷固定在基底上[87],但物理吸附的接枝率受到空间位阻的影响,表面聚合物刷密度较低,水化作用有限。而且,物理吸附的界面结合力通常较差,聚合物刷层极易在剪切作用下脱落,导致润滑失效[88]。相比之下,具有较高接枝率与较强结合能力的化学接枝被广泛用作表面改性手段[89]。目前大多利用表面引发自由基聚合(SI-ATRP)的方法对基底进行处理[90],但是传统的SI-ATRP 聚合物刷只是锚固在基底表面,并没有深度附着,导致聚合物刷层仅有几十到几百纳米厚,在高载荷作用下易磨损[91]。为了解决这个问题,研究者们开始采用在聚合物网络中化学相互渗透的合成策略[92]。Du 等通过将引发剂嵌入聚合物基材中,研发了亚表面引发自由基聚合(sSI-ATRP)的方法。这种方法能够制备出较厚亲水聚合物刷层(几十至几百微米),并且此方法制备的聚合物刷与原始聚合物链之间形成互穿网络,因此界面键合能力好。由亚表面引发制备的聚合物刷系统与传统的聚合物刷系统相比,显示出优异的抗磨损性能[93]。该团队基于此方法,开发了一种新型仿生软骨的双层水凝胶:微米厚的亲水聚电解质刷(甲基丙烯3-磺酸丙酯钾盐和磺基甜菜碱甲基丙烯酸酯)紧密地嵌入在高强度水凝胶基质表面。上层软的聚合物刷与水凝胶的复合层提供了有效的水润滑,下层高强度的水凝胶层作为基底,提供了高的承载能力。在两者的协同作用下,以水为润滑剂,实现了在高载荷(约10 MPa 的接触压力)下的低摩擦系数(~0.010),性能非常接近天然关节软骨(图6)。这种生物激发的层状材料在高接触压力下承受50 000 次往复循环过程中,也能保持低摩擦系数,在接触界面上几乎没有观察到磨损(图6c4)[94]。Liu 等人[95]利用SSI-ATRP 化学反应将聚合物刷接枝到温敏性水凝胶基底上,实现了制备基于温度调控润滑性能的高强度水凝胶。此外,Qu 等人[96]通过采用碱诱导的网络离解策略,设计了一种由软而多孔的表层(可以储存润滑剂)和坚固的底层组成的层状水凝胶材料,实现了表面极低的摩擦系数(3 N 载荷下,COF~0.009;20 N 载荷下,COF~0.035)。因此,在表面润滑和底部承载的协同作用下,层状水凝胶可以实现优异的润滑及耐磨性能。然而,虽然这一类材料表面的摩擦磨损性能优异,但在经过长时间摩擦测试后,基底会出现屈服现象。这是由于在长时间的摩擦过程中,水凝胶内部牺牲键网络断裂而进行能量耗散,造成了水凝胶基底不可恢复的变形与摩擦系数的变化[94,96]。此外,目前虽然有许多研究致力于构造仿关节软骨水凝胶材料,但无法同时达到天然关节软骨的各项性能指标[97],因此合理构筑综合性能优异的水凝胶体系仍需不断探索。

图6 (a) PSPMA 或PSBMA 刷接枝水凝胶的制备示意图;(b) 10 N 载荷下HHy-g-PSBMA 和HHy-g-PSPMA 在5 万次摩擦循环的摩擦系数-循环曲线;(c1) HHy-g-PSPMA 表面经过5 万次摩擦循环后磨损处的横截面光镜图;(c2) 表面磨损的光镜图;(c3) 表面磨损的SEM 照片;(c4) 局部放大的SEM 照片[94]Fig.6 (a) Schematic illustration for the fabrication of PSPMA or PSBMA brush-grafted hydrogels; (b) the friction coefficientcycles curve on the surfaces of HHy-g-PSPMA and HHy-g-PSBMA for 50,000 times friction cycles at applied load 10 N; (c1) the fluorescent image of deformed cross-section; (c2) the optical image of wear surface; (c3) the SEM image of wear morphology; (c4)the local amplification SEM image of wear morphology[94]
3 组织及人工关节材料表面键合水凝胶润滑涂层
水凝胶替代天然软骨的策略除了需要满足机械强度的要求外,还要求其与骨基底的强大键合。目前的研究主要致力于提高机械性能而忽略键合问题。人工关节软骨的移植手术中,最大的风险是由于水凝胶人工关节软骨修复体与骨基底较差的键合导致的。较差的键合能力极易导致人工关节与下骨产生位移,从而导致炎症等创伤,这大大限制了水凝胶作为人工关节软骨的潜在应用。
Gong 等人[98]将鱼鳔胶原蛋白(SBC)作为第一网络,以聚(N,N-二甲基丙烯酰胺)(PDMAAm)作为第二交联网络,组成了复合双网络水凝胶。SBC/PDMAAm 凝胶具有各向异性的溶胀行为,表现出与天然软骨相当的优良力学性能。在表面包覆羟基磷灰石(HAp)涂层后,植入体内骨缺损处,发现HAp/SBC/PDMAAm 凝胶在4 周后与骨紧密结合。该课题组还在DN 水凝胶的表面杂化了羟基磷灰石纳米晶体,通过将DN 水凝胶交替浸泡在氯化钙(CaCl2)与磷酸氢二钾(K2HPO4)溶液中进行矿化处理,形成了具有梯度结构的凝胶-骨杂化层,在植入体内四周后,与缺损骨骼形成了牢固的结合[81]。Wang 等人[99]开发了一种复性水凝胶涂料(RHP),如图7a 所示,首先将未固化的粘合剂涂抹或喷涂在各种基材的表面,然后立即覆盖干凝胶颗粒,再将干凝胶水化成水凝胶。如图7b 所示,人工左股骨头涂有RHP,右股骨头未修饰作为参考样品。通过在给定压力下沿法向旋转人工股骨头与髋臼进行摩擦试验。当连续旋转35 min后,左侧髋臼软骨完全保存,但右股骨头损伤明显。此外,通过生物相容性水凝胶的选择,RHP 在医学应用方面也显示出巨大的潜力。
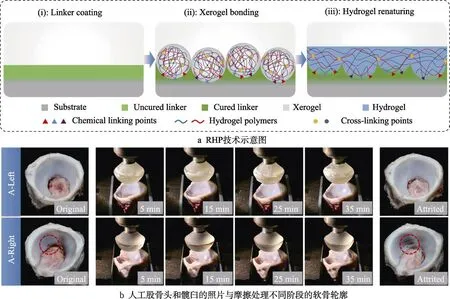
图7 RHP 技术及人工股骨头和髋臼的照片与摩擦处理不同阶段的软骨轮廓[99]Fig.7 Schematic illustration of the RHP technique (a) and photographs of the artificial femur head and acetabulum, and the profile of cartilages at different stages of the friction treatment (b)[99]
Silva 等[100]采用铬酸氧化和马来酸酐接枝,使聚乙烯薄膜表面分别含有活性基团羧酸和酸酐,通过热酯化方法,将活性基团与聚乙烯醇(PVA)超薄层相固定,将PAA 中的羧基与PVA 中的羟基,也通过热酯化作用固定,形成第二层。但只有与界面接触的大分子可应用于热酯化固定方法。2015 年,Ma 等[101]将阳极氧化铝(AAO)与丙烯酸(AA)复合,得到有序排列的水凝胶纤维-氧化铝复合材料。具有限域效应的纳米孔,将水凝胶纤维限域在其内部,而表层凝胶失水收缩将水凝胶纤维部分拉出,从而形成了纤维阵列。如图8b 所示,凝胶纤维阵列结构规整,并且这种软硬复合的界面减小了摩擦剪切过程中的机械形变,从而表现出优异的润滑性能。基于此制备出的双面水凝胶纤维材料,能够实现双界面pH 响应的摩擦调控。

图8 规整的纳米水凝胶纤维阵列的制备[101]Fig.8 The preparation of regular hydrogel nanofibers array[101]: (a) schematic of the preparation process of hydrogel nanofibers embedded into AAO; (b) top view of the as-prepared PAA hydrogel nanofibers array; (c) cross-sectional PAA hydrogel nanofibers array including protrusions out of nanopores after removal of the surface bulk gel layer; (d) bottom part of confined PAA hydrogel nanofibers
Zhang 等[102]使用重铬酸盐氧化UHMWPE,在其表面形成活性基团,然后利用催化剂催化PVA 水凝胶分子中的羟基与UHMWPE 表面活性基团发生化学接枝,并通过正交试验探索了温度、接枝时间、催化剂用量和接枝液浓度对接枝效果的影响。结果表明,通过接枝,人工关节的剪切强度可达1 MPa,UHMWPE的接触角从104°降低到39°,有效提高了表面润湿性。Zhao 等人[103]先用甲基丙烯酸-3(三甲氧基硅基)丙酯(TMSPMA)修饰玻璃、硅片、钛片、铝片和陶瓷表面,然后将聚丙烯酰胺(PAAM)或聚(乙二醇)二丙烯酸酯(PEGDA)交联到各种表面改性过的固体上,实现了水凝胶与不同基底之间的结合。该水凝胶与基底之间的界面韧性(>1000 J/m2)优于肌腱-骨以及软骨-骨界面之间的韧性。该团队[104]还对PVA进行冷冻解冻和干燥-退火的处理,在水凝胶与基底界面引入有序晶域,发现传统高韧性水凝胶粘合的疲劳阈值只有68 J/m2,这和高韧性水凝胶的疲劳阈值相似(~50 J/m2),也与破坏一层无定形分子链所需要的能量吻合。而PVA 水凝胶粘合界面的疲劳阈值能够达到800 J/m2,可比拟结缔组织与骨头连接界面的疲劳阈值。与此同时,他们通过30 000 次的循环剥离实验,进一步验证了这种界面的超高疲劳阈值。此外,由于水凝胶特有的高含水量、低摩擦系数等优势,抗疲劳水凝胶涂层的引入,也能有效地降低金属基底的摩擦系数和磨损系数。通过水凝胶和金属关节的高强度、高韧性、抗疲劳粘合,能有效解决水凝胶作为人造软骨所面临的技术挑战。
4 结语
金属、陶瓷、聚合物等传统关节假体在临床应用中已相当成熟,但其耐磨性、力学性能等方面仍存在各自的不足。这些材料的毒性、生物/组织相容性等方面,与理想的人工关节材料仍有一段差距,为了解决这些材料的摩擦磨损问题,研究人员致力于研究仿生关节软骨并将其修饰、复合到人工关节置换材料表面。水凝胶作为一种与关节软骨类似的湿、软、滑的材料,在生物医药等领域有重要的应用潜力。但传统水凝胶材料的力学性能有限,研究者们通过对其进行改性,可实现低摩擦、高承载、高耐磨等优点,但仍难以满足关节替代材料的要求,特别是其力学综合性能达不到天然关节软骨的水平。其次,在对水凝胶的机械性能与摩擦学性能不断优化与提高的同时,还需要关注其生物安全性,以满足其在生物医学领域的性能需求。
